2. 江苏省海洋水产研究所, 江苏 南通 226007
中华仙影海葵(Cereus sinensis Verrill)是江浙沿海一带常见可食性腔肠动物,隶属海葵目(Actiniaria) 、绿海葵科(Sagartiidae) 、仙影海葵属(Cereus)[1]。中华仙影海葵亦是药用生物,具有消炎、止泻、杀虫等功效[2]。海葵的毒素可用于降血压、凝血,对心脏神经和肌肉有止痛作用,具有安神镇静、止痛、抗衰老、抗癌变的潜在药用价值。近几年来国内也开始开展了相关海葵人工培育的研究工作,吴建平[3]等对中华仙影海葵早期发育研究做了详尽描述。史文军[4]等对中华仙影海葵溶细胞毒素CCT的活性鉴定和影响因素分析从生物化学方面补充了对中华仙影海葵的研究。
海底生境和饵料丰度等因素往往决定着海洋底栖腔肠动物的个体大小和生长速率[5]。由海葵早期幼体的定期饵料投喂实验可知,其生长速率随着投饵方式的不同而变化[6],然而在长达8年的对特定种海葵成体饵料投饵实验中也未能发现海葵个体大小的明显变化[7]。海葵个体经过一定的饥饿处理却会呈现不同程度的萎缩状态[8],所以其个体大小可以用来指示海葵健康生长状况。在大多数腔肠动物中,躯体大小对个体生活史的影响往往比个体年龄、存活率等更加重要[9]。所以腔肠动物的形态特征如柱体的高度、口盘和足盘的直径或者触手的数目都能一定程度地反映个体生长状况。QUIKE等[10]曾使用柱体高度和口盘直径作为等指海葵(Actinia equina)的生长标准。
本研究主要通过对中华仙影海葵个体采取不同底质、控制投喂不同饵料种类、投喂饵料频次和投喂饵料量的研究方式,探讨不同底质和不同饵料投喂方式对中华仙影海葵个体生长的影响,旨在为中华仙影海葵发育生物学研究提供参考资料。
1 材料与方法 1.1 实验材料本实验于2014年4-5月,在江苏省海洋增殖技术和育苗中心进行。人工孵化培育的海葵个体,置于培养缸中培养,以备用。实验用海水经过消毒、过滤、沉淀后使用,温度为22~26 ℃,盐度为20~26,pH为7.8~8.6,溶解氧控制在5 mg/L以上。实验用水槽规格为60 cm×50 cm×30 cm,槽内铺有大量细砂(无底质组实验除外),砂层厚度为20 cm。整个实验过程流水循环培养,实验所用系统属封闭式,各组平行实验相互独立。除不同底质培养实验时间为4月3日-5月3日外,其他实验时间均为4月13日-5月13日。
1.2 实验方法 1.2.1 不同底质培养实验设置底质为砂质培养组和无底质培养组。每组挑选发育同步且良好的海葵个体各10只,放入两组水槽内预培养2 d,每组设置3个重复。每天傍晚足量喂食新鲜文蛤肉,早晚拍照测量海葵个体口盘直径大小。
1.2.2 不同生长密度培养实验将水槽分别编号为A、B、C、D和E,其中分别培养发育同步且良好的海葵个体各10、15、20、25和30只,培育密度分别为33.3 ind/m2、50.0 ind/m2 、66.7 ind/m2、88.3 ind/m2和100.0 ind/m2,预培养2 d,每组设置3个重复。每天傍晚足量喂食新鲜文蛤肉,早晚拍照测量海葵个体口盘直径大小。
1.2.3 不同投喂饵料培养实验分别设置虾肉组、鱼肉组、文蛤肉组3组实验对象,每组挑选发育同步且良好的海葵个体各10只,预培养进行2 d,每组设置3个重复。每天傍晚足量喂食。
1.2.4 不同饵料投喂频次培养实验设置5组实验对象,分别编号为A、B、C、D和E。每组挑选发育同步且良好的海葵个体10只,每1、2、3、4和5天投喂一次,预培养2 d,每组设置3个重复。每次投喂足量饵新鲜文蛤肉。
1.2.5 不同饵料投喂量培养实验设置5组实验对象,分别编号为A、B、C、D和E。每组挑选发育同步且良好的海葵个体各10只,每组个体投喂饵料量控制在0.5 g/d、1.0 g/d、1.5 g/d、2.0 g/d和2.5 g/d的新鲜文蛤肉,预培养2 d,每组设置3个重复。
1.3 生长测定及数据分析采用记录海葵口盘直径工作为指标,用口盘直径描述海葵生长。用CANON 550D相机进行口盘照相记录,用AxioVision Rel.4.8.2 软件进行图象分析。口盘直径增长率和萎缩率参照公式:

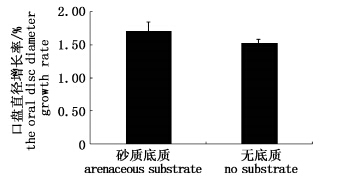
在砂质底质中生长的海葵个体初始口盘直径为(24.88±1.27)mm,经过30 d的生长,口盘长到(44.76±1.37)mm;无底质中的海葵个体初始口盘直径为(26.92±0.86)mm,经过30 d的生长,口盘长到(42.96±0.67)mm(表 1)。实验进行20 d后,砂质底质组和无底质组海葵个体口盘直径趋于一致。经SPSS做样本检验无显著差异(P>0.05)。实验结束后,计算不同底质中海葵个体口盘直径增长率(图 1)。砂质底质海葵口盘直径增长率达到1.71%,而无底质口盘直径增长率为1.53%。
| 表 1 不同底质海葵个体口盘直径变化 Tab. 1 The growth trend of sea anemone oral disc in different stocking substrates |
|
图 1 两种底质的口盘直径增长率比较 Fig. 1 The comparison of oral disc growth rates of sea anemone in two different substrates |
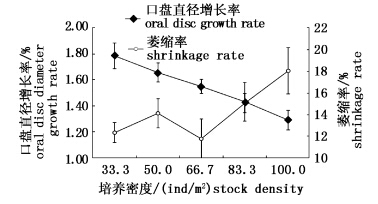
在培养密度实验中海葵个体口盘初始直径为25~27 mm,经过30天生长实验,海葵个体口盘直径达到36~45 mm(表 2)。而随着培育密度逐渐增加,海葵个体生长变得更加缓慢。低密度组(33.3 ind/m2)的海葵个体口盘从初始(25.88±1.27)mm生长到(45.76±1.37)mm,每日口盘增加在0.6 mm以上;而高密度组(100.0 ind/m2)海葵个体口盘从初始(27.22±1.11)生长到(37.06±1.37)mm,其口盘直径每日增加约0.3 mm。实验进行到15 d以后,高培养密度组100.0 ind/m2、83.3 ind/m2与低密度组66.7 ind/m2、50.0 ind/m2、33.3 ind/m2海葵个体口盘生长差异。结束后计算每组海葵口盘直径增长率(图 2),培养密度组33.3 ind/m2海葵个体口盘生长最快,而密度组50.0 ind/m2次之,培养密度组100 ind/m2的海葵个体口盘生长最为缓慢,其口盘直径增长率大小分别为1.73%、1.66%、1.55%、1.43%和1.29%。SPSS分析各组个体之间无显著性差异(P>0.05)。
| 表 2 不同培养密度海葵个体口盘直径变化 Tab. 2 The growth trend of sea anemone oral disc in the different densitymm |
|
图 2 不同培育密度下海葵口盘直径增长率与个体萎缩率 Fig. 2 The average daily growth rate of sea anemone oral disc and shrinkage rate of sea anemone in different density |
在培养过程中,海葵个体会呈现不同比例的萎缩状态(图 2)。低培养密度组(33.3 ind/m2)个体中生长最快,其萎缩率也较小,达到12.35%;高培养密度组(100.0 ind/m2)个体生长最慢,其个体萎缩率达到18.04%。实验结果显示,低密度培养会获得更高的口盘直径增长率和较低的萎缩率,增长率和萎缩率呈负相关。SPSS统计分析表明口盘直径增长率与萎缩率呈显著相关性(P<0.05)。
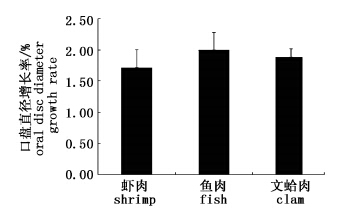
2.3 不同饵料对海葵个体生长影响不同种类饵料投喂实验中,海葵个体口盘直径从初始25~27 mm生长到41~51 mm,其中投喂新鲜鱼肉组的海葵个体口盘生长最快,每日海葵口盘平均增长达0.8 mm,投喂文蛤肉组海葵次之,每日口盘增长约0.6 mm,而投喂新鲜虾肉组的海葵口盘生长最慢,每日口盘增长在0.5 mm左右(表 3)。在实验进行15 d后,鱼肉组海葵个体口盘直径增长超过文蛤肉组和虾肉组。不同饵料虾肉、鱼肉和文蛤肉投喂下海葵个体的口盘直径增长率分别为1.72%、2.01%和1.89%(图 3)。经统计软件SPSS分析差异不显著(P>0.05)。
| 表 3 不同种类饵料海葵个体口盘直径变化 Tab. 3 The growth trend of sea anemone oral disc with the different baitsmm |
|
图 3 不同投喂饵料海葵个体口盘直径增长率 Fig. 3 The average daily growth rate of sea anemone oral disc under the different baits |
不同饵料投喂频次实验中,海葵个体口盘直径从初始28~29 mm生长到35~47 mm(表 4 )。其中以高频次组1 天一次投喂个体生长最快,口盘直径从初始(29.61±1.32)mm生长到(46.96±1.21)mm,每日口盘平均增加达到0.6 mm,其他投喂频次组口盘平均直径分别生长到(42.52±1.67)mm(2天一次)、(43.85±1.32)mm(3天一次)、(37.89±1.23)mm(4天一次)和(35.60±0.99)mm(5天一次),低频次投喂组5天一次海葵个体生长最为缓慢,其口盘每日增加为0.26 mm。培养实验进行20 d后,各组海葵个体口盘停止生长,低频次组(5天一次)甚至出现负增长。SPSS单因素方差分析表明,除频次组1天一次与频次组3天一次、频次组2天一次与频次3天一次、频次组4天一次和频次组5天一次生长差异不显著外(P>0.05),其余各组之间差异显著(P<0.05),其中频次组1天一次与频次组4天一次和频次5天一次、频次组3天一次和频次组5天一次生长差异极显著(P<0.01)。
| 表 4 不同投喂频次海葵个体口盘直径变化 Tab. 4 The growth trend of sea anemone oral disc with different feeding frequencymm |
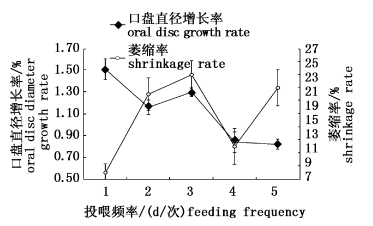
实验中进行不同组别海葵个体萎缩率与海葵个体平均日生长率比较(图 4)。在高频次组1天一次投喂下,口盘直径增长率达到1.51%,而最缓慢的为低频次组5天一次其口盘直径增长率为0.84%。口盘直径增长率大小排序为1天一次>3天一次>2天一次>4天一次>5天一次。高频次投喂组1天一次出现个体萎缩次数较少仅为8.00%,而低频次投喂组5天一次中出现萎缩次数达到21.00%。实验结果显示,高投喂频次培养会获得更高的口盘直径增长率和较低的萎缩率,增长率和萎缩率呈负相关。SPSS相关性分析不同饵料投喂频次下海葵口盘直径增长率与萎缩率呈显著相关性(P<0.05)。
|
图 4 不同饵料投喂频次下海葵口盘直径增长率与萎缩率 Fig. 4 The average daily growth rate of sea anemone oral disc and shrinkage rate with different feeding frequency |
不同饵料投喂量实验,海葵个体口盘直径从初始直径26~29 mm生长到36~46 mm(表 5)。其中高量投喂组2.0 g/d口盘变化最大,口盘终止直径达到(46.69±2.10)mm,每日增长达到0.63 mm;而低量投喂组0.5 g/d口盘变化最小,其口盘终止直径为(35.88±2.31)mm,每日口盘直径平均增加只有0.30 mm。实验进行20 d后,高量投喂组2.5 g/d海葵个体口盘直径变化超过低量投喂组(1.0 g/d和0.5 g/d)。SPSS分析显示,投喂组2.5 g/d与投喂组1.0 g/d和0.5 g/d生长差异显著(P<0.05)。
| 表 5 不同饵料投喂量海葵个体口盘直径变化 Tab. 5 The growth trend of sea anemone in the different feeding levelmm |
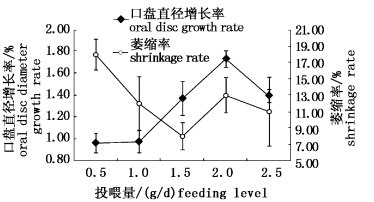
实验结束后计算海葵个体口盘直径增长率(图 5),高饵料量投喂组2.5 g/d、2.0 g/d和1.5 g/d海葵个体口盘直径增长率分别为1.40%、1.73%和1.38%,口盘直径每日增长也达到0.5 mm以上;而营养不足的低量投喂组1.0 g/d和0.5 g/d海葵个体口盘直径增长率只有0.97%和0.96%。可见良好的饵料条件和饵料量是海葵个体发育生长中重要条件。在对不同饵料量投喂海葵个体实验中出现萎缩个体比例与口盘直径增长率的比较中,高量投喂海葵出现低萎缩率,2.5 g/d和2.0 g/d组萎缩比例分别为11.00%和13.00%,而低饵料量投喂组0.5 g/d出现高萎缩率达到18.00%,其萎缩个体比例大小排序为2.0 g/d<2.5 g/d<1.0 g/d<1.5 g/d<0.5 g/d。实验结果显示,高投喂量培养会获得更高的口盘直径增长率和较低的萎缩率,增长率和萎缩率呈负相关。SPSS相关性统计分析表明,不同饵料投喂量下海葵口盘直径增长率与萎缩个体显著相关(P<0.05)。
|
图 5 不同饵料量投喂下海葵口盘直径增长率与萎缩率 Fig. 5 The average daily growth rate of sea anemone oral disc and shrink rate of sea anemone with the different feeding level |
中华仙影海葵是挖掘型足盘海葵,天然泥砂为其提供栖息场所,趋利避害。当遇到外界危险刺激时,触手和柱体收缩排出躯体部分水分,钻进泥砂中从而躲避敌害;沿海泥砂滩涂表层中含有大量的桡足类和其他各种营养丰富的食物[11],从而保证了野生海葵充足的食物来源。无底质培养海葵中因为没有底质供给海葵足盘附着,在流水培养过程中很容易随水流游动,造成触手断裂而更加短小。本实验中采取了砂质底质和无底质两组进行比较。经过30 d的生长实验得出结果:砂质底质培养和无底质培养对海葵个体口盘直径增长的影响不显著。
海葵动物喜单独生长,培养密度是决定个体生长发育的重要因素,如樱花海葵(Urticina felina)和紫点海葵(Cribinopsis crassa)个体生长间隔就要保持在20 cm以上。根据本实验结果,设计生长密度33.3 ind/m2、50.0 ind/m2 、66.7 ind/m2、88.3 ind/m2和100.0 ind/m2对海葵个体口盘直径增长影响差异不显著。各组海葵个体口盘直径增长率与培养过程中个体萎缩率呈显著相关性(P<0.05)。低密度组33.3 ind/m2、50.0 ind/m2 和66.7 ind/m2 海葵个体口盘直径增长率分别为1.73%、1.66%和1.55%,而其同时具有的萎缩率分别为12.35%、14.12%和11.76%。
中华仙影海葵营挖掘型生活方式,固着于泥砂中,自然个体用触手捕获经过其捕食范围内的鱼虾贝类等活体饵料。海葵通过触手捕获麻痹猎物,进而通过口盘送入消化咽腔内进行消化汲取营养物质,从而达到获得生长能量的目的。消化残物隔日会从海葵口盘排出。对中华仙影海葵亲体驯养的初步研究表明,在鱼肉、虾肉、文蛤、白虾、河蟹、海蟑螂和泥螺活体饵料中,除海蟑螂和河蟹基本不摄入外,其他饵料均可作为海葵个体生长发育饵料来源[12]。本实验中,采取投喂等量新鲜鱼肉、虾肉和文蛤肉的措施,比较了不同饵料投喂对中华仙影海葵个体生长的影响。实验结果表明:投喂等量新鲜饵料的前提下,鱼肉和文蛤肉组都能获得较高的口盘直径增长率,不同饵料对海葵个体口盘增长影响差异不显著(P>0.05)。
CHOMSKY等[13]报道了饵料投喂方式对等指海葵(Actinia equina)生长发育的影响,指出在长时间间隔的每2星期喂食一次投喂中,海葵口盘出现负增长同时伴随着净体重的下降。本实验研究表明,饵料投喂频次的不同对海葵个体口盘增长影响差异显著。低频次投喂组4天一次,实验期间海葵口盘直径每天增加0.26 mm,而高频次组1天一次、2天一次和3天一次增长达到0.50 mm以上。频次组1天一次与频次组4天一次和频次5天一次、频次组3天一次和频次组5天一次生长差异极显著(P<0.01)。饵料投喂频次是中华仙影海葵个体生长发育中的关键因素,适宜的饵料和良好的营养条件大大有利于海葵个体的健康发育。不同饵料投喂频次下海葵口盘直径增长率与萎缩率呈显著相关性(P<0.05),高饵料投喂频次获得低个体萎缩率,反之亦然。根据实验结果,实际大规模化人工养殖中饵料投饵频次应该控制在2~3天一次更加适宜。
饵料投喂的多少直接关系到海葵个体摄取能量的多少。实验结果表明,不同饵料投量对海葵个体口盘增长影响差异显著(P<0.05)。实验中低量饵料投喂组1.0 g/d和0.5 g/d两组海葵口盘直径增长率都不到1.00%,生长甚是缓慢;高量投喂组2.0 g/d获得最高增长率为1.73%。SPSS分析显示,投喂组2.5 g/d与投喂组1.0 g/d和0.5 g/d生长差异显著(P<0.05)。
实验过程中都伴随着海葵个体不同程度的萎缩现象,萎缩时间持续6~12 h,极少出现个体死亡现象,萎缩率与口盘直径增长率呈显著相关性(P<0.05),萎缩具体原因还待进一步实验观察研究。
| [1] | 裴祖南.中国动物志:腔肠动物门.海葵目.角海葵目.群体海葵目[M].北京:科学出版社,1998:28-32.PEI Z N. Fauna sinica:Coelenterata actiniaria ceriantharia zoanthidea[M].Beijing:Science Press, 1998:28-32. |
| [2] | 史文军,秦松,张朝晖,等.海葵化学成分及生物活性研究进展[J].海洋科学,2013,37(12):122-131.SHI W, QIN S, ZHANG Z,et al. Review of sea anemones compound and bioactivity[J]. Marine Sciences, 2013,37(12):122-131. |
| [3] | 吴建平,杨海萍,刘海林,等.中华仙影海葵早期发育的初步研究[J].上海海洋大学学报, 2011,20(6):826-830.WU J, YANG H, LIU H,et al. Initial study on early development of the sea anemone Cereus sinensis Verrill[J].Journal of Shanghai Ocean University, 2011,20(6):826-830. |
| [4] | 史文军,张朝晖,秦松,等.中华仙影海葵溶细胞毒素的初步分离及稳定性研究[J].中国海洋药物, 2013,32(5):14-20.SHI W, ZHANG Z, QIN S,et al. Preliminary isolation and stability analysis of cytolytic toxins from Cereus sinensis Verrill[J].Chinese Journal of Marine Drugs, 2013,32(5):14-20. |
| [5] | SEBENS K P. The allometry of feeding, energetics, and body size in three sea anemone species[J]. The Biological Bulletin, 1981,161(1):152-171. |
| [6] | CHIA F S, ROSTRON M. Some aspects of the reproductive biology of Actinia equina [Cnidaria: Anthozoa][J]. Journal of the Marine Biological Association of the United Kingdom, 1970,50(1):253-264. |
| [7] | ASHWORTH J, ANNANDALE N. Observations on some aged specimens of Sagartia troglodytes, and on the duration of life in coelenterates[J]. Proc R Soc Edinb, 1904,25(1):295-308. |
| [8] | SEBENS K P. The ecology of indeterminate growth in animals[J]. Annual Review of Ecology and Systematics,1987,18:371-407. |
| [9] | JACKSON J B, HUGHES T P. Adaptive Strategies of Coral-Reef Invertebrates: Coral-reef environments that are regularly disturbed by storms and by predation often favor the very organisms most susceptible to damage by these processes[J]. American Scientist, 1985,73(3):265-74. |
| [10] | QUICKE D, BRACE R. Phenotypic and genotypic spacing within an aggregation of the anemone, Actinia equina[J]. Journal of the Marine Biological Association of the United Kingdom, 1983,63(3):493-515. |
| [11] | 孟昭翠,徐奎栋.长江口及东海春季底栖硅藻、原生动物和小型底栖生物的生态特点[J].生态学报,2013,33(21):6813-6824.MENG Z C, XU K D. Ecological charateristics of benthic diatoms,protozoa and meiobenthos in the sediments of the Changjiang Estuary and East China Sea in spring[J].Acta Ecologica Sinica, 2013,33(21):6813-6824. |
| [12] | 吴建平,刘海林,杨海萍,等.中华仙影海葵亲体驯养的初步试验[J].水产养殖, 2011(4):47-49.WU J,LIU H,YANG H,et al.The primary experiment on rearing of parental sea anemone Cereus sinensis Verrill[J].Journal of Aquaculture, 2011(4):47-49. |
| [13] | CHOMSKY O, KAMENIR Y, HYAMS M,et al. Effects of feeding regime on growth rate in the Mediterranean Sea anemone Actinia equina (Linnaeus)[J]. Journal of Experimental Marine Biology and Ecology, 2004,299(2):217-229. |
2. Marine Fisheries Research Institute of Jiangsu Province, Nantong 226007, Jiangsu, China
 2015, Vol. 24
2015, Vol. 24


