牙鲆(Paralichthys olivaceus)是我国重要的海水养殖鱼类,也是研究比目鱼类(鲽形目鱼类)变态的主要对象。比目鱼类变态过程中,其中一只眼睛从一侧逐渐移动到头部的另一侧,这种移动是眶下皮肤组织中正在分裂的成纤维细胞的数量要多于眶上的结果,如牙鲆,其右侧眼睛逐渐移到左侧,是右眼眶下正在分裂的成纤维细胞数量多于眶上。而非移动眼则相反,眶上正在分裂的成纤维细胞要多于眶下[1, 2]。变态过程中导致眼睛移动的眶上和眶下成纤维细胞数目的差异,有无可能在胚胎阶段眼睛形成过程中眶上和眶下就存在微小细胞数目上的差异,这种差异到变态阶段在甲状腺激素诱导下,通过细胞分裂使眶上和眶下成纤维细胞数量差异更明显,最终导致眼睛移动呢?
脊椎动物眼睛起源于胚胎神经板前部一个由原始神经外胚层组成的视网膜发生区域,随着眼睛的发育,该区域逐渐被一分为二,各自形成视柄和视泡,最终形成左右眼[3]。在这过程中pax6界定了眼组织区域,tbx3也被检测到在视网膜区域表达[4],rx1确定了视杯的形成范围[5]。本研究调查牙鲆左右视网膜发生区域pax6、tbx3和rx1基因的表达,来探讨这些基因是否有可能在胚胎阶段眼睛形成过程中导致眶上和眶下区域成纤维细胞前体数量上的差异。
1 材料与方法 1.1 实验材料牙鲆胚胎、仔鱼购自青岛忠海水产有限公司,孵化水温为17~18 ℃,从受精后10 h开始采样,每隔5小时采样一次,用4%PFA固定后换成甲醇保存于4 ℃以备原位杂交用。用RNA保护液固定保存于-20 ℃用于RNA抽提。所采样中,受精后10 h和15 h胚胎处于原肠期,20 h胚胎为神经胚时期,25 h到35 h胚胎为器官形成期,40 h到50 h胚胎为尾部游离期,55 h之后为初孵仔鱼。
1.2 总RNA的提取和cDNA的合成取-20 ℃保存的样本于液氮中研磨,参照TRIzol(Invitrogen)说明书抽提RNA,用DNase I去除基因组DNA污染,所得的RNA保存于-80 ℃。利用Promega反转录系统,以总RNA为模板,oligo(dT)为引物于72 ℃反应5 min、冰浴5 min后42 ℃反应1.5 h反转录合成cDNA。
1.3 pax6、tbx3和rx1基因片段克隆简并引物设计方法参照陈彩芳等[6]CODEHOP法进行,分别设计牙鲆pax6引物pax6-F1和pax6-R1(表1),克隆长度为259 bp,退火温度为57.3 ℃;牙鲆tbx3引物tbx3-F1和tbx3-R1(表1),克隆长度为370 bp,退火温度:63.0 ℃;牙鲆rx1引物rx1-F1和rx1-R1(表1),克隆长度为228 bp,退火温度为61.0 ℃。PCR扩增后产物经1%琼脂糖凝胶电泳检测,用AXYGEN琼脂糖凝胶DNA回收试剂盒回收纯化PCR产物。所得产物连接至pGEM-T载体后转化到大肠杆菌感受态细胞Top10,阳性克隆送生工生物工程(上海)有限公司测序。
| 表1 PCR扩增所用引物序列 Tab. 1 PCR amplification primers used in this study |
设计引物(pax6-F2,pax6-R2,tbx3-F2,tbx3-R2,rx1-F2和rx1-R2)进行RT-qPCR,以β-actin作为内参基因(表1),设3个重复,体系为20 μL:上下游引物各1.0 μL(10 μmol),iQTM SYBR Green Supermix(Bio-Rad) 10 μL,cDNA 2 μL,RNase free H2O补足至20 μL。RT-qPCR反应条件如下:95 ℃ 3 min,95 ℃ 10 s,60 ℃ 30 s,72 ℃ 30 s,共40个循环; 65 ℃ 至95 ℃ 5 s,用Bio-Rad CFX-96软件进行溶解曲线分析和Ct值分析,相对表达量计算采用 2-ΔΔCt法,其数值用平均值 ± 标准误( Mean ± SE) 表示。
1.5 RNA整体原位杂交将1.3得到的含pax6、tbx3和rx1序列的阳性克隆经测序验证后大量扩增抽提质粒。分别用限制性内切酶NcoⅠ和SalⅠ线性化质粒,以线性化的质粒为模板分别用SP6和T7 RNA聚合酶体外合成含地高辛标记的pax6、tbx3和rx1基因正义和反义RNA探针。
RNA整体原位杂交步骤主要参考文献[7]进行。甲醇保存的胚胎,首先去掉卵膜。然后经过梯度复水至PBST(137 mmol/L NaCl,2.7 mmol/L KCl,10 mmol/L Na2HPO4,2 mmol/L KH2PO4,pH 7.4,0.1% Tween20)。样品置于双氧水中强光照射去色素,蛋白酶 K消化,用4% PFA于4 ℃固定。将胚胎放置于杂交液中70 ℃杂交过夜。杂交完毕洗脱探针。在37 ℃,1∶5 000的地高辛抗体4 ℃孵育过夜后,用NBT/BCIP暗室中显色(2~3 h)。显色完毕后,0.5×PBST漂洗,4 ℃下4% PFA中保存。用尼康SMZ 1500显微镜观察和记录整体信号。
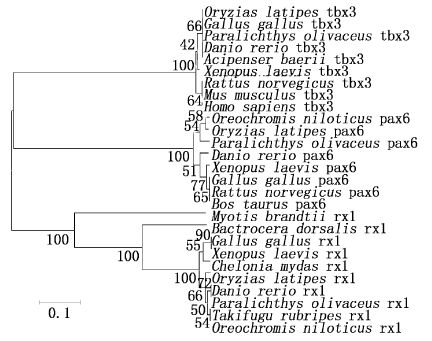
2 结果 2.1 pax6、rx1和tbx3序列分析本研究克隆所得到的牙鲆pax6部分cDNA序列长度为259 bp,与青鳉(Oryzias latipes)、罗非鱼(Oreochromis niloticus)和斑马鱼(Danio rerio)的相似性分别为93%、92%和85%。pax6氨基酸序列进化分析表明,牙鲆先与青鳉和罗非鱼的pax6聚为一支,再与斑马鱼和非洲爪蟾(Xenopus laevis)等pax6聚为一大支。
本研究克隆所得到的牙鲆tbx3部分cDNA序列长度为370 bp,与青鳉、斑马鱼和西伯利亚鲟(Acipenser baerii)的相似性依次为91%、86%和82%。tbx3氨基酸序列进化分析表明,牙鲆先与青鳉、斑马鱼、西伯利亚鲟和鸡(Gallus gallus)聚为一支,再与非洲爪蟾、人(Homo sapiens)和小鼠(Mus musculus)tbx3聚为一大支。
|
图1
基于不同物种的pax6、tbx3和rx1氨基酸序列的系统进化树
Fig.1
The phylogenetic tree of pax6,tbx3 and rx1
Bootstrap置信度百分率在节点标明。 Bootstrap majority consensus values are indicated at each branch point in percent. |
本研究克隆所得到的牙鲆rx1部分cDNA序列长度为228 bp,与斑马鱼、罗非鱼和红鳍东方鲀(Takifugu rubripes)的相似性依次为97%、91%和89%。rx1氨基酸序列进化分析表明,牙鲆先与斑马鱼、罗非鱼、红鳍东方鲀和青鳉等鱼类rx1聚为一支,再与其他物种rx1聚为一大支。
2.2 牙鲆胚胎pax6、tbx3和rx1基因定量表达利用荧光定量PCR检测牙鲆胚胎发育过程pax6、tbx3和rx1基因的表达量(图2),发现pax6在受精后10 h原肠胚早期没有表达,受精后20 h神经胚期才开始表达,之后其表达量逐渐加强;tbx3在受精后20 h开始表达,受精后50 h尾部游离期前表达量逐渐增强,而后减弱;rx1在受精后20 h开始表达,随后持续表达,表达量逐渐增多,在75 h开始减弱。

|
图2 牙鲆胚胎发育过程pax6、tbx3和rx1基因的表达 Fig.2 Detection of pax6,tbx3 and rx1 expression in embryos of Paralichthys olivaceus by reverse transcription qPCR |
牙鲆胚胎在受精后30 h视泡变为椭圆形的视杯,35 h晶体泡初现,50 h为尾部游离期即将进入初孵期,75 h为初孵仔鱼。我们选取上述时期进行RNA原位杂交,检测pax6、rx1和tbx3的时空表达。pax6基因在牙鲆30 h到75 h胚胎左右视网膜及晶状体处均有表达,左侧视网膜表达区域较右侧区略大(图版-1~5),在75 h胚胎左右眼视网膜差异尤为明显(图版-4,5),前脑以及神经管也有表达(图版-1~5);rx1基因只在视网膜区表达(图版-7~11),30 h到50 h胚胎,rx1表达逐渐增强,到了75 h胚胎,rx1只在晶状体一周表达,且表达较弱(图版-10,11),30 h到75 h左右侧视网膜区大小无明显可见差异(图版-7~11)。tbx3基因在牙鲆30 h到50 h胚胎视网膜区表达(图版-13~15),75 h胚胎在视网膜区不表达,而在身体其他部位持续表达(图版-16,17),30 h到75 h左右侧视网膜区大小无明显可见差异(图版-13~17)。pax6、rx1和tbx3原位杂交的阴性对照均没见明显信号(图版-6,12,18)。
3 讨论本研究所克隆到的pax6、tbx3和rx1的核苷酸序列与其他已知鱼类的同源序列的相似性均高于80%以上,表明pax6、tbx3和rx1这3个基因在鱼类各科属间保持着较高的相似性。从氨基酸序列的系统进化树中可以看出,牙鲆pax6序列与青鳉和罗非鱼聚为一支,牙鲆tbx3序列与青鳉、斑马鱼和西伯利亚鲟聚为一支,牙鲆rx1序列与斑马鱼、罗非鱼、红鳍东方鲀和青鳉聚为一支,也表明本研究所克隆到的应是牙鲆pax6、tbx3和rx1部分cDNA序列。此外,pax6、tbx3和rx1牙鲆胚胎阶段的RNA原位杂交信号显示,其主要在眼睛形成区域或神经管表达,与牙鲆上述3个基因同源的非洲爪蟾pax6、tbx3和rx1基因也存在相似的表达情况[4, 5]。
根据荧光定量PCR分析的pax6、tbx3和rx1基因在牙鲆胚胎的表达情况,可以发现pax6,rx1和tbx3均在受精后20 h左右开始表达。此3个基因在牙鲆胚胎过程中的表达时序与非洲爪蟾基本一致,在非洲爪蟾中,pax6在受精后第12阶段(13 h 15 min)开始表达,tbx3在受精后第12.5阶段(14 h 15 min)开始表达,rx1在受精后第14阶段(16 h 15 min)开始在表达[4, 8]。结合牙鲆胚胎眼睛发育时间和荧光定量结果,我们选取受精后30 h至75 h的胚胎和仔鱼作为原位杂交对象。
眼睛的发育很大程度上受pax6和rx1的调节,tbx3也参与了眼睛早期形态建成[4],这3个基因作为眼睛发育的重要基因,对控制细胞的增殖和分化起着重要作用[9, 10, 11, 12]。pax6基因在牙鲆左右视网膜及晶状体处均有表达,前脑以及神经管也有表达。tbx3和rx1基因在视网膜表达,上述基因表达位置与非洲爪蟾中的位置大致相同[4, 12]。视网膜发生区域pax6表达的细胞并不一定会全部形成眼睛,pax6在牙鲆胚胎左侧视网膜发生区域较右侧略大,而与决定视杯形成范围的rx1基因和界定视网膜形成区域的tbx3基因表达在左右侧没有差异,提示我们,左侧的pax6表达的细胞可能有更多的遗留在后续所形成眼睛的周围,这些眼睛周围特定细胞数量上的差异有无可能在牙鲆变态阶段在甲状腺激素诱导下细胞分裂,导致左右眼眶上眶下细胞的差异并最终导致眼睛移动呢?需要今后进一步调查pax6和rx1在其它比目鱼类胚胎阶段眼睛发育过程的表达式型,并进行后续的功能验证。
| [1] | BAO B L, KE Z H, XING J B, et al. Proliferating cells in suborbital tissue drive eye migration in flatfish[J]. Developmental Biology, 2011, 351(1): 200-207. |
| [2] | 鲍宝龙. 比目鱼类的眼睛移位和不对称的进化起源[J]. 上海海洋大学学报, 2012, 21(5): 728-736. BAO B L. The eye migration and evolutionary origin of flatfish asymmetry[J]. Journal of Shanghai Ocean University, 2012, 21(5): 728-736. |
| [3] | YANG X J. Roles of cell-extrinsic growth factors in vertebrate eye pattern formation and retinogenesis[J]. Seminars in Cell & Developmental Biology, 2004, 15(1): 91-103. |
| [4] | LI H S, TIERNEY C, WEN L, et al. A single morphogenetic field gives rise to two retina primordia under the influence of the prechordal plate[J]. Development, 1997, 124(3):603-615. |
| [5] | ZAGHLOUL N A, MOODY S A. Alterations of rx1 and pax6 expression levels at neuralplate stages differentially affect the production of retinal cell types andmaintenance of retinal stem cell qualities[J]. Developmental Biology, 2007, 306(1): 222-240. |
| [6] | 陈彩芳, 温海深, 何峰, 等. 程序化设计的简并引物克隆半滑舌鳎CYP17基因[J]. 中国海洋大学学报, 2009, 39(6): 1213-1218. CHEN C F, WEN H S, HE F, et al. Programming design of degenerate primers and cloning half-smooth tongue sole Cynoglossus semilaevis CYP17 gene[J]. Journal of Ocean University of China, 2009, 39(6): 1213-1218. |
| [7] | 陈文君, 鲍宝龙. 牙鲆纤维蛋白原相关蛋白(FREP1)基因的克隆和表达分析[J]. 上海海洋大学学报, 2013, 22(4): 488-495. CHEN W J, BAO B L. Cloning and expression analysis of a fibrinogen-related protein (FREP1) gene from Japanese flounder (Paralichthys olivaceus)[J]. Journal of Shanghai Ocean University, 2013, 22(4): 488-495. |
| [8] | MATHERS P H, GRINBERG A, MAHON K A, et al. The Rx homeobox gene is essential for vertebrate eye development[J]. Nature, 1997, 387(6633): 603-607. |
| [9] | CVEKL A, PIATIGORSKY J. Lens development and crystalline gene expression: many roles for Pax6[J]. Bioessays, 1996, 18(8): 621-630. |
| [10] | 钟兴武, 葛坚, 邓文国, 等. 光学离焦性近视眼视网膜pax-6基因表达的研究[J]. 中华眼底病杂志, 2003, 19(4): 442. ZHONG X W, GE J, DENG W G, et al. Express ion of pax-6 in retina of eyes with myopia induced by optical defocus[J]. Chinese Journal of Ocular Fundus Diseases, 2003, 19(4): 442. |
| [11] | ASHERY-PADAN R, GRUSS P. Pax6 lights-up the way for eye development[J]. Current Opinion in Cell Biology, 2001, 13(6): 706-714. |
| [12] | NELSON S M, PARK L, STENKAMP D L. Retinal homeobox 1 is required for retinal neurogenesis and photoreceptor differentiation in embryonic zebrafish[J]. Developmental Biology, 2009, 328(1): 24-39. |
 2015, Vol. 24
2015, Vol. 24


