2. 广东省水产经济动物病原生物学及流行病学重点实验室, 广东 湛江 524088;
3. 广东省水产经济动物病害控制重点实验室, 广东 湛江 524088;
4. 仲恺农业工程学院, 广东 广州 510225
弧菌(Vibrio)是引起海水养殖动物细菌性疾病最重要的病原菌之一。铁是弧菌生长、繁殖的必需元素[1]。然而,在宿主体内,大多数的铁离子与蛋白结合成复合物,游离的铁离子不能满足细菌生长的需要,因此从宿主体内获得铁离子是细菌定值感染并发挥毒力的关键[2]。病原弧菌主要形成了两种复杂的掠夺宿主铁的机制,一种是产生对铁高度亲和的螯合剂即铁载体,从转铁蛋白、乳铁蛋白中摄取铁[3, 4];二是产生外毒素破坏宿主组织中的红细胞,释放血红素,再从游离血红素中获得铁。血红素结合蛋白的作用就是吸收自由的亚铁血红素,传递给外膜蛋白上的受体,再通过TonB系统运送到周质内,最后在ATP结合盒的作用下穿过细胞质膜[5, 6]。当弧菌侵入鱼体后,受到宿主体内较低的游离铁离子浓度这一环境信号刺激,摄铁系统开始抢夺宿主体内的铁离子,帮助细菌突破宿主的非特异性防御机制,引发鱼类弧菌病。血红素摄取蛋白在摄取铁离子、感染宿主和发挥毒力等方面具有重要作用,目前该蛋白的形成机制和功能研究已经成为其致病性和慢性感染研究的热点。
溶藻弧菌(Vibrio alginolyticus)是一种嗜盐嗜温性、兼性厌氧的革兰氏阴性短杆菌,广泛存在于海水中,是水生动物弧菌病的主要病原菌之一[7, 8, 9],给水产养殖业造成巨大经济损失。此外,该菌可导致人类的食物中毒、中耳炎以及败血症等多种疾病[10, 11],严重危害人类健康。国内对该菌的研究多在病原分离鉴定、病理变化、疫苗研发等[12, 13, 14],对摄铁系统相关蛋白的研究相对较少。目前,人们已经鉴定了多种生物的血红素结合蛋白,但未见溶藻弧菌血红素结合蛋白HutB的相关报道。本研究以溶藻弧菌hutB为研究对象,通过分子生物学的方法,对其进行克隆和生物信息学分析,并检测其在不同铁源条件下的表达模式,以期初步了解溶藻弧菌血红素摄取系统的功能,为将来以该基因作为靶目标,阻止弧菌血红素结合蛋白的形成,进行免疫和生态防治奠定基础。
1 材料与方法 1.1 实验材料 1.1.1 菌株和载体溶藻弧菌HY9901由本实验室分离并保存[15];克隆载体pMD18-T购自TaKaRa公司。
1.1.2 主要试剂及材料主要试剂及材料包括ExTaq DNA聚合酶(TaKaRa公司);细菌基因组提取试剂盒、核酸切胶回收试剂盒(天根公司);预染蛋白Marker(Ferments公司);RNA提取试剂盒(上海生工生物技术服务有限公司);SYBR Green Master(美国Roche公司)。
1.2 方法 1.2.1 基因组DNA的提取将过夜活化的溶藻弧菌HY9901按1∶100的比例接种于含2%NaCl的胰蛋白胨大豆肉汤培养基(TSB),28 ℃震荡培养18 h。取1 mL菌液,8 000 r/min离心1 min收集菌体,按照细菌基因组DNA提取试剂盒说明书提取溶藻弧菌基因组DNA,-20 ℃保存备用。
1.2.2 hutB基因的克隆根据GenBank上已登录的溶藻弧菌全基因组序列(ACZB01000029.1),设计一对特异性引物,由上海生物工程技术服务有限公司合成,上游引物H1 :5′-ATGAAGTCCACACGCATCAC-3′,下游引物H2:5′-CTATGGGTACTGCAGTGCAT-3′,以1.2.1 提取的基因组DNA为模板,进行PCR反应:94 ℃预变性4 min;94 ℃变性30 s,63.4 ℃退火30 s,72 ℃延伸54 s,共35个循环;72 ℃再延伸10 min。1% 琼脂糖凝胶电泳检测并回收目的片段,-20 ℃保存备用。将切胶回收的PCR产物与 pMD18-T载体16 ℃连接过夜,构建 pMD18-hutB重组质粒,转化大肠杆菌DH5α感受态细胞,菌落PCR鉴定筛选阳性克隆送至上海生工测序。
1.2.3 生物信息学分析测序正确后利用ORF Finder和ExPAsy工具分析开放阅读框和理化性质;通过在线分析软件SoftBerry-Psite预测其氨基酸序列功能位点分布;采用SignalP 4.0 Server预测其信号肽序列 ;TMHMM Server 2.0预测其跨膜结构域;利用InternProscan 4在线预测蛋白质结构功能域;利用DNAMAN Version 6软件进行序列同源比对分析,Clastal 2.0和MEGA 5.0软件构建系统进化树。
1.2.4 不同铁源的设定根据溶藻弧菌对2-2’联吡啶(2,2’-Dipyridyl)抑制的最低浓度[16],设定溶藻弧菌不同的铁源培养条件;
①对照:新鲜(TSB); ②含20 μmol/L FeCl3的TSB(TSB+FeCl3);③含30 μmol/L血红素(Hemin)的TSB(TSB+Hemin);④ 含100 μmol/L 2-2’DP的TSB(TSB+DP);⑤含100 μmol/L 2-2’DP 和200 μmol/L FeCl3的TSB(TSB+DP+FeCl3);⑥含100 μmol/L 2-2′DP 和300 μmol/L的Hemin的TSB(TSB+DP+Hemin)。
溶藻弧菌活化后,按照1∶100的比例分别接种于上述6种不同铁源培养基,28 ℃,200 r/min振荡培养18 h,取1 mL菌液1 000 r/min离心收集菌体。
1.2.5 总 RNA 的提取和cDNA的制备在1.2.4 收集的6管菌体内分别加入1 mL 的Trizol试剂,混合均匀,静置7 min,加入0.2 mL 氯仿(chloroform),振荡15 s,静置3 min,4 ℃,12 000 r/min离心15 min;取上清移入一干净的EP管,加入异丙醇(isopropanol)500 μL,静置15 min,4 ℃,11 800 r/min离心10~20 min;75% 乙醇洗涤沉淀;离心并晾干后加入48 μL无RNase DEPC水溶解RNA,取3 μL电泳检测后-80 ℃超低温保存备用。cDNA制备参考逆转录试剂盒说明书,反转录的反应程序为:25 ℃,30 min;37 ℃,10 min;90 ℃,3 min。-20 ℃保存备用。
1.2.6 qRT-PCR分析根据hutB基因的保守序列设计特异性引物进行qRT-PCR分析,引物hutB-F:CGCCGTCACTGAACTCTTG;引物hutB-R:ACGATGGTAGCCCACTTTA。选取的对照基因为16S rRNA(GeneBank No: NR_044825),引物为16S rRNA-F:TTGCGAGAG TGAGCGAATCC;16S rRNA -R:ATGGTGTGACGGGCGGTGTG。以6种不同铁源培养下溶藻弧菌的RNA为模板进行qRT-PCR,分析hutB基因的表达量。PCR反应程序为:94 ℃预变性3 min;94 ℃变性15 s,55 ℃退火15 s,72 ℃延伸20 s,共40个循环。试验重复3次。
利用iQTM 5 Optical System软件导出实验数据,利用2-△△Ct 法分析不同的铁源培养下hutB的相对表达量。应用SPSS 17.0软件对获得的结果进行统计学分析。当P<0.01时实验组各基因mRNA表达量与对照组差异极显著,P<0.05时实验组各基因mRNA表达量与对照组差异显著。
2 结果与分析 2.1 hutB基因的序列分析所克隆的溶藻弧菌hutB基因(GenBank登录号为KF910677)含有一个870 bp的开放阅读框(ORF),编码299个氨基酸(图1),理论分子量为30.59 ku,等电点为6.45。该基因编码的蛋白HutB在280 nm处的摩尔消光系数为7 450(mol·cm)-1,N末端是甲硫氨酸(Met),蛋白质不稳定系数为29.83(<40),表明该蛋白稳定。

|
图1
hutB基因核苷酸及相应的氨基酸序列
Fig.1
hutB gene sequence and corresponding amino acid sequence
*代表终止子,虚线部分为依赖于cAMP和cGMP的蛋白激酶磷酸化位点,单下划线部分为蛋白激酶C磷酸化位点,方框部分为酪蛋白激酶II磷酸化位点,波浪线部分为N-肉豆蔻酰位点,双下划线部分为微体C-末端靶信号位点。 The stop codon was showed by an asterisk. The cAMP-and cGMP-dependent protein kinase phosphorylation site was under dashline. The four protein kinase C phosphorylation sites were underline. The two casein kinase II phosphorylation sites were in the box. The three N-myristoylation sites were under wavyline. The three microbodies C-terminal targeting signals were double underline. |
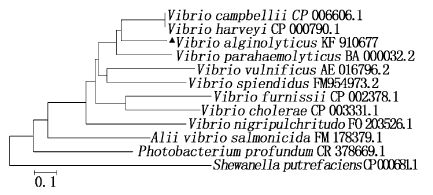
HutB具有5个跟血红素结合有关的酪氨酸,不具有色氨酸、吡咯赖胺酸和硒代半胱氨酸。在酵母和大肠杆菌中表达的半衰期分别大于20 h和10 h,在哺乳动物网状细胞质体外培养表达的半衰期为30 h。HutB含有1个cAMP和1个cGMP依赖性蛋白激酶磷酸化位点,4个蛋白激酶C磷酸化位点,2个酪蛋白激酶Ⅱ磷酸化位点,3个N-豆蔻酰化位点,3个微体C末端靶信号位点。溶藻弧菌HutB蛋白序列中有1个明显的信号肽序列,长度为23个氨基酸,序列为MKNTRITIHAVVTAAISASSANT。HutB多肽链有6个功能域,在第35-265 bp的氨基酸残基存在ABC转运周质结合域,其中有几个周质结合蛋白参与铁的转运;第34-289 bp之间存在铁载体/钴胺素周质结合域;第33-145和146-277 bp之间为固氮酶钼铁蛋白结构域;第33-236 bp之间的氨基酸残基为维生素B12结合域;第1-23 bp为信号肽序列,与SignalP 4.0 Server在线预测分析结果相符;第31-289 bp为“螺旋骨干”金属受体超家族结构域。溶藻弧菌HutB与坎氏弧菌(Vibrio campbellii)和哈氏弧菌(Vibrio harveyi)的同源性最高,皆达到74%;其次是副溶血弧菌(Vibrio parahaemolyticus),为72%。以N-J法构建的HutB氨基酸序列系统进化树显示,溶藻弧菌HY9901 HutB蛋白与坎氏弧菌、哈氏弧菌和副溶血弧菌聚为同一亚族,表明它们之间有较近的亲缘关系,与传统的形态学和生化特征分类结果一致(图2)。
|
图2 以N-J法构建的hutB基因氨基酸序列系统进化树 Fig.2 Construction of hutB phylogenetic tree based on Neighbor-Joining method |
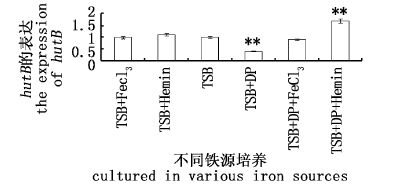
图3显示,不同铁源培养下hutB基因的表达不同。在添加FeCl3和Hemin的富铁环境下,hutB基因的表达与对照组相比差异不大,只是TSB+Hemin比TSB+ FeCl3的表达量略微偏高。当在含铁螯合剂2-2’联吡啶的TSB培养基中培养时,hutB基因的表达量与对照组相比下调极显著(P<0.01),为对照组的一半左右;当在TSB+DP+FeCl3培养基中表达量恢复到正常水平,而在TSB+DP+Hemin培养下hutB表达量极显著高于对照组(P<0.01),提示hutB参与了血红素的利用过程。
|
图3 hutB基因在不同铁源培养下的表达差异 **表示P<0.01。 Fig.3 The mRNA expression level of hutB gene under various iron sources |
铁在细菌毒力发挥中起重要作用。为从宿主体内获得铁,许多革兰氏阴性病原菌在进化过程中形成血红素摄取系统。该系统包括位于细胞表面的血红素受体,位于外周胞质的血红素转运蛋白和位于内膜上的ATP结合匣式转运子[17]。本研究从溶藻弧菌中克隆到血红素结合蛋白hutB基因并对其进行生物信息学分析。多序列比对表明不同弧菌的hutB基因序列的差异主要表现为N端序列的极度不保守,这与先前对美人鱼弧菌hutB基因的结论一致[18]。对不同革兰氏阴性致病菌的外周质血红素结合蛋白序列对比发现:它们的血红素结合位点是保守的。目前报道的铜绿假单胞菌(Pseudomonas aeruginosa)的PhuT和痢疾志贺氏菌(Shigella dysenteriae)的ShuT的血红素结合位点为酪氨酸位点[19]。本研究发现hutB基因具有5个酪氨酸位点,但这些位点是否能与血红素结合还需要进一步的实验证明。
LEMOS和OSORIO等研究发现在含有DP和Hemin的培养基中鳗弧菌(Vibrio anguillarum)的TonB和hutX基因的表达量都会升高,而在富铁的条件下它们的表达量都出现下调[20]。WANG等也发现当添加不同浓度的DP时,TonB1基因的表达量随着DP浓度的升高而升高[16],RO等研究美人鱼弧菌hutA时也有同样的现象[21]。本实验中我们发现溶藻弧菌hutB在含有血红素的环境条件下表达量显著上调,在铁限制且血红素存在时表达量极其显著上调,与前人研究一致,表明溶藻弧菌hutB基因能够利用血红素作为铁源。但hutB基因在铁丰富培养基中表达量维持正常水平,在缺铁培养时hutB基因表达量下降,与前人的研究不一致,值得进一步探索其摄铁机理。本研究初步表明溶藻弧菌hutB基因在血红素摄取中起重要作用,下一步将通过血红素结合实验,验证其是否参与血红素铁的利用;另外通过基因敲除,比较野生株、hutB基因突变株在Hemin为唯一铁源时的生长情况,确定hutB基因体外利用血红素铁的功能。
| [1] | 陈强, 鄢庆枇, 马甡. 溶藻弧菌致病性研究进展[J]. 海洋科学, 2006, 30(8): 83-89. CHEN Q, YAN Q P, MA S. Progress on pathogenicity research of Vibrio alginolyticus [J].Marine Sciences, 2006, 30(8): 83-89. |
| [2] | RATLEDGE C, DOVER L G. Iron metabolism in pathogenic bacteria [J]. Annual Review of Microbiology, 2000, 54(10):881-941. |
| [3] | 王蓬勃,马悦,刘琴,等.溶藻弧菌铁载体合成及外膜蛋白表达的研究[J].微生物学通报,2006,33(2): 48-53. WANG P B, MA Y, LIU Q, et al.Growth, siderophore production and outer membrane protein expression of Vibrio alginolyticus by iron regulation [J].Microbiology China,2006,33(2): 48-53. |
| [4] | WANDERSMAN C, DELEPELAIRE P. Bacterial iron sources: from siderophores to hemophores [J]. Annual Review of Microbiology, 2004, 58(10): 611-647. |
| [5] | SHIBATA Y, HIRATSUKA K, HAYAKAWA M, et al. A 352KDa coaggregation factor is a hemin binding protein in Porphyromonas gingivalis[J]. Biochemical and Biophysical Research Communications, 2003, 300(2):351-356. |
| [6] | PROTCHENKO O, SHAKOURY-ELIZEH M, KEANE P, et al. Role of PUG1 in inducible porphyrin and heme transport in Saccharomyces cerevisiae[J]. Eukaryotic cell, 2008, 7(5): 859-871. |
| [7] | SADOK K, MEJDI S, NOURHEN S, et al. Phenotypic characterization and RAPD fingerprinting of Vibrio parahaemolyticus and Vibrio alginolyticus isolated during Tunisian fish farm outbreaks[J]. Folia microbiologica, 2013, 58(1):17-26. |
| [8] | CHANG C C, YEH M S, LIN H K, et al. The effect of Vibrio alginolyticus infection on caspase-3 expression and activity in white shrimp Litopenaeus vannamei[J]. Fish & shellfish immunology, 2008, 25(5):672-678. |
| [9] | BEN KAHLA-NAKBI A, CHAIEB K, BAKHROUF A. Investigation of several virulence properties among Vibrio alginolyticus strains isolated from diseased cultured fish in Tunisia[J]. Diseases of Aquatic Organisms, 2009, 86(1):21-28. |
| [10] | CAMPANELLI A, SANCHEZ-POLITTA S, SAURAT J H. Cutaneous ulceration after an octopus bite: infection due to Vibrio alginolyticus, an emerging pathogen [J]. Annales de dermatologie et de vénéréologie, 2008, 135(3):225-227. |
| [11] | SGANGA G, COZZA V, SPANU T, et al. Global climate change and wound care: case study of an off-season Vibrio alginolyticus infection in a healthy man [J]. Ostomy Wound Manage, 2009, 55(4):60-62. |
| [12] | 庞兴红,周永灿,徐先栋,等. 基于一种新基因的溶藻弧菌毒力菌株检测方法的建立[J]. 水产科学,2011,30(6):342-346. PANG X H, ZHOU Y C, XU X D et al. Establishment of a method for detection of Vibrio alginoly ticus virulent strains based on a new gene[J].Fisheries science, 2011,30(6):342-346. |
| [13] | 左凤琴, 简纪常, 吴灶和. 溶藻弧菌胞外产物注射赤点石斑鱼后的组织病理学观察[J]. 广东海洋大学学报, 2006, 26(3):13-16. ZUO F Q, JIAN J J, WU Z H. Histpathology of Epinephelus akaara injected with the extracellular products from Vibrio alginolyticus[J]. Journal of Guangdong Ocean University, 2006, 26(3):13-16. |
| [14] | HUANG Z, TANG J, LI M, et al. Immunological evaluation of Vibrio alginolyticus, Vibrio harveyi, Vibrio vulnificus and infectious spleen and kidney necrosis virus (ISKNV) combined-vaccine efficacy in Epinephelus coioides [J]. Veterinary Immunology and Immunopathology, 2012, 150(1/2):61-68. |
| [15] | CAI S H, WU Z H, JIAN J C, et al. Cloning and expression of the gene encoding an extracellular alkaline serine protease from Vibrio alginolyticus strain HY9901, the causative agent of vibriosis in Lutjanus erythopterus (Bloch) [J]. Journal of Fish Diseases, 2007, 30(8):493-500. |
| [16] | WANG Q, LIU Q, MA Y, et al. Isolation, sequencing and characterization of cluster genes involved in the biosynthesis and utilization of the siderophore of marine fish pathogen Vibrio alginolyticus[J]. Archives of microbiology, 2007, 188(4): 433-439. |
| [17] | TONG Y, GUO M. Cloning and characterization of a novel periplasmic heme-transport protein from the human pathogen Pseudomonas aeruginosa [J]. Journal of Biological Inorganic Chemistry, 2007, 12(6):735-750. |
| [18] | ANDREONI F, BIANI R, SERAFINI G, et al. Expression, purification, and characterization of the recombinant putative periplasmic hemin-binding protein (HutB) of Photobacterium damselae subsp.piscicida[J]. Bioscience, biotechnology, and biochemistry, 2009, 73(5):1180-1183. |
| [19] | EAKANUNKUL S, LUKAT-RODGERS G S, SUMITHRAN S, et al. Characterization of the periplasmic heme-binding protein shut from the heme uptake system of Shigella dysenteriae [J]. Biochemistry, 2005, 44(39):13179-13191. |
| [20] | LEMOS M L, OSORIO C R. Heme, an iron supply for vibrios pathogenic for fish [J]. Biometals, 2007, 20(3/4): 615-626. |
| [21] | RÍO S J, OSORIO C R, LEMOS M L. Heme uptake genes in human and fish isolates of Photobacterium damselae: existence of hutA pseudogenes [J]. Archives of microbiology, 2005, 183(5): 347-358. |
2. Guangdong Provincial Key Laboratory of Pathogenic Biology and Epidemilogy for Aquatic Economic Animals, Zhanjiang 524088, China;
3. Key Laboratory of Disease Controlling for Aquatic Economic Animals of Guangdong Higher Education Institutions, Zhanjiang 524088, China;
4. Zhongkai University of Agriculture and Engineering, Guangzhou 510225, China
 2015, Vol. 30
2015, Vol. 30


