扩展功能
文章信息
- 郭慧, 朱晓闻, 欧荣华, 卢芷程, 谭翠婷, 申玉春, 朱春华
- GUO Hui, ZHU Xiaowen, OU Ronghua, LU Zhicheng, TAN Cuiting, SHEN Yuchun, ZHU Chunhua
- Cu2+胁迫对罗氏沼虾血细胞毒性及caspase-3、α-2M基因表达的影响
- Effects of Cu2+ Stress on Hemocytes Toxicity and caspase-3, α-2M Gene Expression in Macrobrachium rosenbergii
- 四川动物, 2017, 36(3): 293-299
- Sichuan Journal of Zoology, 2017, 36(3): 293-299
- 10.11984/j.issn.1000-7083.20170035
-
文章历史
- 收稿日期: 2017-02-08
- 接受日期: 2017-03-14
近年来,随着我国工厂化和集约化水产养殖的快速发展,水环境污染状况日趋严重。在各类环境污染物中,重金属由于其遗传毒性、持久性和不可降解性而备受关注(Wang et al., 2013)。Cu2+是甲壳动物体内必需的微量营养素,参与了多种生理过程,如血蓝蛋白的合成、酶功能和组织完整性等(Bharadwaj et al., 2014)。但是高浓度的Cu2+亦会对甲壳动物产生毒害作用(Santos et al., 2000;Valavanidis & Vlachogianni,2012)。在生产实践中,Cu2+作为矿物营养素、除藻剂或病原抑制药物被广泛应用于水产养殖领域,其中的Cu2+沉淀积累在池塘中,对生态环境构成了极大的威胁(Liao et al., 2006)。据报道,在我国珠江口地区Cu2+的浓度处于污染水平,并具有一定的潜在生物毒性(Wang et al., 2015)。研究表明,Cu2+胁迫影响了对虾的体色(Martínez et al., 2014)、存活和繁殖(Rao & Anjaneyulu,2008),造成鳃和肝胰腺的组织损伤(Frías-Espericueta et al., 2008),增加了对病菌的易感性,降低其免疫功能(Yeh et al., 2004)。当虾类处于胁迫状态时,其血细胞中的细胞凋亡率、活性氧(ROS)含量、一氧化氮(NO)含量和酯酶活性都会发生改变(Xian et al., 2010, 2013;Guo et al., 2013;郭慧等,2015),因此可根据这些指标的变化来判断机体的免疫状态。Caspase-3是细胞凋亡关键的执行分子,在凋亡信号传导途径中发挥主导功能,α2巨球蛋白(α-2M)被认为参与了虾类的先天性免疫,而目前关于Cu2+胁迫下罗氏沼虾Macrobrachium rosenbergii血细胞参数和caspase-3以及α-2M基因表达量的研究尚未见报道。因此,本文拟采用流式细胞术和实时荧光定量PCR的方法,研究Cu2+胁迫对罗氏沼虾血细胞中细胞凋亡率、ROS含量、NO含量、酯酶活性以及caspase-3和α-2M基因表达量的影响,为进一步探究Cu2+胁迫对虾类毒性效应提供参考。
罗氏沼虾,又名大头虾、马来西亚大虾,是目前世界上养殖量最大的三大虾种之一,也是我国重要的经济甲壳动物,在水生态系统中分布较为广泛,江河、湖泊等淡水和河口半咸水水域中均有分布,对水环境中各种理化性质的变化反应较灵敏(吴维福等, 2014)。因此,开展重金属Cu2+对罗氏沼虾毒性效应的研究具有重要的实践意义,为水环境毒理学和生态风险评价的研究奠定理论基础。
1 材料与方法 1.1 实验材料实验用罗氏沼虾购自湛江某养殖场,体质量为10.89 g± 1.42 g,性成熟,非繁殖期。选取大小均匀、体色正常、附肢完整、活力强、无病患且处于蜕皮间期的个体用于实验。将罗氏沼虾在实验室循环水系统中暂养于温度为26 ℃±2 ℃的淡水中2周,所有水质指标均符合《渔业水质标准》的要求(国家海洋局,1989),暂养及胁迫实验期间24 h不间断充氧。暂养期间每日06: 00和18: 00按虾体质量的2%投喂2次,胁迫实验前24 h停止喂食。
2',7'-dichlorofluorescin diacetate(DCFH-DA)、DAF-FM DA购自Sigma公司;二乙酸荧光素(fluorescein diacetate,FDA)、Annexin V FITC/PI(碘化丙啶)凋亡检测试剂盒、总RNA提取试剂Trizol、琼脂糖购自Invitrogen公司;反转录试剂盒PrimeScriptTM RT reagent Kit、rTaq PCR试剂盒、焦炭酸二乙酯(DEPC)、DL2000 Ladder Marker、荧光定量试剂盒(SYBR Green QPCR Super Mix-UDG)购自TaKaRa公司;核酸染料EB替代物、PCR Premix Taq、DNA ladder、6×loading buffer购自东盛公司;其他试剂均为国产分析纯,所用引物由上海生工生物科技有限公司合成。
1.2 胁迫实验实验设对照组和胁迫组,每组3个重复。根据前人研究(Chen & Wang,2001;Mahmood et al., 2009)及预实验结果,设置理论胁迫浓度为0(对照组)、100 μg·L-1(胁迫组),用硫酸铜配置Cu2+溶液。将罗氏沼虾置于塑料箱中,每桶25尾,胁迫组加入180 L硫酸铜溶液。每24 h换水50%。分别在胁迫后的0 h、3 h、6 h、12 h、24 h和48 h从每桶中随机选取3尾(n=9) 罗氏沼虾,参照Guo等(2015)的方法收集血淋巴。
1.3 血细胞悬液的制备用2 mL的一次性注射器吸取冰上预冷的抗凝剂(葡萄糖20.5 g·L-1,柠檬酸钠8 g·L-1,氯化钠4.2 g·L-1,调pH至7.5) 200 μL,然后从虾的围心腔抽取等量的血淋巴至1.5 mL离心管中,取200 μL用预冷的抗凝剂稀释血细胞浓度约为1×106个/mL,用于流式细胞术指标的检测;余下的血淋巴在800 g、4 ℃离心10 min,弃上清,将血细胞重悬于Trizol中,-80 ℃保存,用于基因表达量分析。
1.4 流式细胞仪及参数设置实验所用流式细胞仪为美国BD (Becton Dickinson)公司生产的FACSVerse,数据获取和分析软件为Cell Quest (Becton Dickinson Immunocytometry Systems,San Jose,CA)。每个样品均获取10 000个细胞。异硫氰酸荧光素(FITC)、FDA、DCF、DAF用绿色荧光通道(第一荧光通道,FL1) 获取荧光数据。PI检测用第二荧光通道(FL2) 获取荧光数据。
1.5 血细胞凋亡率参照冼健安等(2015)的方法,以Annexin V-FITC/PI凋亡检测试剂盒检测血细胞的凋亡率。取200 μL血细胞悬液,加入2.5 μL Annexin V-FITC和5 μL PI工作液,轻轻震荡混匀,避光染色15 min后加入50 μL 5×Annexin V结合缓冲液,200目筛网过滤后立即上机检测。结果以Annexin V-FITC和PI双参数散点图显示,设门划分细胞类群:活细胞(Annexin V-FITC-/PI-)位于左下象限,前期凋亡细胞(Annexin V-FITC+/PI-)位于右下象限,后期凋亡细胞和死细胞(Annexin V-FITC+/PI+)位于右上象限。从样品制备到上样的整个过程应控制在30 min以内,以避免血细胞离体时间过长对结果造成不良影响。
1.6 ROS含量的测定以DCFH-DA为标记探针检测ROS含量。取200 μL血细胞悬液,加入DCFH-DA工作液10 μL,混匀后避光孵育30 min,200目筛网过滤后上机检测。
1.7 NO含量测定以DAF-FM DA为标记探针检测NO含量。取血细胞悬液200 μL,加入10 μM的DAF-FM DA工作液,混匀后避光孵育60 min,200目筛网过滤后上机检测。
1.8 酯酶活性采用非特异脂溶性底物FDA进行酯酶活性测定。取血细胞悬液200 μL,加入5 μM FDA,混匀后避光孵育30 min,用200目筛网过滤后上机检测。
1.9 基因表达血细胞总RNA的提取参照Trizol (Invitrogen)说明书进行,cDNA的合成按照TaKaRa公司的PrimeScript RT reagent Kit with gDNA Eraser (Perfect Real Time)试剂盒说明书进行。引物序列均来自美国国家生物技术信息中心(National center for Biotechnology Information,NCBI)数据库,利用Premier Primer 5.0设计引物。引物序列如表 1所示。荧光定量PCR使用TaKaRa公司的SYBR Premix EX Taq试剂盒,按说明书操作。荧光定量PCR扩增程序:95 ℃预变性30 s;95 ℃变性5 s,60 ℃退火60 s,40个循环。在PCR反应过程中,设计用灭菌超纯水代替cDNA模板的阴性对照,每个样品至少设置3个重复。扩增结束后启动熔解曲线收集程序,根据熔解曲线的温度判断扩增过程的特异性并对扩增曲线进行分析。所得数据以ABI 7500 SDS进行分析,以β-actin作为内参,根据目的基因和β-actin的Ct值用2-ΔΔCt法计算目的基因mRNA的相对表达量(Guo et al., 2015)。
| 目的基因Target gene | 序列Sequence (5'-3') |
| caspase-3 F | TGAGGCACTGGTCTTGTCCAGAAT |
| caspase-3 R | GGCACTTGCATTGACTGCTGGATT |
| α-2M F | CTCGGCCATCTTATCCGTATG |
| α-2M R | GGGAGCGAAGTTGAGCATGT |
| β-actin F | CATCACCAACTGGGACGACATGGA |
| β-actin R | GAGCAACACGGAGTTCGTTGT |
数据用SPSS 18.0进行配对t检验,统计结果均表示为平均值±标准差(Mean±SD),P<0.05为差异有统计学意义。用Pearson分析ROS和NO含量与血细胞凋亡率之间的相关性。
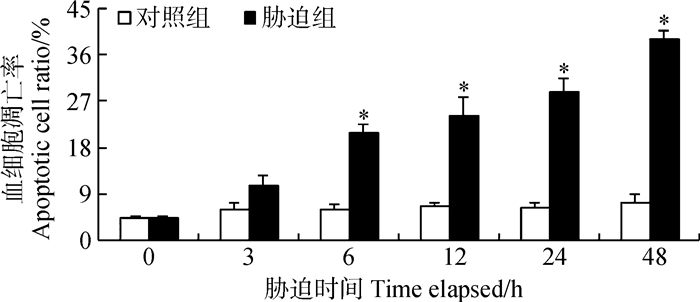
2 结果 2.1 血细胞凋亡率在胁迫后的3 h,Cu2+对血细胞凋亡率无显著影响,在胁迫后的6~48 h,血细胞凋亡显著升高,在48 h时达到39.01%,是对照组的5.38倍(图 1)。
|
| 图 1 Cu2+胁迫对罗氏沼虾血细胞凋亡率的影响 Fig. 1 Effect of Cu2+ on apoptotic cell ratio in hemocyte of Macrobrachium rosenbergii * P<0.05,下同the same below. |
| |
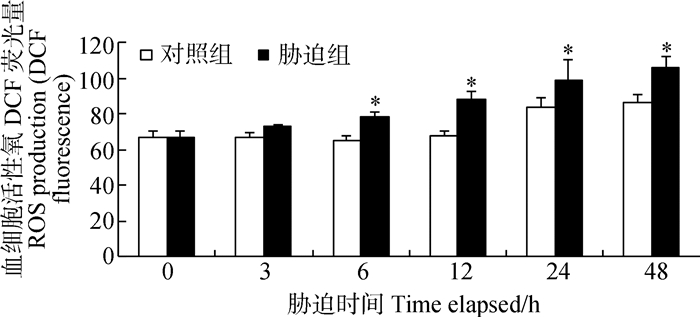
ROS含量的变化趋势和血细胞凋亡率较为一致(图 2),在胁迫后的3 h,ROS含量无显著变化(P>0.05),在胁迫后的6~48 h,ROS的含量显著升高(P<0.05),在48 h由对照组的86.32上升到106.31。
|
| 图 2 Cu2+胁迫对罗氏沼虾血细胞ROS含量的影响 Fig. 2 Effect of Cu2+ on ROS production in hemocyte of Macrobrachium rosenbergii |
| |
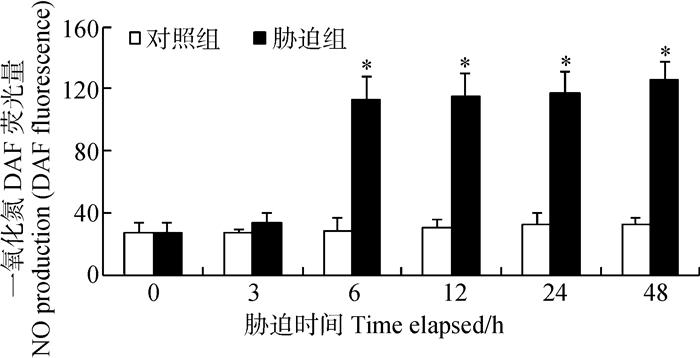
Cu2+对罗氏沼虾血细胞中NO含量的影响如图 3所示,在胁迫的3 h,NO含量变化不显著(P>0.05),在胁迫后的6~48 h,NO含量持续增加,并与对照组有显著性差异(P<0.05),最高值出现在48 h,为126.08。
|
| 图 3 Cu2+胁迫对罗氏沼虾血细胞一氧化氮含量的影响 Fig. 3 Effect of Cu2+ on NO production in hemocyte of Macrobrachium rosenbergii |
| |
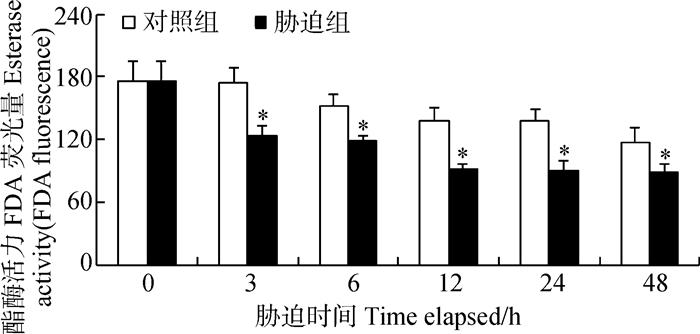
酯酶活性在胁迫后的3~48 h都呈显著下降的趋势(P<0.05),最低值出现在48 h,由对照组的117.78下降到88.40(图 4)。
|
| 图 4 Cu2+胁迫对罗氏沼虾血细胞酯酶活性的影响 Fig. 4 Effect of Cu2+ on esterase activities in hemocyte of Macrobrachium rosenbergii |
| |
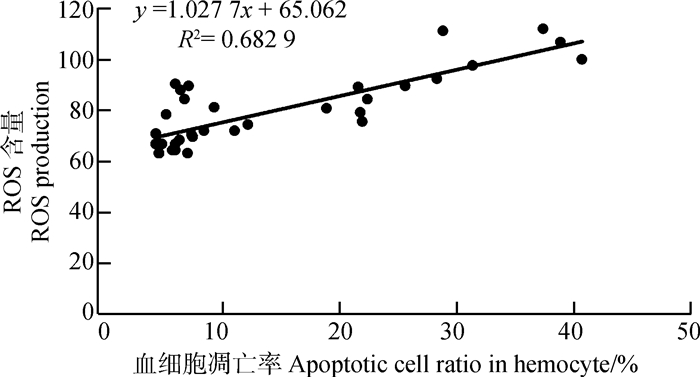
在胁迫48 h后,ROS含量与血细胞凋亡率呈显著正相关(P<0.001),Pearson相关性系数为0.83(图 5)。
|
| 图 5 ROS含量和血细胞凋亡率的相关性(n=36) Fig. 5 Correlation between ROS production and apoptotic cell ratio (n=36) |
| |
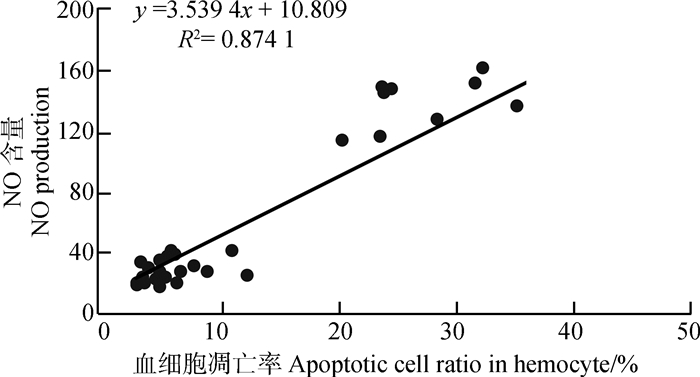
在胁迫48 h后,NO含量与血细胞凋亡率呈显著正相关(P<0.001),Pearson相关性系数为0.93(图 6)。
|
| 图 6 NO含量和血细胞凋亡率的相关性(n=36) Fig. 6 Correlation between NO production and apoptotic cell ratio (n=36) |
| |
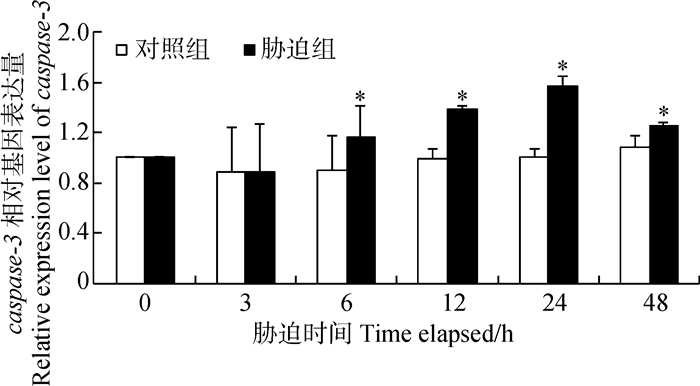
在胁迫后的3 h,Cu2+对罗氏沼虾caspase-3的相对基因表达量无影响,在胁迫后的6~48 h,caspase-3的相对基因表达量均显著增加(P<0.05),并在24 h达到最高值,由对照组的1.01增加到1.56(图 7)。
|
| 图 7 Cu2+胁迫对罗氏沼虾caspase-3相对基因表达量的影响 Fig. 7 Effect of Cu2+ on relative expression of caspase-3 gene in hemocyte of Macrobrachium rosenbergii |
| |
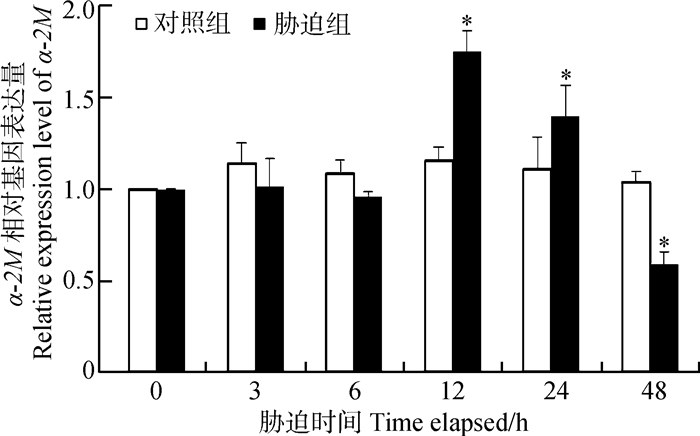
在胁迫后的0~6 h,Cu2+对罗氏沼虾α-2M基因表达量无影响,在胁迫后的12 h,α-2M基因的表达量显著升高(P<0.05) 并达到峰值,24 h时有短暂的降低,但与对照组相比仍有显著增加的趋势(P<0.05),在48 h,α-2M基因的表达量显著降低(P<0.05)(图 8)。
|
| 图 8 Cu2+胁迫对罗氏沼虾α-2M相对基因表达量的影响 Fig. 8 Effect of Cu2+ on relative expression of α-2M gene in hemocyte of Macrobrachium rosenbergii |
| |
血细胞在甲壳动物的免疫功能中起着举足轻重的作用(Havanapan et al., 2016),血细胞参数和血细胞凋亡率是评价机体免疫、生理状态和细胞过程的重要指标(Xian et al., 2010;Silva-Aciare et al., 2013),血细胞的损伤会降低免疫功能,甚至会威胁虾类的生存(Lorenzon et al., 1999;Xian et al., 2010)。据报道,受温度(Chang et al., 2009)、亚硝酸盐(Guo et al., 2013)和脂多糖(Xian et al., 2013)等非生物因素刺激时,凡纳滨对虾Litopenaeus vannamei和斑节对虾Penaeus monodon的血细胞凋亡率均显著增加。本文的研究也发现,在受到Cu2+胁迫时,罗氏沼虾的血细胞凋亡率也显著增加,说明当虾类受到各种环境因子胁迫时,可诱导血细胞发生凋亡。
ROS是一类高活性的化学物质,参与了细胞存活、生长、增殖和分化,并在先天性免疫防御机制中发挥重要作用(Yang et al., 2013),正常情况下ROS的产生与消除处于平衡状态。当机体受到外界刺激或病菌感染时,细胞会行使功能吞噬外来物,在行使吞噬功能的过程中,细胞还会产生一些有毒物质(如ROS)抑制或杀死外来物。而持续不断的刺激会使ROS含量迅速上升,打破了机体内ROS含量的平衡,过高的ROS含量对细胞自身造成伤害,甚至导致细胞凋亡(Gill & Tuteja,2010)。NO是一种广泛存在于各组织器官中的重要信使分子,能维持体内微循环内环境恒定和保护机体非特异性免疫功能(汪义军,1997)。研究表明,ROS和NO具有协同作用,共同调控应答胁迫反应的基因表达(Scheler et al., 2013)。NO和ROS都具有双重的生理效应,低浓度的NO和ROS可以抑制细胞凋亡,对机体是有益的,而高浓度的ROS和NO会对机体产生严重的伤害,诱导细胞凋亡的发生(Simon et al., 2000;Brown,2010)。本研究相关性分析结果显示,ROS、NO和血细胞凋亡率的Pearson相关性系数分别为0.83和0.93,进一步验证了ROS和NO会诱导细胞发生凋亡。
酯酶是一种广泛存在于各种细胞内的水解酶,与外源性物质的消除和降解有关,虽然并不直接参与重金属的解毒,但酯酶系统的状态反映了机体抵抗外界不良环境的能力(Zvereva et al., 2003)。因此,酯酶是毒理学领域具有重要意义的一种酶(Rashid et al., 2013),在农业生产中,被用作检测药物残留的“指示器”(Begum et al., 2008),也用于检测细胞活性。当细胞的酯酶活性下降时,被认为是细胞活性下降,会导致细胞凋亡(郭慧等,2015)。研究表明,斑节对虾在受到Cd2+刺激时,血细胞中的酯酶活性显著降低(Xian et al., 2014)。本研究也发现,在受到Cu2+胁迫时,罗氏沼虾血细胞的酯酶活性也被显著抑制。在胁迫3 h后,酯酶的活力开始显著降低,至48 h时,由对照组的117.78显著下降到88.40。酯酶活性的降低与ROS、NO和细胞凋亡率的升高大体一致。郭慧等(2015)对亚硝酸盐胁迫下凡纳滨对虾的血细胞毒性研究发现,酯酶活性在24 h才开始显著降低,这可能与胁迫因子和实验对象不同有关。
Caspase家族在介导细胞凋亡的过程中起着非常重要的作用,其中Caspase-3为关键的执行分子,它在凋亡信号传导途径中发挥主导功能,因此,细胞或组织中Caspase-3的活性是检测细胞是否发生凋亡的重要方法(Zvereva et al., 2003)。对caspase-3进行RNA干扰以后,对虾的死亡率显著降低(Rijiravanich et al., 2008),说明caspase-3在细胞凋亡中有着举足轻重的作用。本研究发现,在Cu2+胁迫的12 h、24 h和48 h,caspase-3的表达量均显著升高,24 h达到峰值后在48 h略降低,caspase-3的这种表达模式与低温胁迫下凡纳滨对虾血细胞中caspase-3的表达模式类似,即都在表达高峰后出现轻微降低,但与对照组相比仍有显著差异(Chang et al., 2009)。caspase-3表达量的显著升高在12 h出现,而ROS和NO的显著升高是在6 h,推测是ROS和NO的升高诱导了caspase-3的表达。
α-2M是一种在无脊椎动物中参与宿主防御机制的非特异性蛋白酶抑制剂(Shanthi & Vaseeharan,2014),在抑制和清除有害蛋白酶的过程中发挥重要作用(Gonias,1992)。据报道,罗氏沼虾、保罗美对虾Farfantepenaeus paulensis和印度明对虾Fenneropenaeus indicus在注射细菌、真菌和病毒后,血细胞中α-2M的表达量被显著诱导,认为α-2M与虾类的先天免疫有关(Ho et al., 2009;Perazzolo et al., 2011;Shanthi & Vaseeharan,2014)。本研究发现,在Cu2+胁迫下,α-2M的表达量发生了显著变化,推测甲壳动物的α-2M表达模式不仅可以被微生物和病毒调控,还会受到重金属胁迫的影响。α-2M的表达量在12 h和24 h时显著上升,并在24 h达到峰值,在48 h又显著下降,推测在Cu2+胁迫早期,血细胞中的α-2M被激活参与到机体的免疫反应中,在胁迫48 h时,血细胞中的NO和ROS含量以及血细胞的凋亡比例都达到最高值,此时机体的免疫功能显著降低,因此α-2M的表达量也受到显著抑制。
综上所述,在Cu2+胁迫下,机体的酯酶活性受到显著抑制,免疫功能受到影响,机体通过诱导NO和ROS的产生以及免疫相关基因α-2M的表达来对抗Cu2+胁迫带来的损伤。随着胁迫时间的延长,过高浓度的NO和ROS对机体自身造成了氧化损伤,诱导了凋亡相关基因caspase-3的表达,导致细胞凋亡的发生,说明Cu2+对虾类具有免疫抑制性和毒性。相关性分析表明,NO和ROS的升高可能是细胞凋亡的主要诱因。
| 郭慧, 冼健安, 王安利. 2015. 亚硝酸盐对凡纳滨对虾血细胞毒性及p53基因表达的影响[J]. 水生态学杂志, 36(2): 61–67. |
| 国家海洋局. 1989. 渔业水质标准[M]. 北京: 中国标准出版社. |
| 汪义军. 1997. 体内一氧化氮含量测定的几种方法[J]. 国际检验医学杂志(1): 7–9. |
| 吴维福, 陈娈娈, 李郁娇, 等. 2014. 三丁基锡对罗氏沼虾血清中免疫酶活力的影响[J]. 广东海洋大学学报, 34(3): 17–21. |
| 冼健安, 钱坤, 郭慧, 等. 2015. 杂色鲍血细胞分类、结构和免疫功能的流式细胞术分析[J]. 海洋科学, 39(12): 8–14. DOI:10.11759/hykx20150120001 |
| Begum R, Bhadra SC, Shahjahan R, et al. 2008. Esterase banding pattern in different tissues of Pangasius hypophthalmus (Sauvage, 1878)[J]. Bangladesh Journal of Zoology, 36: 287–294. |
| Bharadwaj AS, Patnaik S, Browdy CL, et al. 2014. Comparative evaluation of an inorganic and a commercial chelated copper source in Pacific white shrimp Litopenaeus vannamei (Boone) fed diets containing phytic acid[J]. Aquaculture, 422-423(3): 63–68. |
| Brown GC. 2010. Nitric oxide and neuronal death[J]. Nitric Oxide, 23(3): 153–165. DOI:10.1016/j.niox.2010.06.001 |
| Chang CC, Yeh MS, Cheng W. 2009. Cold shock-induced norepinephrine triggers apoptosis of haemocytes via caspase-3 in the whiteshrimp, Litopenaeus vannamei[J]. Fish & Shellfish Immunology, 27(6): 695–700. |
| Chen W, Wang CH. 2001. The susceptibility of the giant freshwater prawn Macrobrachium rosenbergii to Lactococcus garvieae and its resistance under copper sulfate stress[J]. Diseases of Aquatic Organisms, 47(2): 137–144. |
| Frías-Espericueta MG, Castro-Longoria R, Barrón-Gallardo GJ, et al. 2008. Histological changes and survival of Litopenaeus vannamei juveniles with different copper concentrations[J]. Aquaculture, 278(1-4): 97–100. DOI:10.1016/j.aquaculture.2008.03.008 |
| Gill SS, Tuteja N. 2010. Reactive oxygen species and antioxidant machinery in abiotic stress tolerance in crop plants[J]. Plant Physiology and Biochemistry, 48(12): 909–930. DOI:10.1016/j.plaphy.2010.08.016 |
| Gonias SL. 1992. Alpha 2-macroglobulin:a protein at the interface of fibrinolysis and cellular growth regulation[J]. Experimental Hematology, 20(3): 302–311. |
| Guo H, Miao YT, Xian JA, et al. 2015. Expression profile of antioxidant enzymes in hemocytes from freshwater prawn Macrobrachium rosenbergii exposed to an elevated level of copper[J]. Bulletin of Environmental Contamination and Toxicology, 95(4): 447–451. DOI:10.1007/s00128-015-1618-1 |
| Guo H, Xian JA, Li B, et al. 2013. Gene expression of apoptosis-related genes, stress protein and antioxidant enzymes in hemocytes of white shrimp Litopenaeus vannamei under nitrite stress[J]. Comparative Biochemistry and Physiology Part C:Toxicology & Pharmacology, 157(4): 366–371. |
| Havanapan PO, Taengchaiyaphum S, Ketterman AJ, et al. 2016. Yellow head virus infection in black tiger shrimp reveals specific interaction with granule-containing hemocytes and crustinPm1 as a responsive protein[J]. Developmental & Comparative Immunology, 54(1): 126–136. |
| Ho PY, Cheng CH, Cheng W. 2009. Identification and cloning of the α2-macroglobulin of giant freshwater prawn Macrobrachium rosenbergii and its expression in relation with the molt stage and bacteria injection[J]. Fish & Shellfish Immunology, 26(3): 459–466. |
| Liao CM, Chang CF, Yeh CH, et al. 2006. Metal stresses affect the population dynamics of disease transmission in aquaculture species[J]. Aquaculture, 257(1-4): 321–332. DOI:10.1016/j.aquaculture.2006.02.076 |
| Lorenzon S, de Guarrini S, Smith VJ, et al. 1999. Effects of LPS injection on circulating haemocytes in crustaceans in vivo[J]. Fish & Shellfish Immunology, 9(1): 31–50. |
| Mahmood K, Yang JS, Chen D, et al. 2009. Response of metallothionein gene-1 to laboratory exposure to heavy metals and thermal stress in the freshwater prawn Macrobrachium rosenbergii[J]. Journal of Hazardous Materials, 167(1-3): 523–530. DOI:10.1016/j.jhazmat.2009.01.029 |
| Martínez A, Romero Y, Castillo T, et al. 2014. The effect of copper on the color of shrimps:redder is not always healthier[J]. PLoS ONE, 9(9): e107673. DOI:10.1371/journal.pone.0107673 |
| Perazzolo LM, Bachère E, Rosa RD, et al. 2011. Alpha2-macroglobulin from an Atlantic shrimp:biochemical characterization, sub-cellular localization and gene expression upon fungal challenge[J]. Fish & Shellfish Immunology, 31(6): 938–943. |
| Rao MS, Anjaneyulu N. 2008. Effect of copper sulfate on molt and reproduction in shrimp Litopenaeus vannamei[J]. International Journal of Biological Chemistry, 2(1): 35–41. DOI:10.3923/ijbc.2008.35.41 |
| Rashid MA, Begum RA, Shahzahan RM. 2013. Tissue distribution of esterase isozymes and their responses to cypermethrin in three macrobrachium species[J]. Journal of the Asiatic Society of Bangladesh, Science, 38(2): 227–235. |
| Rijiravanich A, Browdy CL, Withyachumnarnkul B. 2008. Knocking down caspase-3 by RNAi reduces mortality in Pacific white shrimp penaeus Litopenaeus vannamei challenged with a low dose of white-spot syndrome virus[J]. Fish & Shellfish Immunology, 24(3): 308–313. |
| Santos MHS, Cunha NTD, Bianchini A. 2000. Effects of copper and zinc on growth, feeding and oxygen consumption of Farfantepenaeus paulensis postlarvae (Decapoda:Penaeidae)[J]. Journal of Experimental Marine Biology and Ecology, 247(2): 233–242. DOI:10.1016/S0022-0981(00)00152-0 |
| Scheler C, Durner J, Astier J. 2013. Nitric oxide and reactive oxygen species in plant biotic interactions[J]. Current Opinion in Plant Biology, 16(4): 534–539. DOI:10.1016/j.pbi.2013.06.020 |
| Shanthi S, Vaseeharan B. 2014. Alpha 2 macroglobulin gene and their expression in response to GFP tagged Vibrio parahaemolyticus and WSSV pathogens in Indian white shrimp Fenneropenaeus indicus[J]. Aquaculture, 418-419(1): 48–54. |
| Silva-Aciares F, Moraga D, Riquelme C. 2013. Effect of copper on the immunomodulatory activities of haemocytes in juveniles of the abalone Haliotis rufescens cultivated under hatchery conditions[J]. Aquaculture, 410-411: 72–78. DOI:10.1016/j.aquaculture.2013.06.025 |
| Simon HU, Haj-Yehia A, Levi-Schaffer F. 2000. Role of reactive oxygen species (ROS) in apoptosis induction[J]. Apoptosis, 5(5): 415–418. DOI:10.1023/A:1009616228304 |
| Valavanidis A, Vlachogianni T. 2012. Metal pollution in ecosystems. Ecotoxicology studies and risk assessment in the marine environment[J]. Science Advances on Environment, Toxi-Cology & Ecotoxicology Issues. |
| Wang SL, Xu XR, Sun YX, et al. 2013. Heavy metal pollution in coastal areas of south China:a review[J]. Marine Pollution Bulletin, 76(1-2): 7–15. DOI:10.1016/j.marpolbul.2013.08.025 |
| Wang ZH, Feng J, Nie XP. 2015. Recent environmental changes reflected by metals and biogenic elements in sediments from the Guishan Island, the Pearl River Estuary, China[J]. Estuarine Coastal & Shelf Science, 164(1-April): 493–505. |
| Xian JA, Li B, Guo H, et al. 2014. Haemocyte apoptosis of the tiger shrimp Penaeus monodon exposed to cadmium[J]. Bulletin of Environmental Contamination and Toxicology, 92(5): 525–528. DOI:10.1007/s00128-013-1165-6 |
| Xian JA, Miao YT, Li B, et al. 2013. Apoptosis of tiger shrimp (Penaeus monodon) haemocytes induced by Escherichia coli lipopolysaccharide[J]. Comparative Biochemistry and Physiology Part A:Molecular & Integrative Physiology, 164(2): 301–306. |
| Xian JA, Wang AL, Ye CX, et al. 2010. Phagocytic activity, respiratory burst, cytoplasmic free-Ca2+ concentration and apoptotic cell ratio of haemocytes from the black tiger shrimp, Penaeus monodon under acute copper stress[J]. Comparative Biochemistry and Physiology Part C:Toxicology & Pharmacology, 152(2): 182–188. |
| Yang Y, Bazhin AV, Werner J, et al. 2013. Reactive oxygen species in the immune system[J]. International Reviews of Immunology, 32(3): 249–270. DOI:10.3109/08830185.2012.755176 |
| Yeh ST, Liu CH, Chen JC. 2004. Effect of copper sulfate on the immune response and susceptibility to Vibrio alginolyticus in the white shrimp Litopenaeus vannamei[J]. Fish & Shellfish Immunology, 17(5): 437–446. |
| Zvereva E, Serebrov V, Glupov V, et al. 2003. Activity and heavy metal resistance of non-specific esterases in leaf beetle Chrysomela lapponica from polluted and unpolluted habitats[J]. Comparative Biochemistry and Physiology Part C:Toxicology & Pharmacology, 135(4): 383–391. |
 2017, Vol. 36
2017, Vol. 36




