2. 重庆市农业科学院 特色作物研究所,重庆 402160;
3. 重庆市北碚区农业委员会,重庆 400700
2. Institute of Characteristic Crops Research, Chongqing Academy of Agricultural Sciences, Chongqing 402160, China;
3. Agriculture Committee of Beibei District, Chongqing 400700, China
由辣椒疫霉Phytophthora capsici引起的辣椒疫病是一种毁灭性的土传卵菌病害,在世界各辣椒种植区均有发生[1-2]。由于该病的初侵染源主要是卵孢子,其抗逆性强,可在染病植物残体、土壤或种子中越冬,生存力及致病力强,且寄主广泛,因而对农业生产危害严重[3-4]。目前对该病害主要以化学防治为主。近年来,随着卵菌杀菌剂的大量使用,病原卵菌的抗药性问题日益突出。甲霜灵 (metalaxyl) 等苯酰胺类杀菌剂曾是辣椒疫霉等卵菌病害防治中活性最高、使用量最大的药剂,但因其作用位点单一、用量大,已成为高抗性风险杀菌剂[5-6]。烯酰吗啉 (dimethomorph)、双炔酰菌胺 (mandipropamid) 等羧酸酰胺类杀菌剂具有抑菌活性高及内吸传导性强等特点,已逐渐代替苯酰胺类杀菌剂用于防治辣椒疫病等卵菌病害[7]。此外,嘧菌酯 (azoxystrobin) 等甲氧基丙烯酸酯类杀菌剂也逐渐受到重视。但由于这两类杀菌剂的作用位点单一,目前均已出现防治效果下降现象[7-8]。氟吡菌胺 (fluopicolide) 是德国拜耳公司研制的一种新型结构的苯甲酰胺类及吡啶类杀菌剂[9],对卵菌的菌丝生长、孢子囊形成和孢子萌发等阶段均有很好的抑制作用[10-12],其作用机制与目前生产中广泛使用的甲霜灵、霜脲氰、烯酰吗啉等苯基酰胺类和羧酸酰胺类杀菌剂不同。随着中国境内卵菌病害对现有杀菌剂抗性的出现,对氟吡菌胺的引入及应用将成为必要。
Lu等[11]测定了采自美国密歇根洲的126株辣椒疫霉菌株对氟吡菌胺的敏感性,其EC50平均值在0.08~0.24 μg/mL之间,抗性分析表明,辣椒疫霉对氟吡菌胺存在中等抗性风险;Keinath等[13]通过测定药剂对菌丝生长、游动孢子萌发、孢子囊产生和游动孢子产生的影响,建立了美国东南部和中西部的69株辣椒疫霉对氟吡菌胺的敏感基线,且发现氟吡菌胺对采自密歇根洲菌株的EC50值较采自美国中东部地区菌株的高,需及时进行抗性风险监测;闫磊[14]测定了采自中国河北和山东两省的105株黄瓜霜霉病菌Pseudoperonospora cubensis对氟吡菌胺的敏感性,结果均为敏感菌株,抗性风险评估为中等抗性;罗彦涛等[15] 通过对马铃薯晚疫病菌Phytophthora infestans进行的对氟吡菌胺抗性诱导及抗性突变体生物学特性的研究,发现马铃薯晚疫病菌对氟吡菌胺具有高抗性风险。由于黄瓜霜霉病菌、马铃薯晚疫病菌和辣椒疫霉都有不同交配型[3,14-15],有性生殖为其提供了重要的遗传变异来源。
目前关于卵菌类病害对氟吡菌胺的抗性机制及其靶标蛋白仍不清楚[11],且由于不同地区卵菌病原菌自身遗传特性、当地生长环境和用药方式等存在差异,因此,研究各地区辣椒疫霉对氟吡菌胺的抗性风险具有重要意义。重庆地区属于辣椒疫病高发区,为评估该地区辣椒疫霉对氟吡菌胺的抗性风险,本研究采用菌丝生长速率法,测定了采自重庆不同地区的110株辣椒疫霉对氟吡菌胺的敏感性,尝试建立其敏感基线,并在实验室条件下通过药剂驯化及紫外诱导方法诱变得到抗性突变体,测定并分析了不同抗性突变体及亲本菌株的主要生物学性状,以及抗性突变体对甲霜灵、霜脲氰、烯酰吗啉、丁吡吗啉及嘧菌酯之间的交互抗性关系,旨在为氟吡菌胺在生产中的科学使用提供理论依据。
1 材料和方法 1.1 供试材料 1.1.1 菌株2014—2015年,于重庆市璧山区、合川区及九龙坡区等未施用过氟吡菌胺的地区采集感染疫病的辣椒植株,经单孢分离共获得110株菌株,通过形态学观察及致病性试验等[16-17]鉴定为辣椒疫霉Phytophthora capsici。将所有菌株转接到燕麦培养基斜面上,15 ℃保存,备用。
1.1.2 药剂及试剂95%氟吡菌胺 (fluopicolide)、97%甲霜灵 (metalaxyl)、98%霜脲氰 (cymoxanil)、97.5%烯酰吗啉 (dimethomorph) 及94.3%丁吡吗啉 (pyrimorph) 原药,天津市汉邦植物保护剂有限责任公司;96%嘧菌酯 (azoxystrobin) 原药,邯郸市瑞来宝进出口贸易有限公司。IF-0a GN/GP接种液,广州市华粤行仪器有限公司;其余试剂均为分析纯。
1.1.3 培养基马铃薯葡萄糖琼脂培养基 (PDA):马铃薯200 g、琼脂17 g、葡萄糖20 g,用蒸馏水定容至1 L,121 ℃灭菌30 min。
胡萝卜琼脂培养基 (CA):胡萝卜200 g、琼脂17 g,用蒸馏水定容至1 L,121 ℃灭菌30 min。
1.1.4 辣椒种子供试辣椒品种为“北京一号椒王”,于市场购得。
1.2 试验方法 1.2.1 辣椒疫霉对氟吡菌胺的敏感性测定采用菌丝生长速率法[18]。将供试菌株接种至PDA平板上,25 ℃预培养5 d后,沿边缘打取直径6 mm的菌饼,接种到含系列质量浓度 (0.1、0.2、0.4、0.6、0.8及1.0 μg/mL) 氟吡菌胺的PDA平板上,以无药平板为对照,每处理3次重复。25 ℃培养6 d后用十字交叉法测量菌落直径,根据公式 (1) 计算菌丝生长抑制率,进而求出药剂对各供试菌株的毒力回归方程和EC50值。
| $I/{\text{%}} =\frac{{{D_{\rm{0}}}{\rm{ - }}{D_{\rm{t}}}}}{{{D_{\rm{0}}}}}{\rm{ \times 100}}$ | (1) |
式中,I为菌丝生长抑制率 (%);D0为对照菌落增长直径 (mm);Dt为处理菌落增长直径 (mm)。
1.2.2 抗氟吡菌胺突变体的获得 1.2.2.1 药剂选择驯化法参考赵卫松等[19]和翟明涛等[12]的方法并加以改进。选择相对较为敏感的10株菌株,于PDA平板上预培养5 d后,打取直径6 mm的菌饼,依次转接到含氟吡菌胺的PDA平板上,药剂浓度控制在抑制菌丝生长60%左右。25 ℃下培养8 d后开始检查快速生长角变区,每天检查1次,当出现快速生长角变区时,取角变区边缘菌丝转接于含相同浓度氟吡菌胺的PDA平板上继续培养3代,比较所获菌株对氟吡菌胺的抗性变化。逐渐增大药剂浓度,以相同方法进行筛选,直至其能在含有大于或等于最低抑制浓度 (MIC) 氟吡菌胺的PDA平板上较好地生长。每菌株重复10皿,每皿接5个菌饼。计算抗性突变频率及抗性倍数。
1.2.2.2 紫外诱导孢子囊法参照Lu等[11]和Bruin等[20]的方法并加以改进。选取相对较为敏感的10株菌株,在CA平板上于25 ℃、12 h/12 h光暗交替培养10 d,待产生大量孢子囊后,用无菌水将孢子囊洗下,双层纱布过滤,配制成每毫升含5 × 106个孢子囊的悬浮液。取上述孢子囊悬浮液5 mL,黑暗及振荡条件下在紫外灯 (25W,波长254 nm,预热 30 min) 下方25 cm垂直距离处照射亚致死时间 (180 s) 后,立即置于黑暗条件下30 min,以降低光修复。取100 μL照射后的孢子囊悬浮液涂布于氟吡菌胺质量浓度为10 μg/mL (接近10倍MIC浓度) 的CA平板上,25 ℃下黑暗培养7 d,可正常生长的菌落即为疑似抗性突变体。每菌株30个重复。计算抗性突变频率。采用菌丝生长速率法测定抗性突变体的EC50值,计算其抗性倍数。
1.2.2.3 紫外诱导菌丝体法参照Bruin等[20]和翟明涛等[12]的方法并加以改进。选取相对较为敏感的10株菌株,在PDA平板上于25 ℃预培养5 d后,同1.2.2.2节方法进行紫外照射诱变。随后打取直径6 mm的菌饼转接至含15和20 μg/mL (该浓度下敏感菌株不能生长) 氟吡菌胺的PDA平板上,每皿接5个菌饼,每浓度5次重复,于25 ℃黑暗培养14 d,可正常生长的即为疑似抗性突变体。将其转接到无药PDA培养基上活化培养3代后,再转接到含15和20 μg/mL氟吡菌胺的PDA培养基上,获得稳定的抗性菌株,计算其抗性突变频率及抗性倍数。
1.2.3 抗氟吡菌胺突变体的主要生物学性状研究 1.2.3.1 抗性遗传稳定性测定将各抗性突变体及其亲本菌株在不含药的 PDA 平板上继代培养11代后,采用菌丝生长速率法分别测定第1代和第11代菌株对氟吡菌胺的敏感性,根据抗性倍数的变化情况确定病原菌抗药性的遗传稳定性。
1.2.3.2 菌丝生长速率测定将抗性突变体及其亲本菌株在空白PDA平板上、25 ℃黑暗培养5 d后,在靠近菌落边缘处打取直径为6 mm的菌饼,接种到空白PDA平板上,每处理3次重复。每隔24 h测定1次菌落直径。绘制各菌株菌丝生长曲线,比较144 h内抗性突变体与其亲本菌株的菌丝生长速率。
1.2.3.3 适宜生长温度测定将抗性突变体及其亲本菌株于空白PDA平板上、25 ℃黑暗培养5 d后,取直径6 mm的菌饼接种到空白PDA平板中央,分别置于10、15、20、25、30和35 ℃下恒温培养6 d,十字交叉法测量菌落直径。每处理3次重复。根据菌丝的生长情况和菌落大小确定菌株生长的适宜温度。
1.2.3.4 产孢子囊能力和致病力测定CA平板上的离体产孢子囊能力:参照兰成忠等[21]的方法并加以改进。将抗性突变体及其亲本菌株于空白CA平板上、28 ℃持续光照培养,待所有菌株菌丝长满整个平板后,用玻棒涂抹菌丝表面,于28 ℃继续光照培养24 h。沿边缘打取10个直径6 mm的菌饼,置于50 mL离心管中,加入10 mL无菌水,振荡3 min,双层纱布过滤,用血球计数板计数各菌株孢子囊个数,计算单位面积平板上的产孢量。
离体叶片上的致病力和产孢子囊能力:选取同一叶位、相同叶龄的辣椒叶片,置于含有1%琼脂的培养皿中,背面朝上,分别接入直径6 mm的抗性突变体及其亲本菌株菌饼,以空白PDA培养基为对照。每处理10片叶,置于25 ℃、相对湿度80%、光照强度为20 000 lx的培养箱中,于12 h/12 h光暗交替培养3 d后测量病斑面积。每处理取3个叶片放入50 mL离心管中,加入15 mL蒸馏水,振荡3 min后收集孢子囊。用血球计数板计数各菌株孢子囊悬浮液的浓度,计算叶片单位面积病斑上的产孢量。
1.2.3.5 对渗透压的敏感性测定分别采用葡萄糖浓度法和氯化钠浓度法测定不同菌株对渗透压的敏感性[22]。将抗性突变体及其亲本菌株接种至空白PDA平板上活化培养5 d后,取直径为6 mm的菌饼,分别接种于含0、5、10、20、40、80、100及150 g/L葡萄糖和含0、3.75、7.5、15、30、60及80 g/L氯化钠的PDA平板上,每处理3次重复。25 ℃下黑暗培养 5 d后,测量各处理菌落直径,分析各菌株对渗透压的敏感性。
1.2.3.6 Biolog微孔板碳源利用能力测定参照Khalil等[23]的方法并加以改进。将抗性突变体及其亲本菌株接种至空白CA平板上,26 ℃黑暗培养10 d后将菌丝刮下,加入IF-0a GN/GP接种液进行研磨。用IF-0a GN/GP接种液调整菌丝悬浮液浓度,使其透光度为62% T (T为Biolog的标准浓度单位)。迅速将配制好的菌悬液倒入V型槽中,用移液器取菌悬液接种至PM1板各孔中,每孔100 μL。将接种后的PM1板置于26 ℃ 的OmniLog恒温培养箱中培养,7 d后根据各菌株的代谢动力学曲线,分析抗性突变体及其亲本菌株对碳源的代谢利用情况。
1.2.3.7 交互抗性测定采用菌丝生长速率法,分别测定抗性突变体及其亲本菌株对5种防治卵菌病害的常用杀菌剂甲霜灵、霜脲氰、烯酰吗啉、丁吡吗啉及嘧菌酯的敏感性,分析其对上述5种杀菌剂与氟吡菌胺之间是否存在交互抗性关系。
1.2.4 数据处理采用PASW Statistics 18 版软件的Duncan氏新复极差法,对试验数据进行差异显著性分析。采用Biolog D5E_OKA_data.exe软件和Biolog OL_FM_1.2.exe软件对各菌株的碳源代谢表型数据进行收集和转换,以峰面积为比较参数,峰面积越大,说明菌株对碳源物质的代谢利用能力越强。对各药剂的EC50值进行Pearson相关性分析,当P<0.05时,表明抗氟吡菌胺突变体对氟吡菌胺与其他药剂之间存在交互抗性关系。
2 结果与分析 2.1 重庆地区辣椒疫霉对氟吡菌胺敏感基线的建立测定结果表明:采自重庆璧山、合川及九龙坡等地区的110株辣椒疫霉菌株对氟吡菌胺的EC50值范围介于0.10~0.57 μg/mL之间,平均值为 (0.32 ± 0.11) μg/mL。且所有菌株对氟吡菌胺的敏感性频率呈连续性单峰曲线分布 (图1),未出现敏感性明显下降的病原菌亚群体,总体接近正态分布,因此该EC50平均值 (0.32 ± 0.11) μg/mL可作为重庆地区辣椒疫霉对氟吡菌胺田间抗性监测的敏感基线。
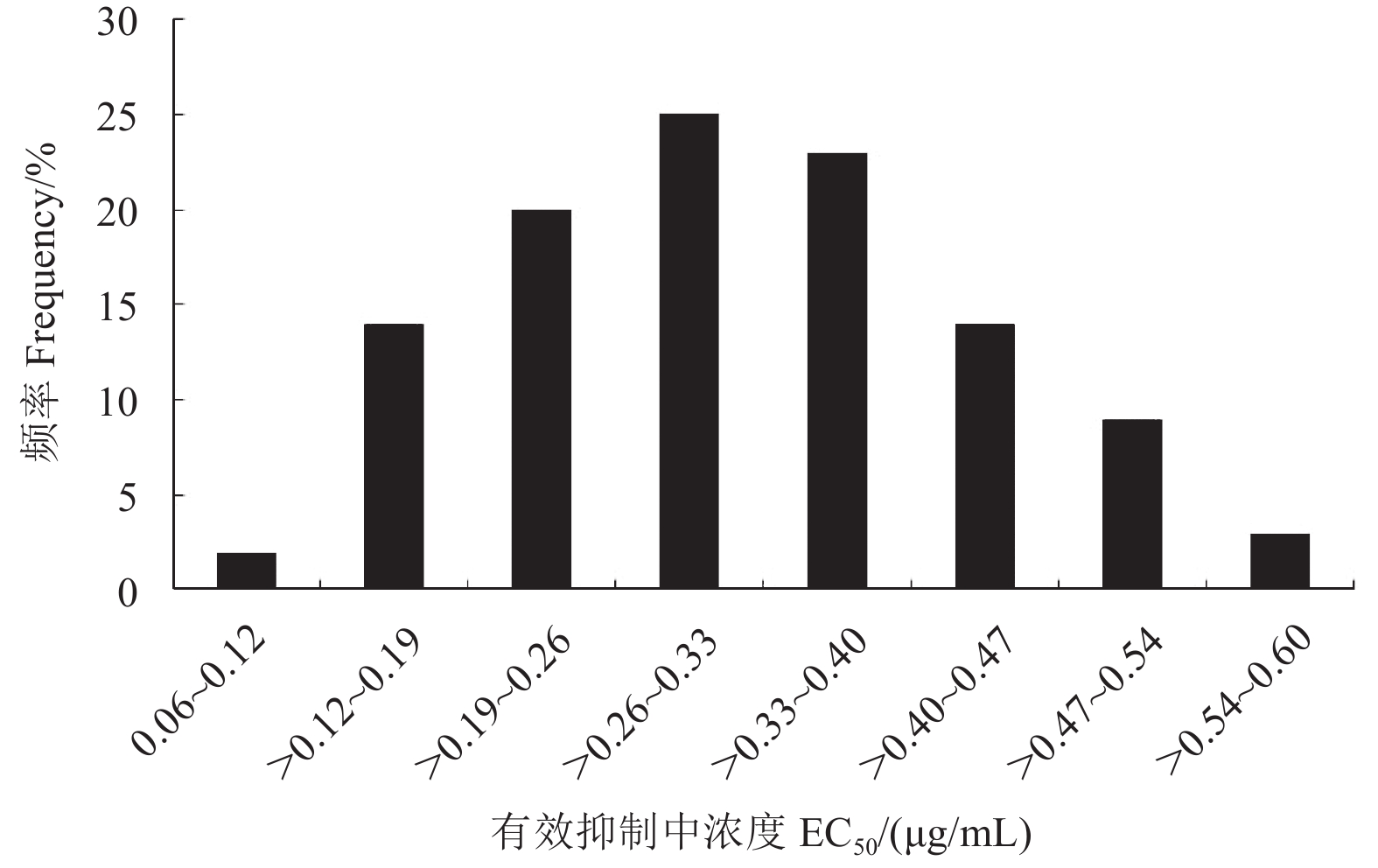
|
图 1 供试110株辣椒疫霉对氟吡菌胺的敏感性频率分布 Fig. 1 Frequency distribution of the sensitivities of 110 isolates of P. capsici to fluopicolide |
2.2 辣椒疫霉抗氟吡菌胺突变体的获得
通过紫外诱导菌丝体共获得3株抗氟吡菌胺的突变体 (分别命名为BS11-5-1、JLP11-4-2和JLP11-4-3),突变频率为0.86%,而药剂驯化和紫外诱导孢子囊均未获得抗性突变体。3株抗性突变体的抗性倍数分别为69.5、98.5和94.2 (表1),表明亲本菌株经紫外线诱导后产生了不同程度的抗药性突变。
|
|
表 1 辣椒疫霉抗性突变体对氟吡菌胺的抗性水平 Table 1 Resistance level of the resistant mutants of P. capsici to fluopicolide |
2.3 辣椒疫霉抗氟吡菌胺突变体的主要生物学性状 2.3.1 抗性遗传稳定性
各抗性突变体及其亲本菌株在无药培养基上转接11代后,菌株对氟吡菌胺的抗性均出现下降情况,但变化不明显,且突变体的抗性倍数均大于50 (表2),说明3个抗性突变体BS11-5-1、JLP11-4-2和JLP11-4-3具有较稳定的抗性遗传性。
|
|
表 2 辣椒疫霉抗氟吡菌胺突变体的抗性遗传稳定性 Table 2 Resistance stability of fluopicolide-resistant mutants of P. capsici |
2.3.2 菌丝生长速率
由图2可知:抗性突变体BS11-5-1的菌丝生长速率与亲本菌株无显著性差异;而JLP11-4-2和JLP11-4-3的菌丝生长速率则显著低于其亲本菌株,尤其是高抗性突变体JLP11-4-2,随着时间的推移其生长能力降低更为明显 (P = 0.05)。
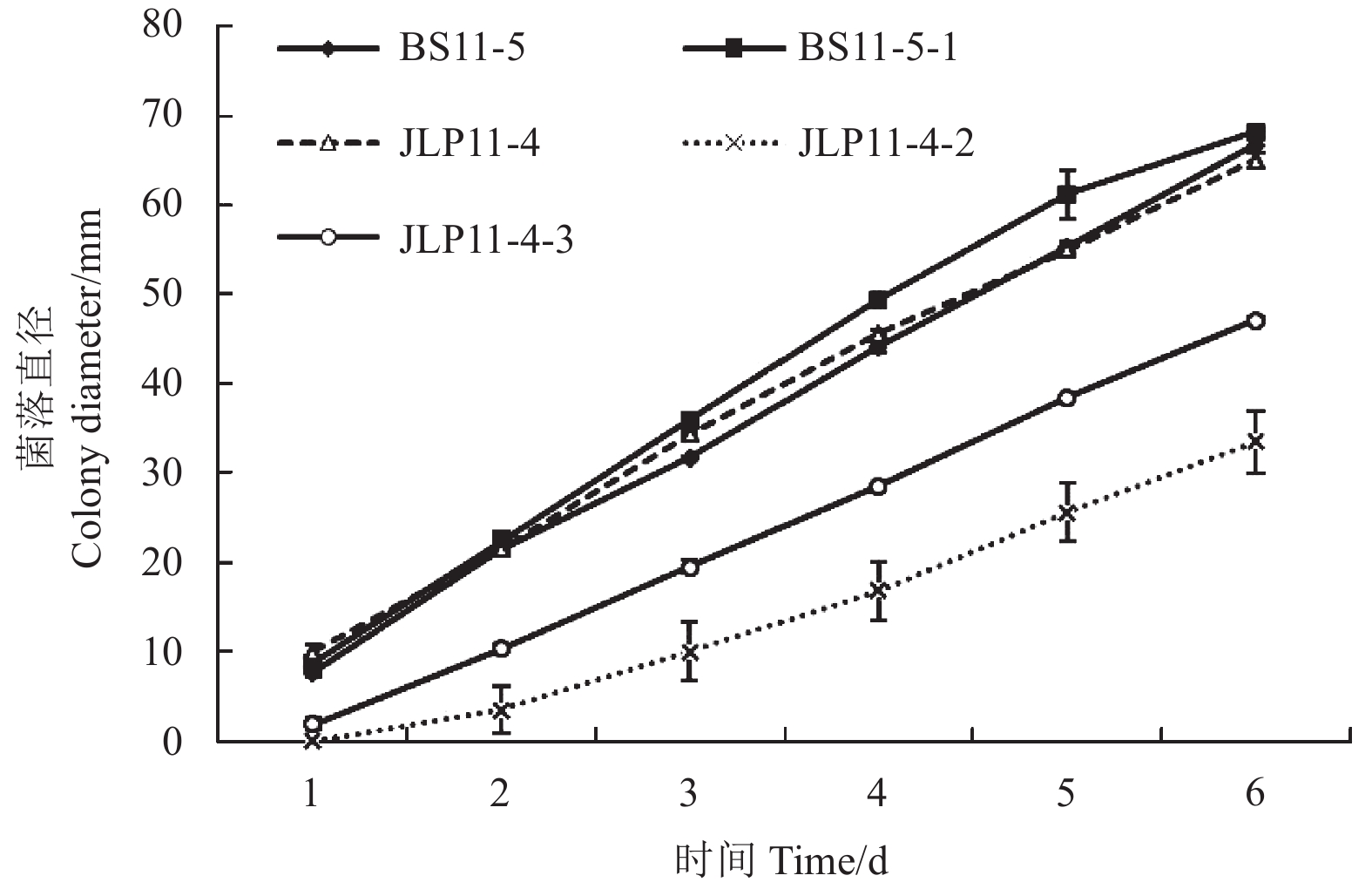
|
图 2 辣椒疫霉抗氟吡菌胺突变体的菌丝生长情况 Fig. 2 Mycelial growth of fluopicolide-resistant mutants of P. capsici |
2.3.3 最适培养温度
结果 (表3) 表明:各抗性突变体及其亲本菌株均能在10~30 ℃条件下生长,最适宜的生长温度范围为25~30 ℃。同一温度下,抗性突变体BS11-5-1与其亲本菌株之间菌落直径无显著差异;而JLP11-4-2和JLP11-4-3在10~35 ℃条件下的菌落直径均显著小于其亲本菌株,且在35 ℃时2个突变体的菌落扩展直径均为0 mm,生长完全受到抑制。由此推断,辣椒疫霉在对氟吡菌胺产生抗性后,抗性菌株对温度的适应能力与抗性产生和菌株之间的特异性差异有关。
|
|
表 3 不同培养温度对辣椒疫霉抗氟吡菌胺突变体及其亲本菌株菌丝生长的影响 Table 3 Effects of different temperatures on the mycelial growth of fluopicolide-resistant mutants of P. capsici and their respective parents |
2.3.4 产孢子囊能力和致病力
离体平板产孢子囊能力测定结果 (表4) 表明:抗性突变体BS11-5-1和JLP11-4-2在CA培养基上的产孢子囊能力与其亲本菌株相当 ,而JLP11-4-3的产孢子囊能力显著低于亲本菌株。表明大多数抗性突变体在CA平板上仍具有与亲本菌株相同的产孢子囊能力。
|
|
表 4 辣椒疫霉抗氟吡菌胺突变体及其亲本菌株的产孢子囊能力和致病性 Table 4 Sporulation and pathogenicity of fluopicolide-resistant mutants and their respective parents of P. capsici |
离体叶片上的产孢子囊能力和致病力测定结果 (表4) 表明:将抗性突变体BS11-5-1接种至离体叶片后所形成的病斑面积和产孢子囊能力与亲本菌株BS11-5之间没有显著性差异,而抗性突变体JLP11-4-2和JLP11-4-3所引致的病斑面积及其产孢子囊能力则显著低于亲本菌株JLP11-4。表明抗性突变体在离体叶片上仍具有较强的致病力和产孢子囊能力,只是不同突变体与亲本菌株之间存在一定的差异。
2.3.5 对渗透压的敏感性结果 (图3A) 表明:在葡萄糖质量浓度为5~10 g/L时,对所有菌株的菌丝生长均表现为促进作用;20~40 g/L时,除对抗性突变体JLP11-4-2和JLP11-4-3的菌丝生长表现为促进作用外,对其余菌株均表现为抑制作用,且随着葡萄糖浓度增加,抑制率逐渐增大。当葡萄糖质量浓度在5~150 g/L之间时,对抗性突变体 BS11-5-1菌丝生长的影响与其亲本菌株之间不存在显著性差异。当葡萄糖质量浓度为150 g/L时,对抗性突变体JLP11-4-3菌丝生长的抑制率与其亲本菌株相当,其余浓度下则均显著低于亲本菌株,而在供试质量浓度范围内,葡萄糖对抗性突变体JLP11-4-2菌丝生长的抑制率均小于其亲本菌株,表明抗性突变体较亲本菌株对渗透压的敏感性有所降低。
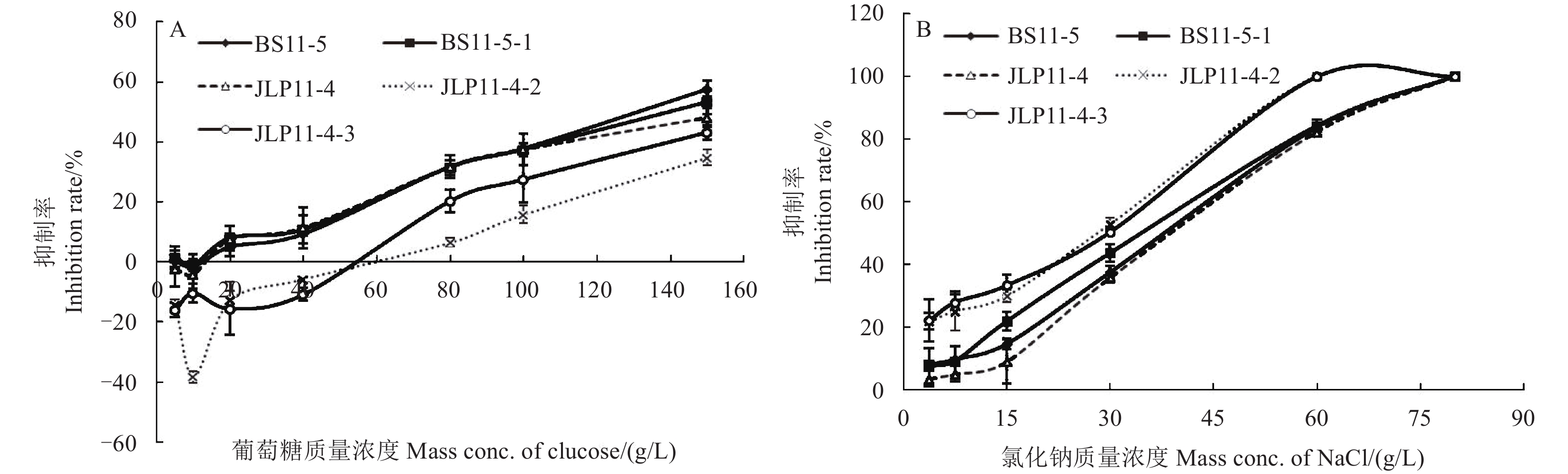
|
图 3 不同浓度葡萄糖(A)及氯化钠(B)对辣椒疫霉抗氟吡菌胺突变体及其亲本菌株菌丝生长的抑制作用 Fig. 3 Inhibition effect of different glucose (A) and NaCl (B) concentrations on the mycelial growth of the parental and fluopicolide-resistant mutants of P. capcisi |
在氯化钠质量浓度为3.75~80 g/L时,抗性突变体及其亲本菌均表现为对渗透压敏感 (图3B)。除15~30 g/L时,氯化钠对抗性突变体BS11-5-1菌丝生长的抑制率显著大于其亲本菌株外,其他质量浓度下二者均不存在显著差异。而抗性突变体JLP11-4-2和JLP11-4-3在氯化钠质量浓度为3.75~80 g/L时菌丝生长能力均显著弱于亲本菌株,表明抗性突变体较亲本菌株对渗透压更为敏感。
2.3.6 对碳源物质的利用情况通过菌株间碳源利用产生的颜色变化叠加分析,发现抗性突变体及其亲本菌株均能利用包括糖类、核苷酸类和羧酸类等在内的95种碳源物质,从而产生颜色反应 (图4)。其中,抗性突变体BS11-5-1对2’-脱氧腺苷 (E11) 的利用较其亲本菌株高,对D-丝氨酸 (B01) 的利用能力则低于亲本菌株,而抗性突变体JLP11-4-2和JLP11-4-3对95种碳源的利用能力与其亲本菌株均相当。说明抗性突变体对PM1中95种碳源的利用情况总体与亲本菌株相近,突变的发生只改变了抗性突变体对个别碳源物质的利用效率。
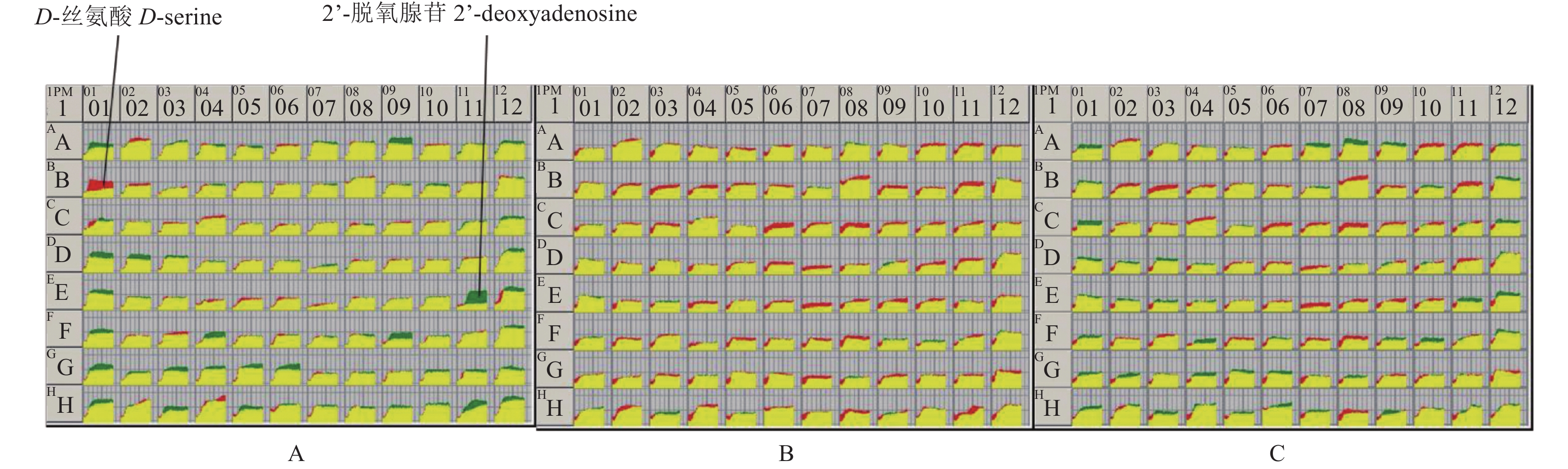
|
A:BS11-5,BS11-5-1;B:JLP11-4,JLP11-4-2;C:JLP11-4,JLP11-4-3。注:图中采用PM1动力学曲线峰面积分别比较了抗性突变体 (BS11-5-1、JLP11-4-2和JLP11-4-3,绿色部分) 以及亲本菌株 (BS11-5和JLP11-4,红色部分) 对碳源的利用能力。黄色部分则是由抗性突变体 (绿色) 和亲本菌株 (红色) 变化曲线叠加而得。 Note: The carbon utilization ability of resistant mutants and parent strains is compared by the peak area of PM1 dynamic curve.The green part of figure is utilization of PM1 carbon sources of resistant mutants BS11-5-1,JLP11-4-2 and JLP11-4-3. The red part indicates parental strains. And the yellow part is the overlay color of the resistant mutants and their respective parents. 图 4 抗性突变体及其亲本菌株对PM1碳源板的代谢利用情况比较 Fig. 4 Metabolic utilization comparison of PM1 carbon sources between resistant mutants and their respective parents |
2.3.7 对氟吡菌胺与其他杀菌剂的交互抗性
比较各药剂的EC50值可知,辣椒疫霉抗氟吡菌胺突变体及其亲本菌株对5种杀菌剂的敏感性由强到弱依次为烯酰吗啉>甲霜灵>丁吡吗啉>嘧菌酯>霜脲氰 (表5)。Pearson相关性分析结果显示,氟吡菌胺EC50值与5种杀菌剂EC50值之间的相关系数 (r) 分别为0.593、–0.863、0.272、0.189和0.569,P>0.05 (表6),表明辣椒疫霉对氟吡菌胺与甲霜灵、霜脲氰、烯酰吗啉、丁吡吗啉及嘧菌酯之间不存在交互抗性关系。
|
|
表 5 辣椒疫霉抗氟吡菌胺突变体及其亲本菌株对不同杀菌剂的敏感性 Table 5 Sensitivities of the parental and fluopicolide-resistant mutants of P. capsici to different fungicides |
|
|
表 6 辣椒疫霉对氟吡菌胺及其他5种杀菌剂的交互抗性 Table 6 Cross-resistance of P. capsici to fluopicolide and the other five fungicides |
3 结论与讨论
植物病原菌对杀菌剂的基本抗性风险是由药剂和病原菌二者共同决定的,可通过抗性菌株的遗传稳定性、对环境的适应能力及交互抗性等指标来评估抗性菌株形成田间优势菌群以及抗药性发生的可能性。本研究测定了重庆地区110株辣椒疫霉对氟吡菌胺的敏感性,得其EC50平均值为 (0.32 ± 0.11) μg/mL,且抗性菌株频率分布呈单峰正态曲线,符合野生敏感型病原菌对药剂敏感性呈正态分布的原则,表明重庆地区辣椒疫霉对氟吡菌胺仍处于野生敏感群体阶段,因此可将该EC50平均值 (0.32 ± 0.11) μg/mL作为重庆地区田间监测辣椒疫霉对氟吡菌胺抗性的敏感基线。
目前通常采用药剂驯化、紫外诱导菌丝或游动孢子的方法获得抗性菌株。赵卫松等[24]通过对辣椒疫霉敏感菌株DX2-3进行双炔酰菌胺驯化和紫外诱导+菌落角变获得抗性菌株,结果表明,经药剂驯化7代后抗性水平达1 959.9倍,紫外诱导菌株的抗性水平超过5万倍,且均能稳定遗传;崔晓岚等[25] 通过紫外诱导辣椒疫霉菌丝和游动孢子获得了适合度较好的辣椒疫霉高抗双炔酰菌胺的突变体,抗性倍数最大值达到680;Bruin等[20]采用紫外诱导辣椒疫霉菌丝和游动孢子的方法获得了大量的抗甲霜灵突变体;Bi等[26]通过药剂驯化和紫外诱导菌丝及孢子等方法获得了抗性倍数达24.5~147.8的辣椒疫霉抗苯酰菌胺 (zoxamide) 菌株,且大多数抗性菌株的抗药性不能稳定遗传。本研究选取2014年采集的相对较为敏感的辣椒疫霉菌株进行室内药剂选择驯化和紫外诱导试验,结果表明:药剂驯化和紫外诱导孢子囊悬浮液均未获得抗性突变体,仅在紫外诱导菌丝角变试验中获得了3株抗性突变体,抗性水平介于69.5~98.5倍之间,突变频率为0.86%,虽然目前抗性水平尚不高,但3株抗性突变体经11代转接培养后其抗药性均能够稳定遗传。因此,田间一旦产生辣椒疫霉对氟吡菌胺的抗性突变体,在药剂持续选择压力存在条件下,抗性菌株仍很可能上升为优势种群,给病害的防治带来困难。交互抗性研究表明,辣椒疫霉对氟吡菌胺与甲霜灵、霜脲氰、烯酰吗啉、丁吡吗啉和嘧菌酯之间均不存在交互抗性。因此,在氟吡菌胺投入生产实践时可与上述杀菌剂轮换或混合使用,以延长药剂的使用寿命。
大多情况下,由杀菌剂所导致的突变会影响病原菌的适合度,使其在自然环境中的侵染力和竞争力发生变化[27]。抗性突变体的适合度是评估杀菌剂抗性风险的重要因素,涉及病原菌的各生长阶段。本研究结果表明:抗性突变体BS11-5-1在菌丝生长能力、对温度的适应性、产孢子囊能力及致病力方面均与亲本菌株相当,而抗性突变体JLP11-4-2和JLP11-4-3的主要生物学特性虽弱于其亲本菌株,但仍具有一定的环境适合度。Lu等[11]和翟明涛等[12]的研究结果表明,辣椒疫霉对氟吡菌胺的抗性菌株在产孢量和致病力方面与其亲本菌株相似。本研究结果与上述结果部分一致,但也存在差别,推测可能是由于采用了不同的驯化或诱导方法以及不同地区菌株遗传背景的差异所致。
对渗透压的敏感性下降可能是辣椒疫霉对氟吡菌胺产生抗性的生理机制之一。本研究中抗性突变体BS11-5-1对渗透压的调节能力与其亲本菌株相当,而较高水平抗性突变体JLP11-4-2和JLP11-4-3对葡萄糖的敏感性低于其亲本菌株,对氯化钠的敏感性高于其亲本菌株。Ellis等[28]认为,菌体在高渗透压环境中需要不断合成甘油来维持细胞膨压而消耗大量能量,故生长受到抑制甚至不能生长。本研究中,在葡萄糖和氯化钠形成的高渗透压环境下,较高水平抗性菌株表现出对渗透压的敏感性与亲本菌株有所不同,推测其对渗透压的调节能力高于亲本菌株。
Biolog表型芯片技术能检测因基因变化或用药所引起的细胞表型变化情况[29]。碳源是病原菌最主要的营养物质,微生物会根据自身的酶类代谢系统对碳源进行选择性吸收和利用[23]。本研究发现:抗性突变体和亲本菌株均能利用PM1中的95种碳源物质,说明抗氟吡菌胺突变菌株对碳源的利用能力与亲本菌株相当,并未出现明显差异;其中抗性突变体BS11-5-1对2’-脱氧腺苷的利用率高于其亲本菌株。研究已证实,2’-脱氧腺苷是DNA的重要结构片段,几乎参与所有生物学细胞的遗传信息传递[30]。本研究中抗性突变体BS11-5-1对2’-脱氧腺苷的充分利用,可能是由于该突变菌株在遗传上发生了某些变化,使其能够通过充分利用2’-脱氧腺苷而更好地适应环境,具体还需进一步研究。
在药剂选择压力下,田间环境适应性较强的抗性突变体可能会累积形成抗性群体,从而导致杀菌剂防治失效[31]。本研究中部分辣椒疫霉菌株在产生抗药性后其生物学性状并未发生明显变化,表明抗性突变菌株对环境的适应性与其亲本菌株相似,由此推测辣椒疫霉对氟吡菌胺存在一定的抗药性风险。因此,生产上在使用氟吡菌胺防治辣椒疫病时,需适时进行抗药性监测并制定合理的病害治理策略,以防止或延缓抗药性群体的发展蔓延,减少因氟吡菌胺防治失效所带来的损失。但由于本研究所获抗性菌株是在室内紫外诱导条件下产生的,在田间连续施药的情况下,辣椒疫霉菌株能否产生抗氟吡菌胺突变体,以及所得抗性菌株的环境适合度、遗传稳定性及交互抗药性等生物学性状与室内紫外诱导产生的抗性突变体是否一致,尚需进一步采用药剂驯化和自然筛选等方式获得抗性菌株进行研究验证。
| [1] |
WHELLER T, ERWIN D C, RIBEIRO O K. Phytophthora diseases worldwide[J]. Mycologia, 1998, 90(6): 1092. DOI:10.2307/3761286 |
| [2] |
HAUSBECK M K, LAMOUR K H. Phytophthora capsici on vegetable crops: research progress and management challenges
[J]. Plant Dis, 2004, 88(12): 1292-1303. DOI:10.1094/PDIS.2004.88.12.1292 |
| [3] |
戚仁德, 汪涛, 李萍, 等. 安徽省辣椒疫霉交配型的分布及在无性后代的遗传[J]. 植物病理学报, 2012, 42(1): 45-50. QI R D, WANG T, LI P, et al. Distribution of mating types of Phytophthora capsici and inheritance in asexual progenies in Anhui Province [J]. Acta Phytopathologica Sinica, 2012, 42(1): 45-50. DOI:10.3969/j.issn.0412-0914.2012.01.007 |
| [4] |
赵卫松, 韩秀英, 王文桥, 等. 辣椒疫霉对杀菌剂抗药性研究进展[J]. 农药, 2010, 49(2): 86-89. ZHAO W S, HAN X Y, WANG W Q, et al. Advance on fungicides resistance of Phytophthora capsici [J]. Agrochemicals, 2010, 49(2): 86-89. DOI:10.3969/j.issn.1006-0413.2010.02.003 |
| [5] |
LAMOUR K H, HAUSBECK M K. Mefenoxam insensitivity and the sexual stage of Phytophthora capsici in Michigan cucurbit fields
[J]. Phytopathology, 2000, 90(4): 396-400. DOI:10.1094/PHYTO.2000.90.4.396 |
| [6] |
罗赫荣, 谢丙炎, 马凤海, 等. 辣椒疫霉对甲霜灵和霜脲氰抗药性遗传的研究[J]. 湖南农业大学学报(自然科学版), 1999, 25(1): 52-56. LUO H R, XIE B Y, MA F H, et al. A study on Phytophthora capsici’s genetic resistance to metalaxyl and cymoxianil [J]. J Hunan Agric Univ (Nat Sci Ed), 1999, 25(1): 52-56. |
| [7] |
RUBIN A E, GOTLIEB D, GISI U, et al. Mutagenesis of Phytophthora infestans for resistance against carboxylic acid amide and phenylamide fungicides
[J]. Plant Dis, 2008, 92(5): 675-683. DOI:10.1094/PDIS-92-5-0675 |
| [8] |
钱忠海. 辣椒疫霉(Phytophthora capsici Leonian)对嘧菌酯的敏感性及其抗药性风险评估[D]. 南京农业大学, 2006. QIAN Z H. Sensitivity and resistance risk assessment of Phytophthora capsici Leonian to azoxystrobin[D]. Nanjing Agricultural University, 2006. |
| [9] |
JACKSON K L, YIN J F, CSINOS A S, et al. Fungicidal activity of fluopicolide for suppression of Phytophthora capsici on squash
[J]. Crop Protection, 2010, 29(12): 1421-1427. DOI:10.1016/j.cropro.2010.08.001 |
| [10] |
COOKE L R, LITTLE G, SCHEPERS H T A M. Evaluation of fluopicolide-containing formulations for the control of potato late blight in Northern Ireland[J]. PflanzenschutzNachr. Bayer, 2006, 59: 303-316. |
| [11] |
LU X H, HAUSBECK M K, LIU X L, et al. Wild type sensitivity and mutation analysis for resistance risk to fluopicolide in Phytophthora capsici
[J]. Plant Dis, 2011, 95(12): 1535-1541. DOI:10.1094/PDIS-05-11-0372 |
| [12] |
翟明涛, 王开运, 许辉, 等. 抗氟吡菌胺辣椒疫霉菌株的诱导及其生物学特性的研究[J]. 植物病理学报, 2014, 44(1): 88-96. ZHAI M T, WANG K Y, XU H, et al. Induction and charcteristics of Phytophthora capsici isolates resistant to fluopicolide [J]. Acta Phytopathologica Sinica, 2014, 44(1): 88-96. |
| [13] |
KEINATH A P, KOUSIK C S. Sensitivity of isolates of Phytophthora capsici from the eastern United States to fluopicolide
[J]. Plant Dis, 2011, 95(11): 1414-1419. DOI:10.1094/PDIS-03-11-0242 |
| [14] |
闫磊. 黄瓜霜霉病菌对氟吡菌胺的抗性风险研究[D]. 保定: 河北农业大学, 2013. YAN L. Studies on risk of resistance in Pseudoperonospora cubensis to fluopicolide[D]. Baoding: Hebei Agricultural University, 2013. |
| [15] |
罗彦涛, 孟润杰, 赵建江, 等. 马铃薯晚疫病菌对氟吡菌胺抗性突变体的获得及其生物学性状[J]. 中国农业科学, 2016, 49(19): 3733-3745. LUO Y T, MENG R J, ZHAO J J. Acquisition and biological characteristics of fluopicolide-resistant isolates in Phytophthora infestans [J]. Scientia Agricultura Sinica, 2016, 49(19): 3733-3745. DOI:10.3864/j.issn.0578-1752.2016.19.006 |
| [16] |
方中达. 植病研究方法[M]. 3版. 北京: 中国农业出版社, 1998. FANG Z D. Plant disease research methods [M]. 3rd Ed. Beijing: China Agriculture Press, 1998. |
| [17] |
魏景超. 真菌鉴定手册[M]. 上海科学技术出版社, 1979. WEI J C. Fungus identification manual [M]. Shanghai Science and Technology Publishing House, 1979. |
| [18] |
慕立义. 植物化学保护研究方法[M]. 北京: 中国农业出版社, 1994. MU L Y. Research methods of plant chemical protection[M]. Beijing: China Agriculture Press, 1994. |
| [19] |
赵卫松. 辣椒疫霉对双炔酰菌胺抗药性风险评估及抗药性生理生化机制研究[D]. 保定: 河北农业大学, 2011. ZHAO W S. Risk evaluation of resistance to mandipropamid of Phytophthora capsici and studies on its physiological and biochemical mechanism[D]. Baoding: Hebei Agricultural University, 2011. |
| [20] |
BRUIN G C A, EDGINGTON L V. Induction of fungal resistance to metalaxyl by ultraviolet irradiation[J]. Phytopathology, 1982, 72(5): 476-480. DOI:10.1094/Phyto-72-476 |
| [21] |
兰成忠, 刘裴清, 李本金, 等. 辣椒疫霉菌产孢培养基及诱导方法筛选[J]. 热带作物学报, 2013, 34(9): 1776-1780. LAN C Z, LIU P Q, LI B J, et al. Screening of medium and induction method for sporangia production of Phytophthora capsici [J]. Chin J Trop Crops, 2013, 34(9): 1776-1780. DOI:10.3969/j.issn.1000-2561.2013.09.026 |
| [22] |
马建英. 灰霉病菌对啶菌噁唑的敏感性及抗药性风险评估[D]. 保定: 河北农业大学, 2009. MA J Y. The study on sensitivity and resistant risk assessment of Botrytis cinerea to SYP-Z048[D]. Baoding: Hebei Agricultural University, 2009. |
| [23] |
KHALIL S, ALSANIUS B W. Utilisation of carbon sources by Pythium, Phytophthora and Fusarium species as determined by biolog® microplate assay
[J]. Open Microbiol J, 2009, 3: 9-14. DOI:10.2174/1874285800903010009 |
| [24] |
赵卫松, 韩秀英, 齐永志, 等. 辣椒疫霉对双炔酰菌胺的敏感性测定及其抗药突变体生物学性状研究[J]. 农药学学报, 2011, 13(1): 21-27. ZHAO W S, HAN X Y, QI Y Z, et al. Study on the sensitivity of Phytophthora capsici to mandipropamid and biological characteristics of resistant mutants [J]. Chin J Pestic Sci, 2011, 13(1): 21-27. DOI:10.3969/j.issn.1008-7303.2011.01.04 |
| [25] |
崔晓岚, 孟庆晓, 毕扬, 等. 辣椒疫霉对烯酰吗啉的敏感性基线及室内抗药突变体研究[J]. 植物病理学报, 2009, 39(6): 630-637. CUI X L, MENG Q X, BI Y, et al. Baseline sensitivity and laboratory mutants of Phytophthora capsici resistant to dimethomorph [J]. Acta Phytopathologica Sinica, 2009, 39(6): 630-637. DOI:10.3321/j.issn:0412-0914.2009.06.010 |
| [26] |
BI Y, CUI X L, LU X H, et al. Baseline sensitivity of natural population and resistance of mutants in Phytophthora capsici to zoxamide
[J]. Phytopathology, 2011, 101(9): 1104-1111. DOI:10.1094/PHYTO-01-11-0010 |
| [27] |
ZIOGAS B N, MARKOGLOU A N, THEODOSIOU D I, et al. A high multi-drug resistance to chemically unrelated oomycete fungicides in Phytophthora infestans
[J]. Eur J Plant Pathol, 2006, 115(3): 283-292. DOI:10.1007/s10658-006-9007-6 |
| [28] |
ELLIS S W, GRINDLE M, LEWIS D H. Effect of osmotic stress on yield and polyol content of dicarboximide-sensitive and-resistant strains of Neurospora crassa
[J]. Mycological Research, 1991, 95(4): 457-464. DOI:10.1016/S0953-7562(09)80846-0 |
| [29] |
DECOROSI F, SANTOPOLO L, MORA D, et al. The improvement of a phenotype microarray protocol for the chemical sensitivity analysis of Streptococcus thermophilus
[J]. J Microbiol Methods, 2011, 86(2): 258-261. DOI:10.1016/j.mimet.2011.05.018 |
| [30] |
路有昌, 张换平. 2’-脱氧腺苷的合成[J]. 应用化工, 2006, 35(7): 564-565. LU Y C, ZHANG H P. Synthesis of 2’-deoxyadenosine[J]. Appl Chem Ind, 2006, 35(7): 564-565. DOI:10.3969/j.issn.1671-3206.2006.07.026 |
| [31] |
王光飞, 马艳. 抗甲霜灵辣椒疫霉菌的环境适合度[J]. 微生物学报, 2015, 55(5): 627-634. WANG G F, MA Y. Environmental fitness of metalaxyl-resistant isolate of Phytophthora capsici [J]. Acta Microbiologica Sinica, 2015, 55(5): 627-634. |
 2019, Vol. 21
2019, Vol. 21


