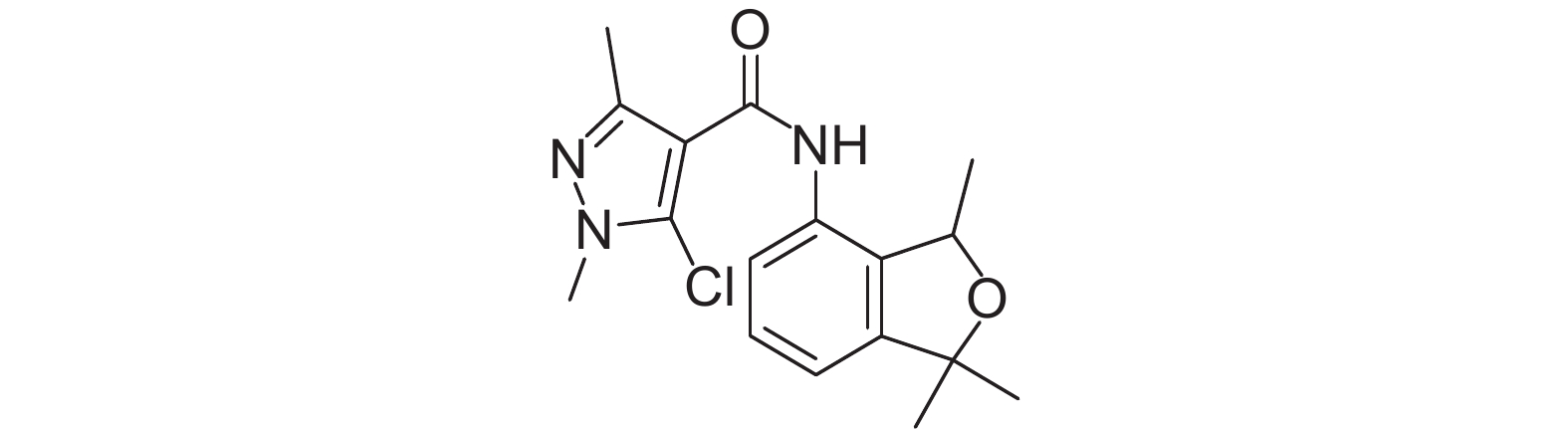
吡唑酰胺类化合物因作用机理独特、安全高效以及吡唑环上取代基变化多样而成为杀菌剂研究的热点。1997年日本住友开发的呋吡菌胺 (furametpyr,图式1) 对水稻纹枯病菌Rhizoctonia solani有特效[1]。
|
图式1 呋吡菌胺的结构式 Scheme1 The structural formula of furametpyr |
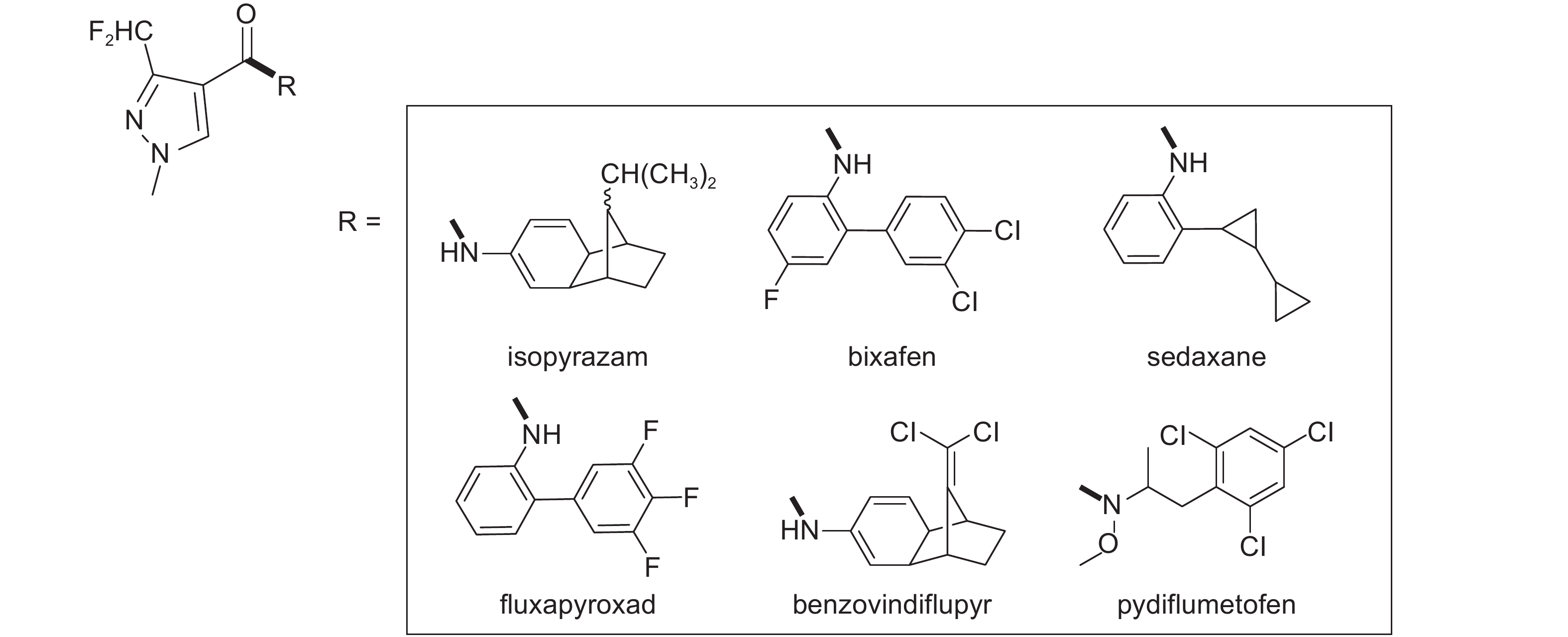
近些年,各大农药公司陆续开发并商品化了吡唑萘菌胺 (isopyrazam,先正达,2010)[2]、联苯吡菌胺 (bixafen,拜耳,2010)[3]、氟唑环菌胺 (sedaxane,先正达,2011)[4]、氟唑菌酰胺 (fluxapyroxad,巴斯夫,2012)[5]、苯并烯氟菌唑 (benzovindiflupyr,先正达,2013)[6]和氟唑菌酰羟胺 (pydiflumetofen,先正达,2016)[7]等吡唑酰胺类杀菌剂 (图式2),而这些化合物都是由中间体1-甲基-3-二氟甲基-1H-吡唑-4-羧酸 (1a,图式3) 合成而来[8]。
|
图式2 近几年新上市的吡唑酰胺类杀菌剂 Scheme2 Novel pyrazole amide fungicides developed in recent years |
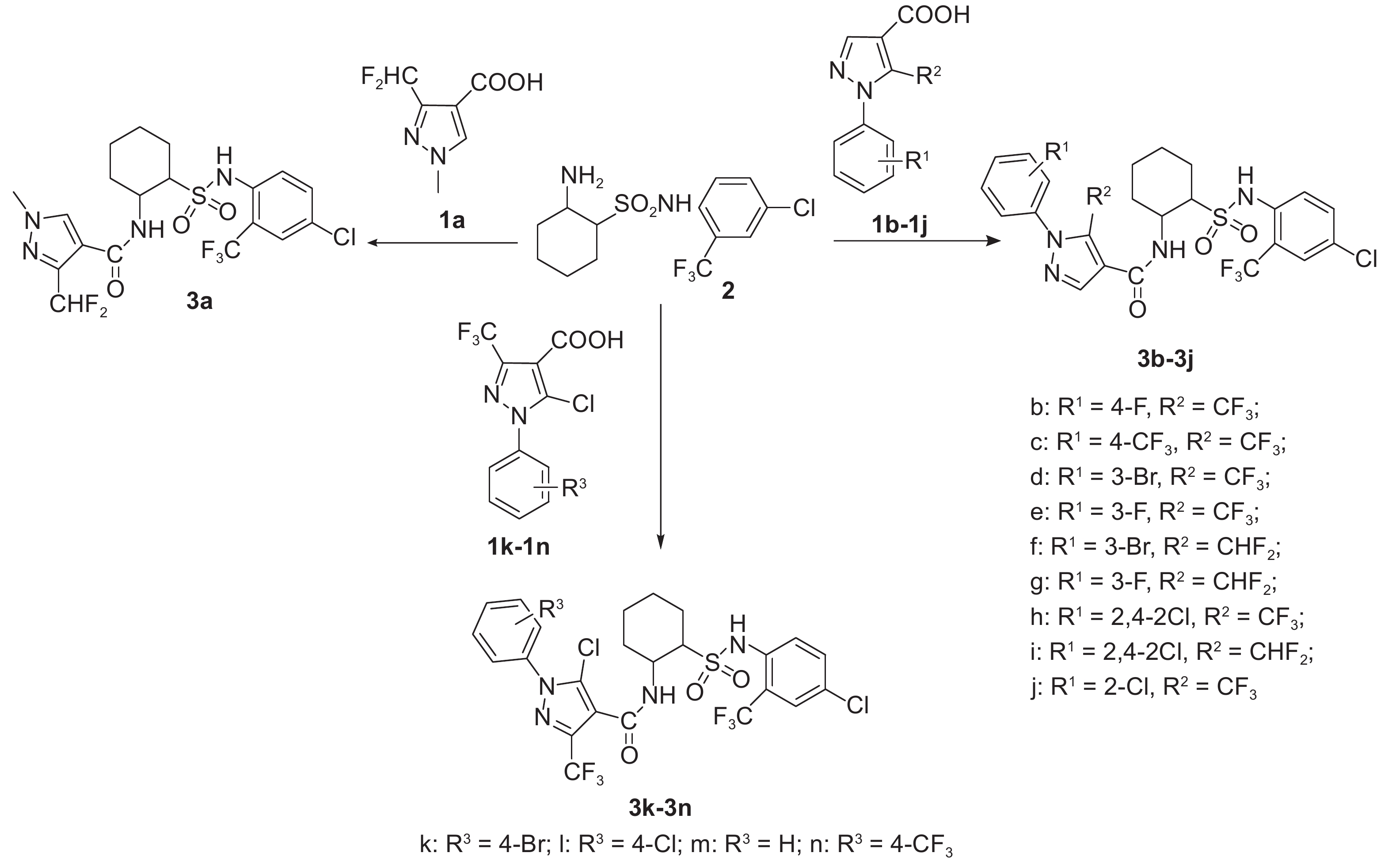
前文报道了将2-氧代环己烷基磺酰胺还原胺化首先得到重要中间体2-氨基环己烷基磺酰胺,继而合成了一系列对番茄灰霉病菌表现出较高杀菌活性的烷基酰胺、苯基酰胺、吡啶酰胺和噻唑酰胺类衍生物[9-12]。在本研究中,笔者以化合物1a和13个1-取代苯基吡唑-4-羧酸类化合物为原料,与N-(2-三氟甲基-4-氯苯基)-2-氨基环己烷基磺酰胺经EDCI/HOBt酰胺化法合成了14个未见报道的吡唑酰胺类化合物3a~3n (合成路线见图式3),对其化学结构进行了鉴定,并分别采用菌丝生长速率法、孢子萌发法和活体盆栽试验测定了目标化合物对番茄灰霉病菌的杀菌活性,旨在筛选出具有较高杀菌活性的新化合物。
|
图式3 目标化合物3a~3n的合成路线 Scheme3 Synthetic route of the title compounds 3a-3n |
1 实验部分 1.1 仪器与试剂
X-5 型熔点测定仪 (温度计未校正);Bruker600-MHz型核磁共振仪 (TMS为内标,氘代DMSO为溶剂);7890B Agilent气相色谱-三重四极杆串联质谱仪 (7000C);Flash EA 1112型元素分析仪。
试剂均为分析纯,二氯甲烷与三乙胺经干燥后使用。缩合剂1-乙基-(3-二甲基氨基丙基) 碳二亚胺盐酸盐 (EDCI) 和1-羟基苯并三唑 (HOBt) 及化合物1a购自摩贝化学品商城,纯度均为98%;化合物1b~1n由中国农业大学黄家兴副教授提供[13]。对照药剂为腐霉利 (procymidone) 与啶酰菌胺 (boscalid) 原药,纯度均为95%,由沈阳化工研究院生物测定中心提供。
1.2 供试菌株番茄灰霉病菌Botrytis cinerea分别采自辽宁省喀左、朝阳和鞍山地区,菌株代号分别为KZ-9、CY-09和AS-11,由沈阳农业大学植物保护学院农药科学研究室分离、培养和保存。
1.3 化合物的制备 1.3.1 化合物N-(2-三氟甲基-4-氯苯基)-2-氨基环己烷基磺酰胺 (2) 的合成参照文献方法[14]合成,得到白色粉末状固体,熔点252~254 ℃,收率73%。
1.3.2 目标化合物3的合成以化合物N-(2-三氟甲基-4-氯苯基)-2-(1-(4-氟苯基)-5-三氟甲基吡唑-4-甲酰氨基) 环己烷基磺酰胺 (3b) 的合成为例:在0 ℃下,向100 mL四口瓶中依次加入30 mL二氯甲烷、化合物1b (3 mmol)、EDCI(3.3 mmol)、HOBt (3.3 mmol) 和三乙胺 (5.1 mmol),搅拌反应1.5 h。加入化合物2 (0.24 mmol),在0 ℃下反应15 min后升温至室温 (25 ℃) 继续反应2~3 h。采用薄层层析 (TLC) 法[V(石油醚) : V (乙酸乙酯) = 2 : 1] 监测至反应液中无原料,停止反应。反应液依次用30 mL饱和碳酸钠溶液和30 mL水洗涤,用无水硫酸钠干燥12 h,抽滤,减压蒸馏去除溶剂,得粗产物。经硅胶柱层析[V(石油醚) : V(乙酸乙酯) = 3 : 1] 提纯,得到目标化合物3b,熔点204.5~206.4 ℃,收率74%。采用相同的方法得到其余目标化合物。
1.4 杀菌活性测定 1.4.1 离体抑菌活性测定 1.4.1.1 菌丝生长速率法按文献方法[15]测定目标化合物对3个番茄灰霉病菌菌株KZ-9、CY-09和AS-11菌丝生长的抑制活性。用丙酮配制质量浓度为5 000 mg/L的供试化合物药液,采用梯度稀释法配制药剂,得到质量浓度为1 250、312.5和78.1 mg/L的系列药液。将药液加入PDA培养基 [m(水) : m(琼脂) : m(葡萄糖) = 50 : 1 : 1] 制得质量浓度为50、12.5、3.13和0.78 mg/L的含毒培养基。接种直径5 mm的供试菌株菌饼,3~5 d后测量菌落直径。计算每个化合物在不同浓度下对菌丝生长的抑制率。通过Excel软件计算相应化合物的EC50值。以防治番茄灰霉病的登记药剂腐霉利和啶酰菌胺原药为药剂对照,以丙酮为空白对照。
1.4.1.2 孢子萌发法采用凹玻片法[16]测定目标化合物对番茄灰霉病菌孢子萌发的抑制活性。首先配制1 000 mg/L的供试化合物药液,然后吸取0.01 mL加入到0.99 mL新配制的灰霉病菌孢悬浮液中 (5 × 105个/mL),得到含有10 mg/L供试化合物的孢子悬浮液。于22 ℃下培养8 h后镜检,计算孢子萌发率及孢子萌发抑制率。
1.4.2 活体盆栽试验采用盆栽法[17]测定目标化合物对番茄灰霉病菌在番茄叶片和花上侵染的防治效果。将0.05 g供试化合物溶解到0.3 mL甲醇中,加入0.007 5 g农乳500和0.042 5 g农乳600,用二甲基亚砜 (DMSO) 补齐至1 mL,得到有效成分质量分数为5%的化合物乳油,再用水稀释成200 mg/L的药液供试。以啶酰菌胺和腐霉利原药配制成的乳油为药剂对照,以不加原药的乳油为空白对照。将供试药液和对照均匀喷施到已长有20~30片叶的番茄幼苗上,5 h后喷施5 × 105个/mL的灰霉病菌孢子悬浮液,于(23 ± 2) ℃、相对湿度80%以上的温室中,待空白对照发病后调查所有番茄叶片 (花) 病情指数,按公式 (1) 计算防治效果。每处理重复4次。
| $P/{\text{%}} = \frac{{{X_1} - {X_2}}}{{{X_1}}} \times 100$ | (1) |
式中:P—防治效果;X1—空白对照病情指数;X2—药剂处理病情指数。
2 结果与分析 2.1 化合物的合成在合成目标化合物3时,曾采用酰氯法进行酰胺化反应,但容易产生极性接近的副产物,目标物不易被分离纯化,且中间体吡唑酰氯活性高,易分解,致使最终酰胺的产率很低。本研究采用缩合剂EDCI和HOBt将吡唑羧酸先转化成活性酯,再与胺反应生成吡唑酰胺。该方法操作简便,低温加料后可在室温下反应,且反应后处理简单。由于催化剂、缩合剂及其脲类副产物均溶于水,而目标产物吡唑酰胺溶于二氯甲烷,故可通过萃取的方法除去副产物及杂质,最后经柱层析纯化获得目标化合物。
目标化合物的理化数据、质谱和元素分析数据见表1,1H NMR和 13C NMR数据见表2。
|
|
表 1 化合物3a~3n的理化、质谱和元素分析数据 Table 1 Physical properties, mass spectrometry and elemental analysis data of compounds 3a-3n |
|
|
表 2 化合物3a~3n的 1H NMR和 13C NMR数据 Table 2 The 1H NMR and 13C NMR data of compounds 3a-3n |
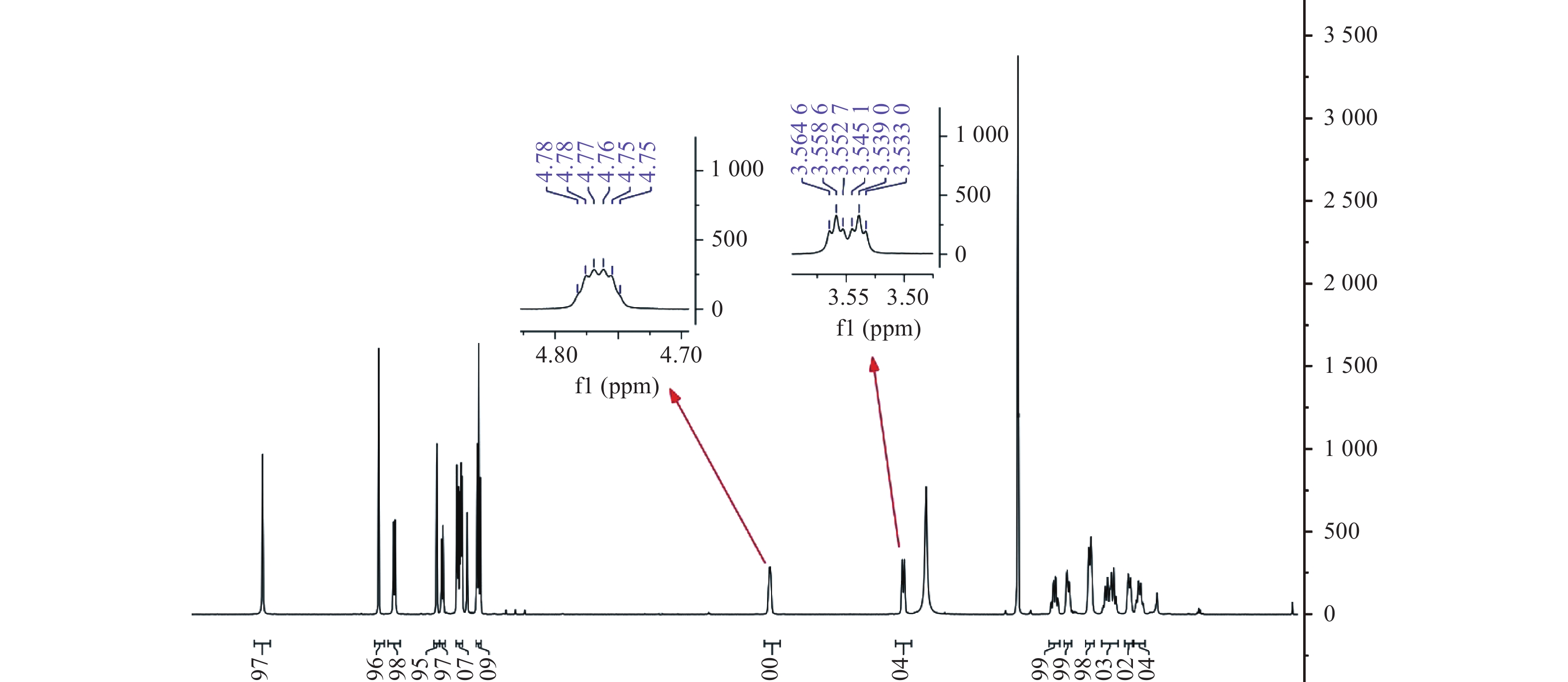
化合物3g的 1H NMR和 13C NMR谱图见图1和图2。
以化合物3g的结构解析为例,在1H NMR谱中 (图1),CONH与SO2NH基团中分别含有1个活泼氢,均为s峰,且位于低场区。由于SO2NH基团的吸电子能力比CONH强,所以在前者所连接的环己烷上CH的化学位移相较于后者向低场区移动,在谱图中一个化学位移在4.7附近,裂分为多重峰;另一个化学位移在3.5附近,裂分为dt峰,偶合常数分别为11.7 Hz和3.6 Hz。
|
图 1 化合物3g的核磁氢谱 Fig. 1 The 1H NMR of compound 3g |
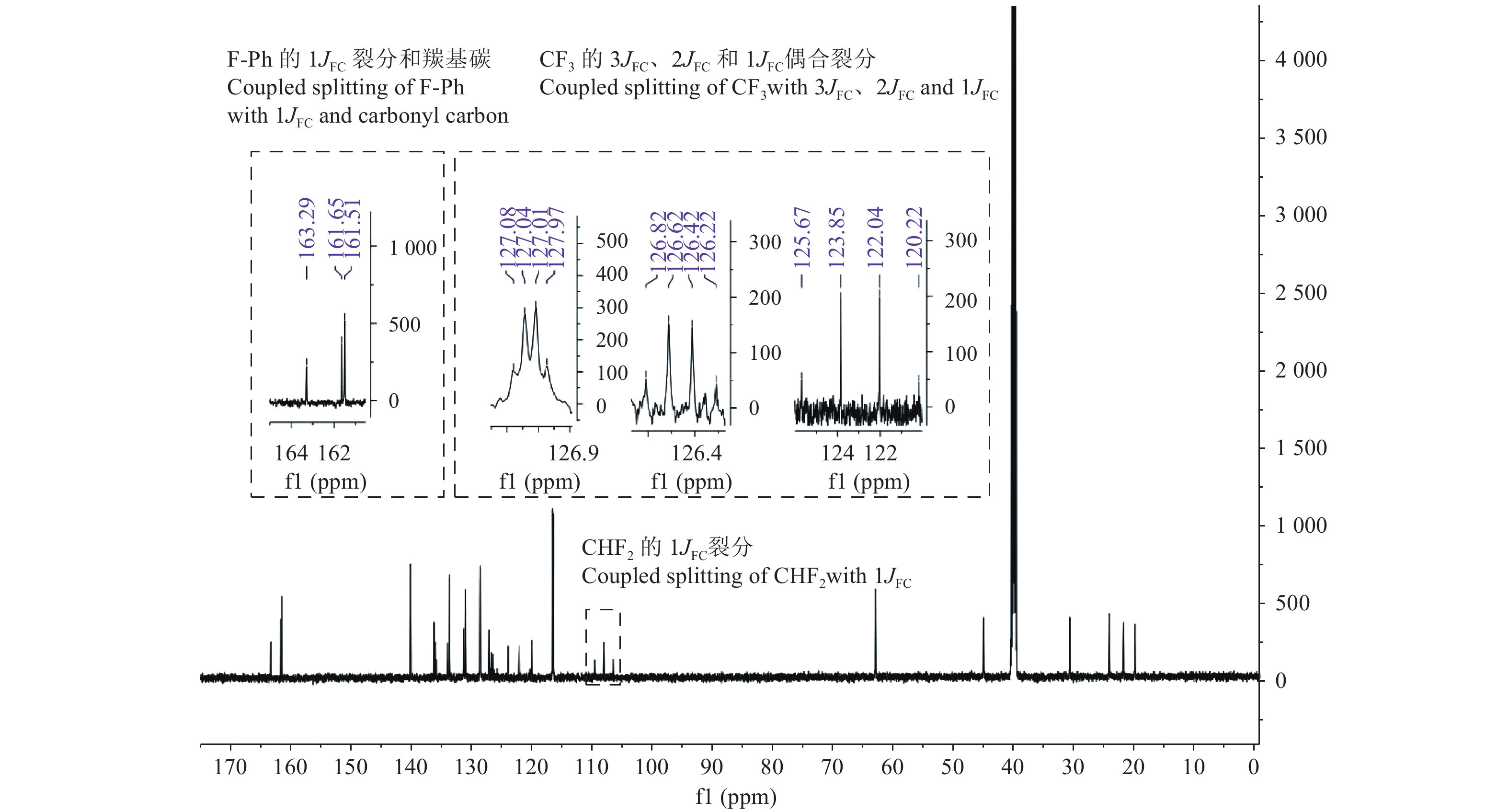
在 13C NMR中 (图2),化合物3g中环己烷上6个碳的化学位移位于19.0~63.0之间,苯环碳的化学位移普遍位于120.0~140.0之间,但连有氟原子的苯环碳位移在162.5附近,并裂分成双峰,偶合常数为246.9 Hz。酰胺结构中的羰基位移在161.5附近;二氟甲基碳位于108.0附近,裂分为三重峰,1JFC=235.6 Hz;三氟甲基碳位于123.0附近,裂分为4重峰,1JFC=274.3 Hz,与其相连的苯环碳的2JFC =30.2 Hz,3JFC=5.5 Hz。多数含有1个二氟甲基和1个三氟甲基的化合物中,两个含氟碳原子的裂分比较清楚。含有2个或3个三氟甲基的结构中,因为偶合裂分峰的重叠,一般只能分辨出较高的2条峰的偶合裂分情况。
|
图 2 化合物3g的核磁共振碳谱 Fig. 2 The 13C NMR of compound 3g |
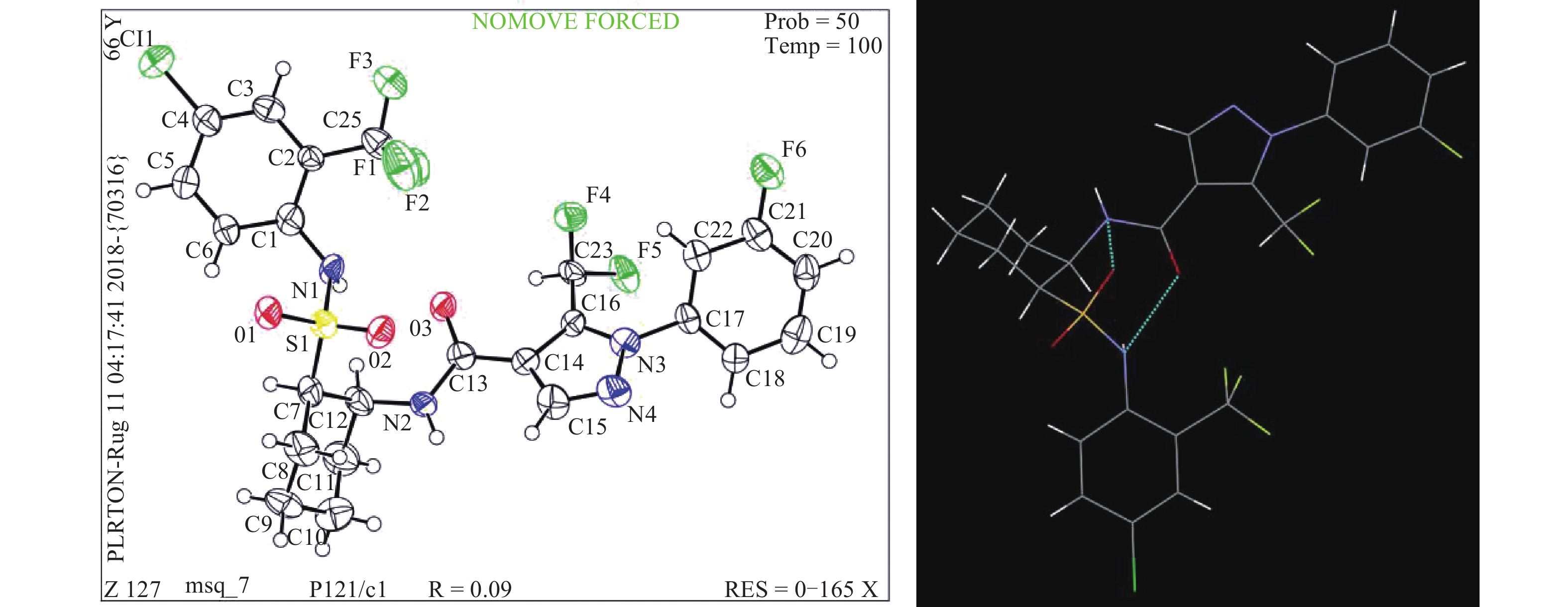
化合物3g的单晶结构 (CCDC:1864629) 见图3,其立体结构为顺式,其中SO2NH基团位于平伏键,C7为S构型,CONH位于直立键,C12为R构型。分子内的2个氢键有利于晶体结构的稳定存在。另外,3g的高分辨质谱理论值为595.100 0,实测值为 595.100 1。
|
图 3 化合物3g的单晶结构 Fig. 3 X-ray crystal structure of compound 3g |
2.2 杀菌活性 2.2.1 离体杀菌活性
由于采自不同地区的灰霉菌株生长环境和用药水平不同,所以对相同化合物的敏感性也不同。菌丝生长速率法测定结果 (表3) 表明:14个目标化合物对敏感性较高的菌株KZ-9的菌丝生长均有不同程度的抑制作用,其中化合物3a、3e和3j的EC50值分别为4.28、10.08和11.31 mg/L,杀菌活性较好,但其对敏感性较低的菌株CY-09和AS-11 活性略差。总体来看,目标化合物对番茄灰霉病菌菌丝生长的抑制活性低于对照药剂啶酰菌胺和腐霉利。孢子萌发试验结果 (表3) 表明,目标化合物对灰霉病菌菌孢子萌发具有较高的抑制活性,在10 mg/L下,有10个化合物的抑制率高于腐霉利 (82%),其中化合物3e和3i抑制率大于90%,接近对照药剂啶酰菌胺 (100%)。
|
|
表 3 化合物3a~3n对番茄灰霉病菌的离体杀菌活性 Table 3 The bioactivity of compounds 3a-3n against B. cinerea in vitro |
2.2.2 活体杀菌活性
盆栽法测定结果 (表4) 表明:在200 mg/L下,大部分目标化合物对番茄叶片上的灰霉病菌具有较好的防治效果,其中有9个化合物的防治效果超过了对照药剂啶酰菌胺 (59.8%) 和腐霉利 (44.9%),化合物3d的防治效果超过了80%。由表4中数据还可看出,包含对照药剂在内的所有药剂在番茄花上的防治效果均明显低于叶片上的,其中化合物3e在叶上的防治效果为77.5%,在花上的也达到65.2%,显示出了优异的杀菌活性。
|
|
表 4 化合物3a~3n对番茄灰霉病菌的活体盆栽试验 Table 4 The bioactivity of compounds 3a-3n against B. cinerea in vivo |
2.2.3 目标化合物的构效关系分析
1-甲基-3-二氟甲基-1H-吡唑-4-酰胺是多种已商品化吡唑酰胺杀菌剂中共有的结构,包含该结构的化合物3a表现出了较好的杀菌活性。与化合物3a相比,其余13个目标化合物均表现出了良好的杀菌活性。从构效关系上来看,当吡唑环上1-位为氟取代苯基时化合物的活性较高,当1位为氯或溴取代苯基时活性相对较差,如化合物3b和3e对菌丝的抑制活性明显优于化合物3d、3f和3n等,其中化合物3e(吡唑环1-位为3-氟苯基、5位为三氟甲基)在菌丝生长、孢子萌发和活体盆栽试验中均表现出较好的杀菌活性。
3 结论笔者以1-甲基-3-二氟甲基吡唑-4-羧酸为对照结构,以系列1-取代苯基吡唑-4-羧酸化合物 (1) 为原料,通过EDCI/HOBt酰胺化法与N-(2-三氟甲基-4-氯苯基)-2-氨基环己烷基磺酰胺 (2)反应,合成了14个未见文献报道的吡唑酰胺类标题化合物 (3),产率均较高 (60%~90%)。
生物活性测试结果表明,目标化合物3对灰霉病菌具有良好的杀菌活性。从初步结构与活性关系看,与吡唑环1-位为甲基的吡唑酰胺 (3a) 相比,在1-位引入氟取代苯基能够提升化合物对灰霉病菌的杀菌活性,特别是化合物3e,对菌丝生长的EC50值为10.08 mg/L,在10 mg/L下对孢子萌发的抑制率高达91%,在200 mg/L时对番茄叶和花上灰霉病菌的防治效果分别为77.5%和65.2%,总体表现出了优异的杀菌活性,有进一步研究的价值。
| [1] |
周卫平. 新颖内吸杀菌剂furametpyr[J]. 农药译丛, 1998, 20(20): 62-63. ZHOU W P. The novel fungicide furametpyr[J]. Nongyao Yicong, 1998, 20(20): 62-63. |
| [2] |
禾丽菲, 李晓旭, 朱佳美, 等. 不同杀菌剂对黄瓜靶斑病菌的毒力作用特性比较[J]. 农药学学报, 2018, 20(1): 25-32. HE L F, LI X X, ZHU J M, et al. Comparison of toxicity properties of different types of fungicides against Corynespora cassiicola on cucumber [J]. Chin J Pestic Sci, 2018, 20(1): 25-32. |
| [3] |
罗梁锋. 新一代琥珀酸脱氢酶抑制剂联苯吡菌胺[J]. 世界农药, 2018, 40(1): 63-64. LUO L F. A new succinic acid dehydrogenase inhibitor: bixafen[J]. World Pesticides, 2018, 40(1): 63-64. |
| [4] |
姜桦韬, 尤祥伟, 张广雨, 等. QuEChERS-液相色谱-串联质谱法检测糙米中氟唑环菌胺的残留[J]. 农药学学报, 2018, 20(1): 124-128. JIANG H T, YOU X W, ZAHNG G Y, et al. Determination of sedaxane in brown rice by QuEChERS-liquid chromatography-tandem mass spectrometry[J]. Chin J Pestic Sci, 2018, 20(1): 124-128. |
| [5] |
顾林玲. 吡唑酰胺类杀菌剂: 氟唑菌苯胺[J]. 现代农药, 2013, 12(2): 44-47. GU L L. Penflufen, a new pyrazole-carboxamide fungicide[J]. Modern Agrochem, 2013, 12(2): 44-47. |
| [6] |
党铭铭, 刘民华. 新型杀菌剂 Benzovindiflupyr[J]. 精细化工中间体, 2017, 47(3): 7-10. DANG M M, LIU M H. A novel fungicide: benzovindiflupyr[J]. FINE CHEMICAL INTERMEDIATES, 2017, 47(3): 7-10. |
| [7] |
RAJAN R, WALTER H, STIERLI D. Preparation of pyrazolecarboxylic acid alkoxyamides as agrochemical microbiocides: WO 2010063700A2[P]. 2010-06-10.
|
| [8] |
仇是胜, 柏亚罗. 琥珀酸脱氢酶抑制剂类杀菌剂的研发进展 (Ⅱ)[J]. 现代农药, 2015, 14(1): 1-7. QIU S S, BAI Y L. Progress on research and development of succinate dehydrogenase inhibitor fungicides (Ⅱ)[J]. Mod Agrochem, 2015, 14(1): 1-7. DOI:10.3969/j.issn.1671-5284.2015.01.001 |
| [9] |
WANG M L, RUI P, LIU C X, et al. Design, synthesis and fungicidal activity of 2-substituted phenyl-2-oxo-, 2-hydroxy- and 2-acyloxyethylsulfonamides[J]. Molecules, 2017, 22(5): 738. DOI:10.3390/molecules22050738 |
| [10] |
LIU C X, YAN X J, WANG M L, et al. Design, synthesis and fungicidal activity of novel 2-substituted aminocycloalkylsulfonamides[J]. Bioorg Med Chem Lett, 2017, 27(2): 271-276. DOI:10.1016/j.bmcl.2016.11.061 |
| [11] |
王闽龙, 曲圣极, 纪明山, 等. 2-吡啶酰氨基环己烷基磺酰胺的合成与杀菌活性[J]. 农药学学报, 2017, 19(2): 169-175. WANG M L, QU S J, JI M S, et al. Synthesis and fungicidal activity of 2-pyridinecarboxamide cyclohexylsulfonamides[J]. Chin J Pestic Sci, 2017, 19(2): 169-175. |
| [12] |
杨永贵, 孟司奇, 祁之秋, 等. 2-噻唑酰氨基环己烷基磺酰胺的合成与杀菌活性[J]. 农药学学报, 2018, 20(3): 287-293. YANG Y G, MENG S Q, QI Z Q, et al. Synthesis and fungicidal activity evaluation of 2-thiazolylamide cyclohexane-sulfonamide[J]. Chin J Pestic Sci, 2018, 20(3): 287-293. |
| [13] |
鲍志远, 黄苇静, 宋涵博, 等. 1-取代苯基-5-三氟甲基 (二氟甲基)-4-吡唑甲酸的合成研究[J]. 化学试剂, 2018, 40(1): 26-30. BAO Z Y, HUANG W J, SONG H B, et al. Synthesis of 5-trifluoromethyl (difluoromethyl)-1-substitutedphenyl-1H-pyrazole-4-carboxylic acid [J]. Chem Reag, 2018, 40(1): 26-30. |
| [14] |
王道全, 李兴海, 梁晓梅, 等. 2-氧代环烷基磺酰胺, 其制备方法和作为杀菌剂的用途: CN1900059A[P]. 2007-01-24. WANG D Q, LI X H, LIANG X M, et al. 2-Keto naphthene sulfamide, its preparing method and use as germicide: CN1900059A[P]. 2007-01-24. |
| [15] |
农药室内生物测定试验准则 杀菌剂 第2部分: 抑制病原真菌菌丝生长试验 平皿法: NY/T 1156.2—2006[S]. 2006. Pesticides guidelines for laboratory bioactivity tests part 2: petri plate test for determining fungicide inhibition of mycelial growth: NY/T 1156.2—2006[S]. Beijing: The Ministry of Agriculture of the People's Republic of China, 2006. |
| [16] |
农药室内生物测定试验准则 杀菌剂 第1部分: 抑制病原真菌孢子萌发试验 凹玻片法: NY/T1156. 1—2006[S]. 北京: 中国农业出版社, 2006. Pesticides guidelines for laboratory bioactivity tests Part 1:Determining fungicide inhibition ofpathogen spore germination on concave slides: NY/T1156. 1—2006[S]. Beijing: China Agriculture Press, 2006. |
| [17] |
农药田间药效试验准则 (一) 杀菌剂防治蔬菜灰霉病: GB/T 17980.28—2000[S]. 北京: 中国标准出版社, 2000. Pesticide-Guidelines for the field efficacy trials(Ⅰ): Fungicides against grey mould of vegetables: GB/T 17980. 28—2000[S]. Beijing: Standards Press of China, 2000. |
 2018, Vol. 20
2018, Vol. 20


