2. 浙江省农药检定管理总站,杭州 310020
2. Station for the Control of Agrochemicals Zhejiang Province, Hangzhou 310020, China
白术Atractylodes macrocephala Koidzz又名贡术,别名于术、浙术,是菊科多年生草本植物,根茎可入药,具有健脾益气、燥湿利水、固表止汗、安胎等功效[1]。白术是浙江地区主产的中药材,为浙八味之一,在全国分布广泛,主要集中在浙江、安徽等省种植,江苏、江西、湖南、重庆、贵州、陕西等省均有零星种植。浙江白术产量占全国的1/2以上,而磐安县白术的产量占浙江全省产量的1/2[2]。在白术生产中有多种病害,其中由细交链格孢Alternaria alternata引起的黑斑病发生普遍,在白术全生育期均可发生,重病株往往茎叶变黑枯死[3-4]。目前生产上对白术黑斑病以化学防治为主,常用药剂有石硫合剂、甲基硫菌灵和腐霉利等[5-7]。由于使用时间长及使用不合理等原因,一些杀菌剂在生产上时有反映防治效果下降甚至失效的现象[8],但目前尚未见有关白术黑斑病菌对常用杀菌剂抗性情况的研究报道。本研究检测了白术黑斑病菌对常用传统杀菌剂的抗性,以期为白术黑斑病的防治及抗药性治理提供依据。
1 材料与方法 1.1 药剂98.0%甲基硫菌灵 (thiophanate-methyl)、98.0%腐霉利 (procymidone)、95.0%咪鲜胺 (prochloraz)、96.0%丙硫菌唑 (prothioconazole)、97.5%四氟醚唑 (tetraconazole)、96.0%苯醚甲环唑 (difenoconazole)、97.6%戊唑醇 (tebuconazole)、95.0%啶酰菌胺 (boscalid) 和96.0%嘧菌酯 (azoxystrobin)9种原药由浙江农林大学植物病害防治与杀菌剂实验室保存, 均用丙酮等相应溶剂溶解,配制成10 000 mg/L的母液备用。
1.2 供试菌株的采集、分离及鉴定于2015—2017年间从浙江省磐安、天台、新昌和嵊州4地随机采集白术黑斑病病样,进行常规组织分离。每个点采集分离5~10株。采样地区主要使用苯并咪唑类及二甲酰亚胺类等杀菌剂进行病害防治。分离所得137株黑斑病菌均保存于常规马铃薯葡萄糖琼脂 (PDA) 斜面上。各菌株均主要通过形态学结合真菌核糖体基因转录间隔区 (ITS) 分析进行鉴定[9]。
1.3 白术黑斑病菌对甲基硫菌灵和腐霉利的抗性测定采用菌丝生长速率法,根据杀菌剂抗性行动委员会 (FRAC) 推荐的病原菌对苯并咪唑类杀菌剂测定方法,设置区分剂量[9-14]。甲基硫菌灵的有效剂量分别设为0、5、50和100 mg/L,以不含药剂的丙酮为对照 (CK),每处理重复3次。在预培养6 d的各菌株同一圆周菌落上制取直径0.5 cm的菌碟,将其转移至含有不同质量浓度药剂的PDA平板中央,25 ℃下培养7 d后观察生长情况。其中:不能在含5 mg/L甲基硫菌灵的PDA平板上生长的菌株为敏感菌株 (Thm S);能在5 mg/L但不能在50 mg/L下生长的为低水平抗性菌株 (Thm LR);能在50 mg/L但不能在100 mg/L下生长的为中等水平抗性菌株 (Thm MR);能在100 mg/L下生长的为高水平抗性菌株 (Thm HR)。
腐霉利的有效剂量分别设为0、5、20和100 mg/L,以不含药剂的丙酮为对照 (CK),每处理重复3次。根据菌株在不同剂量下的生长情况,类似地将其确定为Pro S、Pro LR、Pro MR和Pro HR [9-11]。
1.4 供试杀菌剂离体抑菌活性的测定随机选择PA7、XA3和SA8为供试菌株,采用菌丝生长速率法[15]测定其对供试药剂的敏感性。各药剂根据预试验结果设置5~7个处理浓度。各菌株先在PDA平板上培养6 d后,在同一圆周上制取菌丝块 (直径0.5 cm),接种到含不同质量浓度供试药剂的PDA平板中央,分别以不含药剂但含有相同体积有机溶剂的处理为对照 (CK),每处理重复3次。25 ℃黑暗条件下培养7 d后测量各处理的菌落直径 (cm),取平均值按 (1) 式计算抑制率 (%),通过药剂质量浓度对数值 (x) 和抑制率几率值 (y) 之间的线性回归关系求出毒力回归方程和EC50值。
| $\begin{aligned}{\text{抑制率}}/\text{%}=\frac{{\text{对照的菌落直径}}-{\text{处理的菌落直径}}}{{\text{对照的菌落直径} - 0.5}}\times 100\end{aligned}$ | (1) |
咪鲜胺的质量浓度分别设为0、0.05、0.1、0.2、0.4、0.8和1.6 mg/L。供试137株菌株在PDA平板上预培养6 d后,在同一圆周菌落上制取直径为0.5 cm的菌饼,将其转移到含有不同质量浓度药剂的平板中央及不含药剂的对照平板中央,每处理重复4次,于25 ℃下黑暗培养。6 d后测量各处理的菌落直径 (cm),取平均值,按 (1) 式计算抑制率 (%)。利用DPS软件,通过药剂浓度对数值 (x) 和抑制率几率值 (y) 之间的线性回归关系,求出毒力回归方程及EC50值。
1.6 白术黑斑病菌对咪鲜胺的敏感性分布图制作将病原菌群体对供试药剂的敏感性 (EC50值) 从高到低分成约10个左右的区间,统计各区间菌株在整个群体中出现的频率 (%);同时以EC50值为X轴,相应的频率 (%) 为Y轴,即得到病原菌群体对该种杀菌剂的敏感性分布图[16]。
2 结果与分析 2.1 白术黑斑病菌对甲基硫菌灵的抗性情况在供试的137株白术黑斑病菌菌株中没有检测到对甲基硫菌灵敏感 (Thm S) 和低抗 (Thm LR) 菌株,共检测到31株Thm MR和106株Thm HR,频率分别为22.6%和77.4%。从地区来看:在磐安的91株供试菌株中共检测到75株Thm HR,Thm HR频率最高 (82.4%);其次为新昌 (78.6%);嵊州和天台的Thm HR频率分别为64.3%和61.1%(表1)。
|
|
表 1 浙江省不同地区白术黑斑病菌对甲基硫菌灵的抗性水平及频率 Table 1 Resistance level and frequency of A. alternata isolates collected from different regions in Zhejiang Province to thiophanate-methyl |
2.2 白术黑斑病菌对腐霉利的抗性情况
白术黑斑病菌对腐霉利也产生了抗性,4地共检测到28株抗性菌株,总的抗性频率为20.4%,其中含21株Pro LR和7株Pro MR,未检测到Pro HR菌株。从地区来看:天台、新昌、嵊州和磐安总的抗性频率分别为44.4%、28.6%、21.4%和14.3%;上述4地分别检测到2、0、1和4株Pro MR菌株,频率分别为11.1%、0%、7.1%和4.4%(表2)。
|
|
表 2 浙江省不同地区白术黑斑病菌对腐霉利的抗性水平及频率 Table 2 Resistance level and frequency of A. alternata isolates from different regions in Zhejiang Province to procymidone |
2.3 7种供试杀菌剂对白术黑斑病菌的抑菌活性
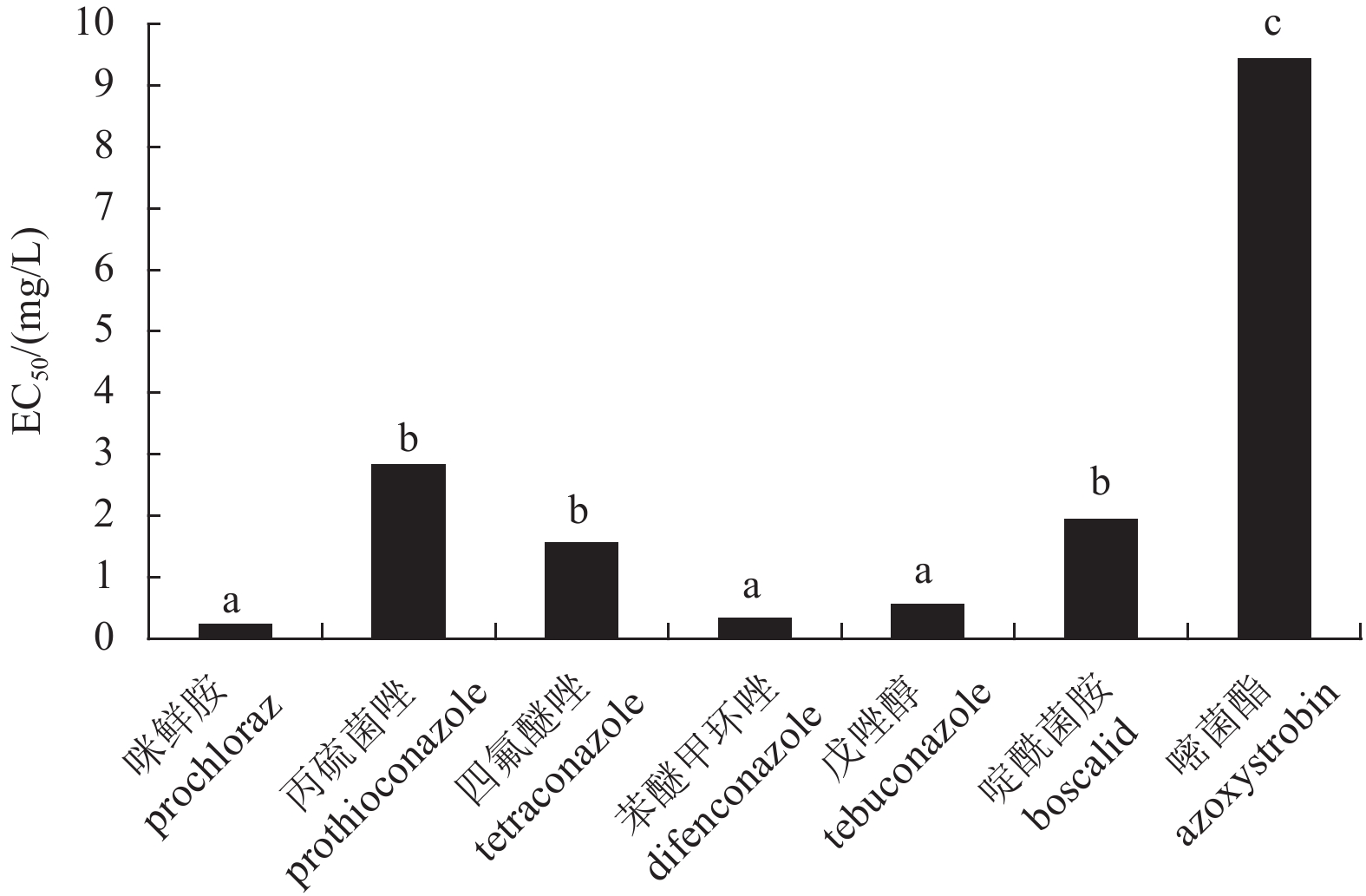
室内毒力测定结果表明:咪鲜胺对白术黑斑病菌的抑菌活性最高,EC50值为0.15 mg/L;苯醚甲环唑和戊唑醇对其的抑菌活性也较高,EC50值分别为0.27 mg/L和0.50 mg/L,而啶酰菌胺、四氟醚唑和丙硫菌唑的抑菌活性显著低于上述3种药剂;嘧菌酯的活性最差,EC50值为9.4 mg/L(图1)。
|
注:柱上不同字母表示不同处理间差异显著 (Turkey氏多重比较, P < 0.05)。 Note:different letters indicate significant differences among different treatments (Turkey’s multiple comparison, P < 0.05). 图 1 7种杀菌剂对白术黑斑病菌的抑菌活性 Fig. 1 Inhibitory effects of 7 fungicides against A. alternate |
2.4 白术黑斑病菌对咪鲜胺的敏感性基线
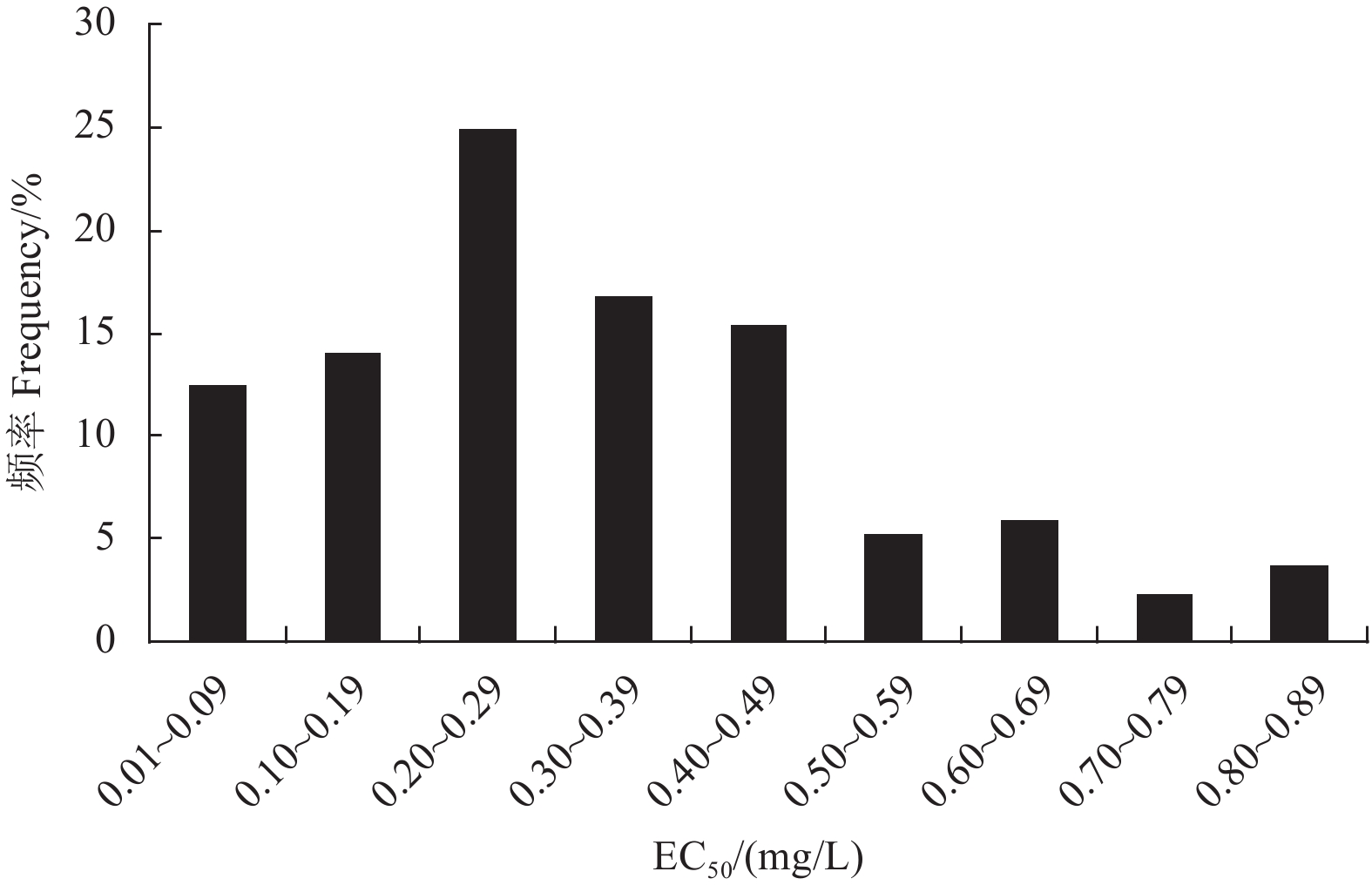
供试137株白术黑斑病菌对咪鲜胺的敏感性分布见图2,其中最高EC50值0.87 mg/L是最低EC50值0.05 mg/L的17.4倍,平均EC50值为 (0.29 ± 0.11) mg/L。从敏感性分布图上看,供试白术黑斑病菌群体对咪鲜胺的敏感性呈连续性分布,其频率分布为近似正态的单峰曲线,因此可将其平均EC50值 (0.29 ± 11) mg/L作为其敏感性基线的参考值,用于监测田间抗药性的演化。
|
图 2 白术黑斑病菌对咪鲜胺的敏感性频率分布 Fig. 2 Distribution of sensitivity frequency of A. alternata to prochloraz |
3 小结与讨论
化学防治一直是中药材植物病害防治中的主要方法,但迄今几乎未见有关中药材植物病原菌抗药性的相关研究报道[8]。苯并咪唑类和二甲酰亚胺类杀菌剂是生产上白术黑斑病防治的主要药剂[5-7]。本研究检测了白术主产省浙江省的天台、新昌、嵊州和磐安4地白术黑斑病菌群体 (n = 137) 的抗药性发生现状。结果表明,白术黑斑病菌对甲基硫菌灵已具有极其严重的抗性,MR和HR的频率分别为22.6%和77.4%。说明苯并咪唑类药剂在白术黑斑病的防治上已无实际应用价值,应该停止使用[13, 17]。本研究只是从生产实际出发借鉴其他病菌的鉴别剂量法[10, 18]检测了白术黑斑病菌对甲基硫菌灵的抗药性。尽管苯并咪唑类杀菌剂已被推荐用于防治一些作物上的链格孢菌病害,但实际上,这类杀菌剂对敏感的灰霉病菌等真菌具有很好的抑菌活性,而对链格孢菌的活性比较低[19],因而并不能高效地防治这类病害。白术黑斑病菌对腐霉利也产生了抗性 (其中LR 15.3%,MR 5.1%)。从地区来看,天台的抗性较为严重,总的抗性频率和中等抗性频率分别为44.4%和11.1%,均明显高于新昌、嵊州和磐安,具体原因有待进一步分析。以往研究报道对二甲酰亚胺类杀菌剂产生抗性的病菌的适合度往往会降低,田间一般检测不到高抗菌株[19-21]。因此,如果能采取合理的抗药性治理措施如与其他类型的杀菌剂混用或轮用,腐霉利等二甲酰亚胺类杀菌剂仍可作为白术黑斑病防治的骨干药剂之一。
本研究表明,在供试的7种杀菌剂中,咪鲜胺对细交链格孢菌的抑制活性最高。而嘧菌酯对白术黑斑病菌菌丝生长的活性最差,可能与测定时未添加旁路氧化酶抑制剂有关[19, 22]。咪鲜胺属于麦角甾醇生物合成抑制剂 (EBIs),与其他类型杀菌剂无交互抗性[23]。过去一般认为EBIs类杀菌剂抗药性风险较低,但近些年也有研究表明,部分病原菌对EBIs类杀菌剂的某些品种也会出现较严重的抗性问题[23],所以病原菌对咪鲜胺的敏感性变化仍需要监测[24]。本研究结果表明,白术黑斑病可以通过采用咪鲜胺与腐霉利等杀菌剂混用或轮用的方式进行防治。本研究中,白术黑斑病菌群体 (n = 137) 对咪鲜胺的敏感性呈近似正态分布,该结果能够反映自然情况下病原菌对该杀菌剂的敏感性特征,因而其平均EC50值 (1.21 ± 0.12) mg/L可作为基线敏感性参考值用于其抗药性监测。
| [1] |
杨娥, 钟艳梅, 冯毅凡. 白术化学成分和药理作用的研究进展[J]. 广东药学院学报, 2012, 28(2): 218-221. YANG E, ZHONG Y M, FENG Y F. Advance on the chemical constituents and pharmacological effects of Atractylodes macrocephala Koidz [J]. J Guangdong Pharmace Univ, 2012, 28(2): 218-221. |
| [2] |
谭国印, 杨志玲, 袁志林, 等. 白术真菌病害的分离鉴定[J]. 浙江农业学报, 2013, 25(5): 1050-1055. TAN G Y, YANG Z L, YUAN Z L, et al. Isolation and identification of fungal pathogens of Atractylodes macrocephala [J]. Acta Agri Zhejiangensis, 2013, 25(5): 1050-1055. |
| [3] |
张礼维, 韦鑫, 曾桂萍, 等. 贵州省2011—2013年白术病虫害种类调查及防治措施[J]. 耕作与栽培, 2014(6): 32-34. ZHANG L W, WEI X, ZENG G P, et al. Investigation and integrated control measure of main diseases and pests on Atractylodes macrocephala in Guizhou province from the year of 2011 to 2013 [J]. Tillag Cultivat, 2014(6): 32-34. |
| [4] |
赵来顺, 杨彦杰, 马耀辉. 白术黑斑病研究初报[J]. 植物病理学报, 1990, 20(3): 178. ZHAO L S, YANG Y J, MAO Y H. Preliminary report on the study of black spot [Alternaria alternata (FR.) Keissler] on Atraetylodes macrocephala Koidz [J]. Acta Phytopathol Sin, 1990, 20(3): 178. |
| [5] |
潘兰兰, 郑永利, 吕先真. 白术主要病害的发生及综合治理[J]. 浙江农业科学, 2006, 1(3): 315-318. PAN L L, ZHENG Y L, LV X Z. Occurrence of main diseases of Atractylodes macrocephala and comprehensive control [J]. Zhejiang Agric Sci, 2006, 1(3): 315-318. |
| [6] |
桑维钧, 练启仙, 宋宝安, 等. 贵州省白术真菌病害种类调查及防治[J]. 贵州农业科学, 2006, 34(3): 40-41. SANG W J, LIAN Q X, SONG B A, et al. Investigation of kinds of fungus diseases for Atractylodes macrocephala Koidzz and their control measures in Guizhou [J]. Guizhou Agric Sci, 2006, 34(3): 40-41. |
| [7] |
臧少先, 卢伟红, 王桂英, 等. 白术黑斑病的发病规律和防治[J]. 河北科技师范学院学报, 2005, 19(2): 46-49, 61. ZANG S X, LU W H, WANG G Y, et al. Study on the occurrence and control of black spot on Atraetylodes macrocephala Koidz [J]. J Heibei Normal Univ Sci Technol, 2005, 19(2): 46-49, 61. |
| [8] |
高微微, 张西梅, 田给林, 等. 探索中前行—中药材病害研究概况与思考[J]. 植物保护, 2016, 42(5): 15-23. GAO W W, ZHANG X M, TIAN G L, et al. Plant diseases of traditional Chinese medicines: 20 years of progress in research on understanding and management[J]. Plant Protect, 2016, 42(5): 15-23. |
| [9] |
刘亚慧, 戴德江, 沈瑶, 等. 梨黑斑病菌抗药性检测及其对啶酰菌胺的敏感性基线[J]. 农药学学报, 2015, 17(3): 274-278. LIU Y H, DAI D J, SHEN Y, et al. Detection of resistance of Alternaria kikuchiana causing pear black spot to fungicides and baseline sensitivity of A. kikuchiana to boscalid [J]. Chin J Pesti Sci, 2015, 17(3): 274-278. |
| [10] |
张传清, 张雅, 魏方林, 等. 设施蔬菜灰霉病菌对不同类型杀菌剂的抗性检测[J]. 农药学学报, 2006, 8(3): 245-249. ZHANG C Q, ZHANG Y, WEI F L, et al. Detection of resistance of Botryotinia fuckeliana from protected vegetables to different classes of fungicides [J]. Chin J Pesti Sci, 2006, 8(3): 245-249. |
| [11] |
ZHANG C Q, ZHU J W, WEI F L, et al. Sensitivity of Botrytis cinerea from greenhouse vegetables to DMIs and fenhexamid
[J]. Phytoparasitica, 2007, 35(2): 300-313. |
| [12] |
BARDAS G A, THOMS V, OLGA K, et al. Multiple resistance of Botrytis cinerea from kiwifruit to SDHIs, QoIs and fungicides of other chemical groups
[J]. Pest Managem Sci, 2010, 66(9): 967-973. DOI:10.1002/ps.v66:9 |
| [13] |
STEHMANN C, DE WAARD M A. Sensitivity of populations of Botrytis cinerea to triazoles, benomyl and vinclozolin
[J]. Eur J Plant Pathol, 1996, 102(2): 171-180. DOI:10.1007/BF01877104 |
| [14] |
SMITH C M, TRIVELLAS A E, JOHSON L E B, et al. Methods for monitoring the sensitivity of a range of fungal pathogens to benzimidazole fungicides[J]. Eppo Bull, 2010, 21(2): 336-341. |
| [15] |
陈年春. 农药生物测定技术[M]. 北京: 北京农业大学出版社, 1991: 1-270. CHEN N C. Pesticide bioassay technology[M]. Beijing: Beijing Agricultural University Press, 1991: 1-270. |
| [16] |
SMITH F D, PARKER D M, KOLLER W. Sensitivity distribution of Venturia inaequalis to the sterol demethylation inhibitor flusilazole: baseline sensitivity and implications for resistance monitoring
[J]. Phytopathology, 1991, 81(4): 392-396. DOI:10.1094/Phyto-81-392 |
| [17] |
BRENT K J, HOLLOMAN D W. Fungicide resistance in crop pathogens: how can it be managed?[M]. FRAC Monograph No 1. 2nd ed. Brussels: FRAC, 2007.
|
| [18] |
FAB Z, YANG J H, FAN F, et al. Fitness and competitive ability of Alternaria alternata field isolates with resistance to SDHI, QoI, and MBC fungicides
[J]. Plant Dis, 2015, 99(12): 1744-1750. DOI:10.1094/PDIS-03-15-0354-RE |
| [19] |
MA Z H, MICHAIDES T J. Advances in understanding molecular mechanisms of fungicide resistance and molecular detection of resistant genotypes of phytopathogenic fungi[J]. Crop Prot, 2005, 24(10): 853-863. DOI:10.1016/j.cropro.2005.01.011 |
| [20] |
GRABKE A, FERNÁNDEZ-ORTUÑO D, AMIRI A, et al. Characterization of procymidone resistance in Botrytis cinerea from strawberry and blackberry
[J]. Phytopathology, 2014, 104(4): 396-402. DOI:10.1094/PHYTO-06-13-0156-R |
| [21] |
FAIRCHILD K L, MILES T D, WHARTON P S. Assessing fungicide resistance in populations of Alternaria in Idaho potato fields
[J]. Crop Prot, 2013, 49: 31-39. DOI:10.1016/j.cropro.2013.03.003 |
| [22] |
张雅, 李红叶, 张传清, 等. 旁路氧化与设施蔬菜灰葡萄孢霉菌菌丝生长对嘧菌酯敏感性的关系[J]. 农药学学报, 2006, 8(4): 306-312. ZHANG Y, LI H Y, ZHANG C Q, et al. Relationship between alternative respiration and sensitivity of growth rate in Botrytis cinerea collected from vegetable greenhouses to azoxystrobin [J]. Chin J Pest Sci, 2006, 8(4): 306-312. |
| [23] |
NENAD T, MILOSAVLJEVIĆ A, STANISAVLJEVIĆ R, et al. Occurrence of Cercospora beticola populations resistant to benzimidazoles and demethylation-inhibiting fungicides in Serbia and their impact on disease management
[J]. Crop Prot, 2015, 75: 80-87. DOI:10.1016/j.cropro.2015.05.017 |
| [24] |
BRENT K J, HOLLOMON D W. Fungicide resistance: the assessment of risk[M]. 2nd ed. FRAC Monograph No 2, Brussels: FRAC, 2007.
|
 2018, Vol. 20
2018, Vol. 20


