2. 扬州大学 园艺与植物保护学院/农业与农产品安全国际合作联合实验室 (扬州大学),江苏 扬州 225009
2. School of Horticulture and Plant Protection, Yangzhou University/Joint International Research Laboratory of Agriculture & Agri-product Safety (Yangzhou University), Yangzhou 225009, Jiangsu Province, China
农药进入环境中后会发生一系列的移动、吸收及演变等行为,其中,在土壤-水环境中的滞留、迁移行为是影响其行为和归宿的支配要素之一,农药的持效性及降解特性都与其在土壤中的吸附-解吸附行为有关[1]。对于应用于土壤的农药来说,吸附-解吸附行为是控制其迁移及淋溶环境行为的重要因素之一[2]。有研究表明,土壤性质,如土壤有机质、阳离子交换量能通过不同的作用机制影响农药的吸附-解吸附行为[3-5]。目前国内外已有农药在土壤中的吸附和解吸附行为及机理探索的研究[6-9],并发现了土壤类型和农药理化性质对土壤中农药的附着和脱附有显著影响。
鱼藤酮属于植物源农药,对多种害虫具有极高的生物活性,是世界上公认的防治蔬菜和茶叶害虫的绿色农药[10],鱼藤酮产品在农药市场上的需求量也非常大[11-12]。但近年来有研究表明,鱼藤酮与帕金森综合症等疾病有关[13-15],对水生生物有极高的毒性[11],且对蜜蜂死亡率有一定影响[15],因此科学合理施药并加强鱼藤酮在农产品、土壤及水体中的监测尤为重要。目前有关鱼藤酮的研究重点在如何提高其在环境中的光稳定性[16-17],由鱼藤酮引起的帕金森综合症[18-23]以及鱼藤酮制剂在植物、土壤中的降解动态[24-27]等。结果表明:鱼藤酮没有挥发性[11],在土壤中的降解动态符合一级动力学方程,土壤性质、环境温度是影响其降解半衰期的最关键因素,在自然土壤中的降解半衰期为1.98~2.76 d[24-27]。目前,鱼藤酮在土壤环境中的吸附和解吸附行为尚未见报道,故笔者对该特性进行了研究,旨在为鱼藤酮在土壤中的环境风险评估提供理论依据。
1 材料与方法 1.1 仪器与药剂L-2000型高效液相色谱仪,日本Hitachi公司;QYC-200型恒温培养摇床,福玛仪器有限公司;BS210S型电子天平 (精确至0.000 1 g),德国Sartorius公司;H/T-16MM型台式高速离心机,湖南赫西仪器装备有限公司;ProElut-NH2固相萃取柱 (1 g/6 mL),迪马科技有限公司。
鱼藤酮 (rotenone) 标准品 (纯度为98.0%),美国Sigma-Aldrich公司。乙腈 (色谱纯),美国Tedia公司;无水氯化钙和叠氮化钠 (NaN3,分析纯),国药集团化学试剂有限公司;试验用水均由Milli-Q超纯水净化器制备。
1.2 供试土壤3种供试土壤样品分别采自山东省聊城市、江苏省南京市和江西省萍乡市,样品取自0~20 cm土层,经自然风干及过0.2 mm筛后备用。土壤类型依次为砂壤土、黏壤土及壤土,土壤性质见表1。
|
|
表 1 供试土壤的基本理化性质 Table 1 The basic physical and chemical properties of the tested soils |
1.3 试验方法 1.3.1 标准储备溶液配制
准确称取鱼藤酮标准品0.01 g(精确至0.000 1 g),用甲醇溶解并定容至100 mL,配制成100.0 mg/L的鱼藤酮标准储备溶液,置于冰箱 (4 ℃) 避光保存,备用。
1.3.2 土壤溶液比的优化分别称取1.0、2.5和5.0 g供试土壤于50 mL锥形瓶中,将鱼藤酮标准储备溶液用0.01 mol/L的CaCl2水溶液稀释至0.50 mg/L后,取25 mL加入上述锥形瓶中,并加入少量NaN3,加盖密封后于恒温振荡器上避光振荡48 h,转速为200 r/min,温度控制在25 ℃ ± 0.1 ℃。每处理重复3次。振荡后再以6 000 r/min的转速离心8 min,取上清液5 mL经0.22 μm的微孔滤膜过滤。采用高效液相色谱 (HPLC) 法分析上清液中鱼藤酮的浓度。
1.3.3 鱼藤酮在土壤中添加回收试验分别称取2.5 g供试土壤,置于50 mL锥形瓶中,加入一定量的鱼藤酮标准溶液,添加水平分别为0.1、0.5和2 mg/kg。同时设置空白对照,每处理重复6次。采用HPLC法检测分析,计算添加回收率及相对标准偏差。
1.3.4 吸附动力学试验分别称取2.5 g供试土壤,置于50 mL锥形瓶中,加入25 mL含有1 mg/L鱼藤酮的0.01 mol/L CaCl2水溶液,加入少量NaN3,加盖密封后于在恒温振荡器上避光振荡,转速为200 r/min,温度控制在25 ℃ ± 1 ℃。按照平行法,吸附时间分别设定为0、2、4、6、8、12、16、24、36和48 h,每个处理重复3次。振荡后以6 000 r/min的转速离心8 min,取上清液5 mL经0.22 μm的微孔滤膜过滤。采用HPLC法分析上清液中鱼藤酮的浓度。
1.3.5 吸附-解吸附等温试验分别称取2.5 g供试土壤,置于50 mL锥形瓶中,分别加入25 mL含有0.10、0.20、0.50、1.00和2.00 mg/L鱼藤酮的0.01 mol/L CaCl2水溶液,加入少量的NaN3后于在恒温振荡器上避光振荡24 h,转速为200 r/min,温度控制在25 ℃ ± 1 ℃,每个处理重复3次。再以6 000 r/min的转速离心8 min,取上清液5 mL经0.22 μm的微孔滤膜过滤,检测分析上清液中鱼藤酮的浓度。随后,弃去上层清液,加入等体积0.01 mol/L的CaCl2水溶液及少量NaN3,经过恒温振荡平衡后,采用HPLC法分析上清液中鱼藤酮的浓度。
1.3.6 不同温度对鱼藤酮在土壤中吸附行为的影响分别称取2.5 g供试土壤,置于50 mL玻璃锥形瓶中,加入25 mL含有0.10、0.20、0.50、1.00和2.00 mg/L鱼藤酮的0.01 mol/L CaCl2水溶液,加入少量的NaN3后于在恒温振荡器上避光振荡24 h,转速为200 r/min,分别设置振荡温度为15 ℃、25 ℃、35 ℃ (± 0.1 ℃),经过恒温振荡平衡后,采用HPLC法分析上清液中鱼藤酮的浓度。
1.4 HPLC分析方法 1.4.1 样品前处理方法采用固相萃取法净化样品。NH2固相萃取柱中,依次加入5 mL V(二氯甲烷) : V(乙酸乙酯) = 1 : 1混合溶液,进行活化。加入5 mL待测样品,分别用5 mLV(二氯甲烷) : V(乙酸乙酯) = 1 : 1混合溶液淋洗2次,最后用10 mL二氯甲烷洗脱,收集洗脱液,用氮气吹干,再用1 mL色谱级乙腈溶解,过0.22 μm有机相滤膜,待HPLC检测分析。
1.4.2 鱼藤酮的检测分析参考文献[16-17]进行。检测条件为:Agilent Eclipse Plus C18色谱柱 (4.6 mm × 150 mm,5 μm);检测波长297 nm;柱温25 ℃;进样量10 μL;流速1 mL/min;流动相为V(乙腈) : V(水) = 70 : 30。
1.5 数据分析 1.5.1 准二级动力学方程鱼藤酮在土壤中的吸附动力学曲线采用准二级动力学方程拟合[28],见 (1) 式。
| $\frac{t}{{q_t}} = \frac{1}{{{k_2}q_{\rm{e}}^2}} + \frac{t}{{q_{\rm e}}}$ | (1) |
其中:qe为鱼藤酮在土壤中的吸附量 (mg/kg);qt为t时刻鱼藤酮在土壤中的吸附量 (mg/kg);k2为准二级吸附率常数 [kg/(mg·min)]。
1.5.2 Freundlich方程鱼藤酮在土壤中的吸附作用采用Freundlich模型进行拟合回归[29],见 (2) 式和 (3) 式。
| ${C_{\rm{s}}} = {K_{\rm{f}}}{C_{{\rm{aq}}}}^{1/n}$ | (2) |
| ${\rm{log}}{C_{\rm s}} = {\rm{log}}{K_{\rm f}} + 1/n{\rm{log}}{C_{\rm {aq}}}$ | (3) |
式中,Cs为吸附或解吸附平衡时土壤中鱼藤酮的吸附量 (mg/kg);Caq为吸附或解吸附平衡时鱼藤酮的质量浓度 (mg/L);Kf、n为Freundlich常数 (吸附过程分别设为Kf-ads及nads,解吸附过程分别设为Kf-des及ndes)。Kf也可与土壤中有机碳含量 (%OC) 及有机质含量 (%OM) 进行换算,得到有机碳吸附常数 (KOC) 及有机质吸附常数 (KOM),换算公式见 (4) 和 (5)[30]。
| ${K_{{\rm{OC}}}} = {K_{\rm{f}}}/\text{%} {\rm{OC}} \times 100$ | (4) |
| ${K_{{\rm{OM}}}} = {K_{\rm{f}}}/\text{%} {\rm{OM}} \times 100$ | (5) |
运用吉布斯自由能方程分析温度对鱼藤酮吸附行为的影响,见 (6) 式[31]。
| $\Delta G = - {\rm{R}}T{K_{{\rm{OM}}}}$ | (6) |
式中,T为绝对温度 (K);R为气体摩尔常数 [8.314 J/(K·mol)];△G(kJ/mol) 为吉布斯自由能。
1.5.4 滞后系数 (H)鱼藤酮在土壤中是否存在滞后现象可用滞后系数 (H) 描述,其公式见 (7)式[32]。
| $H = {n_{{\rm{des}}}}/{n_{{\rm{ads}}}}$ | (4) |
式中,nads和ndes分别为吸附和解吸附的Freundlich常数。
2 结果与分析 2.1 鱼藤酮在3种土壤中的添加回收率在0.1~2 mg/kg范围的3个添加水平下,鱼藤酮在3种土壤中的添加回收率范围为83%~94%,相对标准偏差范围为1.2%~4.6%,符合农药残留分析要求[33](表2)。
|
|
表 2 鱼藤酮在3种不同土壤中的添加回收率及相对标准偏差 Table 2 Recoveries and relative standard deviation (RSD) of rotenone in three different soils |
2.2 土壤溶液比的选择
优化结果 (表3) 表明:当土壤质量(g)与溶液(用CaCl2水溶液稀释至0.50 mg/L的鱼藤酮母液)体积(mL)比为1 : 5时,砂壤土及黏壤土对鱼藤酮的吸附率均高于80%,吸附力太强;而当土壤溶液比为1 : 25时,壤土对鱼藤酮的吸附能力又过低,其吸附率仅为15%。综合考虑,本研究均选择1 : 10作为试验的土壤溶液比。
|
|
表 3 不同土壤溶液比例下鱼藤酮在3种土壤中的吸附率 (n = 3) Table 3 Adsorption rates of rotenone in three different soils with different soil/solution ratios (n = 3) |
2.3 鱼藤酮在3种土壤中的吸附动态
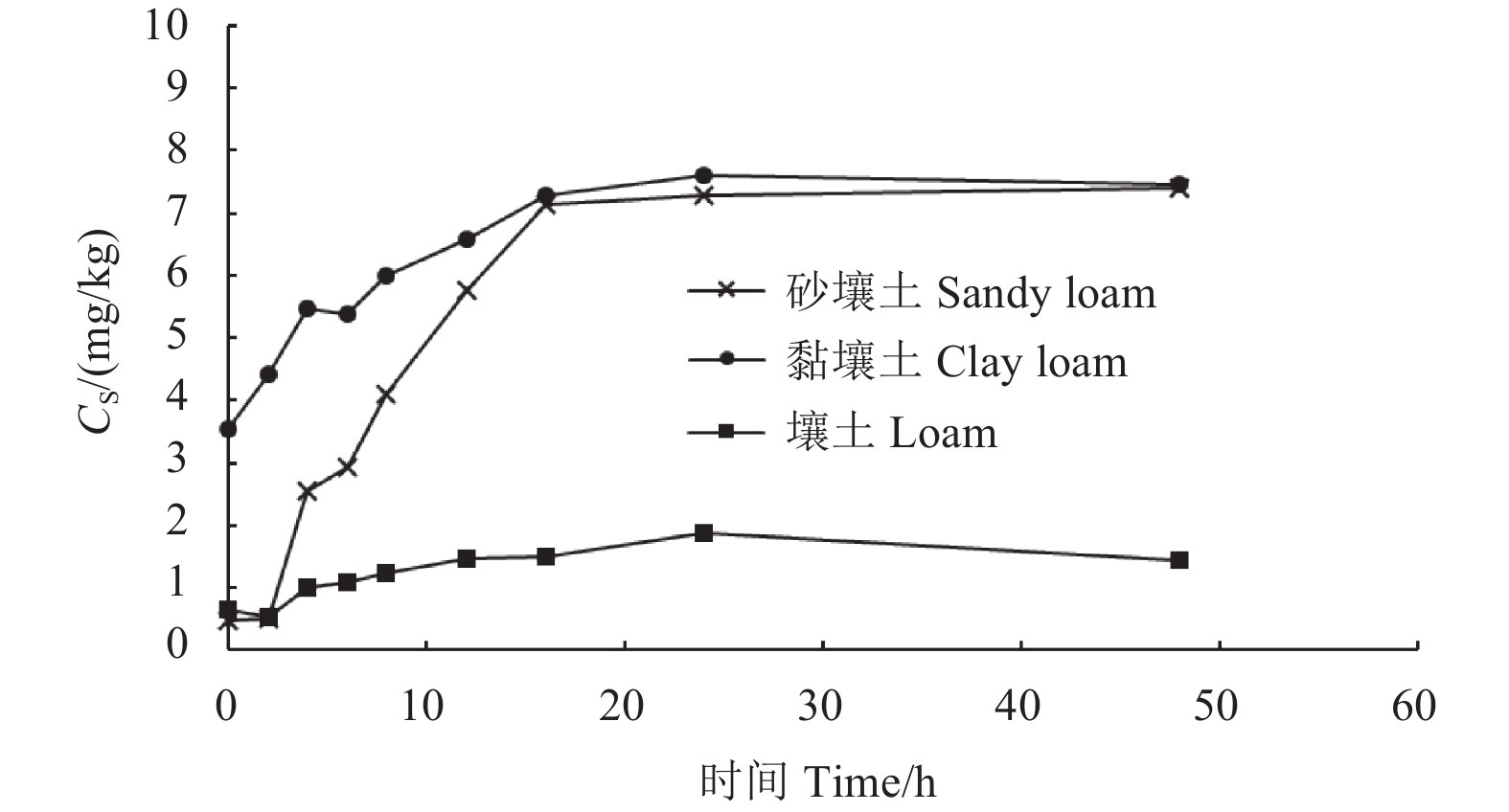
鱼藤酮在3种土壤中的吸附量随时间的变化趋势见图1。由图1可知,鱼藤酮在3种土壤中的吸附率呈先快速上升后缓慢趋于稳定的态势,在0~10 h内快速上升后慢慢变缓,至24 h时吸附量分别稳定在7.59、7.28和1.89 mg/kg。综合考虑,本研究选择以24 h为吸附平衡时间。采用准二级动力学模型进行拟合分析。结果(表4)表明:该模型能较好地拟合鱼藤酮在3种供试土壤中的吸附动力学曲线,其R2分别为0.945 5、0.996 7及0.973 7,进一步说明土壤对鱼藤酮的吸附能力取决于供试土壤表面的吸附位点。
|
图 1 鱼藤酮在3种不同土壤中的吸附动力学曲线 Fig. 1 Adsorption kinetics curves of rotenone in three different soils |
|
|
表 4 鱼藤酮在3种不同土壤中的准二级动力学拟合参数 Table 4 Pseudo-second-order kinetics of rotenone in three different soils |
2.4 鱼藤酮在3种土壤中的吸附行为
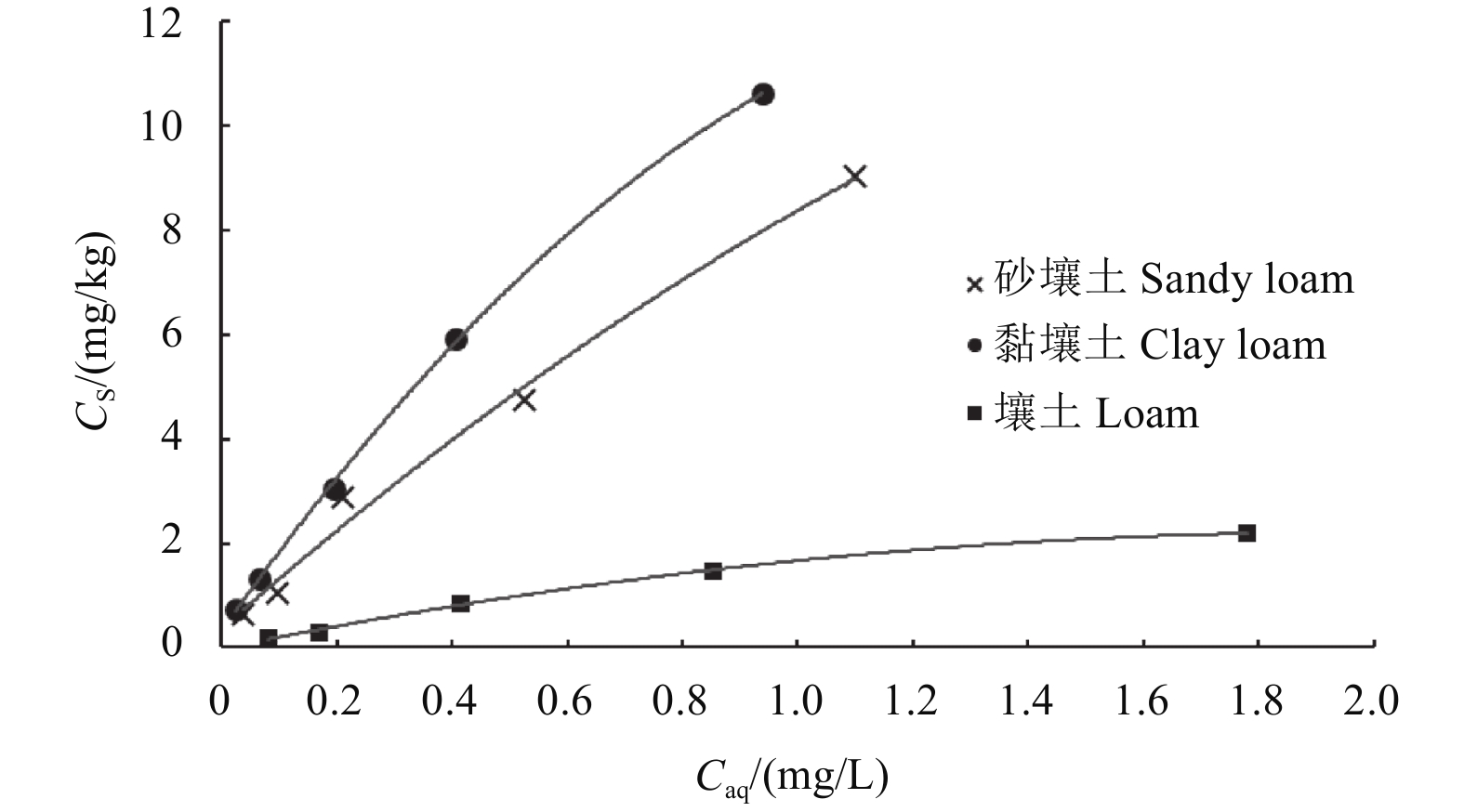
本研究采用Freundlich吸附模型进行拟合 (图2),建立了实际吸附率及吸附模型之间的数学模型参数 (表5)。从吸附数据分析,Freundlich吸附模型能较好地拟合鱼藤酮在3种土壤中的吸附行为,R2均值为0.983 6。3种土壤的Kf-ads值分别为8.25、11.39和1.52,表明黏壤土对鱼藤酮的吸附率最强,其次为砂壤土,而壤土的吸附率最弱。3种土壤的1/nasd值均小于1,表明3种土壤对鱼藤酮的吸附等温线均为非线性,属于L型吸附等温线。本研究结果表明,鱼藤酮在较低浓度下与这3种土壤的亲和力较强,但随着鱼藤酮质量浓度的升高,土壤对其亲和力逐渐降低。
由表5数据还可以看出:3种土壤的KOC值分别为982、1 017和219。参照McCall等报道的有机物在土壤中移动性的分类标准:当KOC的值在0~50范围时,化合物的移动性最强;KOC在50~150时,化合物的移动性强;KOC在150~500时,移动性中等;KOC在500~2 000时,移动性弱;KOC在2 000~5 000时,移动性很弱;KOC > 5 000时,不移动 [28]。本研究中鱼藤酮在砂壤土及黏壤土中的移动性匀在移动性弱范围内,而在壤土中属于移动性中等,此研究结果与前文鱼藤酮在土壤中吸附率强弱结果相符合[34]。
|
图 2 鱼藤酮在3种不同土壤中的吸附等温线 Fig. 2 Adsorption isotherm of rotenone in three different soils |
|
|
表 5 鱼藤酮在3种不同土壤中的吸附参数 Table 5 Adsorption parameters of rotenone in three different soils |
2.5 不同温度对鱼藤酮在土壤中吸附行为的影响
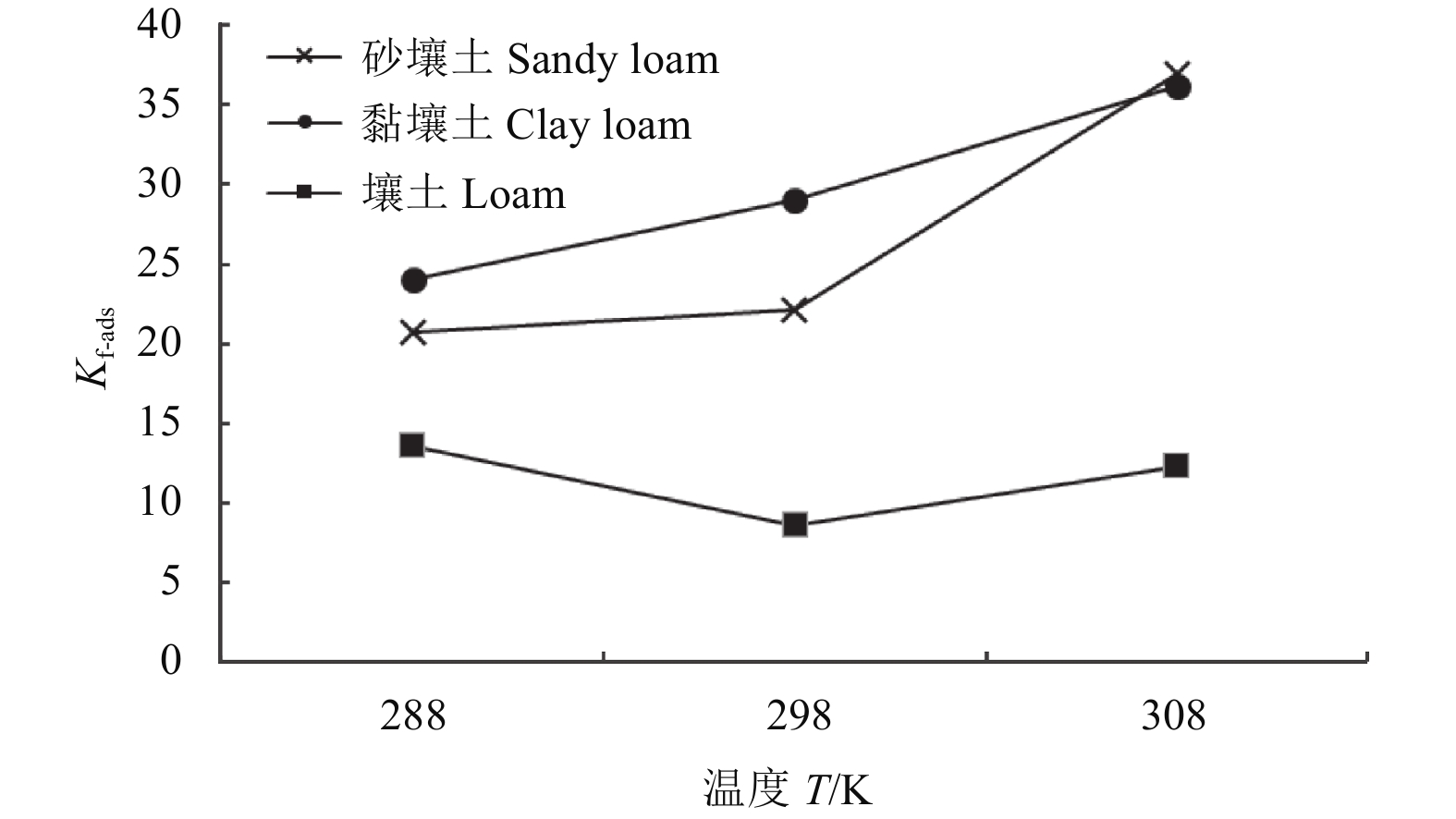
吉布斯自由能 (ΔG) 是一种化学反应过程自发性的重要参数,在恒温恒压且非体积功为0的条件下,系统ΔG < 0说明吸附过程能够自发进行,ΔG = 0时说明处于平衡状态,ΔG > 0则表明吸附过程不能进行 [34]。从表6数据分析,鱼藤酮在土壤中的ΔG均 < 0,表明土壤对鱼藤酮的吸附过程都是自发进行。根据不同温度下土壤对鱼藤酮的吸附情况 ( 图3) 可以看出:吸附平衡时,除壤土外,砂壤土及黏壤土随温度的升高吸附率均呈上升趋势,说明温度的升高能促进土壤对鱼藤酮的吸附,而壤土可能存在物理吸附及化学吸附共存的不稳定状态[35],从而出现随着温度的升高吸附率先下降后升高的趋势。
|
图 3 温度对3种不同土壤吸附鱼藤酮的影响 Fig. 3 Effect of temperature on the adsorption of rotenone in the three different soils |
|
|
表 6 鱼藤酮在3种土壤中的吸附常数及吸附自由能 Table 6 Adsorption free energy and Kf-ads of rotenone in three different soils |
2.6 鱼藤酮在3种土壤中的解吸附行为
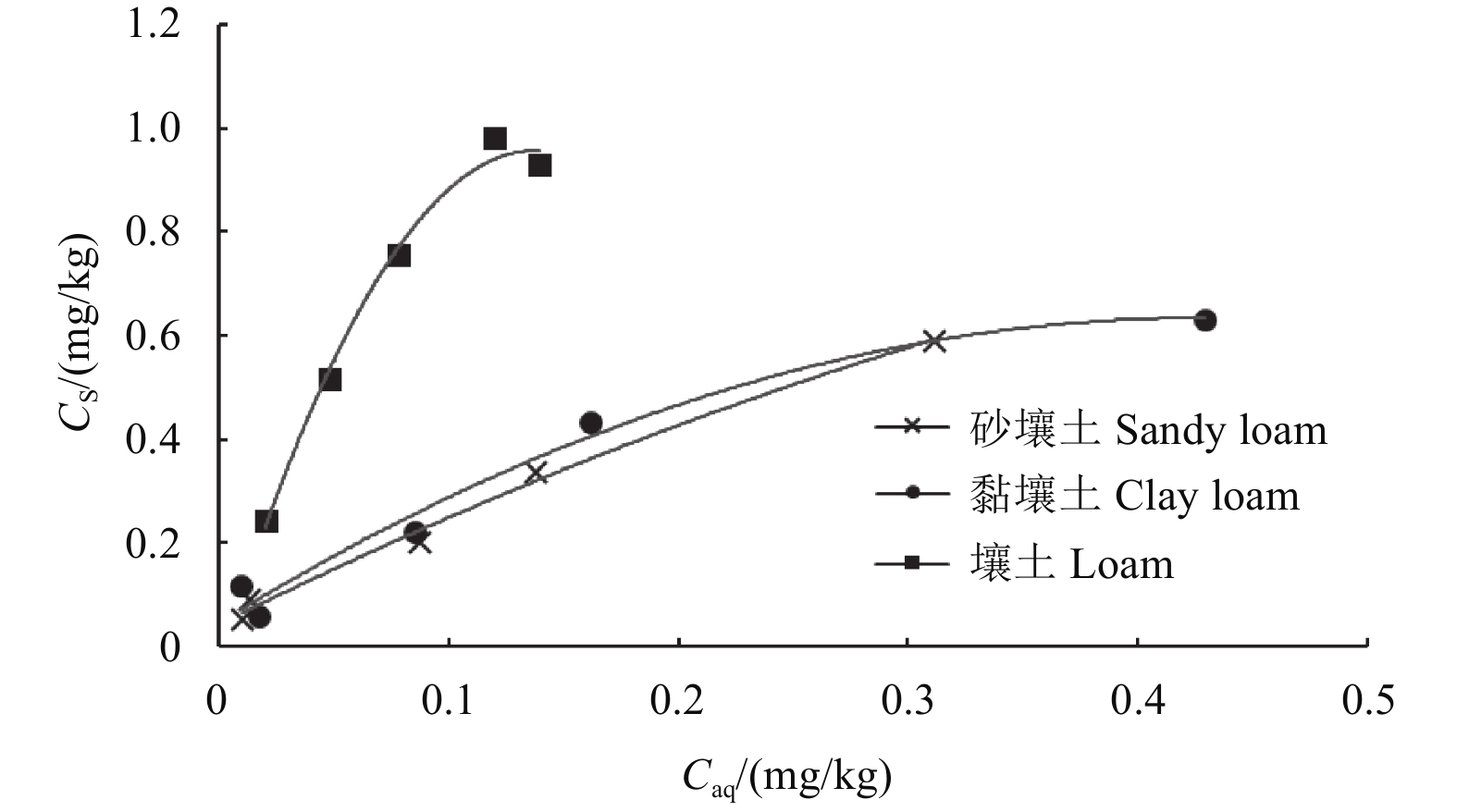
鱼藤酮在土壤中的解吸附过程符合Freundlich模型,R2在0.946 8~0.972 0之间 (图4)。3种土壤的Kf-des值分别为1.02、1.18及4.55(表7),表明鱼藤酮在壤土中的解吸附能力最强。农药的解吸附过程决定了其在土壤中的流动和释放行为。H (滞后系数) 为不可逆吸附程度指标,当0.7 < H ≤ 1.0时,说明解吸附速度和吸附速度相似,无滞后作用;当H小于0.7时,解吸附速度小于吸附速度,为正滞后作用;当H > 1.0时,为负滞后作用 [36]。由表7可知,鱼藤酮在砂壤土及黏壤土中有正迟滞作用,而在壤土中无滞后作用。这说明鱼藤酮不易从砂壤土及黏壤土中解吸附出来,但在壤土中容易被解吸附。
|
图 4 鱼藤酮在3种土壤中的解吸附等温线 Fig. 4 Desorption isotherm of rotenone in three different soils |
|
|
表 7 鱼藤酮在3种土壤中的解吸附参数 Table 7 Desorption parameters of rotenone in three different soils |
2.7 土壤性质与土壤对鱼藤酮吸附的相关分析
氢键、共价键、离子键和范德华力等是土壤-水环境对农药产生吸附行为的主要作用力,而其在不同性质的土壤中有明显差异[1]。通过Freundlich吸附模型参数值与各性质参数进行线性分析(表8)发现,在吸附过程中,Kf-ads值与土壤有机质及有机碳含量呈显著正相关。说明鱼藤酮在土壤中的吸附过程可能与土壤中有机质及有机碳含量相关。对阳离子交换量的数据进行分析,发现吸附相关方程R2仅为0.498 2,表明鱼藤酮在土壤中的吸附和解吸附特性与阳离子交换量无明显相关性。从理化性质与Kf-des值相关性分析,单个因子与Kf-des值的相关性均不显著,说明pH值、有机碳质量分数、有机质质量分数及阳离子交换量不是影响鱼藤酮在土壤中的解吸附过程的主要因素。
|
|
表 8 鱼藤酮在土壤中的Kf和土壤理化性质的相关性 Table 8 Correlation between physical and chemical properties and Kf value for rotenone in soils |
3 结论
本研究结果表明:鱼藤酮在3种土壤中的吸附-解吸附行为符合Freundlich方程,吸附能力依次为黏壤土 > 砂壤土 > 壤土,而解吸附能力依次为壤土 > 黏壤土 > 砂壤土。温度与鱼藤酮在土壤中的吸附行为成正相关,而有机质及有机碳可能直接影响鱼藤酮的吸附-解吸附行为,另外,从有机碳吸附常数 ( KOC) 分析,鱼藤酮在黏壤土、砂壤土中移动性较弱,而在壤土中移动性较强。
目前,关于鱼藤酮在土壤中的吸附和解吸附行为尚未见报道,但鱼藤酮在土壤中的降解行为已有相关报道,并指出土壤性质、环境温度与其降解半衰期紧密相关[24-27]。土壤是一个多组分非均质的混合物,进入土壤环境的农药可以通过物理吸附、化学吸附、氢键结合和配位价键结合等形式吸附在介质表面,因此可很大程度地影响农药的环境行为[37-38]。本研究通过Freundlich吸附模型对鱼藤酮在土壤中的吸附-解吸附行为进行拟合,发现鱼藤酮在较低浓度下与3种供试土壤均具有较强的亲和力,而在较高浓度下鱼与3种土壤的亲和力明显下降。同时,农药的解吸附过程也很重要,它决定了农药在土壤中的释放速率和潜在的流动性。解吸附率较低的农药对连作作物具有较高的风险。此外,解吸附是考察农药污染土壤的重要因素之一。由Freundlich模型对鱼藤酮的解吸附行为进行拟合,同时分析其吸附自由能及滞后系数发现,鱼藤酮在黏壤土和砂壤土中有正迟滞现象,而在壤土中无迟滞现象。本研究可为鱼藤酮的合理使用及土壤修复提供一定的理论依据。
| [1] |
刘维屏. 农药环境化学[M]. 北京: 化学工业出版社, 2006: 165-195.
LIU W P. Pesticide environmental chemistry[M]. Beijing: Chemical Industry Press, 2006: 165-195. |
| [2] | TANG Z W, ZHANG W, CHEN Y M. Adsorption and desorption characteristics of monosulfuron in Chinese soils[J]. J Hazard Mater, 2009, 166(2-3): 1351–1356. doi:10.1016/j.jhazmat.2008.12.052 |
| [3] | SHENG Q, HENG Z, XIONG B L, et al. Adsorption and desorption characteristics of endosulfan in two typical agricultural soils in Southwest China[J]. Environ Sci Pollut Res, 2017, 24(12): 11493–11503. doi:10.1007/s11356-017-8800-4 |
| [4] | LSMAIL B S, CHOO L Y, SALMIJAH S, et al. Adsorption, desorption and mobility of cyfluthrin in three Malaysian tropical soils of different textures[J]. J Environ Biol, 2015, 36(5): 1105–1111. |
| [5] | BENITO P, BORTOLOTTI V, FORNASARI G, et al. Evaluation of effect of soil organic matter on pores by H-1 time-domain magnetic resonance relaxometry and adsorption-desorption of N-2[J]. Eur J Soil Sci, 2016, 67(3): 314–323. doi:10.1111/ejss.2016.67.issue-3 |
| [6] | LIU Y H, XU Z Z, WU X G, et al. Adsorption and desorption behavior of herbicide diuron on various Chinese cultivated soils[J]. J Hazard Mater, 2010, 178(1-3): 462–468. doi:10.1016/j.jhazmat.2010.01.105 |
| [7] | DENG J C, JIANG X, HU W P, et al. Quantifying hysteresis of atrazine desorption from a sandy loam soil[J]. J Environ Sci, 2010, 22(12): 1923–1929. doi:10.1016/S1001-0742(09)60340-5 |
| [8] | DORETTO K M, PERUCHI L M, RATH S. Sorption and desorption of sulfadimethoxine, sulfaquinoxaline and sulfamethazine antimicrobials in Brazilian soils[J]. Sci Total Environ, 2014, 476-477: 406–414. doi:10.1016/j.scitotenv.2014.01.024 |
| [9] |
李昉泽, 冯丹, 邓惠, 等. 阿特拉津在 5 种农业土壤中的吸附解吸特性分析[J]. 生态环境学报, 2015, 24(12): 2056–2061.
LI F Z, FENG D, DENG H, et al. Adsorption and desorption of atrazine in five agriculture soils[J]. Ecol Environ Sci, 2015, 24(12): 2056–2061. |
| [10] | ISMAN M B. Botanical insecticides, deterrents, and repellents in modern agriculture and an increasingly regulated world[J]. Ann Rev Entomol, 2006, 51(1): 45–66. doi:10.1146/annurev.ento.51.110104.151146 |
| [11] |
徐汉虹. 杀虫植物与植物性杀虫剂[M]. 北京: 中国农业出版社, 2001: 276-309.
XU H H. Insecticidal plants and botanical insecticides[M]. Beijing: China Agriculture Press, 2001: 276-309. |
| [12] |
张兴, 马志卿, 李广泽, 等. 生物农药评述[J]. 西北农林科技大学学报(自然科学版), 2002, 30(2): 142–148.
ZHANG X, MA Z Q, LI G Z, et al. A review of biopesticide[J]. J Northwest Agric For Univ (Nat Sci Ed), 2002, 30(2): 142–148. |
| [13] | BETARBET R, SHERER T B, MACKENZIE G, et al. Chronic systemic pesticide exposure reproduces features of Parkinson’s disease[J]. Nat Neurosci, 2000, 3(12): 1301–1306. doi:10.1038/81834 |
| [14] | CABONI P, SHERER T B, ZHANG N J, et al. Rotenone, deguelin, their metabolites, and the rat model of parkinson’s disease[J]. Chem Res Toxicol, 2004, 17(11): 1540–1548. doi:10.1021/tx049867r |
| [15] | ALEŠ G, MAJA I S Š. Toxicological and immunohistochemical testing of honeybees after oxalic acid and rotenone treatments[J]. Apidologie, 2007, 38(3): 296–305. doi:10.1051/apido:2007014 |
| [16] | CHEN X J, XU H H, YANG W, et al. Research on the effect of photoprotectants on photostabilization of rotenone[J]. J Photochem Photobiol B: Biol, 2009, 95(2): 93–100. doi:10.1016/j.jphotobiol.2009.01.003 |
| [17] | CHEN X J, MENG Z Y, REN Y J, et al. Effects of ZnO nanoparticle on photo-protection and insecticidal synergism of rotenone[J]. J Agric Sci, 2016, 8(2): 38–45. |
| [18] | KUANG L H, CAO X B, LU Z N. Baicalein protects against rotenone-induced neurotoxicity through induction of autophagy[J]. Biolog Pharmaceut Bull, 2017, 40(9): 1537–1543. doi:10.1248/bpb.b17-00392 |
| [19] | MICHEL H E, TADROS M G, ESMAT A, et al. Tetramethylpyrazine ameliorates rotenone-induced parkinson’s disease in rats: involvement of its anti-inflammatory and anti-apoptotic actions[J]. Mol Neurobiol, 2017, 54(7): 4866–4878. doi:10.1007/s12035-016-0028-7 |
| [20] | JAGOTA A, MATTAM U. Daily chronomics of proteomic profile in aging and rotenone-induced parkinson’s disease model in male Wistar rat and its modulation by melatonin[J]. Biogerontology, 2017, 18(4): 615–630. doi:10.1007/s10522-017-9711-y |
| [21] | BADAWI G A, ABD EL FATTAH M A, ZAKI HALA F, et al. Sitagliptin and liraglutide reversed nigrostriatal degeneration of rodent brain in rotenone-induced parkinson’s disease[J]. Inflammopharmacology, 2017, 25(3): 369–382. doi:10.1007/s10787-017-0331-6 |
| [22] | MADIHA S, TABASSUM S, BATOOL Z, et al. Assessment of gait dynamics in rotenone-induced rat model of parkinson’s disease by footprint method[J]. Pak J Pharm Sci, 2017, 30(3S): 943–948. |
| [23] | ANUSHA C, SUMATHI T, JOSEPH L D. Protective role of apigenin on rotenone induced rat model of Parkinson’s disease: suppression of neuroinflammation and oxidative stress mediated apoptosis[J]. Chem-Biol Interact, 2017, 269: 67–79. doi:10.1016/j.cbi.2017.03.016 |
| [24] | CAVOSKI I, CABONI P, SARAIS G, et al. Photodegradation of rotenone in soils under environmental conditions[J]. J Agric Food Chem, 2007, 55(17): 7069–7074. doi:10.1021/jf0708239 |
| [25] | CAVOSKI I, CABONI P, SARAIS G, et al. Degradation and persistence of rotenone in soils and influence of temperature variations[J]. J Agric Food Chem, 2008, 56(17): 8066–8073. doi:10.1021/jf801461h |
| [26] | ZHOU Y, ZHANG N, WANG K, et al. Dissipation and residue of rotenone in cabbage and soil under field conditions[J]. Bull Environ Contaminat Toxicol, 2013, 91(2): 251–255. doi:10.1007/s00128-013-1040-5 |
| [27] | ZHOU Y, WANG K, YAN C, et al. Effect of two formulations on the decline curves and residue levels of rotenone in cabbage and soil under field conditions[J]. Ecotoxicol Environ Safety, 2014, 104: 23–27. doi:10.1016/j.ecoenv.2014.02.014 |
| [28] | HO Y S, MCKAY G. Pseudo-second order model for sorption processes[J]. Process Biochem, 1999, 34(5): 451–465. doi:10.1016/S0032-9592(98)00112-5 |
| [29] |
李克斌, 刘维屏, 周瑛, 等. 灭草松在土壤中吸附的支配因素[J]. 环境科学, 2003, 24(1): 126–130.
LI K B, LIU W P, ZHOU Y, et al. Factors dominating the sorption of bentazon in soils[J]. Environ Sci, 2003, 24(1): 126–130. |
| [30] |
张伟, 王进军, 张忠明, 等. 烟嘧磺隆在土壤中的吸附及与土壤性质的相关性研究[J]. 农药学学报, 2006, 8(3): 265–271.
ZHANG W, WANG J J, ZHANG Z M, et al. Adsorption of nicosulfuron on soils and its correlation with soil properties[J]. Chin J Pestic Sci, 2006, 8(3): 265–271. |
| [31] |
王琪全, 刘维屏. 除草剂灭草烟在土壤中的吸附、脱附[J]. 中国环境科学, 1998, 18(4): 314–318.
WANG Q Q, LIU W P. Adsorption and desorption of herbicide imazapyr by soil[J]. China Environ Sci, 1998, 18(4): 314–318. |
| [32] | COX L, KOSKINEN W C, YEN P Y. Sorption-desorption of imidacloprid and its metabolites in soils[J]. J Agric Food Chem, 1997, 45(4): 1468–1472. doi:10.1021/jf960514a |
| [33] |
农药残留试验准则: NY/T 788–2004[S]. 北京: 中国农业出版社, 2004: 5.
Guideline on pesticide residue trials: NY/T 788–2004[S]. Beijing: China Agricultural Press, 2004: 5 |
| [34] | McCALL P J, LASKOWSKI D A, SWANN R L. Test protocols for environmental fate and movement of toxicants[C]//Proceedings of 94th AOAC meeting. Washington DC: Association of Official Analytical Chemists, 1980: 89-109. |
| [35] |
胡英. 物理化学[M]. 2版. 北京: 高等教育出版社, 2014.
HU Y. Physical chemistry[M]. 2nd ed. Beijing: Higher Education Press, 2014. |
| [36] | BARRIUSO E, LAIRE D A, KOSKINEN W C, et al. Atrazine desorption from smectities[J]. Soil Sci Soc Am J, 1994, 58(6): 1632–1638. doi:10.2136/sssaj1994.03615995005800060008x |
| [37] |
姚斌, 徐建民, 张超兰. 除草剂丁草胺的环境行为综述[J]. 生态环境, 2003, 12(1): 66–70.
YAO B, XU J M, ZHANG C L. Behavior of herbicide butachlor in environment[J]. Ecol Environ, 2003, 12(1): 66–70. |
| [38] |
谢显传, 张少华, 王冬生, 等. 阿维菌素土壤吸附特性研究[J]. 中国农业科学, 2007, 40(9): 1959–1963.
XIE X C, ZHANG S H, WANG D S, et al. Adsorption of abamectin in soil[J]. Scienti Agricultura Sinica, 2007, 40(9): 1959–1963. |
 2018, Vol. 20
2018, Vol. 20


