近年来,关于植物韧皮部输导性农药的研究越来越受到关注[1-6]。改善农药在植物韧皮部的输导性,使其具有向下输导的能力,不但可以使农药通过叶面施药防治植物维管束和根部病虫害,解决维管束和根部病虫害难以防治的问题,还可以减轻施药难度和降低施药量[1]。但目前具有韧皮部输导性的农药还比较少,杀菌剂如:甲霜灵、吡氯灵等,除草剂如草甘膦、禾草灵等,而且很多因为长期使用已经出现严重的抗药性[7]。因此,具有植物韧皮部输导性新农药的研究与开发在当前发展“绿色农药”的背景下显得尤为重要。
吩嗪-1-羧酸 (phenazine-1-carboxylic acid, PCA, 1) 和吩嗪-1-甲酰肼 (phenazine-1-carbohydrazide) 作为重要的微生物代谢产物在假单胞菌属 (Pseudomonads) 和链霉菌属 (Streptomycetes) 等微生物分泌物中广泛存在,具有广谱的医用杀菌活性、抗肺癌和白血病活性[8-12],并对水稻纹枯病、西瓜枯萎病、辣椒疫病等病原菌具有广谱性农用抗菌活性[13-19]。吩嗪-1-羧酸已经国家农药定名委员会正式定名为申嗪霉素,已登记用于防治水稻纹枯病[20-22]。但吩嗪-1-羧酸和吩嗪-1-甲酰肼均没有韧皮部输导性[23]。
马来酰肼 (7) 在植物韧皮部具有良好输导性[24],将马来酰肼注入蓖麻的空心叶柄 60 min 后,可以在注射点以下 17 cm 处的韧皮部中检测到马来酰肼[25]。马来酰肼的主要官能团是双酰肼结构,含有该结构的化合物具有广泛的生物活性[26-27]。毛武涛等[28]设计合成的 5-甲基-1,2,3-噻二唑-N-叔丁基双酰肼类化合物 (8),部分化合物具有较好的杀菌活性和诱导抗病活性。马献力等[29]合成了樟脑酸基双酰肼类化合物 (9),部分化合物在 50 mg/L 下对苹果轮纹病菌的抑制率高达 96.3%,优于阳性对照嘧菌酯。
为发现具有更好杀菌活性,同时改善其在植物韧皮部的输导性,笔者以具有抑菌活性的吩嗪-1-羧酸和具有韧皮部输导性的马来酰肼为先导化合物,将马来酰肼中的双酰肼结构引入到吩嗪-1-羧酸中,设计、合成了 17 个新化合物,并初步测定了其杀菌活性和植物韧皮部输导性。目标化合物的合成路线见图式 1 。
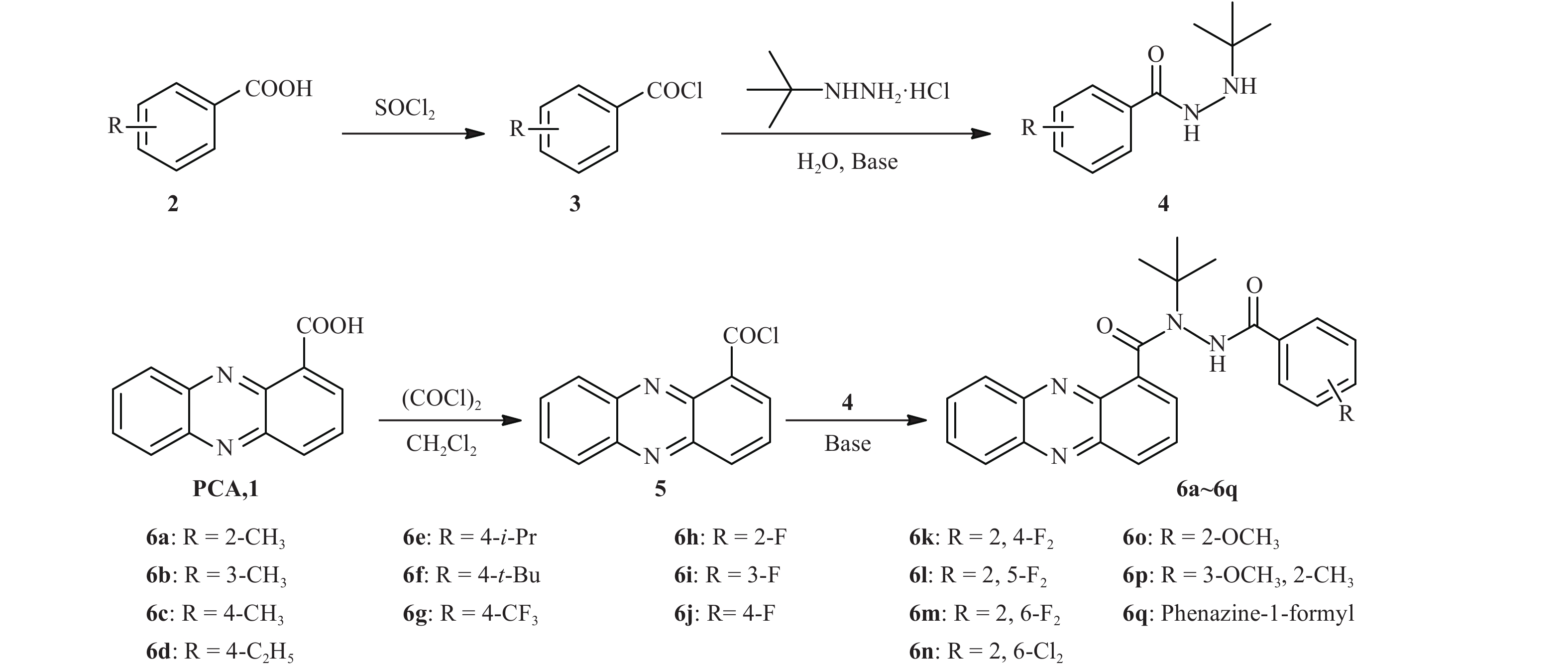
|
图式 1 目标物的合成路线 Scheme1 Synthetic route of target compounds |
1 实验部分 1.1 试剂与仪器
Yanagimoto MFG.熔点测定仪 (温度计未校正);Bruker Avance DPX400 核磁共振仪 (以 TMS 为内标,CDCl3 或 DMSO-d6 为溶剂);X’Pert PRO XRD 单晶 X-射线衍射仪,Bruker APEX IV 傅立叶变换高分辨质谱仪。柱层析硅胶 (筛孔径 50~75 μm) 和薄层层析硅胶板均为青岛海洋化工有限公司生产;试剂均为市售分析纯或化学纯,除特别注明外,未经进一步处理。
1.2 化合物的合成1.2.1 取代苯基甲酰氯 (3) 的合成 参考文献[30]方法。向单口瓶中加入 15.0 mmol 取代苯甲酸 (2),搅拌下缓慢滴加 15 mL 二氯亚砜,加热回流至固体消失,继续回流反应 2~3 h。脱去二氯亚砜,用少量甲苯溶解,再次脱去溶剂。用少量甲苯溶解,用于下步反应。
1.2.2 N-叔丁基-N′-取代苯基甲酰肼 (4) 的合成 参考文献[30]方法。向 100 mL 三口瓶中加入质量分数为 20% 的氢氧化钠溶液 4.20 g (21.0 mmol),冰水浴冷却至 0~5 ℃,分批加入叔丁基肼盐酸盐 2.60 g (21.0 mmol) 和二氯甲烷 30 mL,待固体溶解后,同时滴加取代苯基甲酰氯 (3) 溶液 (15.0 mmol) 和 10% 的氢氧化钠溶液 6.00 g (15.0 mmol),同时滴加完毕,先在 0~5 ℃ 下反应 2 h,再在室温下继续反应 2 h。薄层层析[V (乙酸乙酯):V (石油醚) = 1:1]监测至反应完全。静置,有机层用饱和碳酸钠溶液充分洗涤,再用 10% 的盐酸溶液萃取 2 次。合并酸性水层,加入饱和碳酸钠溶液调节 pH > 10,用二氯甲烷萃取 2 次。合并有机层,无水硫酸钠干燥 1 h。抽滤,滤液脱去溶剂,得化合物 4。
1.2.3 吩嗪-1-甲酰氯 (5) 的合成 向单口瓶中加入 2.5 g (11.2 mmol) 吩嗪-1-羧酸 (1)、二氯甲烷 30 mL 和 0.1 mL DMF,缓慢加入 3.0 g 草酰氯,加热回流至固体消失,继续回流反应 2~3 h,于旋转蒸发仪上脱去溶剂,用少量二氯甲烷溶解后再次脱去溶剂。用少量二氯甲烷溶解,用于下步反应。
1.2.4 目标化合物 6 的合成 以化合物 6a 为例:向 100 mL 三口瓶中加入化合物 4 (10.0 mol) 和 50 mL 二氯甲烷,搅拌使固体溶解,冰浴冷却至 0~5 ℃,同时滴加化合物 5 (11.2 mmol) 的二氯甲烷溶液和 10% 的氢氧化钠溶液 4.00 g (10.0 mmol),同时滴加完毕后,先在 0~5 ℃下反应 2 h 后,再在室温下反应 2 h。薄层层析[V (乙酸乙酯) : V (石油醚) = 3 : 1] 监测至反应完全。分液,有机层用 50 mL 水洗 2 遍,分出有机层,脱溶剂得粗品。用 50 mL V (乙醇) : V (水) = 1 : 1 溶液重结晶,抽滤,烘干得目标产物。采用同样的方法合成化合物 6b~6q。
N-叔丁基-N′-(2-甲基苯甲酰基)-1-吩嗪甲酰肼 (6a):黄色固体,收率 82.5%,m.p. 200~201 ℃,1H NMR (400 MHz, CDCl3), δ: 8.23~8.28 (m, 2H, Phenazine-H),8.13 (dd, 1H, Phenazine-H, J = 7.2, 3.6 Hz),8.06 (d, 1H, Phenazine-H, J = 6.0 Hz),7.83~7.89 (m, 3H, Phenazine-H),7.79 (s, 1H, NH),7.03 (t, 1H, J = 7.6 Hz, Ar-H),6.92 (d, J = 7.6 Hz, 1H, Ar-H),6.66 (t, J = 7.2 Hz, 1H, Ar-H),5.84 (d, J = 7.6 Hz, 1H, Ar-H),1.95 (s, 3H, CH3),1.80 (s, 9H, t-Bu); HRMS, 计算值 C25N4O2H24 (M + H) +: 413.197 2, 实测值 413.196 9.
N-叔丁基-N′-(3-甲基苯甲酰基)-1-吩嗪甲酰肼 (6b):黄色固体,收率 85.0%,m.p. 206~207 ℃,1H NMR (400 MHz, CDCl3), δ: 8.38 (s, 1H, NH),8.21~8.26 (m, 2H, Phenazine-H),8.15 (dd, 1H, Phenazine-H, J = 8.8, 5.2 Hz),7.98 (d, 1H, J = 6.8 Hz, Phenazine-H),7.87~7.92 (m, 2H, Phenazine-H),7.74 (dd, 1H, J = 8.8, 6.8 Hz, Phenazine-H),6.97 (d, 1H, J = 7.6 Hz, Ar-H),6.83 (t, 1H, J = 8.0 Hz, Ar-H),6.56 (d, 1H, J = 8.0 Hz, Ar-H),6.28 (s, 1H, Ar-H),1.86 (s, 3H, CH3),1.76 (s, 9H, t-Bu), HRMS 计算值 C25N4O2H24 (M + H) +: 413.197 2, 实测值 413.196 9.
N-叔丁基-N′-(4-甲基苯甲酰基)-1-吩嗪甲酰肼 (6c):黄色固体,收率 83.2%,m.p. 215~217 ℃,1H NMR (400 MHz, CDCl3), δ: 10.21 (s, 1H, NH),8.25~8.29 (m, 2H, Phenazine-H),8.13 (d, 1H, J = 8.4 Hz, Phenazine-H),8.00~8.03 (m, 2H, Phenazine-H),7.78 (t, 1H, J = 8.4 Hz, Phenazine-H),7.71 (d, 1H, J = 6.8 Hz, Phenazine-H),6.96 (d, 2H, J = 8.0 Hz, Ar-H),6.89 (d, 2H, J = 8.0 Hz, Ar-H),2.30 (s, 3H, CH3),1.65 (s, 9H, t-Bu),HRMS 计算值 C25N4O2H24 (M + H) +: 413.197 2, 实测值 413.196 6.
N-叔丁基-N′-(4-乙基苯甲酰基)-1-吩嗪甲酰肼 (6d):黄色固体,收率 78.0%,m.p. 135~137 ℃,1H NMR (400 MHz, CDCl3), δ: 8.22~8.28 (m, 3H, Phenazine-H & NH),8.14 (d, 1H, J = 8.8 Hz, Phenazine-H),8.00 (d, 1H, J = 6.8 Hz, Phenazine-H),7.90~7.93 (m, 2H, Phenazine-H),7.76 (dd, 1H, J = 8.8, 6.8 Hz, Phenazine-H),6.81 (d, 2H, J = 8.0 Hz, Ar-H),6.69 (d, 2H, J = 8.0 Hz, Ar-H),2.45 (q, 2H, J = 7.6 Hz, CH2),1.77 (s, 9H, t-Bu),1.04 (t, 3H, J = 7.6 Hz, CH3),HRMS 计算值 C26N4O2H26 (M + H) +: 427.212 9, 实测值 427.212 4.
N-叔丁基-N′-(4-异丙基苯甲酰基)-1-吩嗪甲酰肼 (6e):黄色固体,收率 75.8%,m.p. 160~162 ℃,1H NMR (400 MHz, CDCl3), δ: 8.30 (s, 1H, NH),8.21~8.26 (m, 2H, Phenazine-H),8.16 (dd, 1H, J = 5.6, 0.8 Hz, Phenazine-H),7.98 (d, 1H, J = 4.4 Hz, Phenazine-H),7.89~7.90 (m, 2H, Phenazine-H),7.74 (dd, 1H, J = 5.6, 4.4 Hz, Phenazine-H),6.82 (d, 2H, J = 5.6 Hz, Ar-H),6.67 (d, 2H, J = 5.6 Hz, Ar-H),2.66~2.72 (m, 1H, CH),1.76 (s, 9H, t-Bu),1.04 (d, 6H, CH3),HRMS 计算值 C27N4O2H28 (M + H) +: 441.228 5, 实测值 441.228 2.
N-叔丁基-N′-(4-叔丁基苯甲酰基)-1-吩嗪甲酰肼 (6f):黄色固体,收率82.0%,m.p. 227~228 ℃,1H NMR (400 MHz, CDCl3), δ: 8.22~8.25 (m, 3H, Phenazine-H & NH),8.15 (d, 1H, J = 8.4 Hz, Phenazine-H),7.99 (d, 1H, J = 6.4 Hz, Phenazine-H),7.90~7.93 (m, 2H, Phenazine-H),7.76 (q, 1H, J = 7.6 Hz, Phenazine-H),6.98 (d, 2H, J = 8.0 Hz, Ar-H),6.69 (d, 2H, J = 8.0 Hz, Ar-H),1.76 (s, 9H, t-Bu),1.12 (s, 9H, t-Bu),HRMS 计算值 C28N4O2H30 (M + H) +: 455.244 2, 实测值 455.243 8.
N-叔丁基-N′-(4-三氟甲基苯甲酰基)-1-吩嗪甲酰肼 (6g):黄色固体,收率86.0%,m.p. 236~237 ℃,1H NMR (400 MHz, CDCl3), δ: 8.43 (s, 1H, NH),8.22~8.28 (m, 2H, Phenazine-H),8.19 (d, 1H, J = 9.2 Hz, Phenazine-H),8.02 (d, 1H, J = 6.8 Hz, Phenazine-H),7.91~7.95 (m, 2H, Phenazine-H),7.77~7.81 (m, 1H, Phenazine-H),7.25 (d, 2H, J = 8.4 Hz, Ar-H),6.85 (d, 2H, J = 8.4, Ar-H),1.77 (s, 9H, t-Bu), HRMS 计算值 C25N4O2F3H21 (M + H) +: 467.168 5, 实测值 467.168 9.
N-叔丁基-N′-(2-氟苯甲酰基)-1-吩嗪甲酰肼 (6h):黄色固体, 收率 75.6%, m.p. 208~210 ℃, 1H NMR (400 MHz, CDCl3), δ: 8.60 (d, 1H, J = 11.6 Hz, NH),8.22~8.26 (m, 2H, Phenazine-H), 8.13 (d, 1H, J = 8.4 Hz, Phenazine-H),8.00 (d, 1H, J = 6.8 Hz, Phenazine-H),7.88~7.91 (m, 2H, Phenazine-H),7.74 (t, 1H, J = 8.4 Hz, Phenazine-H),7.63 (t, 1H, J = 7.2 Hz, Ar-H),7.21 (dd, 1H, J = 12.8, 6.8 Hz, Ar-H),7.02 (t, 1H, J = 7.2 Hz, Ar-H),6.57 (dd, 1H, J = 11.6, 8.4 Hz, Ar-H),1.77 (s, 9H, t-Bu), HRMS 计算值 C24N4O2FH21 (M + H) +: 417.172 1, 实测值 417.171 6.
N-叔丁基-N′-(3-氟苯甲酰基)-1-吩嗪甲酰肼 (6i):黄色固体, 收率 80.0%, m.p. 157~159 ℃, 1H NMR (400 MHz, CDCl3), δ: 8.41 (d, 1H, J = 18.0 Hz, NH), 8.21~8.26 (m, 2H, Phenazine-H), 8.16 (t, 1H, J = 5.6 Hz, Phenazine-H), 8.00 (t, 1H, J = 3.6 Hz, Phenazine-H), 7.89~7.92 (m, 2H, Phenazine-H), 7.72~7.79 (m, 1H, Phenazine-H), 6.90 (t, 1H, J = 3.6 Hz, Ar-H), 6.79 (dd, 1H, J = 5.6, 3.6 Hz, Ar-H), 6.65 (t, 1H, J = 5.6 Hz, Ar-H), 6.40 (s, 1H, Ar-H), 1.76 (s, 9H, t-Bu), HRMS 计算值 C24N4O2FH21 (M + H) +: 417.172 1, 实测值 417.171 4.
N-叔丁基-N′-(4-氟苯甲酰基)-1-吩嗪甲酰肼 (6j):黄色固体,收率 83.5%,m.p. 219~221 ℃,1H NMR (400 MHz, CDCl3), δ: 8.35 (s, 1H, NH),8.22~8.28 (m, 2H, Phenazine-H),8.15 (dd, 1H, J = 8.8, 1.2 Hz, Phenazine-H),8.01 (dd, 1H, J = 6.8, 1.2 Hz, Phenazine-H),7.90~7.94 (m, 2H, Phenazine-H),7.75~7.79 (dd, 1H, J = 8.8, 6.8 Hz, Phenazine-H),6.80 (dd, 2H, J = 8.8, 5.6 Hz, Ar-H),6.67 (t, 2H J = 8.8 Hz, Ar-H),1.76 (s, 9H, t-Bu), HRMS 计算值 C24N4O2FH21 (M + H) +: 417.172 1, 实测值 417.171 4.
N-叔丁基-N′-(2,4-二氟苯甲酰基)-1-吩嗪甲酰肼 (6k):黄色固体,收率 66.0%,m.p. 155~157 ℃,1H NMR (400 MHz, CDCl3), δ: 8.68 (d, 1H, J = 7.6 Hz, NH),8.21~8.25 (m, 2H, Phenazine-H),8.15 (d, 1H, J = 6.0 Hz, Phenazine-H),7.99 (d, 1H, J = 4.8 Hz, Phenazine-H),7.89~7.91 (m, 2H, Phenazine-H),7.75 (dd, 1H, J = 5.6, 4.8 Hz, Phenazine-H),7.66~7.70 (dd, 1H, J = 10.0, 5.6 Hz, Ar-H),6.72~6.77 (m, 1H, Ar-H),6.29~6.33 (m, 1H, Ar-H),1.76 (s, 9H, t-Bu), HRMS 计算值 C24N4O2F2H20 (M + H) +: 435.162 7, 实测值 435.162 5.
N-叔丁基-N′-(2,5-二氟苯甲酰基)-1-吩嗪甲酰肼 (6l):黄色固体,收率 80.5%,m.p. 176~178 ℃,1H NMR (400 MHz, CDCl3), δ: 8.74 (d, 1H, J = 12.0 Hz, NH),8.22~8.26 (m, 2H, Phenazine-H),8.16 (d, 1H, J = 8.8 Hz, Phenazine-H),7.92 (d, 1H, J = 6.8 Hz, Phenazine-H),7.90~7.92 (m, 2H, Phenazine-H),7.77 (dd, 1H, J = 8.8, 6.8 Hz, Phenazine-H),7.35~7.39 (m, 1H, Ar-H),6.88~6.94 (m, 1H, Ar-H),6.52~6.58 (m, 1H, Ar-H),1.76 (s, 9H, t-Bu), HRMS 计算值 C24N4O2F2H20 (M + H) +: 435.162 7, 实测值 435.162 3.
N-叔丁基-N′-(2,6-二氟苯甲酰基)-1-吩嗪甲酰肼 (6m):黄色固体,收率 88.0%,m.p. > 250 ℃,1H NMR (400 MHz, CDCl3), δ: 8.27 (d, 2H, J = 8.8 Hz, Phenazine-H),8.14~8.16 (m, 1H, Phenazine-H),8.03 (d, 1H, J = 6.4 Hz, Phenazine-H),7.90 (s, 1H, Phenazine-H),7.81~7.89 (m, 3H, Phenazine-H & NH),7.08~7.12 (m, 1H, Ar-H),6.56 (t, 2H, J = 8.0 Hz, Ar-H),1.76 (s, 9H, t-Bu), HRMS 计算值 C24N4O2F2H20 (M + H) +: 435.162 7, 实测值 435.162 0.
N-叔丁基-N′-(2,6-二氯苯甲酰基)-1-吩嗪甲酰肼 (6n):黄色固体,收率 81.2%,m.p. > 250 ℃,1H NMR (400 MHz, CDCl3), δ: 10.43 (s, 1H, NH),8.19~8.24 (m, 3H, Phenazine-H),7.86~7.93 (m, 4H, Phenazine-H),7.06~7.09 (m, 3H, Ar-H),1.73 (s, 9H, t-Bu), HRMS 计算值 C24N4O2Cl2H20 (M + H) +: 467.103 6, 实测值 467.103 8.
N-叔丁基-N′-(2-甲氧基苯甲酰基)-1-吩嗪甲酰肼 (6o):黄色固体,收率 76.0%,m.p. 219~221 ℃,1H NMR (400 MHz, CDCl3), δ: 9.37 (s, 1H, NH),8.28 (d, 1H, J = 5.2 Hz, Phenazine-H),8.23 (d, 1H, J = 5.2 Hz, Phenazine-H),8.05 (d, 1H, J = 5.6 Hz, Phenazine-H),7.95 (d, 1H, J = 4.4 Hz, Phenazine-H),7.86~7.91 (m, 4H, Phenazine-H),7.68 (dd, 1H, J = 5.6, 4.4 Hz, Ar-H),7.18~7.21 (m, 1H, Ar-H),6.86 (t, 1H, J = 5.2 Hz, Ar-H),6.41 (d, 1H, J = 5.6, Ar-H),1.73 (s, 9H, t-Bu), HRMS 计算值 C25N4O3H24 (M + H) +: 429.192 1, 实测值 429.191 7.
N-叔丁基-N′-(2-甲基-3-甲氧基苯甲酰基)-1-吩嗪甲酰肼 (6p):黄色固体,收率 79.5%,m.p. 135~137 ℃,1H NMR (400 MHz, CDCl3), δ: 8.23~8.29 (m, 2H, Phenazine-H),8.12 (d, 1H, J = 7.6 Hz, Phenazine-H),8.06 (d, 1H, J = 7.2 Hz, Phenazine-H),7.82~7.87 (m, 3H, Phenazine-H),7.71 (s, 1H, NH),6.58~6.67 (m, 2H, Ar-H),5.46 (d, 1H, J = 7.2 Hz, Ar-H),3.63 (s, 3H, CH3),1.73 (s, 9H, t-Bu), HRMS 计算值 C26N4O3H26 (M + H) +: 443.207 8, 实测值 443.207 6.
N-叔丁基-N′-(吩嗪-1-甲酰基)-1-吩嗪甲酰肼 (6q):黄色固体,收率 86.6%,m.p. >250 ℃,1H NMR (400 MHz, CDCl3), δ: 12.33 (s, 1H, NH),8.76 (dd, 1H, J = 4.8, 0.8 Hz, Phenazine-H),8.50 (d, 1H, J = 5.6 Hz, Phenazine-H),8.23 (dd, 1H, J = 5.6, 0.8 Hz, Phenazine-H),8.02 (d, 1H, J = 5.6 Hz, Phenazine-H),7.92~7.99 (m, 3H, Phenazine-H),7.78~7.82 (m, 3H, Phenazine-H),7.65~7.68 (m, 1H, Phenazine-H),7.60 (dd, 1H, J = 6.0, 4.8 Hz, Phenazine-H),7.33~7.36 (m, 1H, Phenazine-H),7.07 (d, 1H, J = 5.6 Hz, Phenazine-H),1.88 (s, 9H, t-Bu), HRMS 计算值 C30N6O2H24 (M + H) +: 501.203 4, 实测值 501.202 7.
1.3 目标化合物的晶体结构测定为进一步验证该类系列化合物分子结构,选取化合物 6o 进行了 X-射线单晶衍射分析。将纯化好的化合物 6o 溶于二氯甲烷中,于室温静置使其慢慢挥发,数天后有淡黄色晶体形成,选取尺寸为 0.15 mm × 0.12 mm × 0.10 mm的晶体进行 X-射线衍射分析。
1.4 杀菌活性测试采用离体平皿法[31]测定目标化合物 6a~6q 在 50 mg/L 下对水稻纹枯病菌 Thanatephorus cucumeris、西瓜枯萎病菌 Fusarium oxysporum、油菜菌核病菌 Sclerotinia sclerotiorum (Lib.) de Bary、核桃根腐病菌 Fusarium oxysporum Schlecht、小麦赤霉病菌 Fusarium graminearum 和烟草立枯病菌 (立枯丝核菌) Rhizoctonia solani Kühn 的杀菌活性。以商品化杀菌剂 99.5% 申嗪霉素原药 (上海农乐生物制品股份有限公司提供) 作为对照药剂。
1.5 韧皮部输导性测试参照文献[32]方法,将成熟蓖麻种子在湿脱脂棉上于 27 ℃ 下催芽 48 h。选出发芽的种子,置于人工气候培养箱内采用砂基培养。培养箱温度 27 ℃ ± 1 ℃,相对湿度 80% ± 5%,白天光照 14 h,夜晚关闭。以培养 6 d 的蓖麻幼苗作为供试材料。将蓖麻幼苗小心剥去胚乳,切勿折叠或弄破子叶。将其叶浸泡于含药缓冲液 (含 100 μmol/L 待测化合物、20 mmol/L 脂肪酸甲酯磺酸盐、0.25 mmol/L 氯化镁和 0.5 mmol/L 氯化钙) 中,以含相同浓度的马来酰肼缓冲液为对照。在含药缓冲液中培养 2 h 后,将幼苗子叶至下胚轴弯钩 1 cm 处小心切断,收集 3 h 内切口处渗出的韧皮部液体,用乙腈稀释 3 倍,加入无水硫酸钠干燥 30 min,经 0.22 μm 有机相微孔滤膜过滤,滤液进行 GC-MS 或 HPLC 检测。
2 结果与讨论 2.1 化合物的合成2.1.1 取代苯甲酰肼 (4a~4q) 的合成 在合成化合物 4a~4q 时,为了确保酰氯反应完全,采用叔丁基肼相对过量;另外,商品化的叔丁基肼是以盐酸盐的形式存在,在使用过程中,需先用碱将叔丁基肼游离出来方可使用。在该步反应的后处理过程中,先用碱洗将副产物酸及水溶性物质除去,再通过酸洗将生成的单酰肼成盐溶于酸水中,而中性有机杂质则溶于二氯甲烷中被分离除去,最后将酸洗水溶液的 pH 调至 9~10,用二氯甲烷萃取,有机层经干燥、脱溶剂,即可得较高纯度的取代苯甲酰肼 4a~4q。
2.1.2 吩嗪-1-甲酰氯 (5) 的合成 合成化合物 5 时,曾采用文献[33]的方法用二氯亚砜作为酰氯化试剂,但发现产物复杂,难以纯化;后改用草酰氯作为酰氯化试剂,副产物很少,易纯化。
2.1.3 目标化合物 6a~6q 的合成 在该反应中,酰氯过量有利于目标化合物的分离纯化。因为过量酰氯的副产物为酸,通过用饱和碳酸钠溶液充分洗涤即可将酸除去,再经重结晶即可得目标化合物。
2.2 目标化合物的结构表征在目标化合物 6a~6q 的 1H NMR 中,肼桥 N-H 的化学位移在 δ 12.34~8.23 处。吩嗪环上的氢在 δ 7.00~9.00 处,叔丁基上的氢在 δ 1.80~1.70 处。目标产物的 HRMS [M + H]+ 实测值和计算值误差在 0.5% 以内。结果表明,化合物 6o 的晶体属单斜晶系 (Monoclinic),P2 (1)/c 空间群,晶胞参数为 a = 714.828 (6) Å, b = 10.803 (4) Å,c = 14.126 (5) Å,α = 90°,β = 103.923 (6)°,γ = 90°,Z = 4,V = 2 196.2 (15) Å3,Dc = 1.296 g/cm3,Mu = 0.087 mm–1,F(000) = 904。数据保存于英国剑桥数据中心,CCDC 号为 1506023。化合物的晶体结构见图 1 所示。
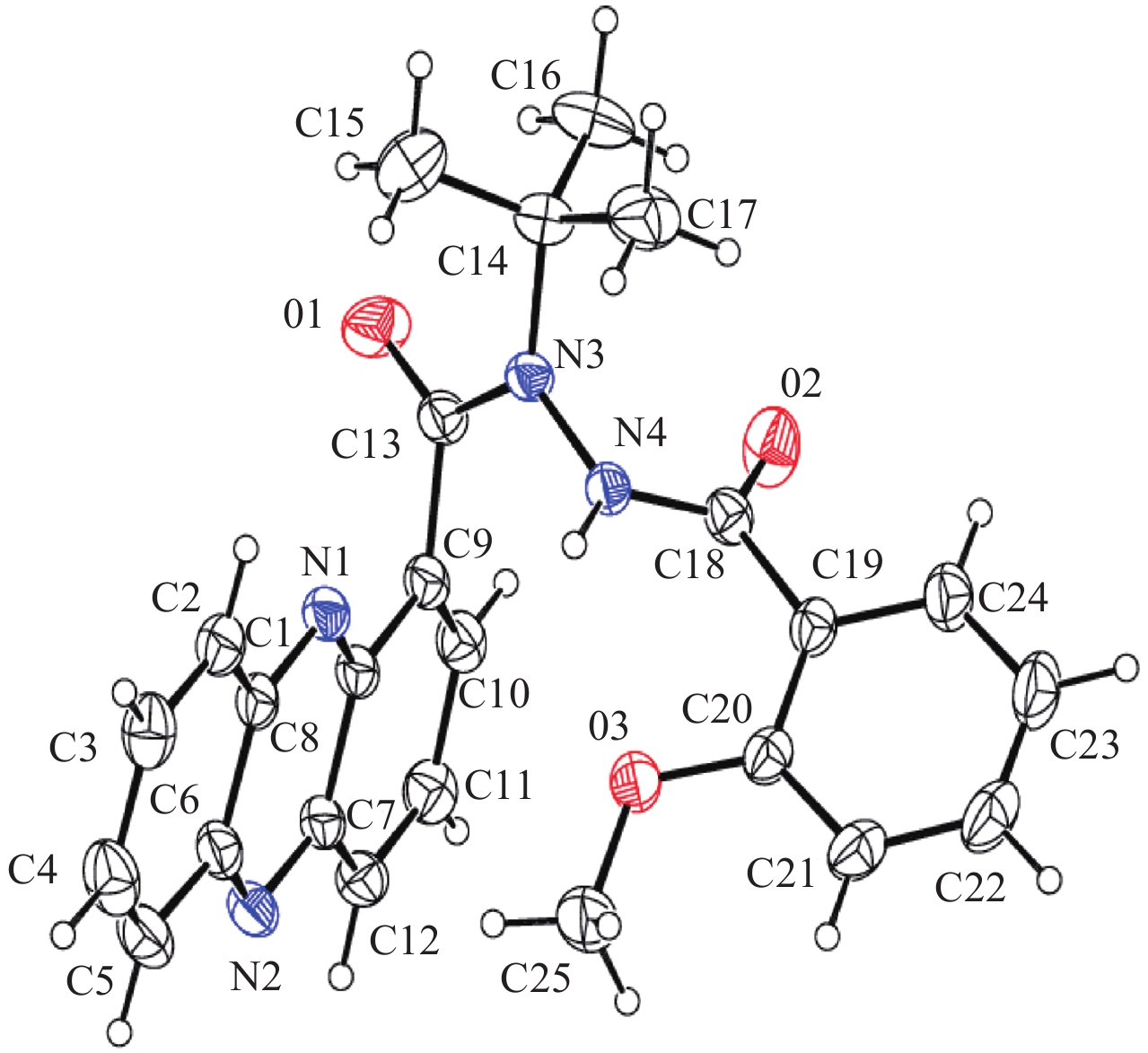
|
图 1 化合物 6o 的晶体结构 Fig. 1 The crystal structure of compound 6o |
2.3 目标化合物的杀菌活性
结果 (表 1) 表明:大部分目标化合物在 50 mg/L 下对水稻纹枯病菌均表现出中等偏上的抑制活性,其中化合物 6m 的抑制率达 92%,但均低于对照药剂兼母体化合物申嗪霉素。初步构效关系分析发现,苯环上含氟、氯等化合物的杀菌活性高于烷基取代苯环的化合物。所有化合物对西瓜枯萎病菌、油菜菌核病菌、核桃根腐病菌、小麦赤霉病菌和烟草立枯病菌的抑制活性均较低。
|
|
表 1 化合物 6a~6q 在 50 mg/L 下对不同植物病原菌的杀菌活性 Table 1 Fungicidal activity in vitro of compounds 6a–6q at 50 mg/L |
2.4 目标化合物的韧皮部输导性
输导性检测结果显示,所有化合物均没有明显的韧皮部输导性。分析认为,以马来酰肼为韧皮部输导性先导化合物,在兼顾生物活性时忽略了目标化合物理化性质的改变。据文献报道,化合物的韧皮部输导性主要取决于化合物的理化性质,尤其是油水分配系数。20 世纪 90 年代,Kleier 等[34-35]在研究系列具有韧皮部输导性化合物的理化性质后,提出化合物的韧皮部输导性取决于化合物的 LogKow 和 pKa 值,LogKow 值位于 0~3.5 区间是化合物具有明显韧皮部输导性的重要条件之一,而本系列化合物经 ALOGPS 2.1 系统预测,其 Log Kow 值为 3.3~4.8,亲油性偏强。因此,在以后的韧皮部输导性化合物设计中,可根据 Kleier 理论模型先进行化合物 LogKow 值的预测。
3 结论以具有抑菌活性的吩嗪-1-羧酸和具有韧皮部输导性的马来酰肼为先导化合物,将马来酰肼中的双酰肼结构引入到吩嗪-1-羧酸中,所得大部分目标化合物在 50 mg/L 下对水稻纹枯病菌都表现出了中等偏上的抑制活性,但均不及先导化合物吩嗪-1-羧酸。输导性研究结果表明,所有目标化合物均没有明显的韧皮部输导性。本研究为吩嗪-1-羧酸的双酰肼类衍生物的构效关系研究,观察双酰肼结构的引入对杀菌活性和韧皮部输导性的影响,为吩嗪-1-羧酸的结构改造与修饰方向打下了一定的基础。
| [1] | CHOLLET J F, ROCHER F, JOUSSE C, et al. Synthesis and phloem mobility of acidic derivatives of the fungicide fenpiclonil[J]. Pest Manag Sci, 2004, 60(11): 1063–1072. doi:10.1002/ps.v60:11 |
| [2] | CHOLLET J F, ROCHER F, JOUSSE C, et al. Acidic derivatives of the fungicide fenpiclonil: effect of adding a methyl group to the N-substituted chain on systemicity and fungicidal activity [J]. Pest Manag Sci, 2005, 61(4): 377–382. doi:10.1002/ps.v61:4 |
| [3] | YUAN J G, WU H X, LU M L, et al. Synthesis of a series of monosaccharide-fipronil conjugates and their phloem mobility[J]. J Agric Food Chem, 2013, 61(18): 4236–4241. doi:10.1021/jf400888c |
| [4] | QIN P W, WANG J, WANG H, et al. Synthesis of rotenone-O-monosaccharide derivatives and their phloem mobility [J]. J Agric Food Chem, 2014, 62(20): 4521–4527. doi:10.1021/jf500197k |
| [5] | YANG W, WU H X, XU H H, et al. Synthesis of glucose-fipronil conjugate and its phloem mobility[J]. J Agric Food Chem, 2011, 59(23): 12534–12542. doi:10.1021/jf2031154 |
| [6] | WU H X, YANG W, ZHANG Z X, et al. Uptake and phloem transport of glucose-fipronil conjugate in Ricinus communis involve a carrier-mediated mechanism [J]. J Agric Food Chem, 2012, 60(24): 6088–6094. doi:10.1021/jf300546t |
| [7] |
李俊凯, 徐汉虹, 王勇. 杀菌剂在韧皮部的传导性研究进展[J]. 世界农药, 2009, 31(1): 26–31.
LI J K, XU H H, WANG Y. Review on the fungicide transportation in plant phleom[J]. World Pestic, 2009, 31(1): 26–31. |
| [8] | ANZAI K, ISONO K, SUZUKI S. The new antibiotics, questiomycins A and B[J]. J Antibiot, 1960, 13: 125–132. |
| [9] | NELSON C D, TOOHEY J I. Method of controlling the growth of noxious plants: US3367765[P]. 1968-02-06. |
| [10] |
刘家峰, 郭松坡, 姜标. 海洋溴吡咯生物碱的研究进展[J]. 有机化学, 2005, 25(7): 788–799.
LIU J F, GUO S P, JIANG B. Progress in the study of marine bromopyrrole alkaloids[J]. Chin J Org Chem, 2005, 25(7): 788–799. |
| [11] | GRIBBLE G W. Naturally occurring organohalogen compounds——a survey[J]. J Nat Prod, 1992, 55(10): 1353–1395. doi:10.1021/np50088a001 |
| [12] | PÉE K H, LIGON J M. Biosynthesis of pyrrolnitrin and other phenylpyrrole derivatives by bacteria[J]. Nat Prod Rep, 2000, 17(2): 157–164. doi:10.1039/a902138h |
| [13] | HU H B, XU Y Q, CHEN F. Isolation and characterization of a new fluorescent Pseudomonas strain that produces both phenazine 1-carboxylic acid and pyoluteorin [J]. J Microbiol Biotechnol, 2005, 15(1): 86–90. |
| [14] | THOMASHOW L S, WELLER D M. Role of a phenazine antibiotic from Pseudomonas fluorescens in biological control of Gaeumannomyces graminis var. tritici [J]. J Bacteriol, 1988, 170(8): 3499–3508. doi:10.1128/jb.170.8.3499-3508.1988 |
| [15] | DUFFY B. Combination of pencycuron and Pseudomonas fluorescens strain 2-79 for integrated control of rhizoctonia root rot and take-all of spring wheat [J]. Crop Prot, 2000, 19(1): 21–25. doi:10.1016/S0261-2194(99)00078-2 |
| [16] | LEE J Y, MOON S S, HWANG B K. Isolation and in vitro and in vivo activity against Phytophthora capsici and Colletotrichum orbiculare of phenazine-1-carboxylic acid from Pseudomonas aeruginosa strain GC-B26 [J]. Pest Manag Sci, 2003, 59(8): 872–882. doi:10.1002/ps.688 |
| [17] |
郑文君, 徐曙, 周明国. 申嗪霉素对油菜菌核病菌生物学活性的初步研究[J]. 农药学学报, 2011, 13(1): 28–32.
ZHENG W J, XU S, ZHOU M G. Preliminary study on biological activity of shenqinmycin against Sclerotinia sclerotiorum [J]. Chin J Pest Sci, 2011, 13(1): 28–32. |
| [18] |
张红艳. 提高申嗪霉素对水稻纹枯病的防治效果的研究[D]. 上海: 上海交通大学, 2008.
ZHANG H Y. Improving control effects of shenqinmycin on rice sheath blight (Rhizoctonia solani) disease[D]. Shanghai: Shanghai Jiao Tong University, 2008. |
| [19] |
龚新进, 冯镇泰, 张红艳, 等. 一种吩嗪-1-甲酰肼生物杀菌剂的制备方法: CN103343150A[P]. 2013-10-09.
GONG X J, FENG Z T, ZHANG H Y, et al. Preparation method of phenazine-1-formylhydrazine biological germicide: CN103343150A[P]. 2013-10-09. |
| [20] |
许煜泉. 绿色微生物源抗菌剂申嗪霉素(M18)[J]. 精细与专用化学品, 2004, 12(20): 8–9.
XU Y Q. Green microorganism based antimicrobial: Shenqinmycin (M18)[J]. Fine Spec Chem, 2004, 12(20): 8–9. doi:10.3969/j.issn.1008-1100.2004.20.004 |
| [21] |
张红艳, 赵胜荣, 许煜泉, 等. 申嗪霉素与增效剂复配对水稻纹枯病菌防治的增效作用[J]. 上海交通大学学报(农业科学版), 2007, 25(6): 556–560.
ZHANG H Y, ZHAO S R, XU Y Q, et al. Synergistic effect of the complex between shenqinmycin and synergistic on rice sheath blight (Rhizoctonia solani) disease [J]. J Shanghai Jiaotong Univ (Agric SciEd), 2007, 25(6): 556–560. |
| [22] |
方运玲, 孙爽, 申阅, 等. 微生物源农药申嗪霉素的研制与应用[J]. 农药学学报, 2014, 16(4): 387–393.
FANG Y L, SUN S, SHEN Y, et al. Progress on the development and application of biopesticide Shenqinmycin[J]. Chin J Pest Sci, 2014, 16(4): 387–393. |
| [23] |
郑文君. 申嗪霉素对水稻白叶枯病菌和油菜菌核病菌的生物学活性及抗性风险评估[D]. 南京: 南京农业大学, 2010.
ZHENG W J. Bioactivities of shenqinmycin against Xanthomonas oryzae PV. Oryzae and Sclerotinia sclerotiorum and the resistance risk[D]. Nanjing: Nanjing Agricultural University, 2010. |
| [24] | KLEIER D A. Phloem mobility of xenobiotics. V. Structural requirements for phloem-systemic pesticides[J]. Pest Manag Sci, 1994, 42(1): 1–11. doi:10.1002/ps.2780420102 |
| [25] | RIGITANO R L O, BROMILOW R H, BRIGGS G G, et al. Phloem translocation of weak acids in ricinus communis [J]. Pest Manag Sci, 1987, 19(2): 113–133. doi:10.1002/ps.v19:2 |
| [26] |
柯少勇, 孙婷婷, 梁英, 等. 具有生物活性的酰肼衍生物的研究进展[J]. 有机化学, 2010, 30(12): 1820–1830.
KE S Y, SUN T T, LIANG Y, et al. Research advance of acylhydrazine derivatives with biological activities[J]. Chin J Org Chem, 2010, 30(12): 1820–1830. |
| [27] |
崔紫宁, 张莉, 黄娟, 等. 含呋喃环双酰肼类衍生物的合成、杀虫活性及3D-QSAR研究[J]. 有机化学, 2010, 30(10): 1482–1491.
CUI Z N, ZHANG L, HUANG J, et al. Synthesis, insecticidal activity and 3D-QSAR studies on diacylhy-drazine derivatives containing furan[J]. Chin J Org Chem, 2010, 30(10): 1482–1491. |
| [28] | MAO W T, ZHAO H, FAN Z J, et al. Synthesis and bioactivity of N-tert-butyl-N′-acyl-5-methy1-1,2,3-thiadiazole-4-carbohydrazides [J]. Chin Chem Lett, 2012, 23(11): 1233–1236. doi:10.1016/j.cclet.2012.09.024 |
| [29] |
马献力, 李芳耀, 段文贵, 等. 樟脑酸基双酰肼化合物的合成及其抑菌活性[J]. 精细化工, 2015, 32(12): 1426–1430.
MA X L, LI F Y, DUAN W G, et al. Synthesis and antifungal activity of camphoric acid-based diacylhydrazine compounds[J]. Fine Chem, 2015, 32(12): 1426–1430. |
| [30] |
胡崇波, 刘建华, 杜晓华. N-叔丁基-N′氟代苯甲酰基-取代吡啶甲酰肼衍生物的合成与杀虫活性研究
[J]. 有机化学, 2016, 36(5): 1051–1059.
HU C B, LIU J H, DU X H. Synthesis and insecticidal activities of N-(tert-butyl)-N′-fluorobenzoyl-substitutedpyridylcarbonyl hydrazide derivatives [J]. Chin J Org Chem, 2016, 36(5): 1051–1059. |
| [31] |
陈小霞, 袁会珠, 覃兆海, 等. 新型杀菌剂丁吡吗啉的生物活性及作用方式初探[J]. 农药学学报, 2007, 9(3): 229–234.
CHEN X X, YUAN H Z, QIN Z H. Preliminary studies on antifungal activity of pyrimorph[J]. Chin J Pest Sci, 2007, 9(3): 229–234. |
| [32] | DELÉTAGE-GRANDON C, CHOLLET J F, FAUCHER M, et al. Carrier-mediated uptake and phloem systemy of a 350-Dalton chlorinated xenobiotic with an alpha-amino acid function[J]. Plant Physiol, 2001, 125(4): 1620–1632. doi:10.1104/pp.125.4.1620 |
| [33] | YE L, ZHANG H Y, XU H, et al. Phenazine-1-carboxylic acid derivatives: design, synthesis and biological evaluation against Rhizoctonia solani Kuhn [J]. Bioorg Med Chem Lett, 2010, 20(24): 7369–7371. doi:10.1016/j.bmcl.2010.10.050 |
| [34] | KLEIER D A, HSU F C. Phloem mobility of xenobiotics. VII. The design of phloem systemic pesticides[J]. Weed Sci, 1996, 44(3): 749–756. |
| [35] | KLEIER D A, GRAYSON B T, HSU F C. The phloem mobility of pesticides[J]. Pestic Outlook, 1998, 9: 26–30. |
 2017, Vol. 19
2017, Vol. 19


