金丝草Pogonatherum crinitum (Thunb.) Kunth为禾本科金发草属多年生草本植物,又名猫尾草、黄毛草;其生长适应能力强,对生长环境要求较低,在山丘石缝、田间地头、河边湿地等均可生长,主要分布于中国浙江、福建、广西、台湾、江西等地[1]。近年已有学者从金丝草中分离得到了黄酮类、酚酸类和甾体类等化合物[2-6],其中黄酮类化合物数量较多,且黄酮及其苷类化合物在抗真菌、抗细菌及抗线虫等方面均表现出一定的活性[7-8]。为寻找新的植物源杀菌剂,探究其次级代谢产物的抑菌活性,笔者研究了金丝草水提取物及其乙酸乙酯和正丁醇萃取物对20种常见植物病原真菌的抑菌活性,并测定了乙酸乙酯萃取物对部分真菌的毒力方程及EC50值;从乙酸乙酯萃取物中分离并鉴定了10个已知化合物,并对其抑菌活性进行了初步研究。
1 材料和方法 1.1 供试植物金丝草全草于2015年6月采集于福建省南平市建阳区,经福建农林大学陈伟教授鉴定为金丝草P. crinitum,标本现存于福建农林大学植物保护学院制药工程系,自然晾晒风干,粉碎,过50目筛(孔径0.30 mm),保存备用。
1.2 供试真菌长柄链格孢菌Alternaria longipes (A1)、茄链格孢菌Alternaria solani Sorauer (A2)、灰葡萄孢菌Botrytis cinerea (B)、甘薯长喙壳菌Ceratocystis fimbriata (C1)、烟草炭疽病菌Colletotrichum destructivum (C1)、芭乐炭疽病菌Colletotrichum gloeosporioides (C2)、小白菜炭疽Colletotrichum higginsianum (C3)、燕麦镰孢菌FusaHum graminearum (F1)、禾谷镰刀菌Fusarium graminearum (F2)、西瓜尖镰孢菌Fusarium oxysporum (F3)、茄病镰刀菌Fusarium solani (F4)、孢粘帚霉Gliocladium catenulatum (G)、玉米小斑病菌Helminthosporium maydis (H)、落花生球腔菌Mycosphaerella arachidis (M)、辣椒疫霉Phytophthora capsici (P1)、稻瘟菌Pyricularia grisea (P2)、棉花立枯丝核菌Rhizoctonia solani(R)、油菜菌核菌Sclerotinia sclerotiorum (S1)、烟草白绢Sclerotium rolfsii (S2)、瓜亡革菌Thanatephorus cucumeris (T) 和苹果黑腐皮壳菌Valsa mali (V) 均由福建农林大学教育部重点实验室提供。
1.3 仪器和试剂SW-CJ-2FD型双人单面净化工作台(苏州净化设备有限公司);JNM-ECS400核磁共振仪(日本电子株式会社);Waters-2695-QDA高效液相色谱-质谱联用仪(美国沃特世科技有限公司)。
乙酸乙酯、正丁醇等溶剂均为分析纯(西陇化工科技有限公司);100~200目硅胶(筛孔径0.08~0.15 mm,青岛海洋化工有限公司);AB-8大孔吸附树脂和聚酰胺树脂(天津浩聚树脂科技有限公司);葡聚糖凝胶LH-20 (美国通用电气公司);Lichroprep RP-18 (德国默克化工技术有限公司)。
1.4 化学成分的提取分离将金丝草干草10 kg用25倍量水煎煮2 h。重复2次。合并两次煎煮液,浓缩,得到金丝草水提物。依次用乙酸乙酯和正丁醇萃取,浓缩,分别得到乙酸乙酯萃取物(60 g) 和正丁醇萃取物(177 g)。
乙酸乙酯萃取物的分离纯化:用适量甲醇溶解乙酸乙酯萃取物(60 g),按质量比为1.0 : 1.5的比例加入90 g硅胶拌样,待溶剂完全挥发后研磨成粉,均匀加于硅胶层析柱柱顶,按V (石油醚) :V (丙酮)=10 : 1、5 : 1、3 : 1、1 : 1依次进行梯度洗脱,收集馏分,旋转蒸发浓缩后,通过硅胶薄层层析[TLC,展开剂为V (石油醚) :V (丙酮)=12 : 1~1 : 1]检测,合并相近组分,分别得到JS-1 (0.63 g)、JS-2 (1.08 g)、JS-3 (1.34 g)、JS-4 (4.81 g)、JS-5 (2.56 g)、JS-6 (31.95 g)、JS-7 (4.32 g) 和JS-8 (10.02 g) 共8个组分,其中JS-6采用聚酰胺树脂柱层析,经水及30%、60%、90%乙醇水溶液依次梯度洗脱,通过TLC [展开剂为V (石油醚) :V (丙酮)=5 : 1]检测,合并相近馏分,分别得到JS-6-1 (5.03 g)、JS-6-2 (14.59 g)、JS-6-3 (7.56 g)、JS-6-4 (3.01 g) 和JS-6-5 (2.33 g) 共5个部分。其中:JS-6-2采用ODS反相柱层析,经10%~35%甲醇水溶液梯度洗脱后,第3、6、17部分有固体析出,用丙酮重结晶分别得到化合物1 (40.5 mg)、2 (10.3 mg) 和3 (3.2 mg);JS-6-3采用ODS反相柱层析,经10%~50%甲醇水溶液梯度洗脱后,第11部分有晶体析出,用丙酮重结晶得到化合物7 (20.2 mg),第3和21部分采用LH-20葡聚糖凝胶柱层析,经甲醇洗脱后,分别得到化合物4 (10.4 mg) 和6 (20.8 mg);JS-6-1采用ODS反相柱层析,经10%~40%甲醇水溶液梯度洗脱后,通过TLC [V (氯仿) :V (甲醇)=8 : 1]检测,合并相近馏分,第6和9部分采用LH-20葡聚糖凝胶柱层析,经甲醇反复洗脱后,通过TLC [V (氯仿) :V (甲醇)=6 : 1]检测,合并相近馏分,用甲醇重结晶得到化合物8 (21.5 mg) 和9 (41.5 mg)。JS-5采用LH-20葡聚糖凝胶柱层析,经甲醇洗脱后,第4部分有晶体析出,用甲醇重结晶得到化合物5 (20.3 mg)。JS-3采用LH-20葡聚糖凝胶柱层析,经V (氯仿) :V (甲醇)=1 : 1洗脱后,第11部分有晶体析出,用甲醇重结晶得到化合物10 (12.6 mg)。
1.5 抑菌活性测定 1.5.1 提取物和萃取物的抑菌活性测定采用菌丝生长速率法[9]。用50%乙醇水溶液将供试样品配制成质量浓度为1.00 × 105 mg/L的样品溶液。取2 mL样品溶液加入98 mL PDA培养基中,制成含药培养基。以加入相同量的50%乙醇水溶液为对照。打取直径为5 mm的菌饼,接种于含药平板上,于(28±0.5) ℃培养箱中培养2~7 d后,计算菌丝生长抑制率。
选取抑制率高、菌落生长规则,且测定周期≤4 d的真菌为目标菌,测定乙酸乙酯萃取物对其的毒力。将乙酸乙酯萃取物按样品在培养基中的质量浓度为4.00 × 103、2.00 × 103、1.00 × 103、5.00 × 102和2.50 × 102 mg/L配制药液。按文献[9]方法测定抑菌活性,并采用几率值分析法计算毒力方程、抑制中浓度(EC50) 和决定系数(R2)。
1.5.2 化合物对病原真菌孢子萌发的抑制作用测定采用滤纸片法[10]测定化合物1~10对目标真菌菌丝生长的抑制作用。
采用孢子萌发法[11]初步测定化合物1~10对棉花立枯丝核菌和辣椒疫霉孢子萌发的抑制作用,对部分活性较好的化合物按文献[11]方法进行毒力测定,计算其EC50及95%置信限。
2 结果与分析 2.1 金丝草水提物及萃取物的抑菌活性结果表明:2.00 × 103 mg/L的金丝草水提物对供试病原真菌中的14种病原菌菌丝生长均有一定的抑制作用;乙酸乙酯萃取物和正丁醇萃取物的抑制作用优于水提物。2.00 × 103 mg/L的乙酸乙酯萃取物对其中8种病原菌菌丝生长的抑制率超过50%,对棉花立枯丝核菌、小白菜炭疽、燕麦镰孢菌和辣椒疫霉的菌丝生长抑制率分别为45.99%、53.52%、61.59%和100.00%。
毒力测定结果表明,乙酸乙酯萃取物对小白菜炭疽病菌、燕麦镰孢菌、棉花立枯丝核菌和辣椒疫霉4种供试真菌的EC50值分别为2.45 × 103、1.56 × 103、1.48 × 103和5.24 × 102 mg/L。
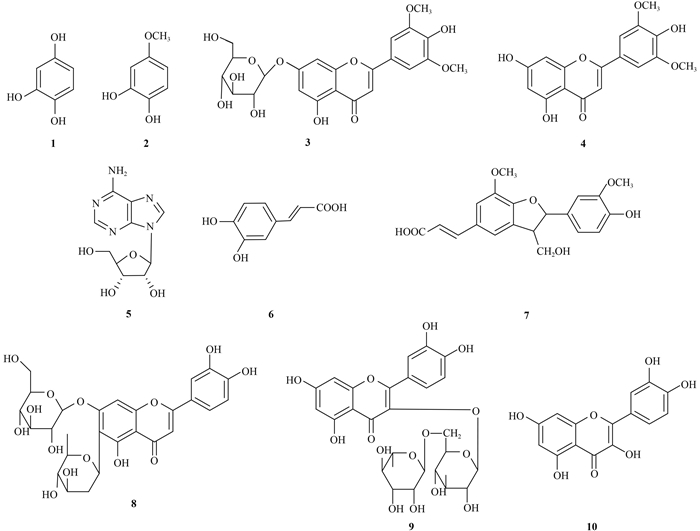
2.2 化合物的结构鉴定采用1H NMR、13C NMR和ESI-MS等分析手段对化合物1~10的结构进行了鉴定,经与相关文献值[12-19]分析比对,确定其化学结构如图式1所示。其中化合物3、4、8、9、10为黄酮类及其苷类,化合物1、2、6为多酚类,化合物5和7分别为生物碱类和木脂素类。
|
图式1 化合物1~10的化学结构 Scheme1 The chemical structure of compounds 1-10 |
化合物1:无色透明晶体,熔点(m.p.) 139~141 ℃(文献[12] 139~140 ℃);ESI-MS (m/z): 127.11 [M+H]+,分子式为C6H6O3,其1H NMR谱和13C NMR谱数据与文献[12]一致,故确定该化合物为1, 2, 4-三羟基苯(1, 2, 4-trihydroxybenzene)。
化合物2:无色透明晶体,m.p. 72~73 ℃ (文献值[12] 72~73 ℃);ESI-MS (m/z): 141.29 [M+H]+, 179.22 [M+K]+,分子式为C7H8O3,其1H NMR谱和13C NMR谱数据与文献[12]一致,确定该化合物为1, 2-二羟基-4-甲氧基苯(1, 2-didroxy-4-methoxybenzene)。
化合物3:黄色粉末状固体,m.p. 272~273 ℃ (文献值[13] 271~273 ℃);ESI-MS (m/z): 493.27 [M+H]+,分子式为C23H24O12,其1H NMR谱和13C NMR谱数据与文献[13]一致,故确定该化合物为小麦黄素-7-O-β-D-吡喃葡萄糖苷(tricin-7-O-β-D-glucopyran-oside)。
化合物4:黄色粉末,m.p. 293~295 ℃ (文献值[13] 293~295 ℃);ESI-MS (m/z): 331.28 [M+H]+, 352.60 [M+Na]+,分子式为C17H14O7,其1H NMR谱和13C NMR谱数据与文献[13]一致,故确定该化合物为小麦黄素(tricin)。
化合物5:白色粉末,m.p. 234~235 ℃ (文献值[14] 234~235 ℃);ESI-MS (m/z): 268.21 [M+H]+,分子式为C10H13N5O4,其1H NMR谱和13C NMR谱数据与文献[14]一致,故确定该化合物为β-腺苷(β-adenosine)。
化合物6:白色粉末,m. p. 193~194 ℃ (文献值[15]193~194 ℃);ESI-MS (m/z): 181.16 [M+H]+,分子式为C9H8O4,其1H NMR谱和13C NMR谱数据与文献[15]一致,故确定该化合物为咖啡酸(caffeic acid)。
化合物7:白色晶体,m. p. 150~153 ℃ (文献值[16]150~152 ℃);ESI-MS (m/z): 373.38 [M+H]+, 395.30 [M+Na]+,分子式为C20H20O7,其1H NMR谱和13C NMR谱数据与文献[16]一致,故确定该化合物为留兰香木脂素B (spicatolignan B)。
化合物8:黄色粉末, m. p. 274~276 ℃(文献值[17] 274~276 ℃);ESI-MS (m/z): 578.64 [M+H]+,分子式为C27H30O14,其1H NMR谱和13C NMR谱数据与文献[17]一致,故确定该化合物为木犀草素6-C-β-波依文糖-7-O-β-葡萄糖苷(luteolin 6-C-β-boivinopyranoside-7-O-β-glucopyran-oside)。
化合物9:黄色粉末, m.p. 176~178 ℃ (文献值[18] 176~178 ℃);ESI-MS (m/z): 611.43 [M+H]+,分子式为C27H30O16;其1H NMR谱和13C NMR谱数据与文献[18]一致,故确定该化合物为芦丁(rutin)。
化合物10:黄色粉末, m.p. 313~314 ℃ (文献值[19] 312~314 ℃);ESI-MS (m/z): 303.13 [M+H]+,分子式为C15H10O7,其1H NMR谱和13C NMR谱数据与文献[19]一致,故确定该化合物为槲皮素(quercetin)。
2.3 化合物的抑菌活性滤纸片测定法结果表明,化合物1~10对供试病原菌的菌丝生长均无明显抑制作用。孢子萌发法测定结果表明,化合物6~10对棉花立枯丝核菌和辣椒疫霉的孢子萌发具有较好的抑制作用,其中化合物8的抑菌效果最好,其EC50值分别为18.54和21.38 mg/L。化合物6~10的毒力方程及EC50值见表 1。
|
|
表 1 化合物6~10对棉花立枯丝核菌和辣椒疫霉孢子萌发的毒力 Table 1 Toxicity of compounds 6-10 against spores ofR. solani andP. capsici |
3 结论与讨论
本研究从金丝草乙酸乙酯提取物中分离得到10个已知化合物,包括5个黄酮及其苷类,3个多酚类,1个生物碱类和1个木脂素类化合物,其中化合物2、3、5、7和10为首次从该植物中分离得到,且β-腺苷(5) 和留兰香木脂素B (7) 分别是首次从该植物属中分离得到的生物碱类化合物和木脂素类化合物。
贤景春等[20]发现,金丝草总多酚对羟基自由基有较好的清除作用;Wang等[21]从金丝草中分离得到的黄酮具有较好的抑制脂多糖诱导NO生成的作用。Ozkan等[22]研究发现,咖啡酸、芦丁对大肠杆菌Escherichia coli、绿脓杆菌Pseudomonas aeruginosa等15种细菌具有抑制作用;Zhou等[23]研究表明,槲皮素、咖啡酸对辣椒斑点病黄单胞菌Xanthomonas campestris和枯草芽孢杆菌Bacillus subtilis都具有较好的抑制作用。本研究首次报道了金丝草水取物对14种常见植物病原真菌有一定的抑制作用,其中乙酸乙酯萃取物对棉花立枯丝核菌、小白菜炭疽、燕麦镰孢菌和辣椒疫霉的EC50值分别为2.45 × 103、1.56 × 103、1.48 × 103和5.24 × 102 mg/L。从乙酸乙酯萃取物分离得到的化合物6~10,对抑制棉花立枯丝核菌孢子萌发的EC50值分别为32.81、103.6、18.54、48.31和40.43 mg/L,对抑制辣椒疫霉菌孢子萌发的EC50值分别为36.13、87.83、21.38、52.19和41.36 mg/L。从化合物分类方面看,黄酮类化合物显示出较好的抑制植物病原真菌的活性。
本研究仅对金丝草水取物的乙酸乙酯萃取物进行了初步分离;而活性初筛结果表明,正丁醇萃取物也具有一定的抑菌活性,其中是否还存在其他活性成分,还有待进一步研究。
| [1] |
黄泰康, 丁志遵, 赵守训.
现代本草纲目[M]. 北京: 中国医药科技出版社, 2001: 1633.
HUANG T K, DING Z Z, ZHAO S X. Modern compendium of materia medica[M]. Beijing: China Medical Science Press, 2001: 1633. |
| [2] |
赵桂琴, 刘丽艳, 毛晓霞, 等. 金丝草黄酮醇苷类化学成分研究[J]. 中国新药杂志, 2011, 20(5): 467–470.
ZHAO G Q, LIU L Y, MAO X X, et al. Flavonol glycosides from Pogonatherum crinitum[J]. Chin J New Drug, 2011, 20(5): 467–470. |
| [3] | ZHU D, YANG J, DENG X T, et al. A new C-glycosylflavone from Pogonatherum crinitum[J]. Chin J Nat Med, 2009, 7(3): 184–186. doi:10.3724/SP.J.1009.2009.00184 |
| [4] |
尹志峰, 高大昕, 王宏伟, 等. 金丝草化学成分[J]. 中国实验方剂学杂志, 2014, 20(20): 104–107.
YIN Z F, GAO D X, WANG H W, et al. Chemical constituents of Pogonatherum crinitum[J]. Chin J Exp Tradit Med Form, 2014, 20(20): 104–107. |
| [5] |
刘丽佳.金丝草的化学成分研究Ⅰ[D].哈尔滨:黑龙江中医药大学, 2013:27-33.
LIU L J. Chemical constituents from Pogonatherum crinitum (Thumb.) Kunth I.[D]. Harbin:Heilongjiang University Of Chinese Medicine, 2013:27-33. |
| [6] |
孙传鑫.金丝草的化学成分研究Ⅱ[D].哈尔滨:黑龙江中医药大学, 2013:21-32.
SUN C X. Chemical constituents from Pogonatherum crinitum (Thumb.) Kunth Ⅱ.[D]. Harbin:Heilongjiang University of Chinese Medicine, 2013:21-32. |
| [7] | DU S S, ZHANG H M, BAI C Q, et al. Nematocidal flavone-C-glycosides against the root-knot nematode (Meloidogyne incognita) from Arisaema Erubescens tubers[J]. Molecules, 2011, 16(6): 5079–5086. |
| [8] | El Din El SOUDA S S, MATLOUB A A, NEPVEU F, et al. Phenolic composition and prospective anti-infectious properties of Atriplex lindleyi[J]. Asian Pac J Trop Dis, 2015, 5(10): 786–791. doi:10.1016/S2222-1808(15)60931-8 |
| [9] |
农药室内生物测定试验准则杀菌剂第2部分:抑制病原真菌菌丝生长试验平皿法:NY/T 1156.2-2006[S].北京:中国农业出版社, 2006.
Pesticides guidelines for laboratory bioactivity tests. Part 2:Petri plate test for determining fungicide inhibition of mycelial growth:NY/T 1156.2-2006[S]. Beijing:China Agriculture Press, 2006. |
| [10] | KABIR S R, RAHMAN M M, TASNIM S, et al. Purification and characterization of a novel chitinase from Trichosanthes dioica seed with antifungal activity[J]. Int J Biol Macromol, 2016, 84: 62–68. doi:10.1016/j.ijbiomac.2015.12.006 |
| [11] |
张绍勇, 李桥, 陈安良. 杨梅叶抑菌活性成分初步分离与鉴定[J]. 农药学学报, 2011, 13(2): 149–154.
ZHANG S Y, LI Q, CHEN A L. Isolation and identification of antifungal constituents from the leaf of Myrica rubra[J]. Chin J Pestic Sci, 2011, 13(2): 149–154. |
| [12] |
于德泉, 杨峻山.
分析化学手册第七分册核磁共振波谱分析[M]. 2版. 北京: 化学工业出版社, 1999: 98-99.
YU D Q, YANG J S. Analytical chemistry handbook 7th[M]. 2nd ed. Beijing: Chemical Industry Press, 1999: 98-99. |
| [13] |
相宇, 李友宾, 张健, 等. 猪毛菜化学成分研究[J]. 中国中药杂志, 2007, 32(5): 409–413.
XIANG Y, LI Y B, ZHANG J, et al. Studies on chemical constituents of Salsola collina[J]. Chin J Chin Mater Med, 2007, 32(5): 409–413. |
| [14] | DOMONDON D L, HE W D, DE KIMPE N, et al. β-Adenosine, a bioactive compound in grass chaff stimulating mushroom production[J]. Phytochemistry, 2004, 65(2): 181–187. doi:10.1016/j.phytochem.2003.11.004 |
| [15] | LEE S Y, KIM K H, LEE I K, et al. A new flavonol glycoside from Hylomecon vernalis[J]. Arch Pharm Res, 2012, 35(3): 415–421. doi:10.1007/s12272-012-0303-8 |
| [16] | ZHENG J, CHEN G T, GAO H Y, et al. Two new lignans from Mentha spicata L[J]. J Asian Nat Prod Res, 2007, 9(5): 431–435. doi:10.1080/10286020500384641 |
| [17] | ZHU D, YANG J, LAI M X, et al. A new C-glycosylflavone from Pogonatherum crinitum[J]. Chin J Nat Med, 2010, 8(6): 411–413. |
| [18] |
李冲, 刘勇, 高燕, 等. 粘毛鼠尾草化学成分研究[J]. 中药材, 2005, 28(2): 101–102.
LI C, LIU Y, GAO Y, et al. Studies on chemical constituents from Salvia roborowskii[J]. Chin Med Mat, 2005, 28(2): 101–102. |
| [19] |
魏太明, 阎玉凝, 关昕璐, 等. 垂盆草的化学成分研究(I)[J]. 北京中医药大学学报, 2003, 26(4): 59–61.
WEI T M, YAN Y N, GUAN X L, et al. Analysis of the chemical constituents of the ground part of Sedum sarmentosum[J]. J Beijing Univ TCM, 2003, 26(4): 59–61. |
| [20] |
贤景春, 林敏. 金丝草总多酚提取工艺及抗氧化性研究[J]. 安徽农业大学学报, 2014, 41(2): 299–302.
XIAN J C, LIN M. Extraction of total polyphenol from Pogonatherum crinitum (Thunb.) Kunth and its antioxidation activity[J]. J Anhui Agric Univ, 2014, 41(2): 299–302. |
| [21] | WANG G J, CHEN Y M, WANG T M, et al. Flavonoids with iNOS inhibitory activity from Pogonatherum crinitum[J]. J Ethnopharmacol, 2008, 118(1): 71–78. doi:10.1016/j.jep.2008.03.005 |
| [22] | OZKAN G, SAGDIC O, EKICi L, et al. Phenolic compounds of Origanum sipyleum L. extract, and its antioxidant and antibacterial activities[J]. J Food Lipids, 2007, 14(2): 157–169. doi:10.1111/jfl.2007.14.issue-2 |
| [23] | ZHOU L G, LI D, WANG J G, et al. Antibacterial phenolic compounds from the spines of Gleditsia sinensis Lam[J]. Nat Prod Res, 2007, 21(4): 283–291. doi:10.1080/14786410701192637 |
 2017, Vol. 19
2017, Vol. 19


