2. 浙江省化工研究院国家南方农药创制中心浙江基地, 杭州 310023
2. Zhejiang Branch of National Pesticide R & DSouth Center, Zhejiang Chemical Industry Research Institute, Hangzhou 310023, China
农药在土壤中的吸附-解吸附被认为是其在土壤-水环境中归趋的主要支配因素,不仅制约着农药在土壤中气、液、固三相间的相对分布,而且决定着其在土壤环境中的迁移、滞留、转化和生物利用等过程[1-2]。目前已有较多关于农药在土壤中吸附-解吸行为及机理的探索研究[3-7],建立了比较完整的研究方法和理论。农药在土壤中的吸附特性是农药环境行为研究的重要内容,对预测和评价新农药的潜在环境风险有着重要意义。
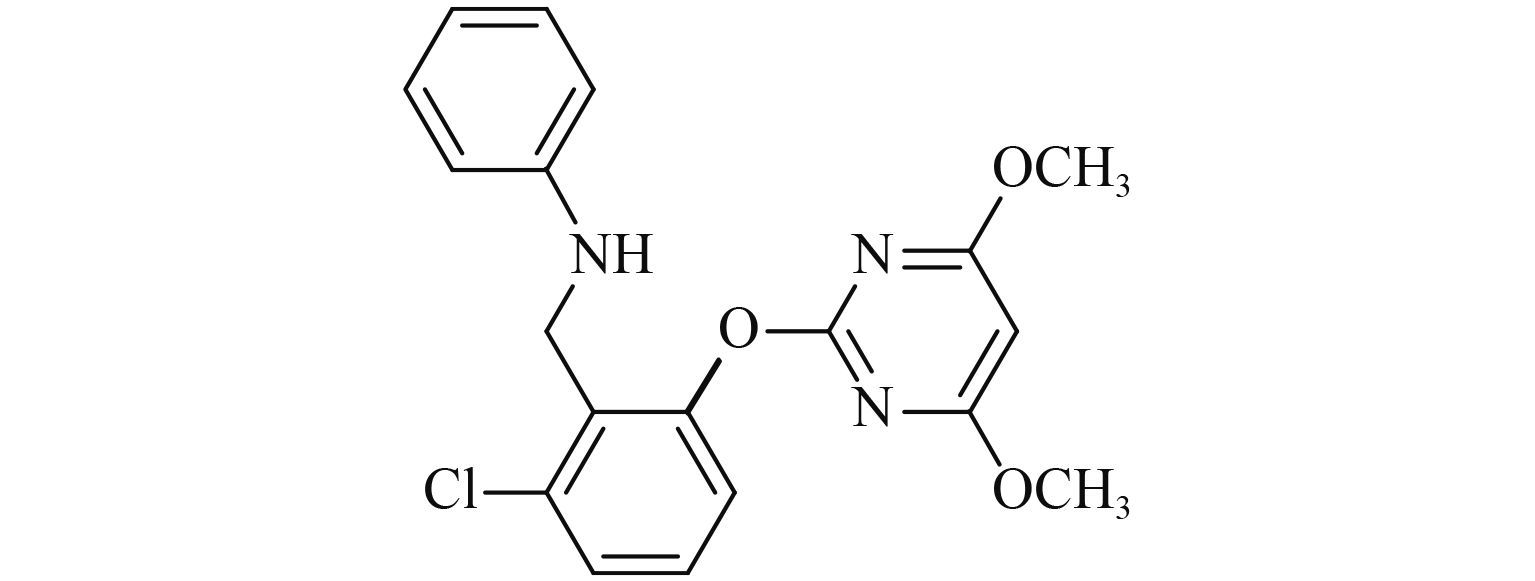
氯胺嘧草醚 (ZJ1835,Scheme 1) 是在 2-嘧啶氧基-N-芳基苄胺类化合物结构基础上优化得到的新型高除草活性化合物,属于嘧啶水杨酸类,由中国浙江省化工研究院和中国科学院上海有机化学研究所共同研发,已获得中国发明专利 (专利号:ZL00130735.5) [8],并申报了 PCT 国际发明专利 (US 6,800,590B2) [9]。氯胺嘧草醚目前主要用于芽前处理防治棉田中的马唐、牛筋草、反枝苋及马齿苋等杂草,具有防效好、持效期长等优点[10-11]。
|
Scheme 1 |
目前尚未见有关氯胺嘧草醚在土壤中环境行为的研究报道。笔者测定了氯胺嘧草醚在 5 种不同土壤中的吸附-解吸附行为,探讨了其吸附特性与土壤性质的关系,旨在为其科学合理使用提供理论指导。
1 材料与方法 1.1 供试材料土壤:红土、潮土、水稻土、黑土和褐土5 种土壤均采自大田表层 0~15 cm 耕作土,经风干碾磨、过 2 mm 筛后密封备用。土壤基本理化性质见表 1。
|
|
表 1 供试土壤的理化性质 Table 1 Physical and chemical properties of the tested soil samples |
药剂及试剂:氯胺嘧草醚 (ZJ1835) 标准品 (≥ 99%,浙江省化工研究院);乙腈和甲醇为色谱纯,其余试剂均为分析纯。
1.2 仪器设备Ultimate 3000 高效液相色谱仪 (HPLC)(美国 Thermo Scientific 公司);ZORBAX SB-C18 液相色谱柱 (美国 Agilent 公司);十万分之一电子天平 (梅特勒·托利多公司);SHZ-A 水浴恒温振荡器 (上海博迅实业有限公司医疗设备厂);LDZ5-2ZI 自平衡离心机 (北京雷博尔离心机有限公司)。
1.3 标准溶液配制准确称取 0.1 g (精确到 0.000 1 g) 氯胺嘧草醚标准品于 100 mL 容量瓶中,用乙腈定容,得到 1 000 mg/L 的氯胺嘧草醚标准母液。试验时再用乙腈梯度稀释,分别获得 100、10.0 和 1.00 mg/L 的标准工作溶液。称取 1.1 g (精确到 0.000 1 g) 氯化钙于 1 L 容量瓶中,用纯水定容,得到 0.01 mol/L 的氯化钙溶液,作为抑菌剂。根据试验需要,用氯化钙溶液配制不同浓度的氯胺嘧草醚溶液,备用。
1.4 吸附动力学试验采用美国环保署 (EPA) 推荐的批量平衡法[12]测定。称取 2.00 g 土样置于 50 mL 具塞磨口锥形瓶中,加入 20 mL 2.00 mg/L 的氯胺嘧草醚氯化钙溶液,加塞后置于水浴恒温振荡器上,25 ℃下振荡,分别于 2、4、6、8、12、16、24 及 48 h 取样,于 4 680 r/min 下离心 10 min。将上清液转移至 100 mL 具塞量筒中,加入 10 g 氯化钠和 30 mL 乙腈,剧烈摇晃 1 min,静置 20 min。取上层清液 10 mL 于圆底烧瓶中,40 ℃ 下旋蒸浓缩至干。用乙腈定容至 2.0 mL,经 0.45 μm 滤膜过滤后,采用 HPLC 测定氯胺嘧草醚的浓度。
1.5 土壤吸附性试验同样采用批量平衡法[12]测定。用 0.01 mol/L 的氯化钙水溶液配制氯胺嘧草醚质量浓度依次为 0.05、0.20、0.80、1.00 及 2.00 mg/L 的氯胺嘧草醚氯化钙溶液。称取 2.0 g 土壤样品于 50 mL 锥形瓶中,按照水土质量比 10:1 分别加入 20 mL 上述浓度的氯胺嘧草醚氯化钙溶液,在恒温 (25 ± 1) ℃、180 r/min 下旋转振荡 24 h,再于 4 680 r/min 下离心 10 min。其余操作同 1.4 节。根据差减法[公式 (1)] 计算氯胺嘧草醚在 5 种土壤中的吸附量。
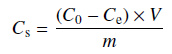
|
(1) |
式中:Cs 为土壤中吸附农药的质量分数(mg/kg);Ce 为吸附平衡时溶液中农药的质量浓度 (mg/L);C0 为平衡浓度为 0 时土壤中吸附农药的质量浓度 (mg/L);V 为溶液体积 (20 mL);m 为土壤质量 (2.00 g)。
于吸附试验结束后立即进行解吸。将上清液全部取出,加入等体积的氯化钙溶液,振荡 24 h,再于 4 680 r/min 下离心 10 min,其余同 1.4 节吸附动力学试验处理。
1.6 土壤中移动性试验分别称取 10.0 g 5 种土壤样品于烧杯中,加入 7.5 mL 水,搅拌至均匀泥浆状,均匀涂布于层析玻璃板上,根据土质粗细,控制土层厚度在 0.5~1.0 mm 之间,(23 ± 5) ℃ 下晾干,制得层析薄板。于距薄板底部 1.5 cm 处点滴 0.1 mL 100 mg/L 的氯胺嘧草醚标准溶液,待溶剂挥发后,在纯水 (液面高度 0.5 cm) 中展开,至展开剂到达薄板 19.5 cm 处停止,晾干。将薄板上的土壤按等距离分成 9 段,参照 1.4 节方法处理,分别测定各段土壤中氯胺嘧草醚浓度及其在薄板上的分布。
1.7 数学模型及数据分析分别采用线性模型 [式 (2)] 和 Freundlich 模型 [式 (3)] 来描述吸附平衡时土壤中吸附的氯胺嘧草醚浓度和溶液中氯胺嘧草醚浓度的关系[13]:
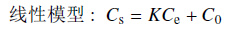
|
(2) |
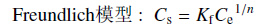
|
(3) |
式中:K 和 Kf 分别为线性模型和 Freundlich 模型的吸附-解吸常数 (在描述解吸时用 Kdes);1/n 为吸附经验常数,其反映了吸附剂表面的非均匀性。
滞后系数 (HI) 是不可逆吸附程度指标,可通过解吸经验常数 (1/ndes) 与吸附经验常数 (1/n) 的比值求得[14]。有机碳吸附常数 (KOC) 的计算参照 Morrica 等[15]的方法;有机质吸附常数 (KOM)、吸附自由能 (G,kJ/mol)和偏摩尔自由能 (−F,J/mol) 参照文献中公式[16]求得。
1.8 HPLC 分析条件ZORBAX SB-C18 液相色谱柱 (4.6 mm × 150 mm);流动相 V (乙腈) : V (水) = 80:20,流速 1.0 mL/min;检测波长 245 nm;进样量 10 μL;色谱工作温度 25 ℃。在上述条件下,氯胺嘧草醚的保留时间为 7.85 min。
2 结果与分析 2.1 氯胺嘧草醚在土壤中的吸附-解吸动力学不同时间点氯胺嘧草醚在 5 种土壤中的吸附结果见图 1。从中可知,氯胺嘧草醚与土壤溶液接触振荡 2 h 内为快速吸附阶段,溶液中氯胺嘧草醚浓度急剧降低;2~8 h 之间溶液中氯胺嘧草醚浓度下降趋于平缓,即进入慢速吸附阶段,但此时各种与吸附有关的化学和物理反应仍可能继续进行;8~24 h 之间,溶液中氯胺嘧草醚的浓度基本保持不变,即吸附达到平衡。为达到充分吸附平衡,确定吸附-解吸附试验的平衡时间为 24 h。
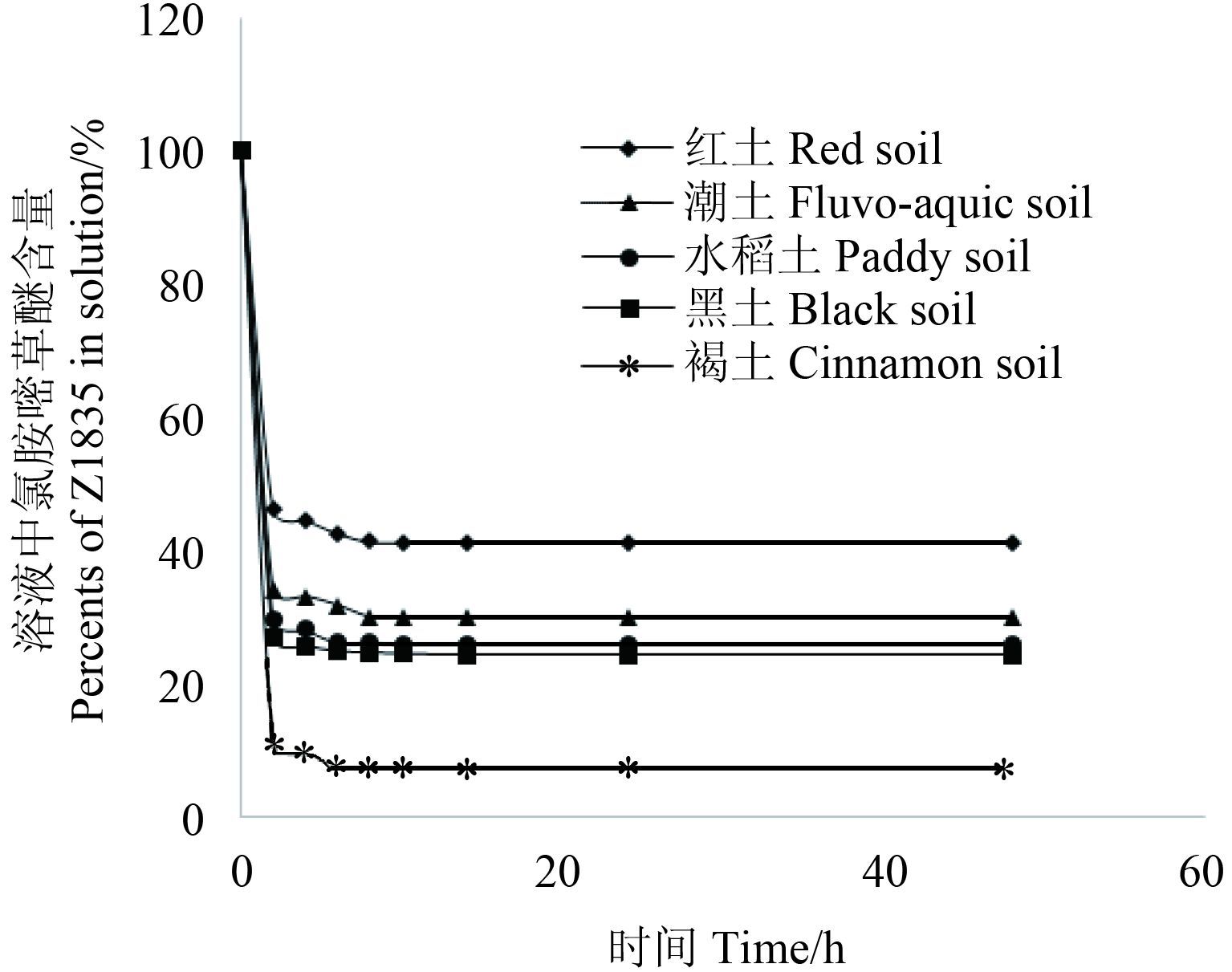
|
图 1 氯胺嘧草醚在土壤中的吸附动力学曲线 (25 ℃) Fig. 1 Kinetic curves of ZJ1835 adsorption in soils at 25 ℃ |
2.2 氯胺嘧草醚在土壤中的等温吸附特性
氯胺嘧草醚在 5 种土壤中的吸附等温曲线见图 2,其吸附线性模型和 Freundlich 模型参数见表 2。结果表明,线性模型所得 r 值小于 Freundlich 模型的 r 值,而且其 C0 有负值,因而采用 Freundlich 模型描述氯胺嘧草醚在 5 种土壤中的吸附相对更为合理。Freundlich 模型的 Kf 值与土壤吸附量和吸附强度有关。5 种土壤的 Kf 值在 6.991~18.49 之间,其大小顺序为:黑土 > 水稻土 > 褐土 > 潮土 > 红土。一般认为吸附常数 Kf 代表着土壤吸附能力的强弱,吸附常数越大,意味着土壤对农药的吸附能力越强。研究表明,氯胺嘧草醚在黑土中的吸附性最强。
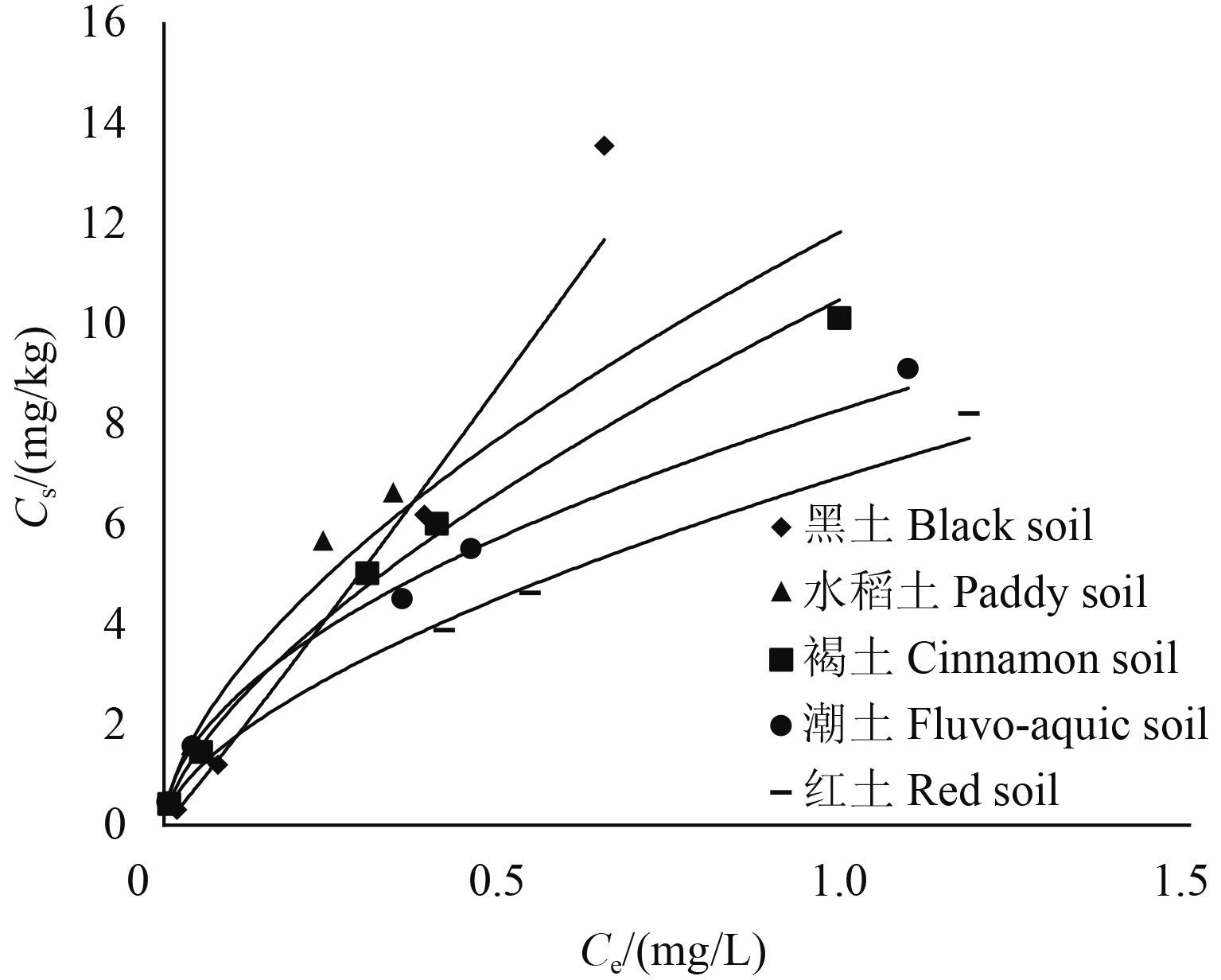
|
图 2 氯胺嘧草醚在 5 种土壤中的吸附等温线 Fig. 2 Adsorption isotherms of ZJ1835 in five soil samples |
|
|
表 2 氯胺嘧草醚在土壤中的等温吸附线性方程与 Freundlich 方程拟和结果比较 Table 2 Comparison of the results obtained from the Linear and Freundlich models for the adsorption of ZJ1835 by soils |
2.3 氯胺嘧草醚在土壤中的等温解吸特性
氯胺嘧草醚在 5 种土壤中的解吸特性也可用线性模型和 Freundlich 模型进行拟合,由表 3 可知,Freundlich 模型更为合适。滞后系数 HI 为不可逆吸附程度指标:当其为 0 或负值时,表示解吸的滞后性可忽略不计;当 0.7 < HI≤1.0 时,意味着解吸速率和吸附速率相似,两者等温线重合,无滞后作用;若 HI < 0.7,表明解吸速率小于吸附速率,为正滞后作用;当 HI > 1.0 时,为负滞后作用[17]。
|
|
表 3 氯胺嘧草醚在 5 种土壤中的解吸参数及滞后系数 Table 3 Desorption parameters and hysteresis coefficients of ZJ1835 in soils |
从表 3 中可看出:黑土和褐土中氯胺嘧草醚解吸过程的 HI 值均在 0.7~1.0 之间,其解吸速率几乎等于吸附速率,表明氯胺嘧草醚在这 2 种土壤中不存在明显滞后现象;其在红土、水稻土和潮土中解吸过程的 HI > 1.0,表明氯胺嘧草醚在这 3 种土壤中的解吸存在明显的负滞后现象。
2.4 氯胺嘧草醚在土壤中的有机碳吸附常数有机碳吸附常数 (KOC) 是评价非离子化合物在土壤中移动性的关键因子之一,通常比较稳定,基本不随土壤性质而变化,可用来表征化合物的疏水性,评估其在水-土系统中的迁移趋势,因而也是预测有机污染物在环境中归趋的重要参数。单正军等[18-20]采用 KOC 值对农药在土壤中的移动性进行了分类,认为:KOC 为 0~50 时,该农药具有高移动性;KOC 为 50~150 时,具有较高移动性;KOC 为 150~500 时,具有中等移动性;而 KOC 为 500~2 000 时,具有低移动性。
由表 4 可看出,氯胺嘧草醚在 5 种土壤中的移动性各不相同,但其 KOC 值范围均在 500~2 000 之间,表明氯胺嘧草醚在这 5 种土壤中均具有低移动性。因此,推测氯胺嘧草醚在田间正常使用不会对地下水和地表水造成风险。
|
|
表 4 氯胺嘧草醚在土壤中的有机碳吸附常数 Table 4 KOC values for ZJ1835 adsorption in soils |
2.5 氯胺嘧草醚在土壤中的移动性
农药在土壤中的移动性是评价其对地下水污染风险的重要指标。土壤薄层层析试验结果 (表 5) 表明,5 种土壤中氯胺嘧草醚含量最大值均位于薄层的 0~2.0 cm 处,从 6.0~8.0 cm 段开始,在各土壤中均未检测到氯胺嘧草醚,表明氯胺嘧草醚在供试 5 种土壤中移动性均很弱。其主要原因一方面可能是由于 5 种土壤对氯胺嘧草醚均具有较强的吸附作用,另一方面氯胺嘧草醚在水相中溶解度极低 (0.5 mg/L 20 ℃),其在水和土壤之间分配时进入水相的可能性较小。
|
|
表 5 氯胺嘧草醚在不同土壤薄层中的含量 Table 5 The determination results of ZJ1835 in different soil plates |
综合 2.4 节中 KOC 值和移动性试验结果,认为氯胺嘧草醚在田间正常使用不易对地下水和地表水造成污染风险。
2.6 氯胺嘧草醚在土壤中的吸附自由能和偏摩尔自由能化学物质在被吸附过程中自由能的变化可作为衡量其吸附作用强弱和推动力大小的依据,如偏摩尔自由能变化量越大则表明吸附作用越强。当吸附自由能绝对值 ΔG 小于 40 kJ/mol 时,为物理吸附,反之为化学吸附。物理吸附的农药,其吸附平衡速率较快,吸附是可逆过程,而化学吸附的平衡速率较慢,是不可逆过程,后者施入土壤后易钝化而失去活性[16]。
由表 6 可知:氯胺嘧草醚在 5 种土壤中的吸附自由能均为负值,其绝对值均小于 40 kJ/mol,说明氯胺嘧草醚在土壤中的吸附以物理吸附为主。其偏摩尔自由能 (−F 值) 大小顺序为: 黑土 > 水稻土 > 褐土 > 潮土 > 红土,和土壤吸附常数顺序一致,两者总体上呈正相关关系 (r = 0.873 4) 。
|
|
表 6 氯胺嘧草醚在 5 种土壤中的吸附自由能及偏摩尔自由能 (25 ℃) Table 6 Free energy (ΔG) and mean partial molar free energy change(−F) values for ZJ1835 adsorption in soils at 25 ℃ |
2.7 Kf 与土壤理化性质的相关性
有机质和黏粒含量被认为是影响土壤中农药吸附的关键因素[21]。此外,土壤 pH 值对农药在土壤中的吸附特性也具有一定影响[22]。本研究中氯胺嘧草醚在 5 种土壤中的 Kf 值与各土壤有机质含量、黏粒含量和 pH 值的单因子和多因子回归分析结果见表 7。从中可知,土壤有机质含量、黏粒含量和 pH 值均对氯胺嘧草醚的吸附有一定影响,其中 Kf 值与有机质含量和黏粒含量呈正相关,而与 pH 值呈负相关。但单个因子与 Kf 值的相关性均不显著,只有 2 个因子或 3 个因子组合时方能表现出较好的相关性。研究表明,土壤有机质含量、黏粒含量和 pH 值是影响氯胺嘧草醚在土壤中吸附的综合且主要支配因素。
|
|
表 7 氯胺嘧草醚在土壤中吸附常数 Kf 与土壤理化性质的相关性 Table 7 Relationship equation between properties and Kf for ZJ1835 adsorption in soils |
3 结论
1) 氯胺嘧草醚在土壤中的吸附过程分为 2 个较为明显的阶段:快速的线性分配阶段和慢速的吸附阶段,确定其吸附平衡时间为 24 h。氯胺嘧草醚的吸附和解吸等温线符合 Freundlich 模型,5 种土壤中 Kf 值大小顺序为:黑土 > 水稻土 > 褐土 > 潮土 > 红土。
2) 氯胺嘧草醚在黑土和褐土中的滞后系数 (HI) 在 0.7 和 1.0 之间,意味着其解吸速率和吸附速率相似,氯胺嘧草醚在这 2 种土壤中的吸附-解吸过程不存在明显的滞后现象。而在红土、水稻土和潮土中则存在明显的负滞后现象,推测其在后 3 种土壤中的迁移能力较弱。
3) 氯胺嘧草醚在供试 5 种土壤中的吸附均以物理吸附为主,其吸附是可逆过程。同时其 KOC 值在 500~2 000 之间,具有较低的移动性;薄层层析试验也表明,其在 5 种土壤中移动性均很弱;因此在正常使用过程中氯胺嘧草醚不易对地表水或地下水造成风险。
4) 氯胺嘧草醚在土壤中的吸附特性与土壤理化性质密切相关。其中土壤有机质含量、黏粒含量和 pH 值是主要的影响因素,吸附常数 Kf 值与土壤有机质含量和黏粒含量呈显著正相关性,而与土壤 pH 值呈负相关性。
| [1] |
刘维屏, 季瑾. 农药在土壤-水环境中归宿的主要支配因素——吸附和脱附[J]. 中国环境科学, 1996,16 (1):25–30.
LIU W P, JI J. One of the most important factors affecting the fate of pesticide in soil-water environmental: sorption and desorption[J]. [J] China Environ Sci, 1996, 16 (1):25–30. |
| [2] |
刘维屏.
农药环境化学[M]. 北京: 化学工业出版社, 2006 : 119 -160.
LIU W P. Pesticide environmental chemistry[M]. Beijing: Chemical Industry Press, 2006 : 119 -160. |
| [3] |
张伟, 王进军, 张忠明, 等. 烟嘧磺隆在土壤中的吸附及与土壤性质的相关性研究[J]. 农药学学报, 2006,8 (3):265–271.
ZHANG W, WANG J J, ZHANG Z M, et al. Adsorption of nicosulfuron on soils and its correlation with soil properties[J]. Chin J Pestic Sci, 2006, 8 (3):265–271. |
| [4] |
罗婧, 贾娜, 施海燕, 等. 丙溴磷在土壤中的吸附与迁移行为研究[J]. 环境科学与技术, 2011,34 (6):16–19.
LUO J, JIA N, SHI H Y, et al. Adsorption and mobility of profenofos in soils[J]. Environ Sci Technol, 2011, 34 (6):16–19. |
| [5] |
许秀莹, 宋稳成, 王鸣华. 氟啶胺在土壤中的吸附解吸与淋溶特性[J]. 中国环境科学, 2013,33 (4):669–673.
XU X Y, SONG W C, WANG M H. Adsorption-desorption and leaching characteristics of fluazinam in soils[J]. China Environ Sci, 2013, 33 (4):669–673. |
| [6] | OE CD. OECD guidelines for testing of chemicals, test guideline 106: adsorption/desorption using a batch equilibrium method[M]. Paris: Revised Draft Document OECD, 2000 : 1 -45. |
| [7] | BERMÚDEZ-COUSO A, FERNÁNDEZ-CALVIÑO D, PATEIRO-MOURE M, et al. Adsorption and desorption behavior of metalaxyl in intensively cultivated acid soils[J]. J Agric Food Chem, 2011, 59 (13):7286–7293. doi:10.1021/jf201028q |
| [8] |
吕龙, 吴军, 陈杰, 等. 2-嘧啶氧基苄基取代苯基胺类衍生物: CN 00130735.5[P]. 2003-11-12
LV L, WU J, CHEN J, et al. 2-Pyrimidinoxal benzyl substituted phenyl amine derivatives: CN 00130735.5[P]. 2003-11-12. |
| [9] | LU L, CHEN J, WU J, et al. New 2-pyrimidinyloxy-N-aryl-benzylamine derivatives, their processes and uses: US 6, 800, 590B2[P]. 2003-07-16. |
| [10] |
徐小燕, 董德臻, 台文俊, 等. N-苯基-2-(4,6-二甲氧基-2-嘧啶氧基)-6-氯-苄胺(ZJ1835)的除草活性研究[J]. 农药学学报, 2011,13 (4):427–430.
XU X Y, DONG D Z, TAI W J, et al. Study on herbicidal activity of innovative compound ZJ1835,[N-phenyl-2-(4,6-dimethoxy-2-oxypyrimidine)-6-chlorobenzylamine][J]. Chin J Pestic Sci, 2011, 13 (4):427–430. |
| [11] |
徐小燕, 唐伟, 姚燕飞, 等. 土壤环境因子对氯胺嘧草醚除草活性的影响[J]. 农药学学报, 2015,17 (3):357–361.
XU X Y, TANG W, YAO Y F, et al. Influence of soil environmental factors on herbicidal activity of ZJ1835[J]. Chin J Pestic Sci, 2015, 17 (3):357–361. |
| [12] | USEPA. Guidelines for registering pesticides in the United States[J]. Federal Register, 1975 (123):26881. |
| [13] |
李克斌, 刘维屏, 周瑛, 等. 灭草松在土壤中吸附的支配因素[J]. 环境科学, 2003,24 (1):126–130.
LI K B, LIU W P, ZHOU Y, et al. Factors dominating the sorption of bentazon in soils[J]. Environ Sci, 2003, 24 (1):126–130. |
| [14] | COX L, KOSKINEN W C, YEN P Y. sorption-desorption of imidacloprid and its metabolites in soils[J]. J Agric Food Chem, 1997, 45 (4):1468–1472. doi:10.1021/jf960514a |
| [15] | MORRICA P, BARBATO F, GIORDANO A, et al. Adsorption and desorption of imazosulfuron by soil[J]. J Agric Food Chem, 2000, 48 (12):6132–6137. doi:10.1021/jf000152d |
| [16] |
逯忠斌, 侯志广, 王秀梅. 新农药HW-02在土壤中的吸附[J]. 环境科学研究, 2009,22 (7):851–855.
LU Z B, HOU Z G, WANG X M. Adsorption of novel herbicide HW-02 on soils[J]. Res Environ Sci, 2009, 22 (7):851–855. |
| [17] | BARRIUSO E, LAIRD D A, KOSKINEN W C, et al. Atrazine desorption from smectites[J]. Soil Sci Soc Amer J, 1994, 58 (6):1632–1638. doi:10.2136/sssaj1994.03615995005800060008x |
| [18] |
单正军, 朱忠林, 华晓梅, 等. 除草剂拉索对地下水影响研究[J]. 环境科学学报, 1994,14 (1):72–78.
SHAN Z J, ZHU Z L, HUA X M, et al. Influence of alachlor on groundwater[J]. Acta Scientiae Circumstantiae, 1994, 14 (1):72–78. |
| [19] |
黄超, 吴文铸, 单正军, 等. 壬基酚在土壤中的吸附和淋溶特性[J]. 生态环境学报, 2015,24 (12):2062–2067.
HUANG C, WU W Z, SHAN Z J, et al. Adsorption and leaching of nonylphenol in soils[J]. Ecol Environ Sci, 2015, 24 (12):2062–2067. |
| [20] |
石利利, 单正军, 蔡道基. 三唑磷农药在土壤中的降解与吸附特性研究[J]. 农业环境科学学报, 2006,25 (3):733–736.
SHI L L, SHAN Z J, CAI D J. Degradation and adsorption characteristics of triazophos in soils[J]. J Agro-Environ Sci, 2006, 25 (3):733–736. |
| [21] | STOUGAARD R N, SHEA P J, MARTIN A R. Effect of soil type and pH on adsorption, mobility, and efficacy of imazaquin and imazethapyr[J]. Weed Sci, 1990, 38 (1):67–73. |
| [22] |
欧晓明, 余淑英, 罗玲, 等. 新农药硫肟醚在土壤上的吸附[J]. 农业环境科学学报, 2007,26 (2):577–582.
OU X M, YU S Y, LUO L, et al. Adsorption of novel oxime insecticide HNPC-A9908 on soils[J]. J Agro-Environ Sci, 2007, 26 (2):577–582. |
 2016, Vol. 18
2016, Vol. 18


