小麦纹枯病,又称小麦尖眼斑病(wheat sharp eyespot),是一种世界性分布的土传真菌病害,其致病菌主要为禾谷丝核菌Rhizoctonia cerealis,主要为害小麦的茎秆基部,可造成植株倒伏、枯死、白穗,影响小麦有效穗数及千粒重,对产量影响较大[1]。近年来该病在中国冬小麦种植区发生普遍,已成为小麦高产、稳产的重大障碍[2]。河南省是中国小麦主产区之一,近几年小麦纹枯病的发生面积连续在300万公顷左右,危害严重[3]。目前尚未发现高抗纹枯病的小麦品种,控制该病害主要依靠三唑酮、苯醚甲环唑和戊唑醇等三唑类药剂种子处理,结合春季井冈霉素茎基部喷雾来进行化学防治[4-5]。随着同类药剂的连续应用,小麦纹枯病菌对井冈霉素及三唑酮的敏感性降低,或产生了不同程度的抗性[6];但Hamda等[7]报道,采自江苏、安徽、河南3省的小麦纹枯病菌菌株对苯醚甲环唑仍较为敏感。到目前为止,尚未见有关河南省小麦纹枯病菌对戊唑醇敏感性现状的报道。为此,本研究采用菌丝生长速率法,测定了2013年从河南省15个地市分离的95株小麦纹枯病菌对戊唑醇和苯醚甲环唑的敏感性,建立了其相对敏感基线,分析了不同地区菌株的敏感性差异及供试菌株对2种杀菌剂敏感性间的相关性,以期为三唑类杀菌剂在小麦纹枯病防治中的合理利用提供依据,为田间病原菌敏感性监测提供信息。
1 材料与方法 1.1 供试菌株2013年4-5月,从河南省各地市大面积种植小麦的乡镇采集纹枯病标本,在同一乡镇尽可能扩大采样地块,5点取样法采样,每个乡镇至少采集50个小麦植株;选取发病典型的小麦植株,去除根部及茎秆上部,剥去叶鞘,保留茎秆基部具有典型云纹状病斑的茎段。室内采用组织分离法分离病菌,共获得343株,转入PSA斜面上,室温保存;每地随机选取4~8株进行单菌丝顶端纯化,共95株用于试验;对95株病菌进行细胞核染色及培养性状测定,经鉴定均为禾谷丝核菌Rhizoctonia cerealis。
1.2 药剂及试剂97%苯醚甲环唑(difenoconazole)原药,先正达(中国)投资有限公司生产;97%戊唑醇(tebuconazole)原药,广西田园生化股份有限公司生产。原药均预溶于甲醇中,配成104 μg/mL母液,于4 ℃冰箱中保存。蔗糖为分析纯,天津科密欧化学试剂有限公司;琼脂粉:生物技术级,合肥新恩源生物技术有限公司。
1.3 病原菌对2种杀菌剂的敏感性测定采用菌丝生长速率法[8]。将供试菌株在PSA平板上25 ℃培养3 d后,在菌落边缘打取直径5 mm的菌饼,菌丝面朝下分别接入含苯醚甲环唑0.025、0.05、0.1、0.5、2.5及5 μg/mL,或戊唑醇0.003、0.005、0.01、0.03、0.05及0.1 μg/mL的PSA平板上。每皿接种1个菌饼,每处理重复3次,以不含药剂的PSA平板上接种的菌饼作对照。25 ℃下培养5 d后采用十字交叉法测量菌落直径(mm),按(1)式计算各浓度处理下药剂对菌丝生长的抑制率(%)。

|
(1) |
参照祁之秋等的方法[9]。将病菌群体对供试药剂的敏感性从高到低分成不同区间,统计EC50值在各个区间的菌株占整个群体的频率(%)。以EC50值为x轴,相应的频率(%)为y轴,即得到病菌群体对该种杀菌剂的敏感性频率分布图。根据病原菌的敏感性频率分布图建立其对苯醚甲环唑和戊唑醇的相对敏感基线。
1.5 小麦纹枯病菌对苯醚甲环唑与对戊唑醇的敏感性比较参照齐永志等的方法[10]。从各地市随机选取3~5株纹枯病菌进行敏感性相关性分析,其中苯醚甲环唑敏感菌株18株,敏感性下降菌株22株,而这40株菌株对戊唑醇的敏感性仅表现为2株下降,其余均敏感。将苯醚甲环唑对菌株的EC50值作为x轴,戊唑醇对菌株的EC50值为y轴,进行线性回归分析,求出线性回归方程y=bx + a,根据决定系数(R2)、b值及F检验的显著水平(P值),分析苯醚甲环唑与戊唑醇对纹枯病菌毒力之间的关系:P < 0.05,b值为正,说明两种药剂间存在正相关性,b值为负,说明两种药剂间存在负相关性,R2越大,则相关性越强;P > 0.05,说明两种药剂间无相关性[10]。
1.6 数据处理所得数据采用Excel 2003进行处理,利用DPS V6.55软件求出药剂对菌株的毒力回归方程、相关系数和有效中浓度值(EC50),并进行Shapiro-Wilk正态性检验[11]和地区间的差异显著性分析(最小显著差异法,Least Significant Difference, LSD);利用SPSS 20.0进行聚类分析[9]。
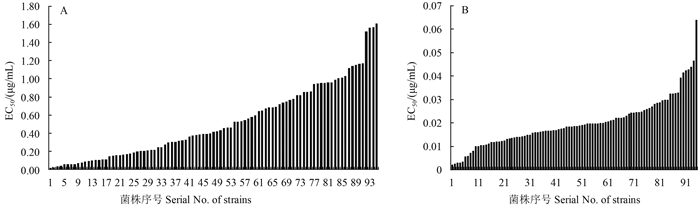
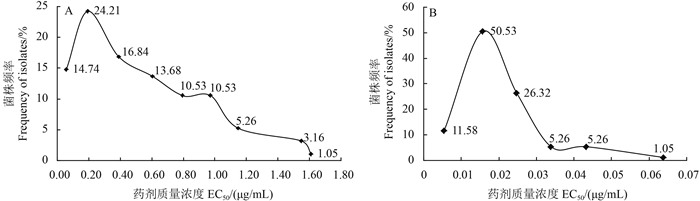
2 结果与分析 2.1 小麦纹枯病菌对苯醚甲环唑及戊唑醇的敏感性及相对敏感基线研究结果表明:供试95株小麦纹枯病菌对苯醚甲环唑的敏感性基本呈连续性分布,EC50值在0.014~1.609 μg/mL之间,最大值为最小值的116倍,平均值为(0.515±0.401) μg/mL (图 1A)。将上述EC50值分为9个区间,每个区间菌株出现的频率如图 2A所示。通过DPS分析Shapiro-Wilk正态性检验结果,显示菌株对苯醚甲环唑的敏感性频率分布不符合正态性分布(W=0.917,P=1.7 × 10-5 < 0.05),表明小麦纹枯病菌对药剂的敏感性发生了分化,并已出现敏感性下降的亚群体,但其中仍有44.2%的菌株(42株)集中位于图 2A中相应的主峰范围内,其敏感性频率分布均为连续单峰曲线,显示该群体对苯醚甲环唑的敏感性频次分布呈近似正态分布(W=0.950,P=0.066 > 0.05),其平均EC50值为(0.165±0.101) μg/mL,可将此值作为小麦纹枯病菌对苯醚甲环唑的相对敏感基线。
|
图 1 小麦纹枯病菌对苯醚甲环唑(A)和戊唑醇(B)的敏感性 Fig. 1 EC50 values of R. cerealis populations to difenoconazole (A) and tebuconazole (B) |
|
图 2 小麦纹枯病菌对苯醚甲环唑(A)和戊唑醇(B)的敏感性频率分布 Fig. 2 Frequency distribution of EC50 values of R. cerealis populations to difenoconazole (A) and tebuconazole (B) |
供试95株小麦纹枯病菌对戊唑醇的敏感性基本呈连续性分布,EC50值在0.002~0.064 μg/mL之间,最大值为最小值的34倍,平均值为(0.020±0.010) μg/mL (图 1B)。将上述EC50值划分为6个区间,每个区间菌株出现的频率如图 2B所示。通过DPS分析Shapiro-Wilk正态性检验结果,显示菌株对戊唑醇的敏感性频率分布不符合正态性分布(W=0.923,P=3.2 × 10-5 < 0.05),表明小麦纹枯病菌对药剂的敏感性出现了分化,并已出现敏感性下降的亚群体,但其中仍有95.8%的菌株(91株)集中位于图 2B中相应的主峰范围内,其敏感性频率分布为连续单峰曲线,显示此部分菌株对戊唑醇的敏感性频率分布呈近似正态分布(W=0.977,P=0.112 > 0.05),其平均EC50值为(0.019±0.008) μg/mL,将此值作为小麦纹枯病菌对戊唑醇的相对敏感基线。
苯醚甲环唑的平均EC50值是戊唑醇的26倍,表明病原菌对戊唑醇更为敏感。
2.2 小麦纹枯病菌对苯醚甲环唑和戊唑醇的敏感性比较由表 1可以看出,不同地区病原菌群体间对苯醚甲环唑和戊唑醇的敏感性均存在显著性差异。苯醚甲环唑的平均EC50值变化范围在0.055~1.317 μg/mL,漯河菌株最为敏感,而驻马店菌株则最不敏感,敏感性相差24倍;戊唑醇的平均EC50值变化范围在0.003~0.037 μg/mL,鹤壁菌株最为敏感,而信阳菌株则最不敏感,敏感性相差12倍。由表 1还可发现,小麦纹枯病菌对2种杀菌剂的敏感性菌株并非来自同一地区。
|
|
表 1 河南省不同地区小麦纹枯病菌对苯醚甲环唑及戊唑醇的敏感性比较 Table 1 Sensitivity (EC50 value) to difenoconazole and tebuconazole of R. cerealis strains from different areas in Henan province |
2.3 不同地理来源菌株对苯醚甲环唑和戊唑醇敏感性水平的系统聚类分析
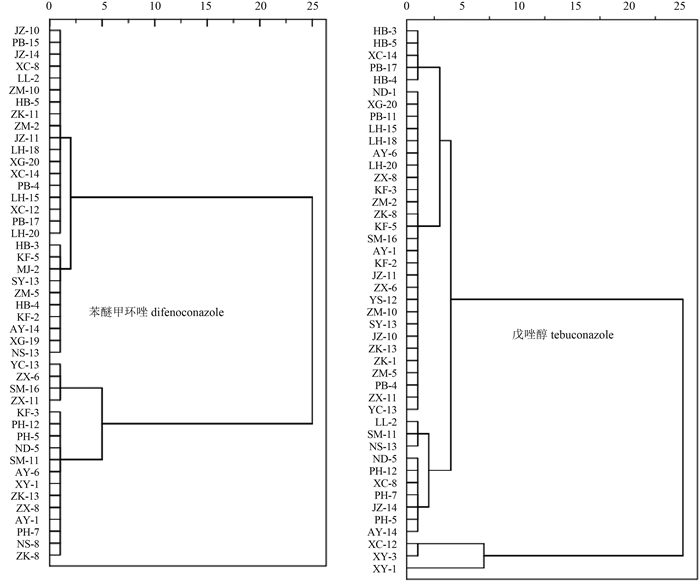
每个地区随机选择3株,共45株小麦纹枯病菌,采用SPSS软件对苯醚甲环唑和戊唑醇抑制病菌菌丝生长的EC50值进行聚类分析。结果(图 3)表明:苯醚甲环唑对45个菌株的EC50值共分在4个聚类组中,包括的菌株数分别为18、10、4和13个;戊唑醇对45个菌株的EC50值分在6个聚类组中,包括的菌株数分别为5、27、3、7、2和1个。不同来源的菌株系列出现在同一聚类组中,表明小麦纹枯病菌对2种杀菌剂的敏感性差异与菌株来源的地理位置无明显相关性,这与最小显著差异法的分析结果相对应。尽管每种杀菌剂对菌株的EC50值可分为不同的聚类组,但2种杀菌剂的聚类组所包含的菌株并无相似之处。
|
图 3 苯醚甲环唑和戊唑醇对小麦纹枯病菌EC50值的系统聚类分析 Fig. 3 Hierarchical cluster analysis on EC50 values of difenoconazole and tebuconazole to R. cerealis |
2.4 小麦纹枯病菌对苯醚甲环唑与对戊唑醇敏感性的相关性
EC50值线性回归分析结果表明:小麦纹枯病菌菌株对苯醚甲环唑的敏感性与其对戊唑醇敏感性的决定系数(R2)为0.026 (y=0.003x + 0.016),F检验的显著水平(P值)为0.000 1,小于0.05,即在P=0.05水平上差异显著,b值为正,说明病菌对2种药剂的敏感性间存在正相关性,但R2较小,相关性较弱。
3 小结与讨论本研究结果表明:戊唑醇对小麦纹枯病菌菌丝生长的抑制作用优于苯醚甲环唑;不同菌株之间对药剂的敏感性差异较大,这可能源自病原菌本身的生理差异以及其群体组成的复杂多样性;不同地区来源的病菌群体对苯醚甲环唑和戊唑醇的敏感性均存在显著性差异,个别地区的菌株对苯醚甲环唑的敏感性已表现下降,说明不同地区或地块的用药水平已引起病原菌对苯醚甲环唑敏感性的变化。由此可以看出,河南省小麦纹枯病菌株对戊唑醇仍表现敏感,但对苯醚甲环唑的敏感性已出现分化,生产中应密切监测不同地区菌株对苯醚甲环唑的抗药性发展动态。
苯醚甲环唑和戊唑醇同属于脱甲基抑制剂中的三唑类化合物,其作用靶标是病原真菌体内的C14-α-脱甲基酶。两类药剂作用于小麦纹枯病菌后,均可导致菌丝生长受阻、菌体内麦角甾醇含量降低[12-13];苯醚甲环唑还对真菌的孢子萌发有抑制作用[14];两种药剂在田间均对小麦纹枯病有很好的防效[15]。本研究结果表明:两种药剂对小麦纹枯病菌的菌丝生长均具有较高的抑制活性。祁之秋[16]在2001年测定了采自中国江苏及安徽两省的50个小麦纹枯病菌菌株对戊唑醇的敏感性,得其平均EC50值及敏感性基线分别为0.038和0.046 μg/mL。Hamda等[7]用采自江苏、河南、安徽的95个菌株,建立了对苯醚甲环唑的敏感性基线为0.062 μg/mL。本研究结果与祁之秋及Hamda等的结果有所差异,这可能是由于菌株的地理来源及用药年份不同造成的。
尽管两种药剂对小麦纹枯病菌均有很好的抑制活性,但两种药剂对同一地区菌株的毒力相差较大,均表现出同一地区菌株对戊唑醇较苯醚甲环唑更为敏感的特点,如本研究中苯醚甲环唑对驻马店和鹤壁菌株的EC50值分别是戊唑醇的83和117倍。王文桥等[17]的研究结果也表明:戊唑醇对小麦纹枯病菌的抑制活性明显高于苯醚甲环唑。这可能是由于测定菌株数较少造成的。另外,不同地块的用药水平、菌株基因突变等也可能造成此结果的出现。
刘英华等[18]的研究表明:室内通过药剂驯化获得的小麦纹枯病菌戊唑醇抗性菌株,对其他三唑类杀菌剂,包括三唑酮、丙环唑等均具有交互抗性。本研究表明:小麦纹枯病菌对同属于三唑类杀菌剂的苯醚甲环唑和戊唑醇的敏感性间也存在着微弱的正相关性。但同刘英华等在药剂毒力相关性的试验及分析方法上有所区别,刘英华等所用的亲本敏感菌株只有1个,采自中国山东省泰山中天门狗尾草上[4],而本文进行相关性测定所用菌株中敏感性菌株占近50%,且敏感性下降菌株抗性倍数较低;刘英华等直接用药剂对抗性菌株的EC50值同对亲本菌株的EC50值做比较,得出不同药剂毒力间的关系,本研究则是建立在数学统计分析的基础上分析病原菌对药剂敏感性的关系。
由于小麦纹枯病菌对三唑类杀菌剂的抗药性属于低度风险,故三唑类药剂依然可用于生产中防治小麦纹枯病,但应根据各地区菌株对不同药剂的敏感性水平来选择合适的药剂;同时为避免抗药性的产生,应同其他防治方法相结合施用。Peng等[19]将苯醚甲环唑同枯草芽孢杆菌NJ-18协同使用,不但防治效果比单剂高,而且还降低了剂量,延缓了抗药性的产生。这为三唑类药剂在小麦纹枯病化学防治上的应用指明了新的方向。
| [1] | LEMAŃCZYK G, KWAŚNA H. Effects of sharp eyespot (Rhizoctonia cerealis) on yield and grain quality of winter wheat[J]. Eur J Plant Pathol, 2013, 135 (1):187–200. doi:10.1007/s10658-012-0077-3 |
| [2] | HAMADA M S, YIN Y N, CHEN H G, et al. The escalating threat of Rhizoctonia cerealis, the causal agent of sharp eyespot in wheat[J]. Pest Manag Sci, 2011, 67 (11):1411–1419. doi:10.1002/ps.2236 |
| [3] |
汪敏, 吕柏林, 邢小萍, 等. 河南省小麦纹枯病菌的群体组成及其致病力分化研究[J]. 植物病理学报, 2011,41 (5):556–560.
WANG M, LV B L, XING X P, et al. Composition and virulence variation of the pathogen of wheat sharp eyespot from Henan Province[J]. Acta Phytopathologica Sinica, 2011, 41 (5):556–560. |
| [4] |
孙海燕, 丁晓菲, 杜文珍, 等. 江苏、河南、安徽和山东四省小麦纹枯病菌对井冈霉素的敏感性监测[J]. 农药学学报, 2011,13 (6):653–656.
SUN H Y, DING X F, DU W Z, et al. Monitoring of sensitivity of Rhizoctonia cerealis to jinggangmycin in Jiangsu, Henan, Anhui and Shandong provinces[J]. Chin J Pestic Sci, 2011, 13 (6):653–656. |
| [5] | ZHOU M G, JIA X J. Wheat pathogens in China[M]//ISHⅡ H, HOLLOMON D W. Fungicide resistance in plant pathogens:principles and a guide to practical management. Tokyo:Springer, 2015:313-328. |
| [6] |
胡燕, 王怀训, 夏晓明, 等. 四地区小麦纹枯病菌对6种杀菌剂的抗性比较[J]. 植物保护学报, 2006,33 (4):423–427.
HU Y, WANG H X, XIA X M, et al. Susceptibility of Rhizoctonia cerealis to six fungicides in four wheat areas[J]. Acta Phytophylacita Sinica, 2006, 33 (4):423–427. |
| [7] | HAMADA M S, YIN Y N, MA Z H. Sensitivity to iprodione, difenoconazole and fludioxonil of Rhizoctonia cerealis isolates collected from wheat in China[J]. Crop Prot, 2011, 30 (8):1028–1033. doi:10.1016/j.cropro.2011.04.004 |
| [8] |
慕立义.
植物化学保护研究方法[M]. 北京: 中国农业出版社, 1994 : 79 -81.
MU L Y. Research techniques of plant chemical protection[M]. Beijing: China Agriculture Press, 1994 : 79 -81. |
| [9] |
祁之秋, 鞠雪娇, 纪明山, 等. 辽宁省稻瘟病菌对咪鲜胺敏感基线的建立[J]. 农药学学报, 2012,14 (6):673–676.
QI Z Q, JU X J, JI M S, et al. Sensitive baseline of Magnaporthe grisea to prochloraz in Liaoning province[J]. Chin J Pestic Sci, 2012, 14 (6):673–676. |
| [10] |
齐永志, 李海燕, 苏媛, 等. 小麦纹枯病菌对噻呋酰胺的敏感性及抗药性突变体的主要生物学性状[J]. 农药学学报, 2014,16 (3):271–280.
QI Y Z, LI H Y, SU Y, et al. Sensitivity to trifluzamide and main biological characteristics of resistant mutants of Rhizoctonia cerealis[J]. Chin J Pestic Sci, 2014, 16 (3):271–280. |
| [11] |
甘林, 代玉立, 滕振勇, 等. 福建省玉米小斑病菌对丙环唑、烯唑醇和咪鲜胺的敏感性[J]. 农药学学报, 2016,18 (2):194–200.
GAN L, DAI Y L, TENG Z Y, et al. Sensitivity of Bipolaris maydis to propiconazole, diniconazole and prochloraz in Fujian province[J]. Chin J Pestic Sci, 2016, 18 (2):194–200. |
| [12] |
祁之秋, 周明国. 戊唑醇对小麦纹枯病菌的抑菌作用[J]. 农药学学报, 2003,5 (3):80–84.
QI Z Q, ZHOU M G. Antifungal activity of tebuconazole to Rhizoctonia cerealis[J]. Chin J Pestic Sci, 2003, 5 (3):80–84. |
| [13] |
吴学宏, 肖建华, 张文华, 等. 2%三唑醇·戊唑醇种衣剂对小麦纹枯病菌麦角甾醇含量的影响[J]. 农药学学报, 2005,7 (4):372–375.
WU X H, XIAO J H, ZHANG W H, et al. Effect of triadimenol and tebuconazole on the content of ergosterol of wheat Rhizoctonia cerealis[J]. Chin J Pestic Sci, 2005, 7 (4):372–375. |
| [14] | MUNKVOLD G P. Seed pathology progress in academia and industry[J]. Annu Rev Phytopathol, 2009, 47 :285–311. doi:10.1146/annurev-phyto-080508-081916 |
| [15] |
孙炳剑, 雷小天, 袁虹霞, 等. 小麦纹枯病化学防治药剂的筛选[J]. 麦类作物学报, 2007,27 (5):914–918.
SUN B J, LEI X T, YUAN H X, et al. Screening of the fungicides for the chemical control of wheat sharp eyespot[J]. J Triticeae Crops, 2007, 27 (5):914–918. |
| [16] |
祁之秋.小麦纹枯病菌对常用杀菌剂敏感性基线及化学防治原理研究[D].南京:南京农业大学, 2001:21-23.
QI Z Q. Study on the sensitivity baseline of Rhizoctonia cerealis to modern fungicides and the principle of chemical control[D]. Nanjing:Nanjing Agricultural University, 2001:21-23. http://cdmd.cnki.com.cn/article/cdmd-10307-2001012921.htm |
| [17] |
王文桥, 韩秀英, 张小风, 等. 防治小麦纹枯病的杀菌剂筛选[J]. 华北农学报, 2007,22 (Suppl):230–234.
WANG W Q, HAN X Y, ZHANG X F, et al. Selection of fungicides in controlling wheat sharp eyespot caused by Rhizoctonia cerealis[J]. Acta Agriculturae Boreali-Sinica, 2007, 22 (Suppl):230–234. |
| [18] |
刘英华, 王开运, 姜兴印, 等. 禾谷丝核菌对戊唑醇的抗性及抗药性菌系生物学特性[J]. 植物保护学报, 2003,30 (4):423–428.
LIU Y H, WANG K Y, JIANG X Y, et al. Resistance of Rhizoctonia cerealis to tebuconazole and the biological characters of tebuconazole-resistant strains[J]. Acta Phytophylacita Sinica, 2003, 30 (4):423–428. |
| [19] | PENG D, LI S D, CHEN C J, et al. Combined application of Bacillus subtilis NJ-18 with fungicides for control of sharp eyespot of wheat[J]. Biol Control, 2014, 70 :28–34. doi:10.1016/j.biocontrol.2013.11.013 |
 2016, Vol. 18
2016, Vol. 18


