农药的光解和水解特性是农药环境行为的重要组成部分,是评价农药对生态环境影响的重要指标[1]。对农药光解和水解特性的研究有利于了解农药在环境中的降解转化规律,对于农药的安全性评价,解决农药带来的环境污染问题有重要作用[2]。
噻呋酰胺 (thifluzamide),化学名称为 2',6'-二溴-2-甲基-4'-三氟甲氧基-4-三氟甲基-1,3-噻唑-5-羧酰苯胺 (结构式见图式 1),是由美国孟山都公司开发的噻唑酰胺类杀菌剂,商品名为满穗[3]。噻呋酰胺具有用量少、毒性低、药效高、内吸传导性强和持效性长等特性,对致病真菌有良好活性,尤其对担子菌纲真菌引起的纹枯病、立枯病等有效。目前,对噻呋酰胺的研究主要限于合成、药效和残留方面[4-7],有关噻呋酰胺在溶液中的光解和水解特性的研究未见报道。本研究采用室内模拟方法,对噻呋酰胺光解和水解特性及影响因素进行了系统的研究,旨在为噻呋酰胺的合理使用和环境安全性评价提供科学依据。
|
图式 1 噻呋酰胺结构式 Scheme1 Structure of thifluzamide |
1 材料与方法 1.1 主要仪器与试剂
Agilent1260 型高效液相色谱仪 (配 UV 检测器,美国 Agilent 科技有限公司);XT5409 型光稳定性试验箱 (杭州雪中炭恒温技术有限公司)。
99.8% 噻呋酰胺 (thifluzamide) 标准品 (上海市农药研究所);乙腈 (色谱纯,美国 TEDIA 试剂公司);其余试剂均为分析纯。
柠檬酸盐缓冲液 (pH 4.0)、磷酸盐缓冲液 (pH 7.0) 和硼酸盐缓冲液 (pH 9.0) 均按标准方法[8]现配现用。
1.2 HPLC 检测条件Eclipse XDB-C18 色谱柱 (25.0 cm × 4.6 mm,5.0 μm),流动相为 V (乙腈):V (水) = 70:30,检测波长 225 nm,流速 1.0 mL/min,进样量 20 μL,柱温 30 ℃。在此条件下,噻呋酰胺的保留时间为 6.80 min。
1.3 标准溶液的配制及标准曲线的绘制称取噻呋酰胺标准品,用甲醇溶解并配制成 1 000 mg/L 的标准母液,再用 V (乙腈) : V (水) = 70 : 30 溶液梯度稀释成质量浓度分别为 0.5、1.0、2.0、5.0 和 10.0 mg/L 的标准溶液,在上述 HPLC 条件下进行测定,以噻呋酰胺峰面积为纵坐标,噻呋酰胺质量浓度为横坐标绘制标准曲线。
1.4 光解试验按文献[9]进行。1) 噻呋酰胺在不同 pH 缓冲溶液 (噻呋酰胺 5 mg/L,pH 值分别为 4、7、9)、不同溶剂 (正己烷、乙腈、甲醇、乙酸乙酯和超纯水) 中的光解试验;2) 分别在噻呋酰胺标准溶液中添加 0、0.5、1、5 和 10 mmol/L 的 Fe2+ 和 Fe3+ 及 0、0.5、5、25、50 mg/L 的腐殖酸 (噻呋酰胺 5 mg/L),研究环境共存物质对噻呋酰胺光解的影响。
光源为紫外灯,辐照度为 3.00 mW/cm2,额定功率为 8 W × 2,石英管距光源 10 cm,温度保持 (25 ± 1) ℃。光照不同时间后分别取样,按 1.2 节的色谱条件检测溶液中噻呋酰胺的含量。每处理 3 次重复,同时设黑暗对照。
1.5 水解试验根据文献[10]进行不同 pH 值 (4、7、9) 的缓冲溶液和不同温度 (15、25 和 35 ℃) 对噻呋酰胺水解的影响,噻呋酰胺质量浓度为 5 mg/L,分别于 0、10、30、50、70、100 和 120 d 采集水样,按 1.2 节的色谱条件检测噻呋酰胺的含量,每处理 3 次重复。分别在噻呋酰胺标准溶液中添加 0、100、300 和 500 mg/L 的十二烷基磺酸钠 (SDS) 和十六烷基三甲基溴化铵 (CTAB),于 35 ℃、pH 7 的条件下进行水解试验,研究表面活性剂对噻呋酰胺水解的影响。
1.6 数据处理噻呋酰胺在溶液中的光解和水解可按一级动力学方程描述。分别按 (1)~(4) 式计算噻呋酰胺在不同条件下的降解方程、半衰期 (t1/2,min或d)、温度效应系数 (Q) 和反应活化能 (Ea,kJ/mol)。

|
(1) |
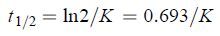
|
(2) |
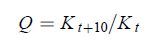
|
(3) |
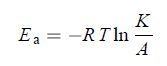
|
(4) |
式中:ct 为 t 时刻噻呋酰胺残留的质量浓度 (mg/L);c0 为噻呋酰胺的初始质量浓度 (mg/L);K 为速率常数 (min-1);R 为气体常数 [8.314 J/(K•mol)];T 为热力学温度 (K);A 为频率因子。
2 结果与讨论 2.1 噻呋酰胺标准曲线在 0.5~10.0 mg/L 范围内,噻呋酰胺质量浓度与峰面积间呈良好线性关系,线性回归方程为 y = 36.773x + 0.609 7,R2 = 1,表明此方法可满足噻呋酰胺定量检测要求。
2.2 噻呋酰胺光解速率的影响因素 2.2.1 pH 值从表 1 可以看出:噻呋酰胺在 pH 值为 9 的碱性条件下最易光解,其光解速率比酸性条件 (pH = 4) 下提高了 22 倍。表明酸性条件可降低其光解速率。
|
|
表 1 噻呋酰胺在不同 pH 值中的光解动力学参数 Table 1 The photolytic kinetics parameters of thifluzamide buffer solutions with different pH value |
2.2.2 溶剂
噻呋酰胺在不同溶剂中的光解速率存在显著差异,表现为正己烷 > 乙腈 > 甲醇 > 乙酸乙酯 > 超纯水 (表 2)。其原因可能与溶剂性质、溶剂与噻呋酰胺分子间的作用力以及溶剂本身对光的吸收有关。正己烷、乙腈和甲醇的最大吸收波长均小于 220 nm,而乙酸乙酯的最大吸收波长为 260 nm。在正己烷、乙腈和甲醇中,噻呋酰胺能吸收到较多的光能,能量增加,被激活而进行光分解;而在乙酸乙酯中则大部分光量子被乙酸乙酯吸收,较少的光能被噻呋酰胺吸收,所以噻呋酰胺降解较慢。
|
|
表 2 噻呋酰胺在不同溶剂中的光解动力学参数 Table 2 The photolytic kinetics parameters of thifluzamide in different organic solvents |
2.2.3 环境共存物质
如图 1 所示,噻呋酰胺光解速率常数随铁离子浓度的增加而减小,即铁离子抑制噻呋酰胺光解,且 Fe2+ 对其抑制作用较 Fe3+ 大。
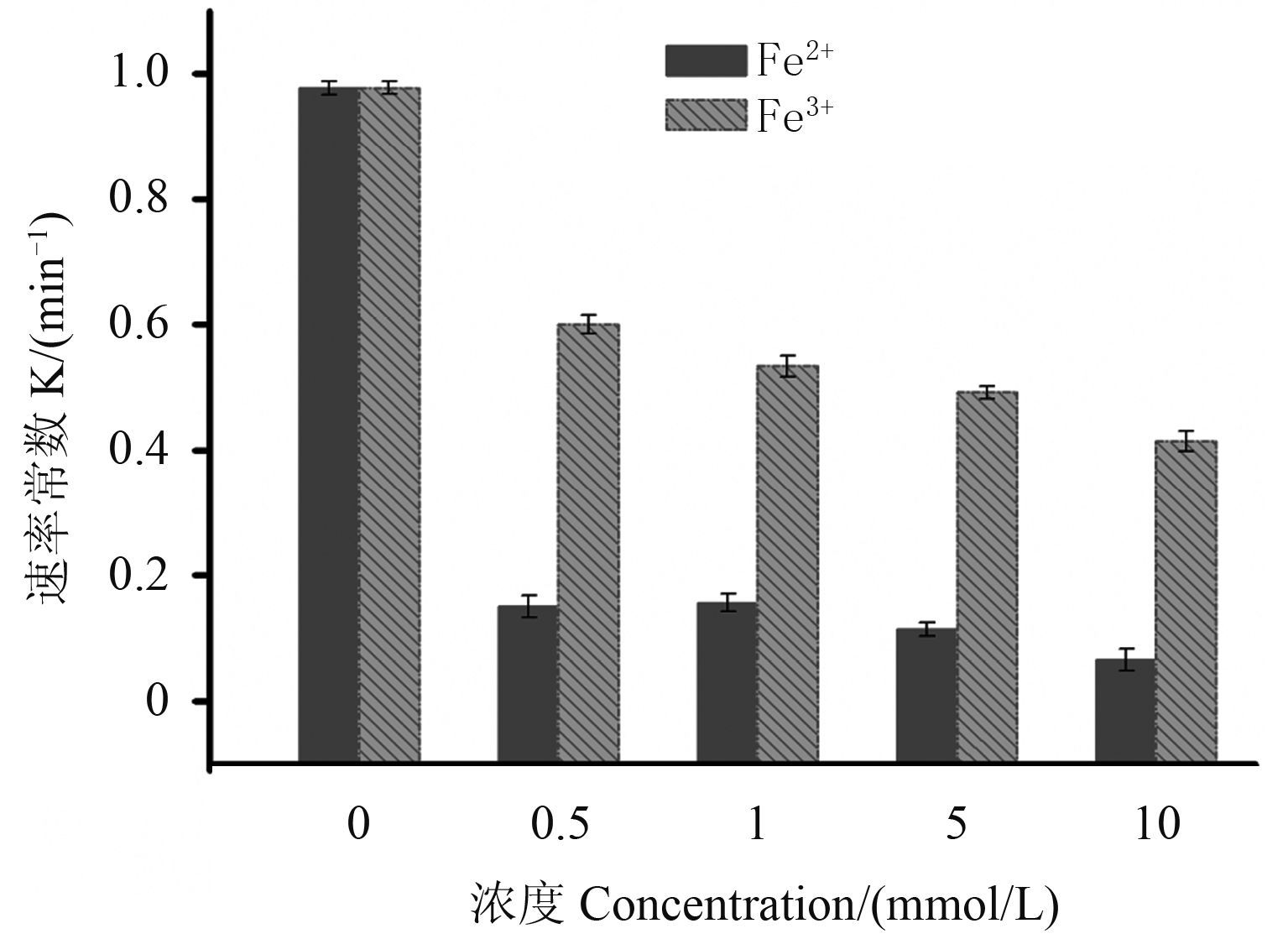
|
图 1 Fe3+ 和 Fe2+ 浓度对噻呋酰胺光解的影响 Fig. 1 Effects of ferrous and ferric ions on photodegradation of thifluzamide |
随着光照时间的增加,溶液的颜色加深,说明铁离子对噻呋酰胺的光吸收起到屏蔽作用。在中性溶液中,存在 Fe(OH)3、Fe(OH)2、水合铁离子、光解产物及各种羟基络合物,不仅增大了溶液的浊度,起到屏蔽作用,而且会竞争对光的吸收,从而抑制噻呋酰胺的光解。另外,Fe3+ 可以在光照条件下产生羟基自由基促进噻呋酰胺的间接光氧化降解,所以 Fe3+ 抑制作用比 Fe2+ 抑制作用弱[11]。
由表 3 中可以看出:添加腐殖酸可抑制噻呋酰胺的光解,且抑制作用随添加浓度的升高而加强。这与花日茂等[12]关于腐殖酸对丁草胺光解的影响结果一致。而黑暗条件下噻呋酰胺在以上所有光解试验中均未降解。
|
|
表 3 腐殖酸对噻呋酰胺光解的影响 Table 3 Effects of humic acid on the photodegradation of thifluzamide |
2.3 噻呋酰胺水解的影响因素 2.3.1 温度和 pH 值
结果 (表 4) 表明:相同 pH 值条件下,温度越高,噻呋酰胺的水解速率常数越大,反应速率越快。不同 pH 值条件下升高相同温度,噻呋酰胺水解速率可以用温度效应系数 Q 值来评价,Q 值越大,反应越快。本研究结果表明,在酸性条件下反应速率受温度影响更大。
|
|
表 4 噻呋酰胺在不同 pH 值和不同温度下的水解动力学参数 Table 4 Hydrolytic kinetics parameters of thifluzamide solutions with different pH value under different temperatures |
反应活化能 (Ea) 是基态反应物分子与过渡态之间的能量差,决定反应发生的快慢程度[13],其大小也反映了温度对反应速率常数 (K) 影响的程度。Ea 值越高,K 值受温度的影响越大,如升高温度,K 值显著增大;反之,则变化不明显[14]。本研究中,噻呋酰胺在酸性和碱性条件下 Ea 值均大于在中性条件下的,且在酸性条件下的水解速率受温度影响的程度要比碱性条件下的大。
由表 4 还可以看出,温度一定时,噻呋酰胺在 pH 7 时水解最快。根据《化学农药环境安全评价试验准则[8],噻呋酰胺在 pH 4 和 pH 7 时较难水解,pH 9 时难水解。
2.3.2 表面活性剂由图 2 可知:SDS 和 CTAB 均可抑制噻呋酰胺的水解,且随其质量浓度的增加,抑制作用增强,其中 CTAB 对其抑制作用比 SDS 更大。
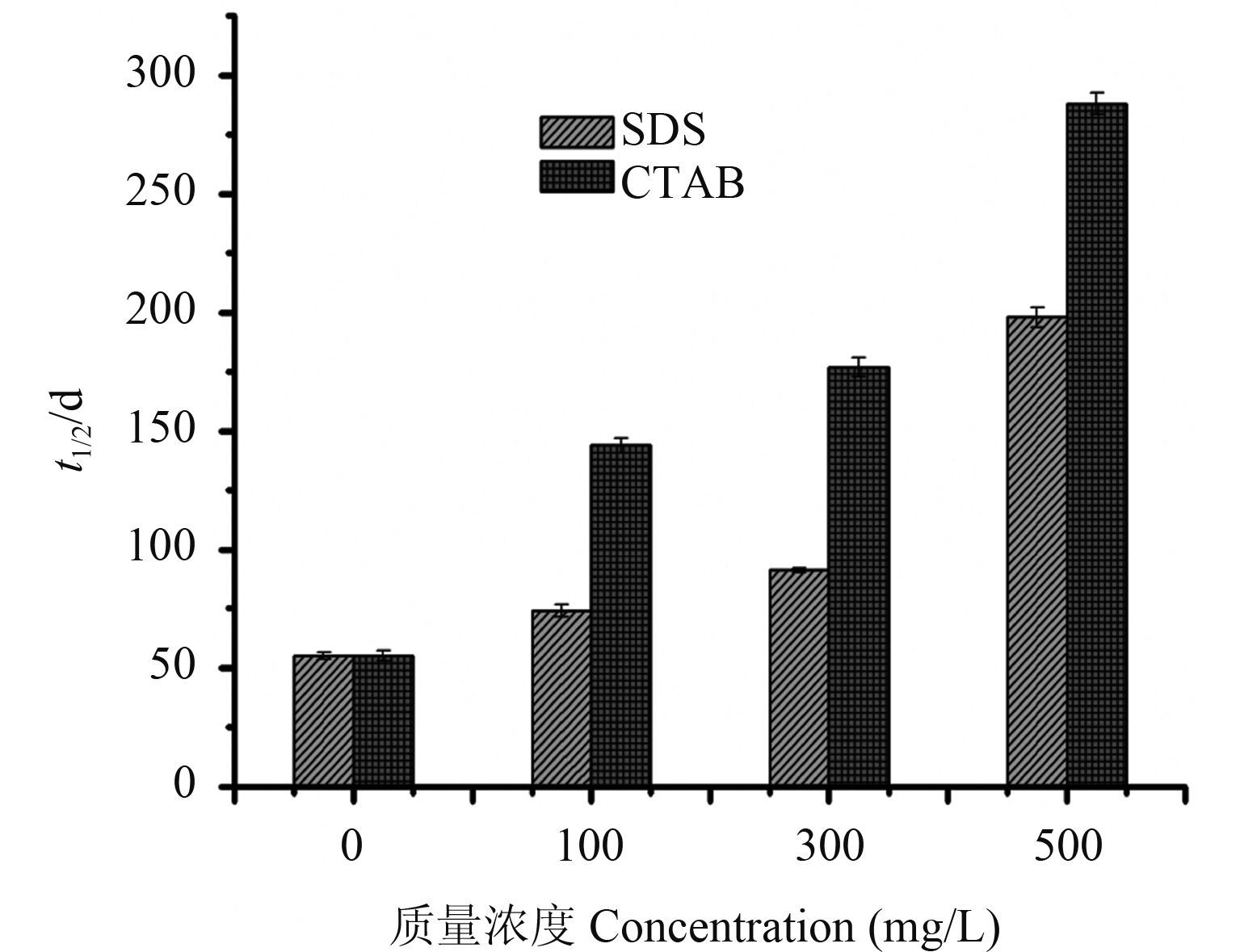
|
图 2 SDS 和 CTAB 表面活性剂对噻呋酰胺水解的影响 Fig. 2 Effects of SDS and CTAB on the hydrolytic process of thifluzamid |
3 结论
紫外灯照射下,噻呋酰胺在不同溶剂中的降解均符合一级动力学方程。不同pH值条件下噻呋酰胺的光解速率从大到小依次为 pH 9 > pH 7 > pH 4;噻呋酰胺在不同溶剂中的光解速率从大到小依次为:正己烷 > 乙腈 > 甲醇 > 乙酸乙酯 > 超纯水,即光解速率与溶剂的极性大小无关,而与最大吸收波长有关;Fe3+ 和 Fe2+ 以及腐殖酸均可抑制噻呋酰胺的光解。
噻呋酰胺的水解速率随反应温度的升高而加快;中性条件下噻呋酰胺水解最快;不同缓冲溶液中,温度效应系数从大到小依次为 pH 4 > pH 9 > pH 7,噻呋酰胺在酸性条件下反应速率受温度影响更大;在 35 ℃、pH 值为 7 的条件下,表面活性剂 SDS 和 CTAB 均能抑制噻呋酰胺的水解,且随浓度的增加,抑制作用增强。
| [1] | ATKINSON S K, MARLATT V L, KIMPE L E, et al. Environmental factors affecting ultraviolet photodegradation rates and estrogenicity of estrone and ethinylestradiol in natural waters [J]. Arch Environ Contam Toxicol, 2011, 60 (1) :1–7 . doi:10.1007/s00244-010-9515-4 |
| [2] |
肖曲, 郝冬亮, 刘毅华, 等. 农药水环境化学行为研究进展 [J]. 中国环境管理干部学院学报, 2008,18 (3)
:58–61.
XIAO Q, HAO D L, LIU Y H, et al. Research progress in chemistry behavior of pesticides in aquatic environment [J]. J Environ Manage Coll China, 2008, 18 (3) :58–61 . |
| [3] | GUPTA S, GAJBHIYE V T. Adsorption-desorption,persistence and leaching behavior of thifluzamide in alluvial soil [J]. Chemosphere, 2004, 57 (6) :471–480 . doi:10.1016/j.chemosphere.2004.06.033 |
| [4] |
韦利娜, 张静静, 汪芙蓉, 等. 水稻田样品中噻呋酰胺残留检测方法研究 [J]. 农药学学报, 2013,15 (3)
:311–315.
WEI L N, ZHANG J J, WANG F R, et al. Study on determination of thifluzamide residues in rice [J]. Chin J Pestic Sci, 2013, 15 (3) :311–315 . |
| [5] |
冷鹏, 吴书宝, 徐升华, 等. 噻呋酰胺240克/升悬浮剂防治花生白绢病田间药效试验 [J]. 农药科学与管理, 2012,33 (2)
:51–53.
LENG P, WU S B, XU S H, et al. Field trails of thifluzamide 240 g/L SC on peanut Sclerotium rolfsii Sacc [J]. Pest Sci Admin, 2012, 33 (2) :51–53 . |
| [6] | WEI L N, WU P, WANG F R, et al. Dissipation and degradation dynamics of thifluzamide in rice field [J]. Water Air Soil Pollut, 2015, 226 :130. doi:10.1007/s11270-015-2387-5 |
| [7] |
郭利丰, 丁佩, 徐永. 噻呋酰胺原药的高效液相色谱分析 [J]. 现代农药, 2014,13 (4)
:28–29.
GUO L F, DING P, XU Y. Analysis of thifluzamide TC by HPLC [J]. Mod Agrochem, 2014, 13 (4) :28–29 . |
| [8] |
化学农药环境安全评价试验准则:GB/T 31270-2014[S].北京:中国标准出版社,2015.
Test guidelines on environmental safety assessment for chemical pesticides:GB/T 31270-2014[S].Beijing:Standard Press of China,2015. |
| [9] |
孙晓燕, 赵百萍, 王鸣华. 溴虫腈在不同溶剂中的光化学降解 [J]. 农药学学报, 2013,15 (4)
:469–474.
SUN X Y, ZHAO B P, WANG M H. Study on photochemical degradation of chlorfenapyr in different solvents [J]. Chin J Pestic Sci, 2013, 15 (4) :469–474 . |
| [10] |
孙晓燕.溴虫腈的环境行为及稻田中的残留动态研究[D].南京:南京农业大学,2013.
SUN X Y.Study on the environmental behavior and residual dynamics in paddy field environment of chlorfenapyr[D].Nanjing:Nanjing Agricultural University,2013. |
| [11] | BEATRIZ S M, PILAR S E, JESUS M V A, et al. Study of alloxydim photodegradation in the presence of natural substances:Elucidation of transformation products [J]. J Photoch Photobio A, 2008, 198 :162–168 . doi:10.1016/j.jphotochem.2008.03.005 |
| [12] |
花日茂, 岳永德, 潘学冬, 等. 腐殖质对丁草胺在水中的光解效应研究 [J]. 安徽农业大学学报, 1999,26 (1)
:63–67.
HUA R M, YUE Y D, PAN X D, et al. The photolysis effects of humus substances on the butachlor in water [J]. J Anhui Agric Univ, 1999, 26 (1) :63–67 . |
| [13] | MARTÍNEZ-ZAPATA M, ARISTIZÁBAL C, PEÑUELA G. Photodegradation of the endocrine-disrupting chemicals 4n-nonylphenol and triclosan by simulated solar UV irradiation in aqueous solutions with Fe (Ⅲ) and in the absence/presence of humic acids [J]. J Photochem Photobiol A Chem, 2013, 251 :41–49 . doi:10.1016/j.jphotochem.2012.10.009 |
| [14] |
欧晓明, 雷满香, 裴晖, 等. 新农药硫肟醚的水解研究 [J]. 农业环境科学学报, 2007,26 (6)
:2309–2315.
OU X M, LEI M X, PEI H, et al. Hydrolysis of novel insecticide sulfoxime in buffered solutions [J]. J Agro-environ Sci, 2007, 26 (6) :2309–2315 . |
 2016, Vol. 18
2016, Vol. 18


