2. 中国农业大学 理学院, 北京 100193
2. College of Sciences, China Agriculture University, Beijing 100193, China
烟嘧磺隆 (nicosulfuron) 是一种磺酰脲类、玉米田苗后除草剂,具有活性高、杀草谱广、田间使用量低等特性[1],该药剂及其复配制剂可防除玉米田阔叶杂草、一年生禾本科杂草及部分莎草科杂草,已成为中国北方夏玉米田的首选除草剂[2]。但由于烟嘧磺隆具有很强的淋溶性,易对土壤及地下水造成污染[3-5],因此容易对生态环境和人类健康造成潜在的威胁。此外,该药剂还具有长残留的特性,易对许多后茬敏感作物产生药害[6]。
微生物降解是土壤中农药消解的重要途径之一,微生物因其种类丰富、分布广泛、适应性强和代谢途径多样的特点已逐渐在土壤污染修复领域表现出自身的优势。其中,降解菌株产生的降解酶作为净化农药污染的有效手段而备受关注,具有广阔的应用前景[7]。探明微生物降解酶对农药的降解特性是开发控制农药残留酶制剂的基础[8]。粪产碱杆菌 Alcaligenes faecalis ZWS11 是从被磺酰脲类除草剂污染的农田土壤中分离筛选得到的一株能够降解烟嘧磺隆的菌株,笔者前期已对影响 ZWS11 菌株降解特性的环境因素及降解途径进行了较为系统的研究[9]。本文拟通过探讨 ZWS11 菌株粗酶液的降解特性及环境条件对其降解活性的影响,以期为将该降解酶用于被烟嘧磺隆污染土壤的生物修复提供理论依据和技术支持,同时为其酶制剂的工业化生产奠定基础。
1 材料与方法 1.1 供试材料 1.1.1 菌株粪产碱杆菌Alcaligenes faecalis ZWS11 菌株,由中国农业大学理学院农药环境毒理实验室分离、筛选并保存。该菌株 16S rRNA 基因片段长度为 1 337 bp,其序列已提交至 GeneBank 数据库,登录号为 KM015485。
1.1.2 主要试剂及培养基97.8% 烟嘧磺隆 (nicosulfuron) 原药 (山东淄博新农基农药化工有限公司);色谱级乙腈和丙酮 (北京迈瑞达科技有限公司);十二烷基磺酸钠 (SDS) 和苯甲基磺酰氟 (PMSF) 由中国农业大学农药环境毒理实验室提供。酶活测定所用缓冲液:PBS 缓冲液 (K2HPO4-KH2PO4缓冲液,pH 值 6.0~8.0,0.05 mol/L)、醋酸钾缓冲液 (pH 值 4.0~5.0,0.05 mol/L) 及 Tris-HCl 缓冲液(pH 值 9.0,0.05 mol/L);LB 培养基 (蛋白胨 10 g,酵母粉 5 g,氯化钠 10 g)。准确称取一定量烟嘧磺隆原药,用乙腈溶解、配制成1 000 mg/L 的母液,4 ℃ 保存,试验时再用缓冲液稀释至终浓度为 10 mg/L (即 24.9 μmol/L)。
1.1.3 主要仪器设备VCX150 超声波细胞破碎仪 (美国 Sonics 公司);Agilent 1260 型高效液相色谱仪 (美国安捷伦科技有限公司);RP-Welch materials column XB C18 色谱柱 (250 mm × 4.0 mm,内径 5 μm);Lambda 35 型紫外-可见分光光度计 (美国 PerkinElmer 公司)。
1.2 试验方法 1.2.1 菌株活化将保存的 ZWS11 菌株转接到 LB 平板上,划线分离培养 24 h,挑取单菌落接种于灭菌的 LB 培养液中,30 ℃、180 r/min 培养 48 h,备用。
1.2.2 菌株降解酶的制备胞外粗酶液提取:采用丙酮沉淀法并略作修改[10-11]。将培养好的菌体发酵液于 15 000 r/min、4 ℃ 下离心 15 min,取离心后的上清液与 -20 ℃ 预冷的丙酮,按体积比分别为 1 : 0.5、1 : 1、1 : 2、1 : 3 和 1 : 4 的比例于 250 mL 锥形瓶中充分混匀,置于 -20 ℃ 冰箱中过夜。混合液于 15 000 r/min、4 ℃ 离心 15 min,收集沉淀并用少量 PBS 缓冲液 (pH 7.0,0.05 mol/L) 悬浮;同时将锥形瓶风干后用少量 PBS 缓冲液溶解、悬浮聚集在瓶底的沉淀;合并悬浮液,过 0.45 μm 滤膜即得胞外粗酶液。采用考马斯亮蓝法[12]测定胞外粗酶液的蛋白含量。
胞内粗酶液提取:采用细胞超声波破碎法[13-15]。将培养好的菌体发酵液于 15 000 r/min、4 ℃ 下离心 15 min,取适量沉淀按照 m (沉淀) : V (PBS 缓冲液) = 1 : 5 的比例充分混匀,冰浴下将细胞超声破碎 (超声功率 150 W,强度 80%,工作 5 s、停 8 s,共破碎 20 min),15 000 r/min、4 ℃ 下离心 15 min,上清液过 0.45 μm 滤膜后即得到胞内粗酶液。
菌体碎片悬浮液制备:提取胞内粗酶液时,离心后所产生的菌体沉淀用 PBS 重悬后即得到菌体碎片悬浮液。
分别测定上述于菌株不同部位获得的粗酶液及菌体碎片悬浮液对烟嘧磺隆的降解率,确定起关键降解作用的酶的位置。并以其中对烟嘧磺隆具有较高降解能力的粗酶液或菌体悬浮液作为降解酶,开展后续研究。
1.2.3 相对酶活力测定取 800 μL 降解粗酶液,加入到含有 24.9 μmol/L 烟嘧磺隆的 PBS 缓冲液 (pH 7.0,0.05 mol/L) 中,反应总体积为 1.0 mL,35 ℃ 水浴反应 30 min。以未加降解酶的处理为对照,每处理设 3 次重复。取反应结束后的缓冲液,加入等体积的乙腈 (含 0.1% 乙酸) 超声提取 30 min,加入过量无水氯化钠使其饱和;涡旋振荡 2 min,12 000 r/min 离心 5 min;吸取上层有机相过 0.22 μm 滤膜,采用 HPLC 检测烟嘧磺隆的浓度。计算降解酶对烟嘧磺隆的降解率及酶活力。除特殊说明外,一般以最高酶活力定为 100%,计算相对酶活力。酶活力定义为:在单位时间内,单位质量的降解酶消耗 1 μmol/L 烟嘧磺隆的能力。

|
分别取培养不同时间 (0、0.5、1、2、3、4、5 和 6 d)的菌株发酵液,采用 1.2.2 节中的方法提取胞外粗酶液。取 800 μL 粗酶液,加入到含有 24.9 μmol/L 烟嘧磺隆的 PBS 缓冲液中,反应总体积为 1.0 mL,35 ℃ 水浴反应 30 min。以未加粗酶液的处理为对照,每处理 3 次重复。按照 1.2.3 节方法测定反应体系中烟嘧磺隆的浓度,计算不同培养时间下的酶活力及相对酶活力,分析培养时间对菌株降解酶活力的影响。
1.2.4.2 温度对降解酶活力的影响取 800 μL 胞外降解粗酶液,加入到含有 24.9 μmol/L 烟嘧磺隆的 PBS 缓冲液中,反应总体积为 1.0 mL,分别在不同温度 (4、20、30、35、40、50、60 和 70 ℃,其中 4 ℃ 试验在冰箱中进行) 下水浴反应 30 min。按照 1.2.3 节方法测定反应体系中烟嘧磺隆的浓度,计算不同温度下的酶活力及相对酶活力,分析温度对降解酶活力的影响。
1.2.4.3 温度对降解酶稳定性的影响参考宋金龙[16]42-43的方法并稍作修改:将胞外降解粗酶液分别于 35、40、50、60 和 70 ℃ 水浴中保温处理 2 h 后,取 800 μL 粗酶液加入到含有 24.9 μmol/L 烟嘧磺隆的 PBS 缓冲液中,反应总体积为 1.0 mL,再于该系列温度下水浴反应 30 min。测定反应体系中烟嘧磺隆的浓度,计算不同温度下保温 2 h 后的酶活力,以不保温处理时的酶活力为 100%,计算相对酶活力,分析降解酶在不同温度下的稳定性。
1.2.4.4 pH 值对降解酶活力的影响取 800 μL 胞外降解粗酶液,加入到含有 24.9 μmol/L 烟嘧磺隆、pH 值分别为 4.0、5.0、6.0、7.0、8.0 和 9.0 的缓冲溶液中,反应总体积为 1.0 mL,35 ℃ 水浴反应 30 min。测定反应体系中烟嘧磺隆的浓度,计算不同 pH 值下的酶活力及相对酶活力,分析 pH 值对降解酶活力的影响。
1.2.4.5 pH 值对降解酶稳定性的影响参考宋金龙[16]43的方法并稍作修改:将胞外粗酶液分别于 pH 值为 4.0、5.0、6.0、7.0、8.0 和 9.0 的缓冲液中、室温下放置 2 h 后,分别取 800 μL 酶液加入到含有 24.9 μmol/L 烟嘧磺隆、相应 pH 值的缓冲溶液中,反应总体积为 1.0 mL,35 ℃ 水浴反应 30 min。测定反应体系中烟嘧磺隆的浓度,计算不同 pH 下室温放置 2 h 后的酶活力,以未进行放置处理的酶活力为 100%,计算相对酶活力,分析不同 pH 值下降解酶的稳定性。
1.2.4.6 降解酶用量对酶活力的影响取 800 μL 不同浓度 (转换成质量后在 22.7~204.2 μg 之间) 的胞外降解粗酶液,加入到含有 24.9 μmol/L 烟嘧磺隆的 PBS 缓冲液中,反应总体积为 1.0 mL,35 ℃ 水浴反应 30 min。测定反应体系中烟嘧磺隆的浓度,计算不同降解酶用量下的酶活力及相对酶活力,分析降解酶用量对酶活力的影响。
1.2.4.7 反应时间对酶活力的影响取 800 μL 胞外降解粗酶液,加入到含有 24.9 μmol/L 烟嘧磺隆的 PBS 缓冲液中,反应总体积为 1.0 mL,于 35 ℃ 水浴下分别反应 15、30、60、90、120 和 150 min 后,测定反应体系中烟嘧磺隆的浓度,计算不同反应时间下的酶活力及相对酶活力,分析反应时间对降解酶活力的影响。
1.2.4.8 化学试剂 SDS 和 PMSF 对降解酶活力的影响参考宋金龙[16]43的方法并稍作修改:取 800 μL 胞外降解粗酶液,加入到含有 24.9 μmol/L 烟嘧磺隆的 PBS 缓冲液中,再分别向其中加入 SDS (浓度分别为 1、10 和 350 mmol/L) 和 PMSF (分别为 0.1、5 和 10 mmol/L),反应总体积为 1.0 mL,35 ℃ 水浴反应 30 min。以未加化学试剂的处理为对照,每处理 3 次重复。测定反应体系中烟嘧磺隆的浓度,计算酶活力,以对照的酶活力为 100%,计算相对酶活力,分析不同浓度下 2 种化学试剂对酶活力的影响。
1.2.5 烟嘧磺隆的提取及检测向 PBS 缓冲液中分别添加浓度为 2.49、24.9 和 249 μmol/L 的烟嘧磺隆,取 1 mL 药液于 5 mL 离心管中,加入等体积含 0.1% 乙酸的乙腈,超声提取 30 min;加入无水氯化钠使其饱和,涡旋振荡 2 min,于 12 000 r/min 离心 5 min;吸取上层有机相过 0.22 μm 滤膜,通过 HPLC 检测烟嘧磺隆的浓度[9-17]。试验重复 3 次。在该添加水平下,平均回收率分别为 90% ± 6.1%、85% ± 1.0% 和 98% ± 1.0% (均值 ± 标准偏差),表明该提取方法能够满足试验的要求。
1.3 数据统计分析试验数据通过 SPSS 中的 Duncan 新复极差法进行差异显著性分析 (P<0.05);采用 Microsoft Excel 2007 和 SigmaPlot 12.0 软件进行数据整理并作图。
2 结果与分析 2.1 降解酶的最佳提取条件及定位采用丙酮沉淀法提取菌株的胞外粗酶液,当发酵液与丙酮体积比分别为 1 : 0.5、1 : 1、1 : 2、1 : 3 和 1 : 4 时,所得粗酶液对烟嘧磺隆表现出了不同程度的降解作用,其相对酶活力见表 1。差异显著性分析表明,发酵液与丙酮体积比为 1 : 3~1 : 4 时,粗酶液的相对酶活力之间不存在显著性差异 (P<0.05),由此确定提取胞外粗酶液时发酵液与丙酮的体积比为 1 : 3。
|
|
表 1 丙酮沉淀法中发酵液与丙酮不同比例混合提取的胞外粗酶液的酶活力 Table 1 Extraction of extracellular crude enzymes by acetone precipitation at different mix proportions of fermentation broth and acetone, and the enzyme activity |
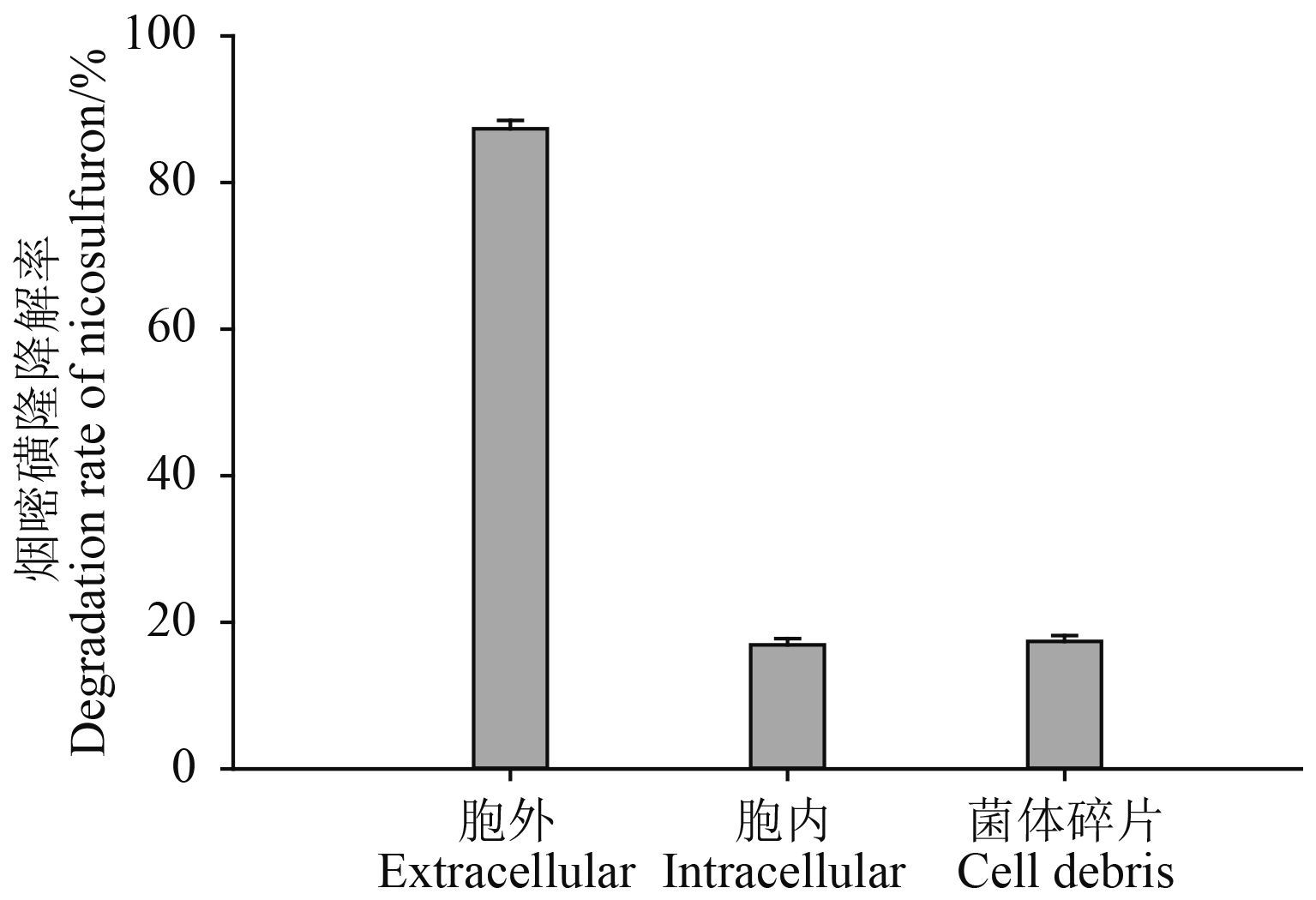
比较于 ZWS11 菌株不同部位提取的降解酶对烟嘧磺隆的降解率发现,胞外粗酶液对烟嘧磺隆的降解率在 87.4% ± 1.2% 以上,而胞内粗酶液和菌体碎片悬浮液对烟嘧磺隆的降解率很低,分别仅为 16.9% ± 0.9% 和 17.4% ± 0.8% (图 1)。表明 ZWS11 菌株对烟嘧磺隆起关键降解作用的部位在胞外,属于胞外酶。因此选择胞外粗酶液作为降解酶开展后续研究。
|
图 1 降解酶的定位 Fig. 1 Localization of degrading enzymes |
2.2 培养时间对降解酶活力的影响
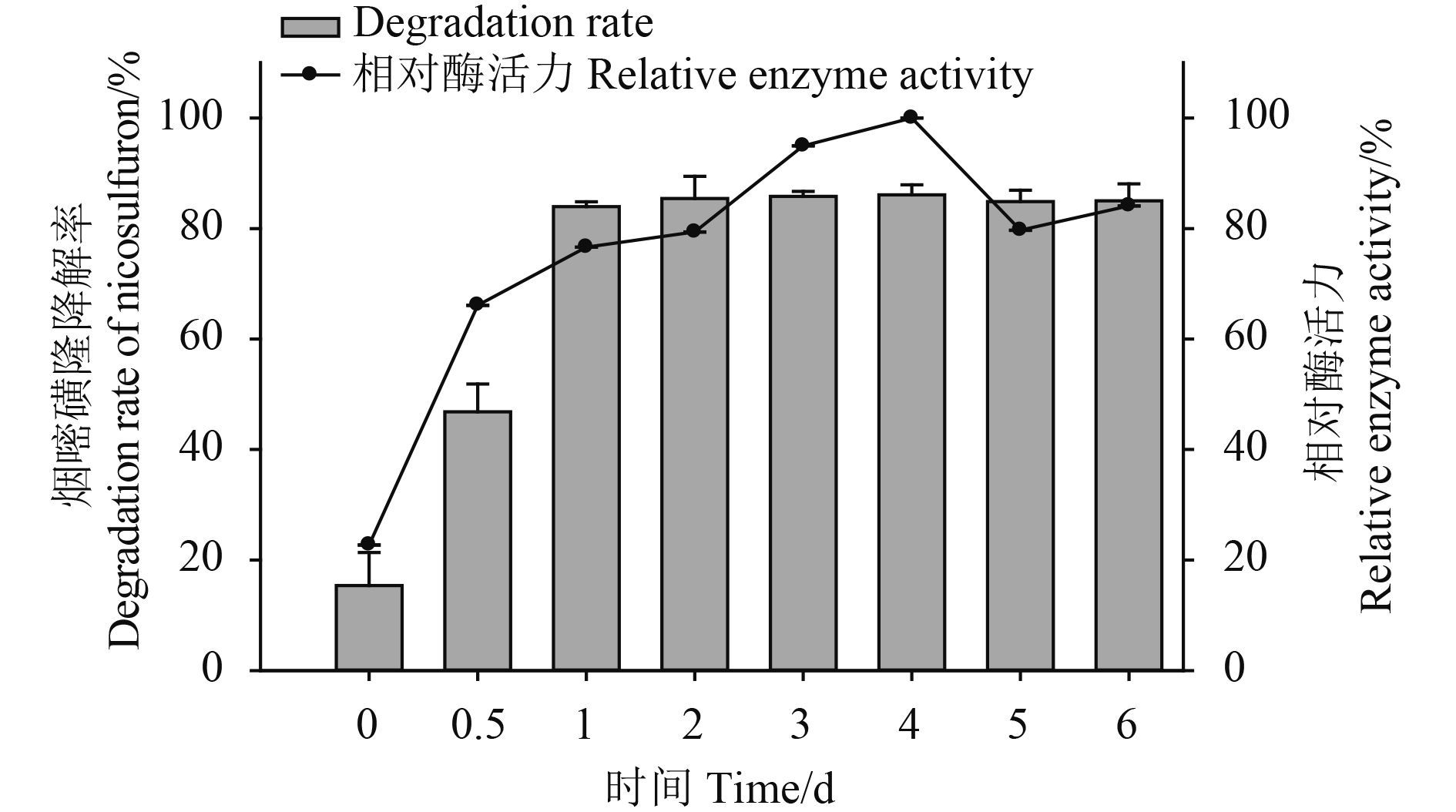
ZWS11 菌株分别培养 0、0.5、1、2、3、4、5 和 6 d 后提取的胞外降解酶对烟嘧磺隆的降解率分别为 15.4% ± 6.0%、46.8% ± 5.1%、84.0% ± 0.9%、85.4% ± 4.0%、85.8% ± 0.9%、86.1% ± 1.8%、84.9% ± 2.1% 和 85.0% ± 3.1%,其对应的相对酶活力分别为 22.7%、66.1%、76.6%、79.4%、95.0%、100.0%、79.7% 和 84.1% (图 2)。其中,培养时间为 4 d 时酶活性最高,大于或小于 4 d,其酶活性均下降,但培养时间在 6 d 时相对酶活力仍在 80% 以上。由此确定 ZWS11 菌株培养 3~4 d 时提取的降解酶具有较高的酶活力。
|
图 2 ZWS11 菌株培养时间对降解酶活力的影响 Fig. 2 Effect of different incubation times on enzyme activity of degrading enzymes of strain ZWS11 |
2.3 温度对降解酶活力的影响
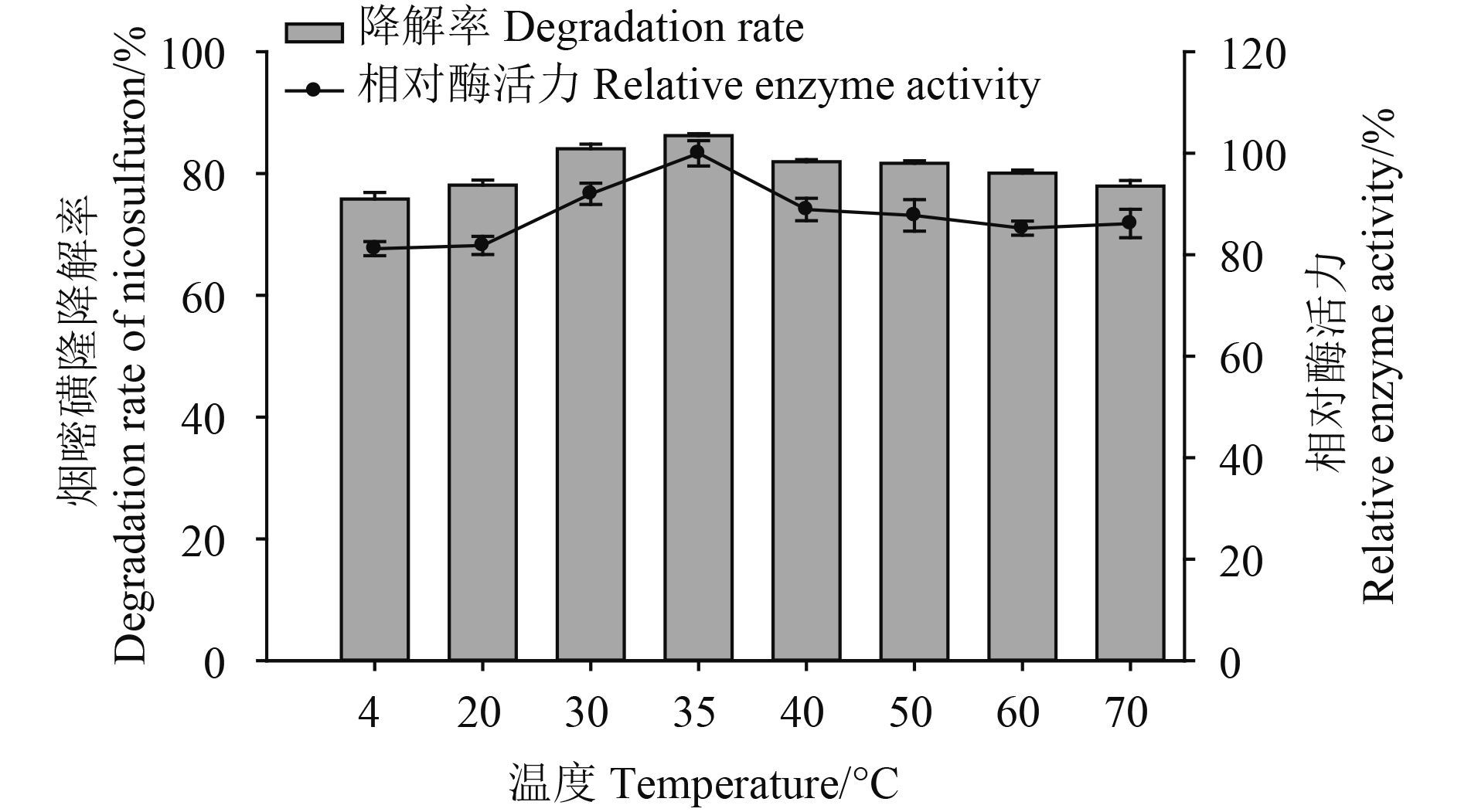
在 4~70 ℃ 范围内,降解酶均可有效降解烟嘧磺隆,降解率分别为 75.8% ± 1.1%、78.1% ± 0.8%、84.1% ± 0.8%、86.2% ± 0.3%、82.0% ± 0.4%、81.7% ± 0.4%、80.1% ± 0.51% 和 78.0% ± 0.9%,对应的相对酶活力分别为 81.2%、81.9%、92.0%、100.0%、88.9%、87.8%、85.3% 和 86.2% (图 3)。其中较适宜的反应温度为 35 ℃;在 4~35 ℃ 范围内时,酶活力随温度的升高呈现上升趋势;而在 35~70 ℃ 范围内时,酶活力随温度的升高呈现下降趋势。温度过高会对降解酶造成破坏,从而使其活力下降,本研究结果进一步验证了 De Gonzalo 等[18]的这一观点。由此确定使降解酶具有较好活力的反应温度为 35 ℃。
|
图 3 温度对降解酶活力的影响 Fig. 3 Effect of different temperatures on enzyme activity of degrading enzymes |
2.4 温度对降解酶稳定性的影响
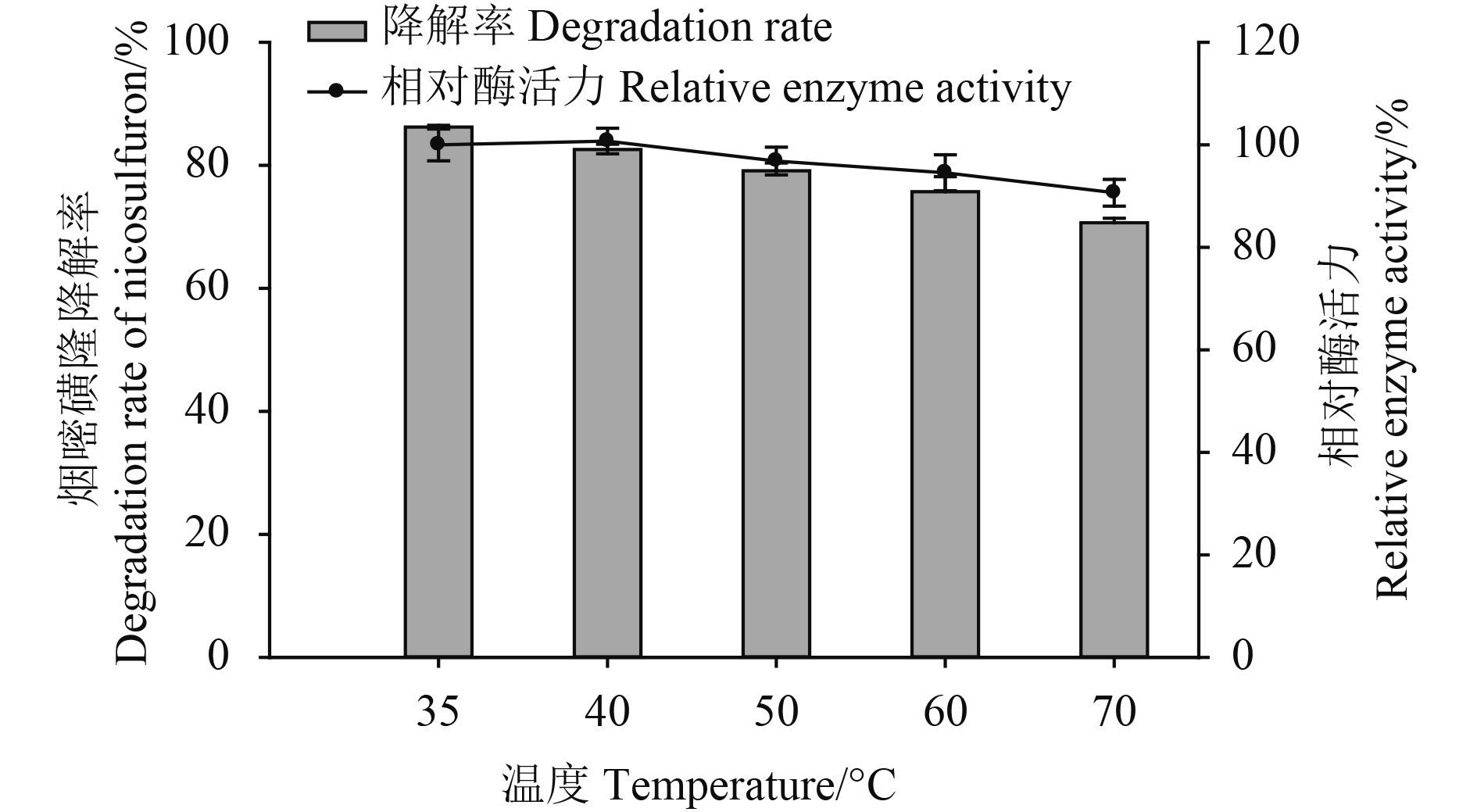
降解酶在相对较高的温度 (35、40、50、60、70 ℃)下保温处理 2 h 后,仍然可以有效降解烟嘧磺隆,其降解率分别为 86.2% ± 0.3%、82.6% ± 0.9%、79.1% ± 1.3%、75.7% ± 2.4% 和 70.7% ± 0.7% (图 4)。在试验温度范围内,热处理前后降解酶的相对酶活力均大于 90%,且保温处理温度达到 70 ℃ 时仍可保持较高的酶活力。表明该降解酶具有较广的温度适应范围,可在较高的温度条件下使用。
|
图 4 温度对降解酶稳定性的影响 Fig. 4 Effect of different temperatures on the stability of degrading enzymes |
2.5 pH 值对降解酶活力的影响
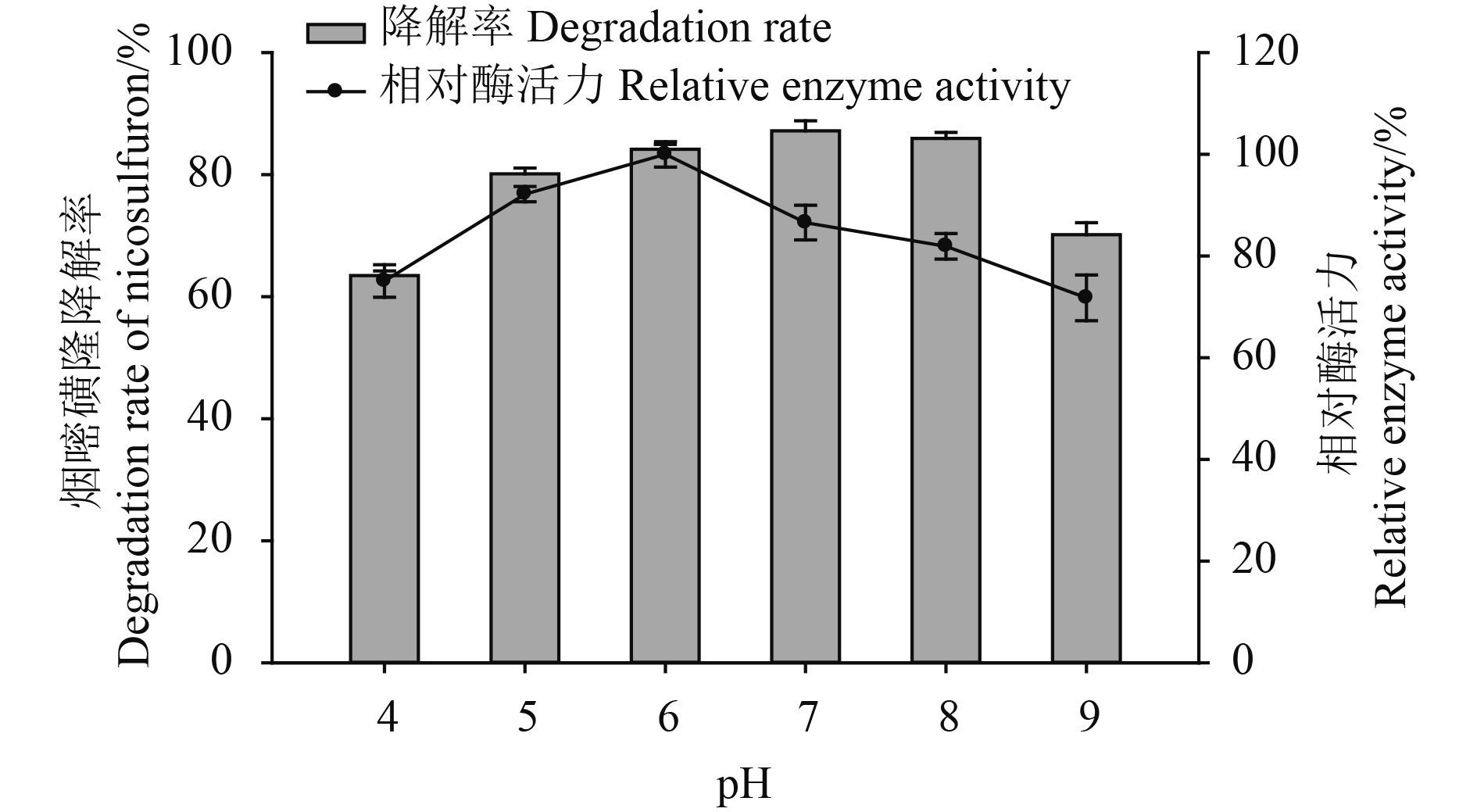
降解酶在 pH 值分别为 4.0、5.0、6.0、7.0、8.0 和 9.0 时均能够有效降解烟嘧磺隆,降解率分别为 63.5% ± 0.8%、80.2% ± 1.0%、84.2% ± 0.8%、87.2% ± 1.7%、86.0% ± 1.0% 和 70.2% ± 2.0%,其对应的相对酶活力分别为 75.1%、92.2%、100.0%、86.6%、81.9% 和 71.8% (图 5)。其中较适宜的 pH 值为 6.0,当 pH 值小于或大于 6.0 时,酶活性均开始下降。由此确定降解酶具有较好酶活力的 pH 值为 6.0。
|
图 5 pH 值对降解酶活力的影响 Fig. 5 Effect of different pH values on the activity of degrading enzymes |
2.6 pH 值对降解酶稳定性的影响
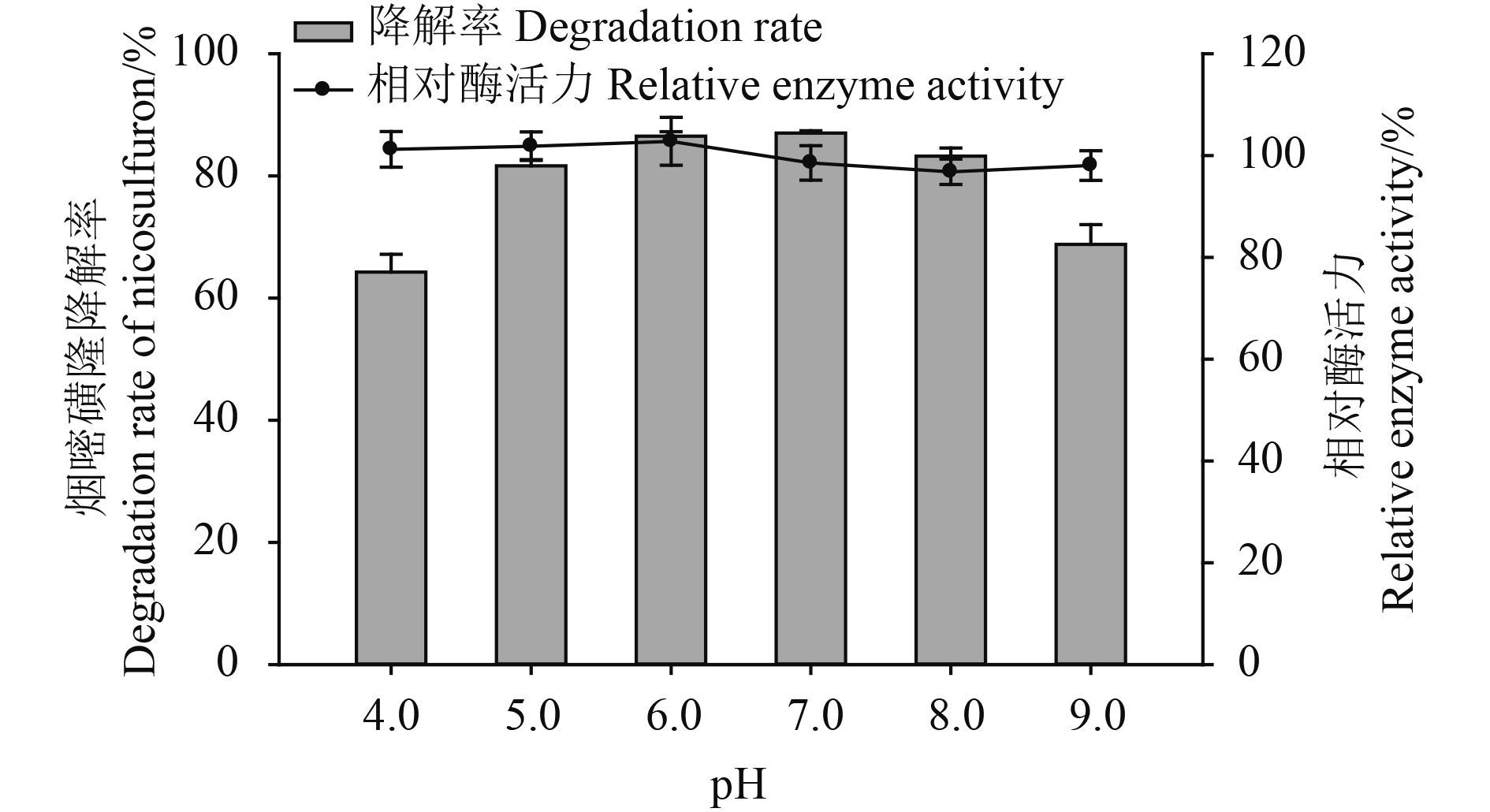
降解酶在 pH 值为 4.0、5.0、6.0、7.0、8.0 和 9.0 的缓冲液中分别保存 2 h 后,对烟嘧磺隆的降解率分别为 64.3% ± 2.9%、81.7% ± 1.0%、86.5% ± 0.7%、87.0% ± 0.4%、83.2% ± 1.3% 和 68.8% ± 3.2% (图 6)。即在上述 pH 值范围内,降解酶能够保持较高的酶活力,具有很好的稳定性,表明降解酶具有较广的 pH 适用范围,在微酸性或微碱性条件下亦可很好地发挥作用。
|
图 6 pH 值对降解酶稳定性的影响 Fig. 6 Effect of different pH values on the stability of degrading enzymes |
2.7 降解酶用量对酶活力的影响
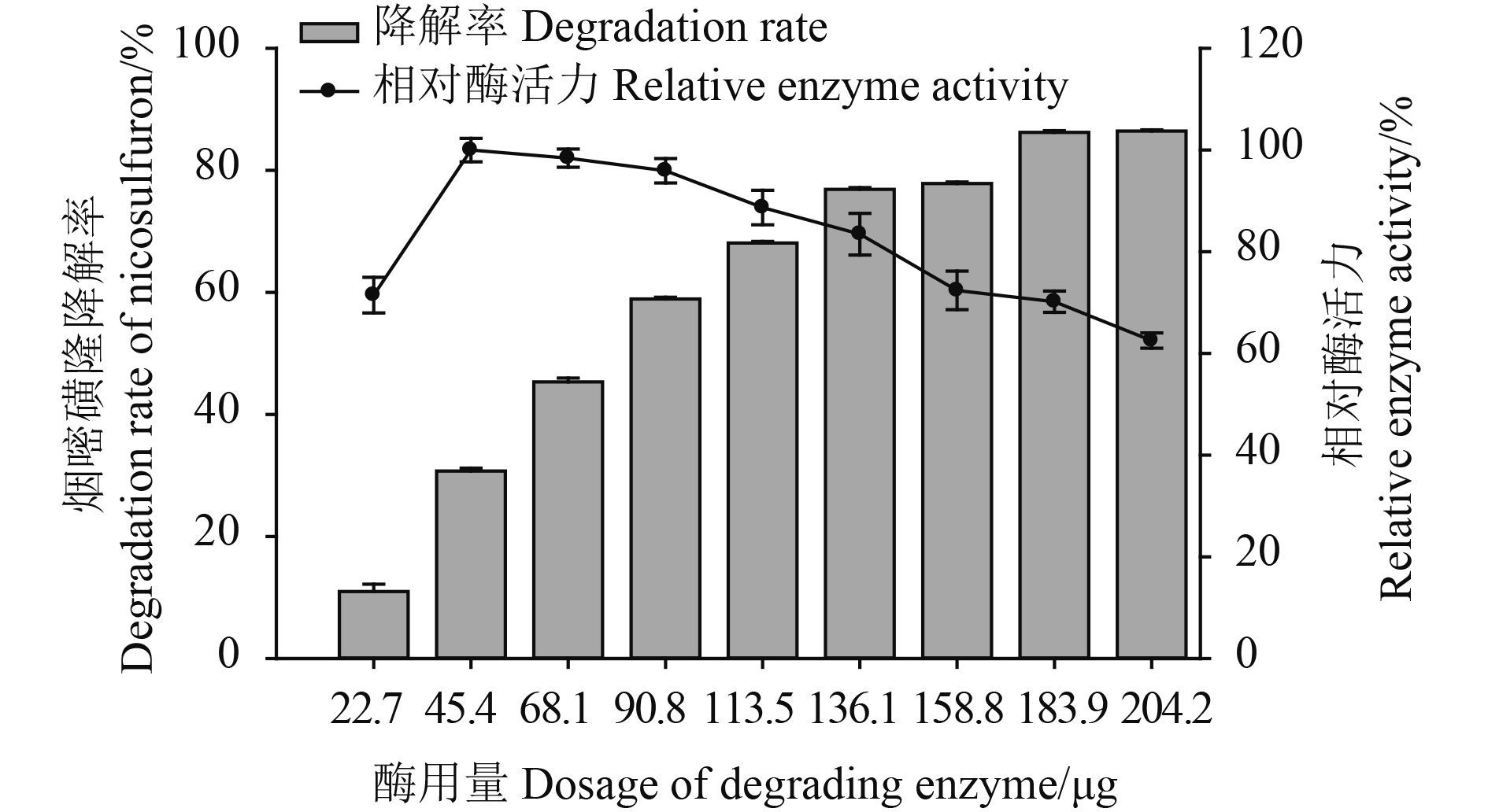
降解酶用量在 22.7~204.2 μg 范围内时,对烟嘧磺隆的降解率分别为 11.0% ± 1.2%、30.7% ± 0.5%、45.4% ± 0.6%、58.9% ± 0.3%、68.1% ± 0.2%、76.9% ± 0.3%、77.9% ± 0.3%、86.2% ± 0.3% 和 86.5% ± 0.2%,其对应的相对酶活力分别为 71.5%、100.0%、98.4%、95.9%、88.7%、83.5%、72.4%、70.2% 和 62.6% (图 7)。其中,降解酶用量在 45.4 μg 时酶活力最高,随着其用量增加,酶活力呈现下降趋势。
|
图 7 降解酶用量对酶活力的影响 Fig. 7 Effect of different dosages on the activity of degrading enzymes |
2.8 反应时间对降解酶活力的影响
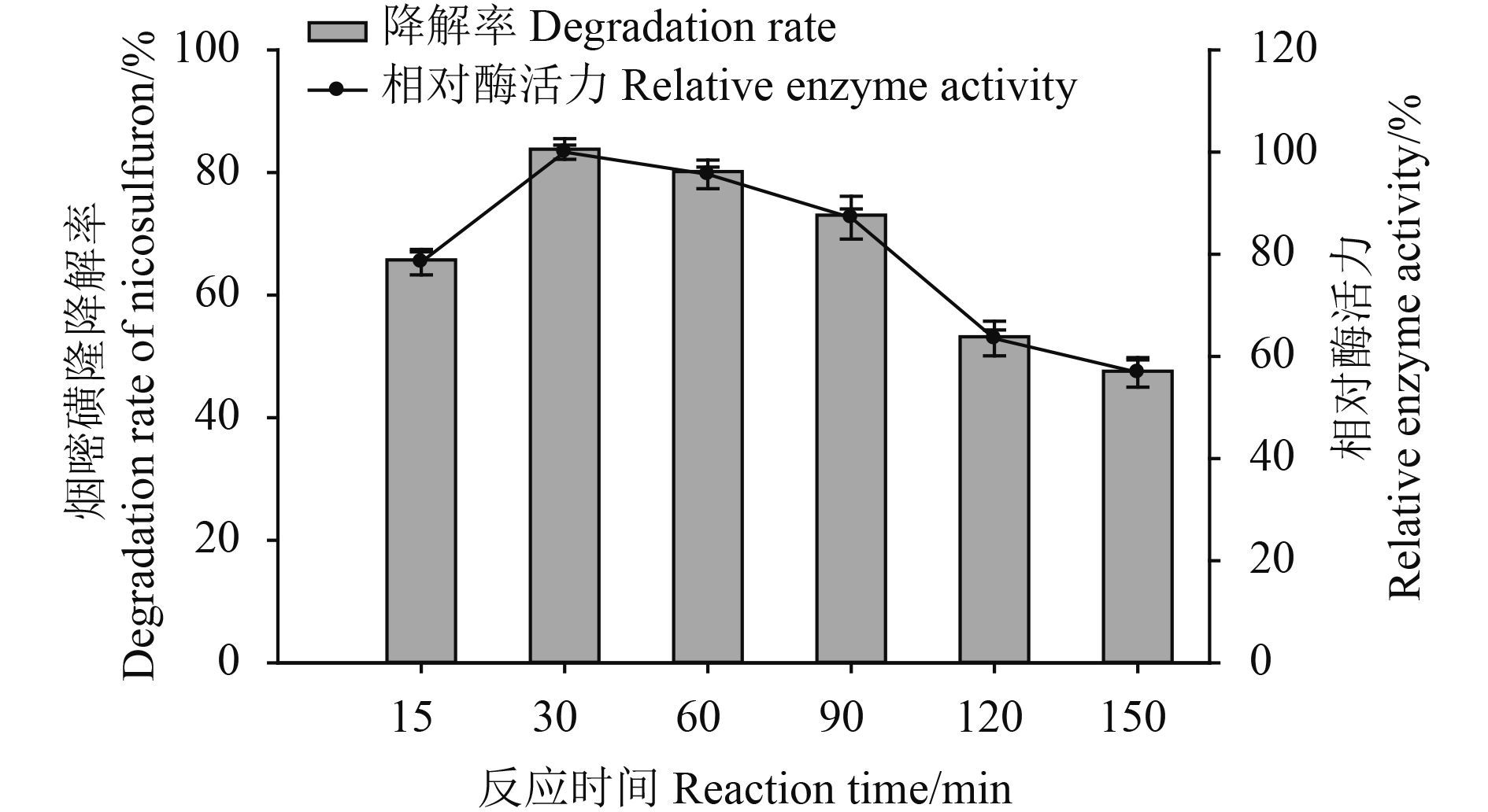
当反应时间在 15~150 min 时,降解酶对烟嘧磺隆的降解率分别为 65.8% ± 1.3%、83.8% ± 1.7%、80.2% ± 0.7%、73.1% ± 1.0%、53.2% ± 1.1% 和 47.6% ± 1.8%,对应的相对酶活力分别为 78.5%、100.0%、95.7%、87.2%、63.5% 和 56.9% (图 8)。其中最适宜的反应时间为 30 min,之后随着时间的延长酶活力呈现下降趋势。由此确定降解酶具有较高酶活力的反应时间为 30 min。
|
图 8 反应时间对降解酶活力的影响 Fig. 8 Effect of different reaction times on the activity of degrading enzymes |
2.9 SDS 和 PMSF 对降解酶活力的影响
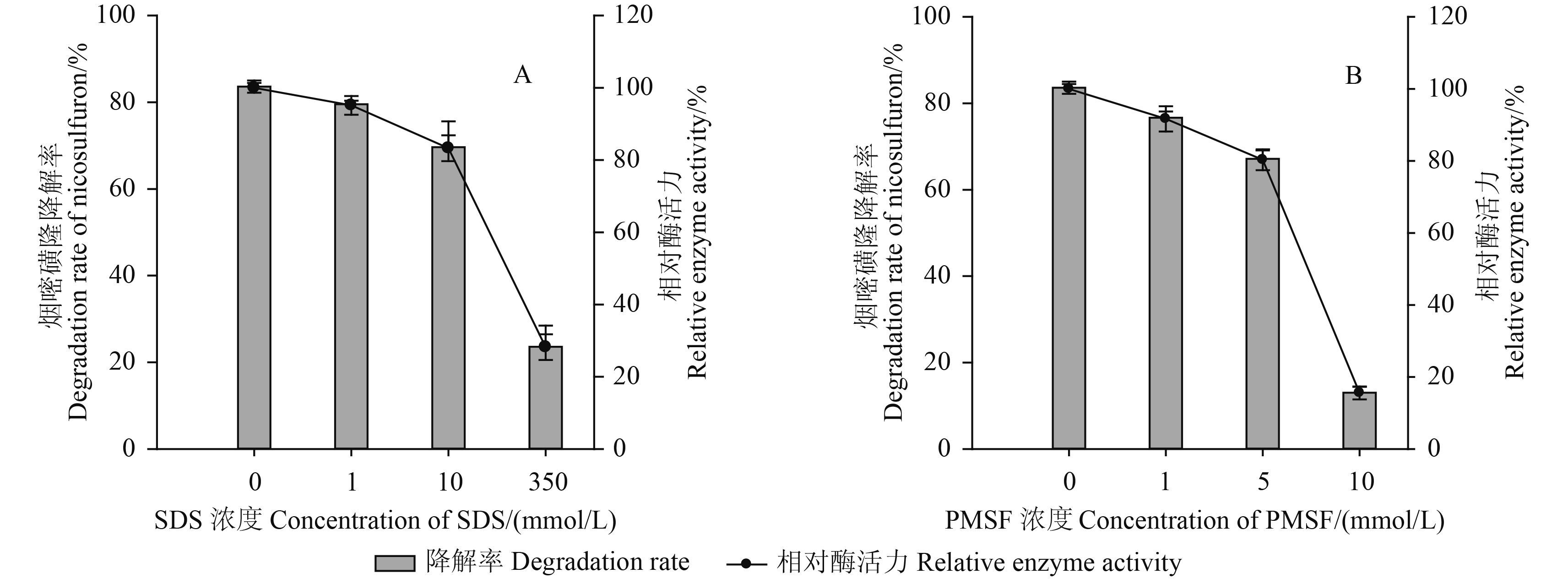
SDS 是一种蛋白质变性剂,为了明确反应体系中烟嘧磺隆浓度的下降是否完全由降解酶所致,在其中加入 SDS,研究了其对酶活力的影响。当 SDS 浓度分别为 1、10 和 350 mmol/L 时,降解酶对烟嘧磺隆的降解率分别为 79.5% ± 0.8%、69.6% ± 6.0% 和 23.6% ± 4.9%,而未加入 SDS 时的降解率为 83.6% ± 1.4%;其相对酶活力分别为 95.1%、83.3% 和 28.2% (图 9-A)。表明该变性剂的加入能够造成酶活力下降,且随 SDS 浓度增大,其影响程度加剧。
PMSF 是一种丝氨酸蛋白酶抑制剂,在研究酶的性质时常被用作酯酶 (esterase,EC 3.1.1.1) 或脂肪酶 (lipase,EC 3.1.1.3) 的抑制剂[19-20],通过加入该类物质后酶活力的变化可以初步判断酶液中起作用的相关位点及酶的种类[21]。当 PMSF 浓度分别为 0.1、5 和 10 mmol/L 时,降解酶对烟嘧磺隆的降解率分别为 76.7% ± 1.4%、67.2% ± 1.9% 和 13.0% ± 1.4%,而未加入 PMSF 时的降解率为 83.6% ± 1.4%;其相对酶活力分别为 91.7%、80.3% 和 15.6% (图 9-B)。表明该降解酶对5 mmol/L 的 PMSF 有一定耐受力,而当 PMSF 浓度增加到 10 mmol/L 时,酶活力迅速下降。
|
图 9 加入不同浓度 SDS 和 PMSF 对降解酶活力的影响 Fig. 9 Effect of different concentrations of SDS and PMSF on the activity of degrading enzyme |
3 结论与讨论
利用降解酶解决农药残留污染问题是当前环境科学研究的热点之一。降解酶具有降解速度快、效率高、反应底物浓度低、外界环境适应性强、比微生物更直接等优点,表现出了良好的应用潜力[22-23]。目前该领域研究比较广泛的是有机磷类[7-13-15-22]、拟除虫菊酯类[8-14]和三氮苯类化合物[24-25]等,有关磺酰脲类除草剂微生物降解酶方面的研究鲜有报道[26-27]。粪产碱杆菌对烟嘧磺隆、噻吩磺隆及甲磺隆等具有很好的降解效果[9],但尚未见有关粪产碱杆菌对烟嘧磺隆降解酶的研究报道。
降解酶具有多样性的特点,其在微生物细胞中的分布位置 (胞内酶、胞外酶或胞间质酶)、最适反应温度、pH 值、反应时间等性质因微生物种类的不同而存在差异。Kang 等[26]采用丙酮沉淀法从Bacillus subtilis YB1 菌株中提取的胞外粗酶液对烟嘧磺隆具有较高的降解能力,其在 35 ℃、pH 9.0 培养条件下对初始质量浓度为 5 mg/L 的烟嘧磺隆的降解率为 66%,并且该酶在碱性条件下能够保持较高的活性,但对高于 40 ℃ 的温度非常敏感。宋金龙[16]49-50通过研磨和超声波破碎法得到了Talaromyces flavus LZMl 菌株的胞内粗酶液,发现其对烟嘧磺隆具有较好的降解能力,对粗酶液进一步分离纯化后,得其最适降解温度为 40 ℃,最适 pH 值为 7.0。周珊[28]研究得到 Oceanisphaera psychrotolerans LAM-WHM-ZC 菌株降解酶降解烟嘧磺隆的最适反应温度为 45 ℃,酶活保持在 80% 以上,且该降解酶比较稳定,在较广的温度 (25~60 ℃) 和 pH (7.0~8.5) 范围内酶活性均较好。
本研究采用丙酮沉淀法从 ZWS11 菌株发酵液中提取的胞外粗酶液对烟嘧磺隆的平均降解率为 87.4%,是该菌株中主要起降解作用的酶。其降解烟嘧磺隆的最适反应温度为 35 ℃,pH 值为 6.0,且在 35~70 ℃、pH 值 4.0~9.0 范围内均能够保持较高的酶活力,具有很好的温度稳定性和酸碱稳定性,优于文献报道的降解酶对温度和 pH 值的稳定性[16-27]。同时确定了该酶促反应的较适宜反应时间为 30 min,菌株培养 3~4 d 时提取的胞外降解酶具有较高的酶活力。
已有研究表明,SDS 和 PMSF 是能够影响降解酶中全部或部分酶性质的化合物[19-21]。本研究表明,当反应体系中加入高浓度 (350 mmol/L) 的变性剂 SDS 后,胞外粗酶液对烟嘧磺隆的降解率从 83.6% 下降到了 23.6%,酶活力丧失了 70% 以上,说明 SDS 的加入抑制了胞外粗酶液中部分降解酶的活性,从而对降解率产生了影响。当加入的 PMSF 浓度为 5 mmol/L 时,胞外降解酶活力下降不明显,但随着 PMSF 浓度升高酶活力下降加快,可能是由于 PMSF 的加入导致了胞外粗酶液中与丝氨酸蛋白酶相关的位点发生了改变,从而抑制了降解酶的活力。Bhosale 等[19]研究发现,将 5 mmol/L 的 PMSF 加入到从 Bacillus sonorensis 4R 菌株得到的碱性脂肪酶中,结果使得酶活力下降了 83.33%,推测可能 PMSF 导致合成丝氨酸的关键位点发生了改变,从而直接或间接影响了酶活力。然而 Santi 等[20]却发现酯酶 lip3 对 10 mmol/L 的 PMSF 具有较强的耐受能力,酶活力仅下降了 45%。Velusamy 等[21]从 Bacillus tequilensis CWD-67 菌株中分离纯化得到具有溶解纤维蛋白能力的酶,发现 2 mmol/L 的 PMSF 即可使该酶的活力完全受到抑制,据此推测该酶是与丝氨酸有关的蛋白酶。宋金龙[16]52的研究表明,SDS 和 PMSF 浓度为 1 mmol/L 时对降解酶 FMO 的活力具有很强的抑制作用。谢香庭[29]研究发现,10 mmol/L 的 SDS 和 PMSF 对羧酸酯酶的活力表现出完全的抑制作用。本研究结果表明,当 SDS 浓度为 1 mmol/L 时对胞外粗酶液的酶活力表现出轻微的抑制作用,与周珊[28]的研究结果相似,但当 SDS 浓度为 10 mmol/L 时,酶活力下降较为明显,与谢香庭[29]的研究结果不同,可能的原因是来源于不同微生物的降解酶其酶活力存在差异,这与宋金龙[16]52的观点相同。
在利用丙酮沉淀法提取胞外粗酶液时,应在低温下提取,原因在于其提取率随温度的升高而降低,且较高的温度容易使蛋白质发生变性,导致部分酶失活。本研究优化筛选结果表明,当发酵液与丙酮体积比为 1 : 3 时,所得胞外粗酶液具有较好的降解效果和酶活力。研究结果可为进一步分离纯化 ZWS11 菌株的胞外粗酶液奠定基础。
虽然 ZWS11 菌株的胞外粗酶液对温度和 pH 值范围具有较好的适应性,但由于自然条件下外界的影响因子较多,因此其对烟嘧磺隆污染土壤的生物修复能力如何还有待进一步通过室内模拟试验深入探讨。此外,有关降解酶的分离纯化及编码降解酶的基因等方面还需进一步研究。
| [1] | SABADIE J. Nicosulfuron:alcoholysis,chemical hydrolysis,and degradation on various minerals [J]. J Agric Food Chem, 2002, 50 (3) :526–531 . doi:10.1021/jf010873s |
| [2] |
霍静倩, 许文超, 康占海, 等. 50%烟嘧磺隆·甲基磺草酮·氯氟吡氧乙酸异辛酯水分散粒剂防除夏玉米田杂草防效与安全性 [J]. 农药, 2013,52 (5)
:374–376.
HUO J Q, XU W C, KANG Z H, et al. Control effect and security of nicosulfuron·mesotrione·fluroxypr-mepthyl 50% WG against weeds in summer corn field [J]. Agrochemicals, 2013, 52 (5) :374–376 . |
| [3] | TRIGO C, SPOKAS K A, COX L, et al. Influence of soil biochar aging on sorption of the herbicides MCPA,nicosulfuron,terbuthylazine,indaziflam,and fluoroethyldiaminotriazine [J]. J Agric Food Chem, 2014, 62 (45) :10855–10860 . doi:10.1021/jf5034398 |
| [4] | REGITANO J B, KOSKINEN W C. Characterization of nicosulfuron availability in aged soils [J]. J Agric Food Chem, 2008, 56 (14) :5801–5805 . doi:10.1021/jf800753p |
| [5] |
张伟, 王进军, 张忠明, 等. 烟嘧磺隆在土壤中的吸附及与土壤性质的相关性研究 [J]. 农药学学报, 2006,8 (3)
:265–271.
ZHANG W, WANG J J, ZHANG Z M, et al. Adsorption of nicosulfuron on soils and its correlation with soil properties [J]. Chin J Pestic Sci, 2006, 8 (3) :265–271 . |
| [6] | SIKKEMA P H, SOLTANI N, MCNAUGHTON K, et al. Broccoli,cabbage and cauliflower tolerance to sulfonylurea herbicides [J]. Crop Prot, 2006, 25 (3) :225–229 . doi:10.1016/j.cropro.2005.04.011 |
| [7] |
王利, 余贤美, 贺春萍, 等. 毒死蜱降解细菌WJI-063的鉴定及酶促降解特性 [J]. 热带作物学报, 2009,30 (3)
:357–361.
WANG L, YU X M, HE C P, et al. Identification of a chlorpyrifos-degrading bacterial strain and characterization of its enzymatic degradation [J]. Chin J Trop Crops, 2009, 30 (3) :357–361 . |
| [8] |
廖敏, 马爱丽, 谢晓梅. 缺陷假单胞菌M5R14粗酶液降解拟除虫菊酯类农药特性初探 [J]. 环境科学, 2011,32 (6)
:1793–1798.
LIAO M, MA A L, XIE X M. Primary study on the characteristics of crude pyrethroid pesticide-degrading enzyme extracted from Pseudomonas diminuta strain M5R14 [J]. Environ Sci, 2011, 32 (6) :1793–1798 . |
| [9] | ZHAO W S, WANG C, XU L, et al. Biodegradation of nicosulfuron by a novel Alcaligenes faecalis strain ZWS11 [J]. J Environ Sci, 2015, 35 :151–162 . doi:10.1016/j.jes.2015.03.022 |
| [10] |
刘永锋, 陈志谊, 周明国, 等. 枯草芽孢杆菌Bs-916的抑菌活性及其抑菌物质初探 [J]. 农药学学报, 2007,9 (1)
:92–95.
LIU Y F, CHEN Z Y, ZHOU M G, et al. Analysis on the antifungal activity of Bacillus subtilis strain Bs-916 and its extract [J]. Chin J Pestic Sci, 2007, 9 (1) :92–95 . |
| [11] |
张美珍, 徐文韬, 何义亮, 等. 壬基酚降解酶的提取及其活性研究 [J]. 环境科学与技术, 2013,36 (9)
:17–20.
ZHANG M Z, XU W T, HE Y L, et al. Extraction and activity of nonylphenol degrading enzyme [J]. Environ Sci Technol, 2013, 36 (9) :17–20 . |
| [12] | BRADFORD M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding [J]. Anal Biochem, 1976, 72 (1-2) :248–254 . doi:10.1016/0003-2697(76)90527-3 |
| [13] |
肖鹏飞, 秦必达, 王剑桥. 白腐菌Phlebia brevispora TMIC34596对林丹的酶促降解特性 [J]. 安全与环境学报, 2014,14 (6)
:161–164.
XIAO P F, QIN B D, WANG J Q. Enzymatic degradation of lindane by white rot fungus Phlebia brevispora TMIC34596 [J]. J Saf Environ, 2014, 14 (6) :161–164 . |
| [14] |
董园, 唐爱星, 刘幽燕, 等. 来源于铜绿假单胞菌GF31的氯氰菊酯降解酶的提取及其降解动力学研究 [J]. 山东农业大学学报(自然科学版), 2012,43 (4)
:529–533.
DONG Y, TANG A X, LIU Y Y, et al. Extraction of cypermethrin-degradation enzyme from Pseudomonas aeruginosa GF31 and its degradation kinetic [J]. J Shandong Agric Univ (Nat Sci), 2012, 43 (4) :529–533 . |
| [15] |
兰亚红, 谢明, 陈福良, 等. 施氏假单胞菌JHY01菌株毒死蜱降解酶的定位及其提取条件的优化 [J]. 中国生物防治, 2008,24 (4)
:349–353.
LAN Y H, XIE M, CHEN F L, et al. Localization and extraction conditions of chlorpyrifos-degrading enzyme from Pseudomonas stutzeri [J]. Chin J Biol Control, 2008, 24 (4) :349–353 . |
| [16] |
宋金龙.烟嘧磺隆降解菌黄篮状菌(Talaromyces flavus)的分离鉴定及降解机理研究[D].北京:中国农业科学院,2013.
SONG J L.Isolation and identification of nicosulfuron-degradtive fungus (Talaromyces flavus) and study of degradation mechanism[D].Beijing:Chinese Academy of Agricultural Sciences,2013. |
| [17] | ZHAO W S, XU L, LI D Z, et al. Biodegradation of thifensulfuron-methyl by Ochrobactrum sp.in liquid medium and soil [J]. Biotechnol Lett, 2015, 37 (7) :1385–1392 . doi:10.1007/s10529-015-1807-3 |
| [18] | DE GONZALO G, RODRÍGUEZ C, RIOZ-MARTÍNEZ A, et al. Improvement of the biocatalytic properties of one phenylacetone monooxygenase mutant in hydrophilic organic solvents [J]. Enzyme Microb Technol, 2012, 50 (1) :43–49 . doi:10.1016/j.enzmictec.2011.09.006 |
| [19] | BHOSALE H, SHAHEEN U, KADAM T. Characterization of a hyperthermostable alkaline lipase from Bacillus sonorensis 4R [J]. Enzyme Res, 2016, 2016 :4170684. |
| [20] | SANTI C D, ALTERMARK B, PIERECHOD M M, et al. Characterization of a cold-active and salt tolerant esterase identified by functional screening of arctic metagenomic libraries [J]. BMC Biochem, 2016, 17 (1) :1. doi:10.1186/s12858-016-0057-x |
| [21] | VELUSAMY P, PACHAIAPPAN R, CHRISTOPHER M, et al. Isolation and identification of a novel fibrinolytic Bacillus tequilensis CWD-67 from dumping soils enriched with poultry wastes [J]. J Gen Appl Microbiol, 2015, 61 (6) :241–247 . doi:10.2323/jgam.61.241 |
| [22] |
贾开志, 李晓慧, 何健, 等. 久效磷降解菌的分离及其酶促降解特性的研究 [J]. 环境科学, 2007,28 (4)
:908–912.
JIA K Z, LI X H, HE J, et al. Isolation of a monocrotophos-degrading bacterial strain and characterization of enzymatic degradation [J]. Environ Sci, 2007, 28 (4) :908–912 . |
| [23] |
和文祥, 蒋新, 朱茂旭, 等. 酶修复土壤农药污染的研究进展 [J]. 生态学杂志, 2001,20 (3)
:47–51.
HE W X, JIANG X, ZHU M X, et al. Advance on enzymes bioremediation of pesticides-polluted soil [J]. Chin J Ecol, 2001, 20 (3) :47–51 . |
| [24] |
张颖, 葛世杰, 姜昭, 等. 阿特拉津降解酶固定化条件优化 [J]. 东北农业大学学报, 2013,44 (8)
:23–28.
ZHANG Y, GE S J, JIANG Z, et al. Optimization for the immobilized conditions of atrazine degradation enzyme [J]. J Northeast Agric Univ, 2013, 44 (8) :23–28 . |
| [25] |
王秀国, 朱鲁生, 王军, 等. 细菌HB-5对除草剂莠去津的酶促降解研究 [J]. 环境科学学报, 2006,26 (4)
:579–583.
WANG X G, ZHU L S, WANG J, et al. Enzymatic degradation of herbicide atrazine by strain HB-5 [J]. Acta Sci Circum, 2006, 26 (4) :579–583 . |
| [26] | KANG Z H, REN C C, ZHANG J L, et al. Purification and cloning of nicosulfuron-degrading enzymes from Bacillus subtilis YB1 [J]. Appl Biochem Microbiol, 2014, 50 (1) :30–34 . doi:10.1134/S0003683814010049 |
| [27] | HANG B J, HONG Q, XIE X T, et al. SulE,a sulfonylurea herbicide de-esterification esterase from Hansschlegelia zhihuaiae S113 [J]. Appl Environ Microbiol, 2012, 78 (6) :1962–1968 . doi:10.1128/AEM.07440-11 |
| [28] |
周珊.烟嘧磺隆降解菌的分离鉴定及降解特性研究[D].武汉:华中农业大学,2015:94-96.
ZHOU S.Isolation,classification and degradation characteristics study of nicosulfuron-degrading bacteria[D].Wuhan:Huazhong Agricultural University,2015:94-96. |
| [29] |
谢香庭.菌株Hansschlegelia zhihuaiae S113水解甲磺隆的羧酸酯酶分离纯化及其酶学特性研究[D].南京:南京农业大学,2012:46.
XIE X T.Separation,purification and enzymatic properties of a carboxylesterase responsible for the hydrolysis of metsulfuron-methyl in strain Hansschlegelia zhihuaiae S113[D].Nanjing:Nanjing Agricultural University,2012:46. |
 2016, Vol. 18
2016, Vol. 18


