随着化学农药的长期大量使用,农药在环境中的残留污染问题已越来越引起人们的关注,其中,农药对地下水的污染问题尤其受研究者的高度重视[1-2]。影响农药对地下水污染情况的主要因素是农药在土壤中的迁移性和持久性[3],而农药在土壤中的迁移与农药的水溶性及吸附特性等因素密切相关,是评价农药生态环境安全性的重要指标[4]。
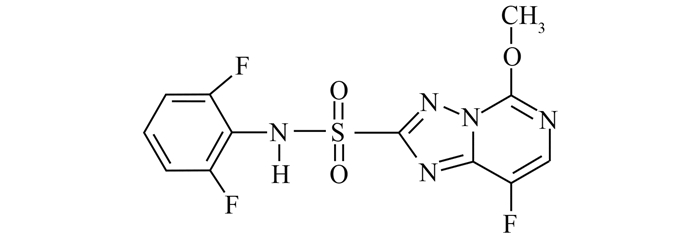
双氟磺草胺(florasulam,2’,6’-二氟-5-甲氧基-8-氟[1,2,4]三唑并[1,5-C]嘧啶-2-磺酰苯胺,CAS: 145701-23-1,结构式见图式 1)是近年来在中国获得登记开发的新型广谱除草剂,主要用于冬小麦、春小麦、大麦及草坪等苗后茎叶处理防除阔叶杂草[5],因其适用范围广及适配性好等特点,现已被大面积推广使用。目前已报道对杂草防除效果较好的双氟磺草胺制剂及其复配剂达数十种之多,而有关双氟磺草胺环境行为的研究报道却较少[6-8]。
|
图式 1 双氟磺草胺结构式 Scheme1 The structural formula of florasulam |
笔者通过批量平衡法和土柱淋溶法,研究了双氟磺草胺在3种不同类型土壤中的吸附和淋溶特性,并对其相关影响因素进行了分析探讨,以期为深入评价双氟磺草胺在环境中的安全性与其科学合理施用提供依据。
1 材料与方法 1.1 供试土壤供试土壤分别采自中国安徽省合肥市、山东省济南市及河南省郑州市3个主要的小麦种植区,均为麦田0~20 cm耕作层土壤,其理化性质见表 1。经风干、研碎、过筛后备用。试验用水及土壤在使用前均经高压蒸汽灭菌(121 ℃,0.5 h)。
|
|
表 1 供试土壤基本理化性质 Table 1 Physical and chemical properties of the tested soils |
1.2 药品和试剂
双氟磺草胺(florasulam)原药(纯度98.5%),陕西上格之路生物科学有限公司;乙腈、甲酸、磷酸为色谱纯;石墨化碳黑(GCB,178~250 μm)、N-丙基乙二胺(PSA,40~63 μm)、无水氯化钙、氯化钠及腐殖酸均为分析纯。
1.3 仪器和设备1260型高效液相色谱仪,美国Agilent科技有限公司;WHY-2恒温水浴振荡器,江苏金城国胜实验仪器厂;QL-901涡旋仪,海门其林贝尔仪器制造有限公司;SC-3610低速离心机和TGL-16高速离心机,安徽中科中佳科学仪器有限公司;BT1-100V-LCD智能恒流泵及SBS-100-LCD数控计滴自动部份收集器,上海琪特分析仪器公司。
1.4 试验方法 1.4.1 标准溶液配制称取1.110 g(精确至0.001 g)氯化钙置于1 L容量瓶中,以纯水定容,制得0.01 mol/L的氯化钙水溶液。称取0.102 g(精确至0.001 g)双氟磺草胺原药置于100 mL容量瓶中,用0.01 mol/L氯化钙水溶液溶解并定容,制得1 000 mg/L的标准母液,按要求梯度稀释后备用。
1.4.2 吸附动力学试验采用批量平衡法[9]。选用不同水土比进行预试验,结果表明,水土比为1∶1(体积:质量)时,双氟磺草胺在3种不同土壤中的吸附率均大于20%,符合批量平衡法[9]标准的要求。取3 mg/L的双氟磺草胺溶液(以0.01 mol/L的氯化钙为介质,下同)5 mL于20 mL玻璃样品瓶中,加入5.0 g(过0.25 mm筛)土壤,于25 ℃±2 ℃下水浴振荡,分别于0、1、2、3、4、6、8、10、12及24 h取样,经提取净化后测定上清液中双氟磺草胺的浓度。同时分别设置双氟磺草胺原药水溶液与空白土壤水溶液(均以0.01 mol/L的氯化钙为介质)对照处理,每处理3次重复,下同。
1.4.3 等温吸附试验分别取质量浓度为0.5、1、5、10及50 mg/L的双氟磺草胺溶液5 mL于20 mL样品瓶中,各加入5.0 g(过0.25 mm筛)土壤,于25 ℃±2 ℃下水浴振荡24 h,经提取净化后测定上清液中双氟磺草胺的浓度。
1.4.4 土柱淋溶试验称取540 g(过0.85 mm筛)土壤,均匀严实地装柱(自制有机玻璃柱:长35 cm,直径5 cm),土柱高度为25 cm(为保证处理之间的一致性,应控制土壤密度尽量一致),预加0.01 mol/L的氯化钙溶液至土壤饱和持水量的60%,静置24 h。将10 mL、100 mg/L的双氟磺草胺溶液均匀滴加在土壤表层,静置(使农药与土壤之间吸附达到平衡)。在土柱表面覆盖1 cm石英砂,并加盖一层滤纸(以防土层扰动),用智能恒流泵将300 mL、0.01 mol/L的氯化钙溶液从土柱上端淋溶(30 mL/h)。淋出液按每10 mL收集一次,直至淋溶结束,将土柱均匀分成5段,测定计算每段土壤和所有淋出液中双氟磺草胺的含量。
1.4.5 双氟磺草胺初始添加量对其在土壤中淋溶迁移的影响以安徽黏土为供试土壤,分别添加50、100和200 mg/L的双氟磺草胺溶液10 mL,使双氟磺草胺初始量分别为0.5、1.0和2.0 mg,其他步骤同1.4.4节。
1.4.6 腐殖酸对双氟磺草胺在土壤中淋溶迁移的影响以安徽黏土为供试土壤,分别添加0、5.4和10.8 g腐殖酸,使土壤中腐殖酸含量分别为0、1.0%和2.0%,充分混匀后装柱,其他步骤同1.4.4节。
1.4.7 样品中双氟磺草胺的提取及测定土样中双氟磺草胺的提取:称取5 g土壤样品于50 mL离心管中,加入5 g氯化钠、5 mL甲酸水溶液(调节pH=5)和10 mL乙腈,涡旋3 min后于3 500 r/min离心5 min;取上清液1 mL于2 mL离心管中,加入100 mg PSA和10 mg GCB,充分涡旋1 min,于8 500 r/min离心5 min;上清液过0.22 μm滤膜,待HPLC检测。
水样直接过0.22 μm滤膜,待HPLC检测。
色谱检测条件:ZORBAX ODS色谱柱(4.6 mm×250 mm,5 μm);流动相:V(乙腈):V(0.1%磷酸)=50 : 50,流速1 mL/min;柱温30 ℃;进样体积20 μL;DAD检测器检测波长260 nm。在此条件下,双氟磺草胺的保留时间为4.80 min。
1.4.8 添加回收试验向空白土壤和水样中分别添加0.5、1、5 mg/kg和0.1、5、50 mg/L水平的双氟磺草胺标准工作溶液,采用所建立的方法测定回收率及相对标准偏差(RSD),试验重复5次。
2 结果与讨论 2.1 分析方法的准确度和精密度在0.5~5 mg/kg添加水平下,土壤样品中双氟磺草胺的回收率为79%~94%,RSD为1.5%~2.9%,最小检测浓度为0.1 mg/kg;在0.1~50 mg/L添加水平下,水样中双氟磺草胺的回收率为99%~100%,RSD为1.1%~1.2%,最小检测浓度为0.05 mg/L。结果符合分析标准要求[10],表明所建立分析方法有效、可行。
2.2 双氟磺草胺在土壤中的吸附动力学特性空白试验表明,在24 h振荡过程中,未发现双氟磺草胺因微生物分解、水解或光解而明显消解。
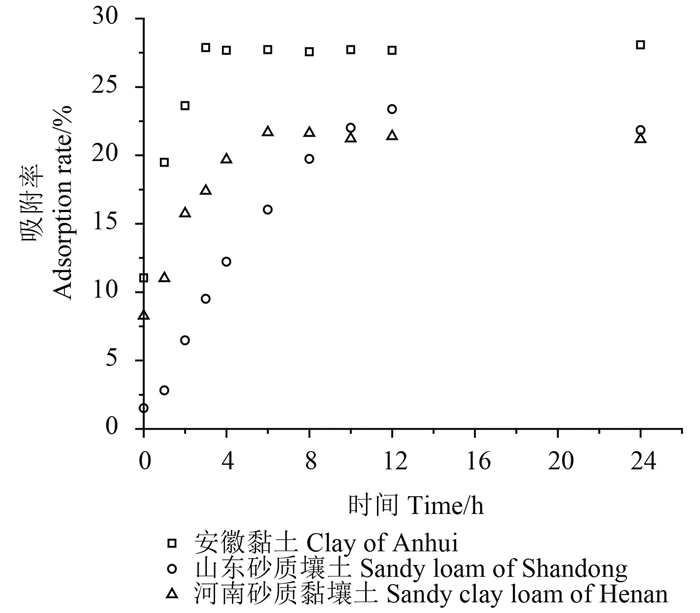
吸附动力学过程见图 1。结果表明:双氟磺草胺在3种土壤中的吸附在8~12 h内基本达到平衡;3种土壤对双氟磺草胺的吸附能力由强到弱依次是:安徽黏土>山东砂质壤土>河南砂质黏壤土,其平衡吸附率分别为28.08%、23.40%和21.39%。
|
图 1 双氟磺草胺在3种土壤中的吸附动力学过程 Fig. 1 The adsorption kinetics process of florasulam in three soils |
2.3 双氟磺草胺在土壤中的等温吸附特性
通过比较发现,双氟磺草胺在3种土壤中的吸附规律可以较好地用Freundlich方程[11](式1)进行拟合,相关参数见表 2。
|
|
表 2 双氟磺草胺在3种土壤中的等温吸附Freundlich拟合方程及参数 Table 2 Freundlich equation and parameters for adsorption isotherms of florasulam on soils |
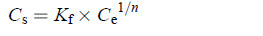
|
(1) |
式中:Cs为被土壤吸附的农药的质量分数(mg/kg);Ce为吸附平衡时溶液中农药的质量浓度(mg/L);Kf为土壤吸附系数;n为经验常数(反映吸附剂表面的非均匀性)。
吸附系数Kf值的大小表示土壤对农药吸附能力的强弱。双氟磺草胺在安徽黏土、山东砂质壤土和河南砂质黏壤土中的Kf值分别为0.622 9、0.434 7和0.385 5,表明在供试3种土壤中,河南砂质黏壤土对双氟磺草胺的吸附作用最弱,安徽黏土的吸附作用最强。研究表明,n值的大小与土壤有机质的均匀性及熟化程度,以及土壤吸附位点的分布等因素有关,n值越小,则土壤吸附位点的分布越复杂,有机质熟化程度越高,吸附能力越强[12]。由表 2可知,安徽黏土的土壤有机质熟化程度较高,吸附位点的分布更复杂,因此其对双氟磺草胺的吸附作用较强。
为了统一描述不同土壤对化合物的吸附行为,通常采用土壤有机碳归一化吸附系数Koc(单位mL/g)进行表征[9],其计算公式见式(2)。

|
(2) |
式中:OC%为土壤有机碳质量分数,OC%=OM%/1.724(OM%为土壤有机质质量分数)。
双氟磺草胺在安徽黏土、山东砂质壤土和河南砂质黏壤土中的Koc值分别为81.35、66.91和73.84,根据《化学农药环境安全评价试验准则》[13],表明双氟磺草胺在3种土壤中均属难吸附型。
土壤对农药的吸附作用与土壤的理化性质密切相关[14]。将吸附系数Kf与土壤有机质含量、黏粒含量、阳离子交换量以及pH值进行回归分析,得其决定系数R2分别为0.880 2、0.857 4、0.999 8和0.966 7,表明土壤有机质含量、黏粒含量、阳离子交换量和pH值与吸附系数间均存在显著正相关性,说明双氟磺草胺在土壤中的吸附可能受土壤理化性质中多个因素的综合影响。
2.4 双氟磺草胺在土壤中的吸附自由能土壤吸附自由能(ΔG,式3)是反映土壤吸附特性的重要参数,根据其大小可以推断土壤的吸附机制:当吸附自由能变化–ΔG<40 kJ/mol时,为物理吸附;反之,则为化学吸附[15]。
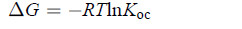
|
(3) |
式中:R为气体摩尔常数[8.314 J/(K· mol)];T为绝对温度(K)。
双氟磺草胺在安徽黏土、山东砂质壤土和河南砂质黏壤土中的吸附自由能分别为–10.90、–10.42及–10.66 kJ/mol,均为负值,且其绝对值小于40 kJ/mol,表明双氟磺草胺在3种土壤中的吸附均为物理吸附,且都是自发的可逆吸附过程,即双氟磺草胺在施入土壤后不会与土壤组分发生化学反应而失去活性。
2.5 双氟磺草胺在土壤中的移动性及其影响因素 2.5.1 双氟磺草胺在3种土壤中的淋溶迁移淋溶作用是农药在水-土壤颗粒之间吸附、解吸和分配的一个综合过程,该过程同时受到农药自身理化性质和土壤理化性质的影响[16-17]。
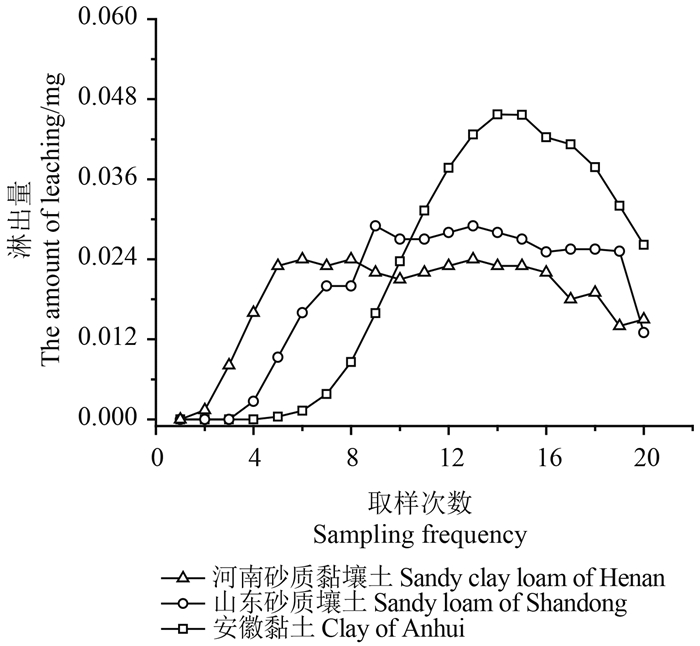
图 2表明:双氟磺草胺在3种土壤中的淋出顺序依次为河南砂质黏壤土、山东砂质壤土和安徽黏土,与其在3种土壤中的吸附作用强弱顺序刚好相反,符合土壤对农药的吸附作用弱则其在土壤中移动性就强的一般理论[18]。
|
图 2 双氟磺草胺在3种土壤各段淋出液中的含量 Fig. 2 The content of florasulam in each segment ofthe leachates of soils |
土柱淋溶法中农药的分布情况可以根据各段土层及淋出液中的农药含量占添加总量的百分比来描述[16](式4)。
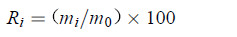
|
(4) |
式中:Ri为各段土层及淋出液中双氟磺草胺的质量分数(%);mi为各段土层及淋出液中双氟磺草胺的质量(mg),i=1、2、3、4、5、LR,分别表示0~5、5~10、10~15、15~20及20~25 cm土层和淋出液;m0为双氟磺草胺的添加总量(mg)。
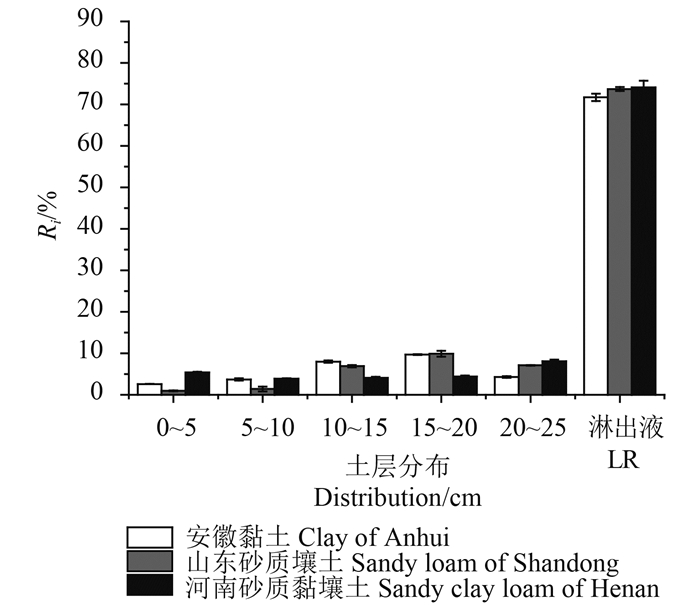
双氟磺草胺在3种土壤各段土层及淋出液中的分布见图 3。结果表明:双氟磺草胺主要集中在10~25 cm土层和淋出液中;其在安徽黏土、山东砂质壤土和河南砂质黏壤土中的淋出率分别为71.7%、73.7%和74.1%,说明双氟磺草胺在3种土壤中的淋溶性均较强,这可能与其在水中的溶解度较高(6.36 g/L,pH=7,20 ℃)有关。
|
图 3 双氟磺草胺在3种土壤各段土层及淋出液中的分布 Fig. 3 The distribution of florasulam in three soils and leachates |
此外,双氟磺草胺在安徽黏土中的淋出率显著低于在山东砂质壤土和河南砂质黏壤土中的淋出率(P<0.05)。将双氟磺草胺在3种土壤中的淋出率与土壤有机质含量、黏粒含量、阳离子交换量以及pH值进行回归分析,得其决定系数R2分别为0.851 9、0.885 1、0.999 3和0.979 9,均呈显著正相关性,表明除农药自身性质外,土壤理化性质也是导致双氟磺草胺淋溶特性差异的重要因素。
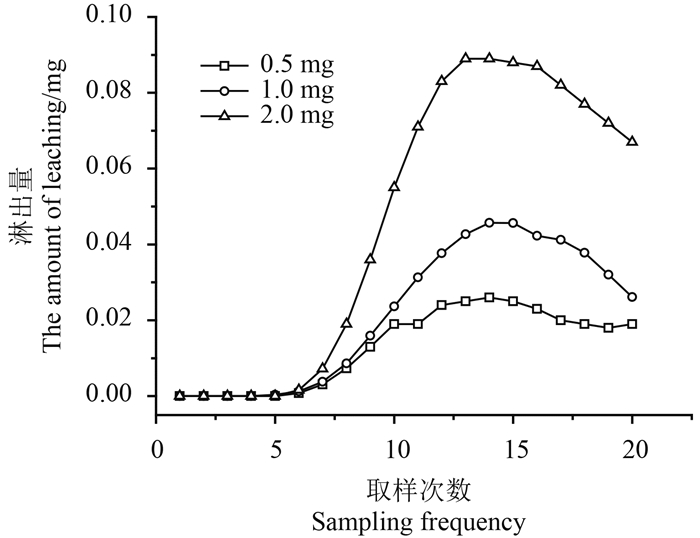
2.5.2 双氟磺草胺初始添加量对其淋溶迁移的影响在评价农药对地下水的污染风险时,需综合考虑其吸附和淋溶特性、施药地点与施药量等多种因素。图 4表明:当初始添加量为0.5、1.0和2.0 mg时,双氟磺草胺的淋出速率相近,其在安徽黏土中的淋出率分别为88.7%、71.7%和71.4%。
|
图 4 初始添加量对双氟磺草胺在各段淋出液中含量的影响 Fig. 4 The influence of initial amount on the content of florasulam in each segment of leachate |
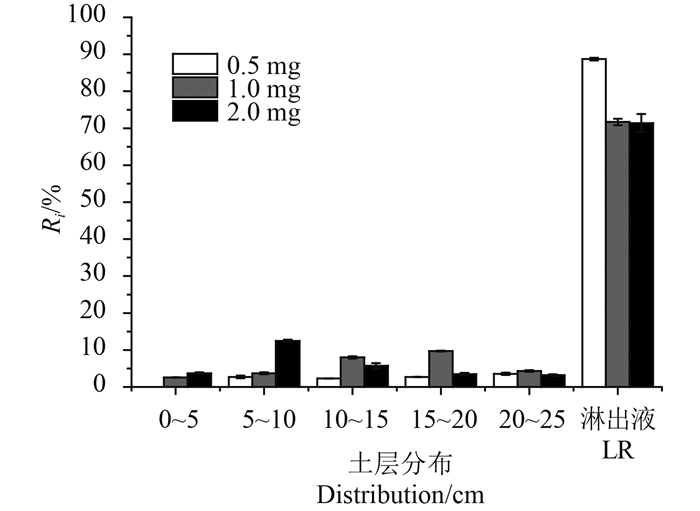
图 5表明:当初始添加量为0.5 mg时,双氟磺草胺主要集中在20~25 cm土层;初始添加量为2.0 mg时,则主要集中在5~15 cm土层。在3个添加水平下,初始添加量为0.5 mg时双氟磺草胺的淋出率与初始添加量为1.0和2.0 mg时的淋出率之间均存在显著性差异(P<0.05),表明土壤中双氟磺草胺初始添加量较低时较易淋出。
|
图 5 初始添加量对双氟磺草胺在各段土层及淋出液中分布的影响 Fig. 5 The influence of initial amount on distribution of florasulam in the soil and leachate |
2.5.3 腐殖酸对双氟磺草胺淋溶迁移的影响
腐殖酸作为常用的土壤改良剂,不仅会影响土壤肥力及其理化性质,而且会影响各种污染物在土壤中的环境行为[19-21]。
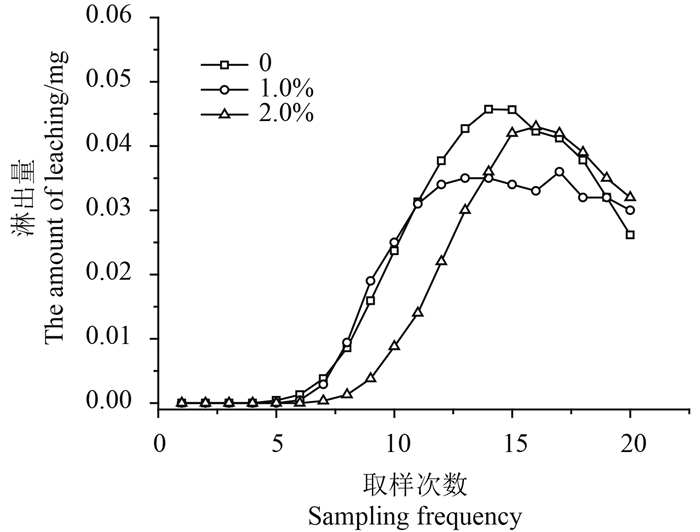
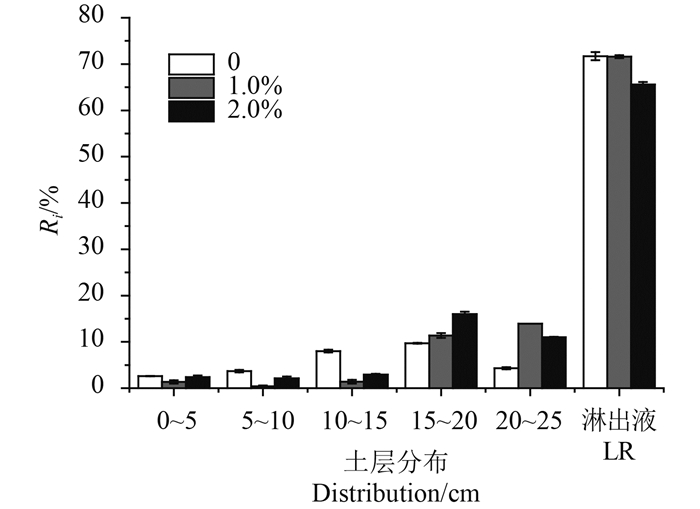
由图 6和图 7可以看出,添加腐殖酸对双氟磺草胺在土壤中的分布会产生一定的影响,且可降低其淋出率。当土壤中腐殖酸的添加量为0、1.0%和2.0%时,双氟磺草胺的淋出率分别为71.7%、71.6%和65.6%,即腐殖酸的添加量越大,双氟磺草胺的淋出率越低,且腐殖酸添加量为2.0%时的淋出率与0和1.0%时相比均存在显著性差异(P<0.05)。添加腐殖酸对土壤中双氟磺草胺向下的淋溶迁移有延阻作用,其原因可能是由于双氟磺草胺被腐殖酸的网状体系所吸附,从而导致其向下淋溶迁移的能力减弱。
|
图 6 腐殖酸对双氟磺草胺在各段淋出液中含量的影响 Fig. 6 The influence of humic acid on the content of florasulam in each segment of leachate |
|
图 7 腐殖酸对双氟磺草胺在各段土层和淋出液中分布的影响 Fig. 7 The influence of humic acid on distribution of florasulam in the soil and leachate |
3 结论
1)添加回收试验表明:土壤样品中双氟磺草胺的回收率为79%~94%,RSD为1.5%~2.9%,最低检测浓度为0.1 mg/kg;水样中双氟磺草胺的回收率为99%~100%,RSD为1.1%~1.2%,最低检测浓度为0.05 mg/L。分析方法符合吸附、淋溶特性研究的分析要求。
2)双氟磺草胺在安徽黏土、山东砂质壤土和河南砂质黏壤土中的吸附均可采用Freundlich方程较好地拟合,其吸附常数(Kf)分别为0.62、0.43和0.39,土壤有机碳归一化吸附系数(Koc)分别为81.35、66.91和73.84,表明双氟磺草胺在3种土壤中均属于难吸附型,3种土壤中的吸附自由能(ΔG)分别为–10.90、–10.42和–10.66 kJ/mol,其吸附机制均为物理吸附。
3)双氟磺草胺在安徽黏土、山东砂质壤土和河南砂质黏壤土中的淋出率分别为71.7%、73.7%和74.1%,在3种土壤中均具有较强的淋溶性。双氟磺草胺初始添加量和腐殖酸对其淋溶具有一定影响。
综合双氟磺草胺的吸附及淋溶特性,表明该农药对地下水的污染风险较大,因此应引起高度重视。
| [1] | SCHIPPERP N M, ⅥSSERSM J M, VANDER LINDEN A M A. Pesticides in groundwater and drinking water wells: overview of the situation in the Netherlands [J]. Water Sci Technol, 2008,57 (8) :1277–1286. |
| [2] |
林绿, 覃志豪, 李文娟. 我国农药地下水环境风险评估场景体系的建立 [J]. 农业环境科学学报, 2014,33 (11)
:2194–2203.
LIN L, QIN Z H, LI W J. Development of a GIS-based scenario analysis system for pesticide groundwater risk assessment in China [J]. J Agro-Environ Sci, 2014, 33 (11) :2194–2203 . |
| [3] | ARIAS-ESTVEZ M, LPEZ-PERIAGO E, MARTNEZ-CARBALLO E, et al. The mobility and degradation of pesticides in soils and the pollution of groundwater resources [J]. Agric Ecosyst Environ, 2008, 123 (4) :247–260 . |
| [4] |
吴文铸, 孔德洋, 郭敏, 等. 甲羧除草醚在土壤中的吸附和淋溶特性 [J]. 生态环境学报, 2012,21 (12)
:2013–2017.
WU W Z, KONG D Y, GUO M, et al. Adsorption and leaching behavior of bifenox in soil [J]. Ecol Environ Sci, 2012, 21 (12) :2013–2017 . |
| [5] |
赵青山, 付颖, 叶非. 三唑并嘧啶磺酰胺类除草剂的研究概况 [J]. 植物保护, 2011,37 (2)
:14–19.
ZHAO Q S, FU Y, YE F. Study summary of triazolo [1,5-a] pyrimidine-2-sulfonanilide herbicides [J]. Plant Prot, 2011, 37 (2) :14–19 . |
| [6] | DEBOER G J, THORNBURGH S, EHR R J. Uptake, translocation and metabolism of the herbicide florasulam in wheat and broadleaf weeds [J]. Pest Manage Sci, 2006, 62 (4) :316–324 . |
| [7] | LI Z N, GUAN W B, HONG H J, et al. Determination and study on residue and dissipation of florasulam in wheat and soil under field conditions [J]. Bull Environ Contam Toxicol, 2013, 90 (3) :280–284 . |
| [8] |
赵亚洲, 段亚玲, 王睿, 等. 双氟磺草胺在土壤中的残留分析 [J]. 中国农学通报, 2015,31 (7)
:180–184.
ZHAO Y Z, DUAN Y L, WANG R, et al. Residue analysis of florasulam in soil [J]. Chin Agric Sci Bull, 2015, 31 (7) :180–184 . |
| [9] |
化学品 批平衡法检测-吸附/解吸附试验: GB/T 21851—2008[S]. 北京: 中国标准出版社, 2008.
Chemicals-adsorption-desorption using a batch equilibrium method: GB/T 21851—2008[S]. Beijing: China Standards Press, 2008. |
| [10] |
农药残留试验准则: NY/T 788—2004[S]. 北京: 中国农业出版社, 2004.
Pesticide residue test guidelines: NY/T 788—2004[S]. Beijing: China Agriculture Press, 2004. |
| [11] | BETRAN J, HERNANDEZ F, LOPEZ F J, et al. Study of sorption processes of selected pesticides on soils and ceramic porous cups used for soil solution sampling [J]. Int J Environ Anal Chem, 1995, 58 (1-4) :287–303 . |
| [12] | TANG Z W, ZHANG W, CHEN Y M. Adsorption and desorption characteristics of monosulfuron in Chinese soils [J]. J Hazard Mater, 2009, 166 (2-3) :1351–1356 . |
| [13] |
化学农药环境安全评价试验准则: GB/T 31270.1—2014[S]. 北京: 中国标准出版社, 2015.
Test guidelines on environmental safety assessment for chemical pesticides: GB/T 31270.1—2014[S]. Beijing: China Standards Press, 2015. |
| [14] |
罗婧, 贾娜, 施海燕, 等. 丙溴磷在土壤中的吸附与迁移行为研究 [J]. 环境科学与技术, 2011,34 (6)
:16–19.
LUO J, JIA N, SHI H Y, et al. Adsorption and mobility of profenofos in soils [J]. Environ Sci Technol, 2011, 34 (6) :16–19 . |
| [15] | JANA T K, DAS B. Sorption of carbary (1-napthyl-N-methyl carbamate) by soil [J]. Bull Environ Contam Toxicol, 1997, 59 (1) :65–71 . |
| [16] |
许秀莹, 宋稳成, 王鸣华. 氟啶胺在土壤中的吸附解吸与淋溶特性 [J]. 中国环境科学, 2013,33 (4)
:669–673.
XU X Y, SONG W C, WANG M H. Adsorption-desorption and leaching characteristics of fluazinam in soils [J]. China Environ Sci, 2013, 33 (4) :669–673 . |
| [17] |
鞠超, 徐军, 董丰收, 等. 磺草酮在土壤中的淋溶特性研究 [J]. 农药学学报, 2015,17 (2)
:246–250.
JU C, XU J, DONG F S, et al. Study on the leaching behavior of sulcotrione in soil [J]. Chin J Pestic Sci, 2015, 17 (2) :246–250 . |
| [18] |
张鹏, 慕卫, 刘峰, 等. 噻虫嗪在土壤中的吸附和淋溶特性 [J]. 环境化学, 2015,34 (4)
:705–711.
ZHANG P, MU W, LIU F, et al. Adsorption and leaching of thiamethoxam in soil [J]. Environ Chem, 2015, 34 (4) :705–711 . |
| [19] | CABRERA A, COX L, KOSKINEN W C, et al. Availability of triazine herbicides in aged soils amended with olive oil mill waste [J]. J Agric Food Chem, 2008, 56 (11) :4112–4119 . |
| [20] | CHIU C C, CHENG C J, LIN T H, et al. The effectiveness of four organic matter amendments for decreasing resin-extractable Cr(Ⅵ) in Cr(Ⅵ)-contaminated soils [J]. J Hazard Mater, 2009, 161 (2-3) :1239–1244 . |
| [21] | RAWAJFIH Z, NSOUR N. Effect of organic and inorganic amendments on sorption of Cr(Ⅵ) and Cr(Ⅲ) in soil[C]//GILKES R J, PRAKONGKEP N. Proceedings of the 19th world congress of soil science: soil solutions for a changing world. Brisbane, Australia, 2010: WCSS, 58-61. |
 2016, Vol. 18
2016, Vol. 18


