2. 福建农林大学资源与环境学院, 福州 350002
2. College of Resource and Environment, Fujian Agriculture and Forest University, Fuzhou 350002, China
已有研究表明,除草剂的大量施用对农田土壤微生物种群数量和酶活性影响很大[1-2]。氮素在土壤中的转化过程是全球氮循环的中心环节之一,而这一过程大多是由微生物参与的生物学和生物化学过程。施用除草剂会对土壤中氮素的氨化[3-4]、硝化[5]和反硝化[6]过程产生影响,从而影响土壤氮肥的有效性和生物利用率。笔者等前期的研究也表明,除草剂对土壤中尿素态氮的转化过程具有一定影响,且这种影响在不同除草剂品种间存在明显的差异[7]。
近年来随着农业生产的快速发展,中国化肥使用量持续迅速增加,单位面积用量已远高于225 kg/hm2 的国际上限标准[8],特别在一些设施菜地,土壤中氮肥施用量 (以有效成分氮计) 甚至超过了900 kg/hm2 [9]。大量研究表明,在不同的施氮量水平下,土壤的脲酶活性、氨氧化微生物活性和种群数量以及硝化作用[10-11]等均存在较大差异,这可能会直接导致除草剂施用效果的差异。然而,目前尚未见针对不同施氮量条件下,除草剂对土壤中氮素转化过程影响情况的相关研究报道。乙草胺是应用很广泛的一种氯乙酞苯胺类除草剂[12],据统计,中国乙草胺的年使用量已超过1×107 kg (原药),是使用量最大的3种除草剂之一[13]。因此,开展在不同施氮量水平下乙草胺对土壤氮转化过程影响的相关研究十分必要,可为氮肥和除草剂的施用效应评价及安全合理施用提供科学依据。
1 材料与方法 1.1 试验材料50% 乙草胺乳油 (acetochlor 50% EC,杭州庆丰农化有限公司);氮肥为尿素 (含氮量46%,上海国药集团化学试剂有限公司)。供试土壤取自中国福建省福州市郊区菜田,土壤类型为灰泥土,有机质质量分数21.30 g/kg,全氮质量分数1.65 g/kg,土壤 C/N 比为7.49,碱解氮质量分数为123.70 mg/kg,土壤容重为1.22 g/cm3,pH 5.6。
1.2 试验设计共设7个处理:施氮量0、75、150和300 mg/kg 4个水平处理,分别用 N0、N1、N2和 N3表示;施氮量75、150和300 mg/kg + 乙草胺处理,分别用 HN1、HN2和 HN3表示,其中乙草胺的用量为有效成分10 mg/kg (根据田间施用量及施药方法,估算得到的乙草胺在大田1次施用后全部集中于2 cm 土层的含量)。野外采回的新鲜土壤经微风干 (以保持土壤微生物活性,其质量含水率为13.2%) 后立即过2 mm 筛。称取约折合150 g 烘干土的微风干土,装入300 mL 的广口瓶中。将氮肥和乙草胺先按比例混合,溶于水后再定量加入广口瓶中,使土壤含水量达到土壤孔隙度的60%。用封口膜封口,保持瓶内外自由通气,于28 ℃ 下恒温好气培养。
试验采用破坏性取样,每次取8瓶,其中4瓶用于测定土壤中氮素的动态变化,4瓶用于测定反硝化损失,取样时间分别为培养后1、2、4、8、12、16、20、26、32、38及44 d。反硝化作用测定采用乙炔抑制法[14]:于取样前24 h 用带有2根玻璃管的软木塞塞住瓶口,每根玻璃管分别接1段硅胶管,其中1根连接三通阀,密封2根通气管。将注射器接到三通阀上,从培养瓶中抽出10% 自由体积的空气,再回注等量纯净乙炔,并混合均匀,以达到扩散均匀以及抑制硝化作用及 N2O 还原酶活性的目的。置于培养箱中培养24 h 后,抽取20 mL 瓶中气体,用于测定反硝化作用产生的 N2O 气体。氮素动态变化测定:在取样当天,直接将培养瓶中的土壤整瓶取出,充分混匀,用于测定土壤中尿素态氮、铵态氮和硝态氮含量。
1.3 样品测定方法土壤尿素态氮采用二乙酰一肟-硫代氨基脲法[15]测定;土壤铵态氮采用靛酚蓝比色法[16]测定;土壤硝态氮采用紫外分光光度法[16]测定。采用经中国科学院大气物理所改装、美国 Agilent 公司生产的气相色谱仪 GC7890A[17] 对反硝化产生的 N2O (N2O + N2) 气体样品进行分析。
1.4 数据统计分析采用 SPSS 13.0和 Excel 2003软件进行试验数据统计分析及图表制作。
2 结果与分析 2.1 土壤中尿素态氮的动态变化尿素施入土壤后可在脲酶的作用下迅速水解成铵态氮。从表 1 中可看出,在不施用乙草胺的情况下,随着尿素施用量的增加,其水解成铵态氮的速率明显降低,24 h 后,尿素的水解率从 N1处理的99.4% 降低至 N3处理的67.3%。
|
|
表 1 土壤中尿素态氮含量动态变化 Table 1 Temporary changes of urea content in soil under different treatments |
乙草胺的施用会对尿素的水解过程产生影响,且在不同的施氮量水平下其影响效果不同。从表 1 中可看出,施氮量为75 mg/kg 时 (处理 HN1),乙草胺对尿素的水解过程基本无影响;施氮量为150和300 mg/kg 时 (处理 HN2和 HN3),在培养的前24 h 乙草胺可明显抑制尿素的水解过程 (P < 0.05),其24 h 时的水解率分别比不施乙草胺的 N2和 N3处理降低了10.1% 和9.8%;培养48 h 后,施用和不施用乙草胺处理组土壤中尿素态氮的含量无明显差异。研究表明,乙草胺的施用会抑制土壤中脲酶的活性,从而对尿素的水解过程产生不利影响,但在低氮量 (75 mg/kg) 条件下其表现并不明显。这可能是由于在较低尿素用量下,土壤中脲酶的水解能力还远未饱和,根据酶促反应动力学原理,酶未饱和时,尿素的水解速率仅取决于其起始浓度[18] ,因而在此情况下乙草胺对尿素的水解基本无影响。
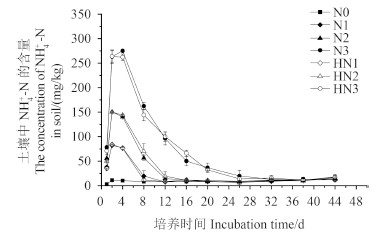
2.2 土壤中铵态氮的动态变化从图 1 中可看出,在培养的前期,由于尿素水解转化成铵态氮,因此土壤中铵态氮的含量随尿素施用量的增加而不断升高,其中 N1和 N2处理的铵态氮含量在培养第2天达到最大值 (82.4和150.4 mg/kg),而 N3处理组则在第4天达到最大值 (275.1 mg/kg)。之后由于铵态氮逐渐经硝化作用转化为硝态氮,因此各处理组土壤中的铵态氮含量逐渐降低,至第26天后,所有施氮肥处理组的铵态氮含量均和空白对照无显著差异。
|
注:N0、N1、N2和 N3分别表示施氮量为0、75、150和300 mg/kg 的4个处理,HN1、HN2和 HN3分别表示施氮量75、150和300 mg/kg + 乙草胺10 mg/kg 的处理。
Note: N0, N1, N2 and N3 refers to the nitrogen (0, 75, 150 and 300 mg/kg) treatment, HN1, HN2 and HN3 refer to the nitrogen (75, 150 and 300 mg/kg) + acetochlor (10 mg/kg, active ingredient) treatment. 图 1 不同氮肥水平下乙草胺对土壤中铵态氮含量的影响 Fig. 1 Effects of acetochlor on temporary changes of NH4+-N content in soil at different nitrogen fertilizer application rates |
和土壤中尿素的水解过程 (表 1) 基本类似,在整个培养过程中,N1和 HN1处理组的铵态氮含量均无显著差异;第1天时,HN2和 HN3处理组铵态氮含量显著低于 N2和 N3处理组 (P < 0.05),但从第2天开始,乙草胺对尿素的转化过程不再产生影响,因此添加和未添加除草剂处理间铵态氮的含量无显著差异。
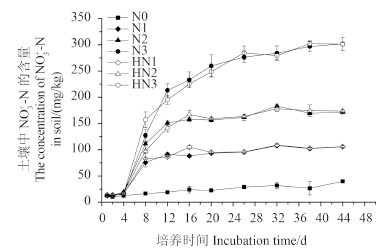
2.3 土壤中硝态氮的动态变化结果见图 2。在整个培养过程中,仅施肥各处理组土壤中硝态氮的含量均随着尿素施用量的增加及培养时间的延长而升高。整个培养过程中,HN1和 N1处理组硝态氮含量无显著差异,说明当施氮量为75 mg/kg 时,乙草胺对土壤中铵态氮的硝化过程无影响;培养至第8天时,HN2处理的硝态氮含量显著低于 N2处理 (P < 0.05),说明当施氮量为150 mg/kg 时,乙草胺对土壤中氮素的硝化过程表现为抑制作用;培养至第8天时,HN3处理组硝态氮含量显著高于 N3处理组 (P < 0.05),至第12天时则恰好相反,HN3处理组的硝态氮含量显著低于 N3处理组 (P < 0.05),即当氮肥用量为300 mg/kg 时,乙草胺对土壤氮素的硝化过程表现为先促进后抑制的作用。分析这可能是由于不同施氮量水平下,土壤中硝化微生物的群落和种群数量不同,因而导致其对除草剂施用的响应不同造成的。
|
注:N0、N1、N2和 N3分别表示施氮量为0、75、150和300 mg/kg 的4个处理,HN1、HN2和 HN3分别表示施氮量75、150和300 mg/kg + 乙草胺10 mg/kg 的处理。
Note: N0, N1, N2 and N3 refers to the nitrogen (0, 75, 150 and 300 mg/kg) treatment, HN1, HN2 and HN3 refer to the nitrogen (75, 150 and 300 mg/kg) + acetochlor (10 mg/kg, active ingredient) treatment. 图 2 不同氮肥水平下乙草胺对土壤中硝态氮含量的影响 Fig. 2 Effects of acetochlor on temporary changes of NO3--N content in soil at different nitrogen fertilizer application rates |
2.4 乙草胺对土壤氮素反硝化作用的影响
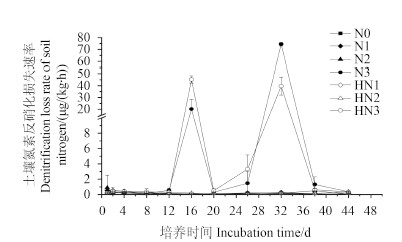
土壤反硝化作用是指在反硝化细菌的作用下,土壤中的硝酸盐被还原成氮气的过程。从图 3 中可看出,整个培养过程中,HN1和 HN2处理的反硝化损失速率一直处于较低的水平,与 N0处理无明显差异,表明当施氮量为75和150 mg/kg 时,施用乙草胺对土壤氮素的反硝化过程没有明显影响。当施氮量为300 mg/kg 时,HN3和 N3处理的反硝化损失速率在培养的第16天和第32天时分别出现了两个明显的峰值:第16天时,HN3处理反硝化损失速率为45.3 μg/(kg·h),显著高于 N3处理 (P < 0.05);第32天时,HN3处理的反硝化损失速率为39.6 μg/(kg·h),反而比 N3处理显著降低了46.82% (P < 0.05)。
|
注:N0、N1、N2和 N3分别表示施氮量为0、75、150和300 mg/kg 的4个处理,HN1、HN2和 HN3分别表示施氮量75、150和300 mg/kg + 乙草胺10 mg/kg 的处理。
Note: N0, N1, N2 and N3 refers to the nitrogen (0, 75, 150 and 300 mg/kg) treatment, HN1, HN2 and HN3 refer to the nitrogen (75, 150 and 300 mg/kg) + acetochlor (10 mg/kg, active ingredient) treatment. 图 3 不同氮肥水平下乙草胺对土壤氮素反硝化损失速率的影响 Fig. 3 Effects of acetochlor on temporary changes of denitrification in soil at different nitrogen fertilizer application rates |
从表 2 中可看出:整个培养期间,N1和 N2处理土壤中氮素的反硝化损失总量 (以有效氮计) 和空白对照 (N0) 无显著差异,其反硝化损失总量占施氮量的0.07%~0.09%;而 N3处理的反硝化损失总量急剧增加至13 221 μg/kg,为空白对照的117倍,差异极显著 (P < 0.01),占到了施氮量的4.37%。当施氮量为75和150 mg/kg 时,施用乙草胺对土壤氮素的反硝化损失总量无明显影响,HN1和 N1、HN2和 N2处理之间差异不显著;而施氮量为300 mg/kg 时,HN3处理组的反硝化损失总量为10 814 μg/kg,比 N3处理减少了18.20%,表明在此条件下施用乙草胺极显著地降低了土壤中氮素的反硝化损失 (P < 0.01)。
|
|
表 2 土壤中尿素氮肥的反硝化作用损失 Table 2 Loss amount of urea nitrogen by denitrification in soil |
3 结论与讨论 3.1 除草剂对土壤中尿素态氮水解过程的影响
施用除草剂会影响土壤中微生物和酶的活性,进而对土壤中氮素转化过程产生影响。脲酶是目前发现的惟一一种能够转化酰胺态氮肥 (尿素) 中氮的酶,其活性与土壤中营养物质转化能力及肥力水平密切相关[19]。本研究结果表明,当施氮量为75 mg/kg 时,施用乙草胺对土壤中尿素的水解过程无明显影响;施氮量为150和300 mg/kg 时,乙草胺在前24 h 可显著抑制尿素的水解过程。已有不少研究报道证实,乙草胺可抑制土壤中脲酶的活性[3, 20],且随着其施用量增加,抑制作用时间越长[21]。这可能是由于乙草胺与脲酶之间具有较强的结合作用,且能进入脲酶的分子结构中并形成一个结合位点,部分掩盖或占据了脲酶的活性中心,导致酶促反应速率减缓,即发生了与底物的非竞争性抑制作用[22]。
3.2 除草剂对土壤中氮素硝化过程的影响Kara 等[23]的研究显示,特丁津 (terbuthylazine) 在3种土壤中可抑制硝化微生物的活性,从而降低硝态氮含量,而在另一种土壤中可提高硝态氮的含量,对亚硝态氮含量则无影响。Gigliotti 等[24]发现,苄嘧磺隆 (bensulfuron) 和醚磺隆 (cinosulfuron) 在田间推荐施药量和100倍推荐施药量时,对土壤中细菌和硝化细菌数以及土壤呼吸作用均无影响,但可降低土壤的硝化活性。总之,多数研究均表明,除草剂对土壤氮素的硝化有一定的抑制作用[25-26]。而本研究发现:在150和300 mg/kg 氮肥用量下,乙草胺对土壤中氮素的硝化过程有一定的抑制作用,但在75 mg/kg 的氮肥用量下,其影响却不明显。这可能是由于不同氮量水平下,土壤中硝化微生物的群落和种群数量不同造成的。卞碧云[27]的研究表明,在不同施氮量的土壤中,硝化 (氨氧化) 微生物的组成存在明显差异,氨氧化古菌 (ammonia-oxidizing archaeon,AOA) 在适度施氮的土壤中占主导作用,而氨氧化细菌 (ammonia-oxidizing bacteria,AOB) 在氮素高度富集的土壤中占主导作用。然而目前关于不同硝化微生物对乙草胺施入后的响应机理尚不清楚,有关其对土壤硝化过程的贡献也缺乏准确的评估,因此还需针对不同氮肥用量下土壤硝化微生物种群及活性的变化,以及其对除草剂施用后的响应机理等进一步展开深入研究。
3.3 除草剂对土壤中氮素反硝化过程的影响土壤中的反硝化作用是指化能异养型的好气细菌在无氧或微量氧条件下,将硝酸、亚硝酸或其他氮氧化物还原为 N2O 或 N2 的过程。Somda 等[28]报道,2-氯-6-三氯甲基吡啶 (nitrapyrin)、莠去津 (atrazine) 或西玛津 (simazine) 对液态介质中 NO3- 的反硝化过程具有抑制作用。也有研究表明,在田间推荐使用剂量下,农药一般对反硝化过程无持久性抑制作用,只在较高剂量时才会产生明显的抑制作用[29]。Yeomans 等[6]研究发现,特丁津在4种土壤中均可刺激反硝化细菌的活性,因此有可能会对土壤中氮素的反硝化产生促进作用。笔者等在前期研究中发现,丁草胺对土壤中氮素的反硝化表现为显著促进作用,而草甘膦则表现为显著的抑制作用[7],且在田间条件下,乙莠 (40% 乙草胺 · 莠去津悬浮剂)、丁莠 [48% 丁草胺 (butachlor) · 莠去津悬浮剂] 和旱锄 [39% 噻磺隆 (thiameturon-methyl) · 乙草胺可湿性粉剂] 3种除草剂均可显著减少土壤中氮素的反硝化损失量[30]。总体来看,不同除草剂对土壤中氮素反硝化作用的影响不同。本研究发现:当施氮量为300 mg/kg 时,施用乙草胺极显著地降低了氮肥的反硝化损失总量 (HN3比 N3处理组反硝化损失总量减少了18.20%),而施氮量为75和150 mg/kg 时,整个培养期内其反硝化损失总量和空白对照无显著差异,且乙草胺对反硝化过程影响不明显。分析这可能和中、低氮肥用量时土壤本身的反硝化损失量也比较低有关。因此,在当今大量施用氮肥的农业生产环境下,施用除草剂乙草胺可减少土壤氮素的反硝化损失,在一定程度上有利于提高土壤肥力和温室气体减排。但目前关于除草剂施用后究竟是如何作用于土壤氮素反硝化过程的仍不是很清楚,还需进一步研究。
| [1] | MIN H, YE Y F, CHEN Z Y, et al. Effects of butachlor on microbial populations and enzyme activities in paddy soil [J]. J Environ Sci Health B, 2001, 36 (5) :581–595 . |
| [2] | DAMIN V, TRIVELIN P C O. Herbicides effect on nitrogen cycling in agroecosystems[C]//KORTEKAMP A. Herbicides and environment. Rijeka, Croatia: in Tech, 2011: 107-124. |
| [3] | KUCHARSKI J, BAC’MAGA M, WYSZKOWSKA J. Effects of herbicides on the course of ammonification in soil [J]. J Elementol, 2009, 14 (3) :477–487 . |
| [4] | PARIDA C S, MONDAL S, SIDDIQUI M Z. Effect of urea, vermicompost and pendimethalin on nitrogen transformation in lateritic soil [J]. Progr Agric, 2010, 10 (2) :252–255 . |
| [5] | TU C M. Effect of selected herbicides on activities of microorganisms in soils [J]. J Environ Sci Health B, 1996, 31 (6) :1201–1214 . |
| [6] | YEOMANS J C, BREMNER J M. Denitrification in soil: effects of herbicides [J]. Soil Biol Biochem, 1985, 17 (4) :447–452 . |
| [7] |
丁洪, 郑祥洲, 雷俊杰, 等. 除草剂对尿素氮在土壤中转化的影响 [J]. 生态环境学报, 2012,21 (3)
:551–554.
DING H, ZHENG X Z, LEI J J, et al. Effects of herbicides on transformation of urea nitrogen in vegetable plantation soil [J]. Ecol Environ Sci, 2012, 21 (3) :551–554 . |
| [8] |
栾江, 仇焕广, 井月, 等. 我国化肥施用量持续增长的原因分解及趋势预测 [J]. 自然资源学报, 2013,28 (11)
:1869–1878.
LUAN J, QIU H G, JING Y, et al. Decomposition of factors contributed to the increase of China's chemical fertilizer use and projections for future fertilizer use in China [J]. J Nat Resour, 2013, 28 (11) :1869–1878 . |
| [9] | SHI W M, YAO J, YAN F. Vegetable cultivation under greenhouse conditions leads to rapid accumulation of nutrients, acidification and salinity of soils and groundwater contamination in South-Eastern China [J]. Nutr Cycl Aroecosys, 2009, 83 (1) :73–84 . |
| [10] |
蒲小鹏, 胡自治, 张德罡, 等. 高寒地区土壤脲酶活性与尿素用量的关系 [J]. 草地学报, 2007,15 (1)
:95–96.
PU X P, HU Z Z, ZHANG D G, et al. Relationship between urease activity and urea application rate in alpine regions [J]. Acta Agrestia Sinica, 2007, 15 (1) :95–96 . |
| [11] |
贾俊仙, 李忠佩, 刘明, 等. 施用氮肥对不同肥力红壤性水稻土硝化作用的影响 [J]. 生态与农村环境学报, 2010,26 (4)
:329–333.
JIA J X, LI Z P, LIU M, et al. Nitrification in red paddy soils different in soil fertility under N fertilization [J]. J Ecol Rural Environ, 2010, 26 (4) :329–333 . |
| [12] |
苏少泉. 除草剂作用靶标的分类与使用 [J]. 农药, 1998,37 (11)
:1–7.
SU S Q. Classification of herbicides by target of action and herbicides use [J]. Pesticides, 1998, 37 (11) :1–7 . |
| [13] |
郑和辉, 叶常明. 乙草胺和丁草胺的水解及其动力学 [J]. 环境化学, 2001,20 (2)
:168–171.
ZHENG H H, YE C M. Hydrolysis of chloroacetanilide herbicides acetochlod and butachlor [J]. Environ Chem, 2001, 20 (2) :168–171 . |
| [14] | MÜLLER C, SHERLOCK R R, WILLIAMS P H. Field method to determine N2O emission from nitrification and denitrification [J]. Biol Fert Soils, 1998, 28 (1) :51–55 . |
| [15] | MULVANEY R L, BREMNER J M. Modified diacetyl monoxime method for colorimetric determination of urea in soil extracts [J]. Commun Soil Sci Plan, 1979, 10 (8) :1163–1170 . |
| [16] |
鲁如坤.
土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 1999 : 150 -160.
LU R K. Analysis methods of soil agricultural chemistry[M]. Beijing: Chinese Agricultural Science and Technology Press, 1999 : 150 -160. |
| [17] |
郑祥洲, 丁洪, 雷俊杰, 等. 吡虫啉和毒死蜱对尿素氮在土壤中转化的影响 [J]. 农药学学报, 2013,15 (6)
:648–654.
ZHENG X Z, DING H, LEI J J, et al. Effects of imidacloprid and chlorpyrifos on transformation of urea nitrogen in soil [J]. Chin J Pestic Sci, 2013, 15 (6) :648–654 . |
| [18] |
王镜岩.
生物化学[M]. 北京: 高等教育出版社, 2002 : 351 -367.
WANG J Y. Biochemistry[M]. Beijing: Higher Education Press, 2002 : 351 -367. |
| [19] | BENDING G D, TURNER M K, RAYNS F, et al. Microbial and biochemical soil quality indicators and their potential for differentiating areas under contrasting agricultural management regimes [J]. Soil Biol Biochem, 2004, 36 (11) :1785–1792 . |
| [20] |
刘惠君, 刘维屏, 杨炜春, 等. 均三氮苯类除草剂对土壤酶活性的影响 [J]. 土壤学报, 2003,40 (2)
:286–292.
LIU H J, LIU W P, YANG W C, et al. Effect of triazine on soil enzyme activity [J]. Acta Pedol Sinica, 2003, 40 (2) :286–292 . |
| [21] |
荆瑞勇, 王丽艳, 王彦杰, 等. 乙草胺对土壤微生物数量和酶活性的影响 [J]. 中国生态农业学报, 2010,18 (6)
:1302–1305.
JING R Y, WANG L Y, WANG Y J, et al. Effect of acetochlor application on soil microorganism number and enzymes activities [J]. Chin J Eco-Agri, 2010, 18 (6) :1302–1305 . |
| [22] |
张昀, 可欣, 查春梅, 等. 吡嘧磺隆对土壤中与氮素转化有关微生物活性的影响 [J]. 土壤通报, 2008,39 (4)
:950–952.
ZHANG Y, KE X, ZHA C M, et al. Effect of pyrazosulfuron-ethyl on microbiological activity related with N transformation in paddy soil [J]. Chin J Soil Sci, 2008, 39 (4) :950–952 . |
| [23] | KARA E E, ARLI M, UYGUR V. Effects of the herbicide topogard on soil respiration, nitrification, and denitrification in potato-cultivated soils differing pH [J]. Biol Fertility Soils, 2004, 39 (6) :474–478 . |
| [24] | GIGLIOTTI C, ALLIEVI L. Differential effects of the herbicides bensulfuron and cinosulfuron on soil microorganisms [J]. J Environ Sci Health B, 2001, 36 (6) :775–782 . |
| [25] | KIM J E, HONG J U. Effects of herbicides on enzyme activities in soil environment [J]. J Korean Agric Chem Soc, 1988, 31 (1) :79–85 . |
| [26] | CSITARI G, DEBRECZENI K, SISAK I. Progress in nitrogen cycling studies[C]//Proceedings of the 8th nitrogen workshop held at the University of Ghent, Belgium, 5-8 September 1994. Dordrecht: Kluwer Academic Publishers, 1996: 191-194. |
| [27] |
卞碧云. 氮肥用量对设施栽培蔬菜土壤氨氧化微生物及氨氧化作用的影响[D]. 南京: 南京师范大学, 2013: 38-40.
BIAN B Y. Effects of different nitrogen fertilizer application rates on ammonia oxidizing bacteria and ammonia oxidation in greenhouse vegetable soil[D]. Nanjing: Nanjing Normal University, 2013: 38-40. |
| [28] | SOMDA Z C, PHATAK S C, MILLS H A. Nitrapyrin, terrazole, atrazine and simazine influence on denitrification and corn growth [J]. J Plant Nutrition, 1990, 13 (9) :1195–1208 . |
| [29] | CARLISLE S M, TREVORS J T. Effect of the herbicide glyphosate on nitrification, denitrification and acetylene reduction in soil [J]. Water Air Soil Poll, 1986, 29 (2) :189–203 . |
| [30] |
丁洪, 王跃思. 除草剂对氮肥反硝化损失和 N2O 排放的影响 [J]. 中国环境科学, 2004,24 (5)
:596–599.
DING H, WANG Y S. Influence of herbicides on denitrification loss of nitrogen fertilizer and emission of N2O [J]. China Environ Sci, 2004, 24 (5) :596–599 . |
 2016, Vol. 18
2016, Vol. 18


