芒果Mangifera indica Linn已成为世界五大水果之一[1],主要分布在印度、泰国、中国、墨西哥、印尼、菲律宾、越南和巴西等热带国家和地区。我国芒果种植主要集中在海南、广东、台湾和四川等热带地区,产量居世界第二。热带地区高温高湿的气候特点使得病虫害在农作物上的发生较为普遍,由于芒果缺乏优良的抗病品种,炭疽病、黑斑病和白粉病发病较为常见。吡唑醚菌酯、腈苯唑和烯唑醇(结构式见Scheme 1)均为内吸传导型杀菌剂,用于防治芒果炭疽病、叶斑病、黑星病、白粉病和霜霉病等[2, 3, 4, 5],使用不合理会造成在芒果果实中的累积,导致其残留量超标,引发农产品质量安全问题[6]。欧盟制定了芒果中吡唑醚菌酯、腈苯唑和烯唑醇的最大残留限量标准(MRLs)分别为0.05、0.5和0.01 mg/kg,我国制定了芒果中吡唑醚菌酯的MRLs为0.05 mg/kg[7, 8]。
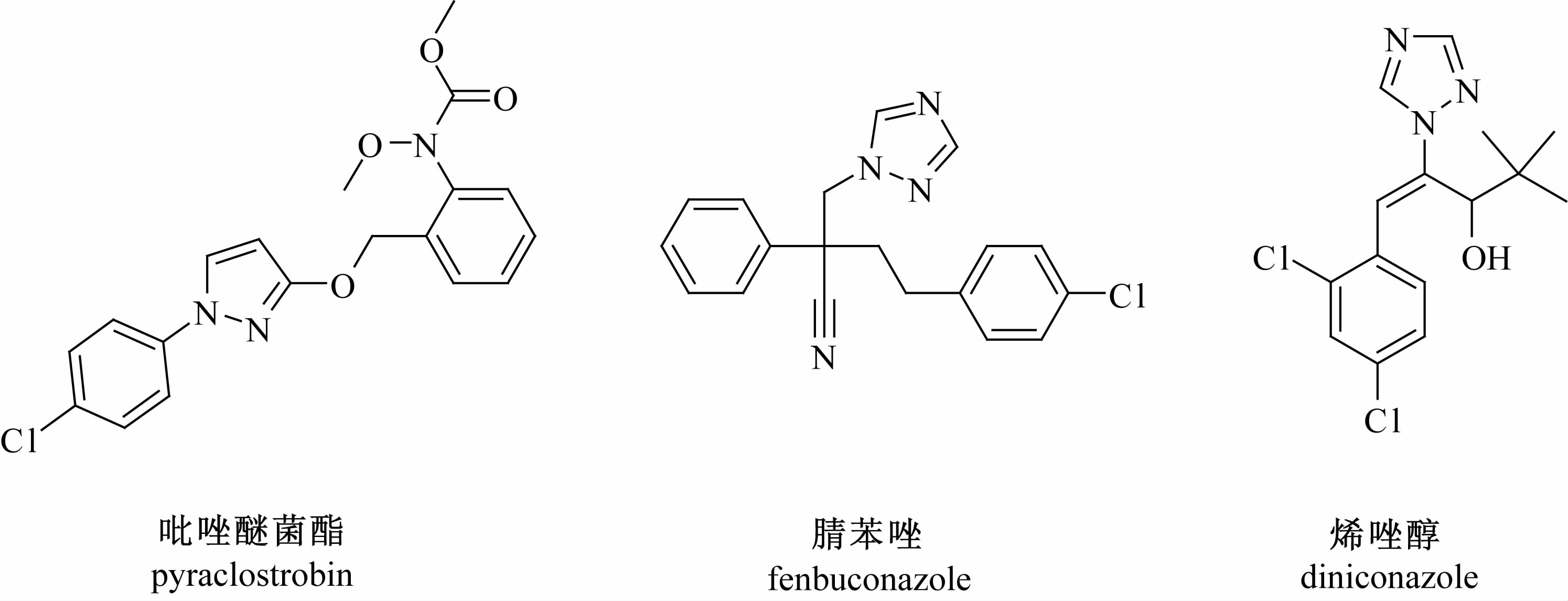
|
Scheme 1 |
Anastassiades等[9]于2003年提出的QuEChERS(Quick,Easy,Cheap,Effective,Rugged and Safe)方法,具有回收率高、速度快、操作简单和可分析的农药范围广等优点,但净化能力较弱。为了提高净化能力,除N-丙基-乙二胺(PSA)外,研究人员在寻找更多吸附剂,如C18粉、石墨化碳黑粉末(GCB)和氨丙基粉等[10, 11, 12]。PSA能去除强极性的有机酸和酚类及部分糖和脂类干扰物,C18可以去除非极性的糖类、脂类等,GCB能去除色素。目前,国内外已有利用气相色谱法检测腈苯唑和液相色谱法检测吡唑醚菌酯在芒果中残留的报道[13, 14, 15, 16, 17],但尚未见同时检测芒果中吡唑醚菌酯、腈苯唑和烯唑醇3种杀菌剂残留的报道。本研究拟利用QuEChERS方法净化芒果提取液,采用UPLC-MS/MS同时检测芒果中吡唑醚菌酯、腈苯唑和烯唑醇3种杀菌剂的残留。
1 材料与方法 1.1 仪器与试剂Waters超高效液相色谱-三重四极杆串联质谱仪(ACQUITY UPLC/Quattro PremierTM XE)配有电喷雾离子源(ESI)和MasslynxTM 4.0 工作站、ACQUITY UPLCTM BEH C18(2.1 mm× 100 mm,1.7 μm)色谱柱,美国Waters公司;电子分析天平,瑞典梅特勒托利多公司;离心机,上海安亭科学仪器厂。
99.0%吡唑醚菌酯(pyraclostrobin)、98.7%腈苯唑(fenbuconazole)和99.0%烯唑醇(dinicona-zole)标准品,农业部环境保护科研监测所;甲醇和乙腈均为色谱纯,美国Fisher公司; PSA吸附剂,美国Agilent公司;C18吸附剂和GCB粉末,上海安谱科学仪器有限公司;试验用水为Milli-Q净化系统经0.22 μm滤膜过滤的纯化水。
1.2 样品前处理芒果样品购自海南省海口市南北水果批发市场,去核取可食部分,用组织捣碎机捣碎,于-18 ℃下密封保存,备用。
准确称取10.00 g芒果样品于50 mL具塞离心管中,加入10.0 mL乙腈、3.0 g 硫酸镁、1.0 g 氯化钠,于18 000 r/min下均质1 min,再于5 000 r/min下离心5 min。取1.00 mL上清液置于预先加有35 mg PSA、35 mg C18及150 mg 硫酸镁的离心管中,涡旋60 s,再于5 000 r/min下离心5 min,上清液经0.22 μm微孔滤膜过滤,待UPLC-MS/MS分析。
1.3 标准溶液的配制 1.3.1 标准储备液的配制将吡唑醚菌酯、腈苯唑和烯唑醇标准品用甲醇溶解,配制成质量浓度为100 μg/mL的混合标准储备液,于-18 ℃避光保存,有效期3个月。
1.3.2 基质匹配标准溶液的配制取芒果样品按1.2节的方法进行前处理,制得空白芒果基质溶液。将1.3.1节的混合标准储备液用空白芒果基质溶液稀释成质量浓度为5.0、10、20、50、100、200和500 ng/mL的系列混合标准溶液,现配现用。
1.4 检测条件色谱条件:流动相A为甲醇,流动相B为1 mmol/L的乙酸铵水溶液;柱温35 ℃;样品室温度10 ℃;进样体积5 μL;流速0.25 mL/min。梯度洗脱程序见表 1。
|
|
表 1 梯度洗脱程序 Table 1 Gradient elution program |
质谱条件:正离子电离模式;毛细管电压3.00 kV;脱溶剂气温度350 ℃;脱溶剂气流量900 L/h;锥孔气流量50 L/h;离子源温度110 ℃;碰撞气流速0.21 mL/min。多反应监测(MRM)分析的质谱参数见表 2。
|
|
表 2 多反应监测模式下的质谱参数 Table 2 MS conditions under MRM mode |
基质效应是指样品分析液中除分析物以外的共流出组分改变了分析物的响应值,从而影响定量分析的准确度和重现性,其机制可能是共流出组分影响了电喷雾接口的离子化效率[18]。本研究通过测定各农药在基质匹配溶液中的响应值(A)及其在纯溶剂中的响应值(B),得到基质效应(Matrix Effect,ME)/%=[(A-B)/B]×100。ME为正值表示基质增强效应,ME为负值表示基质抑制效应。
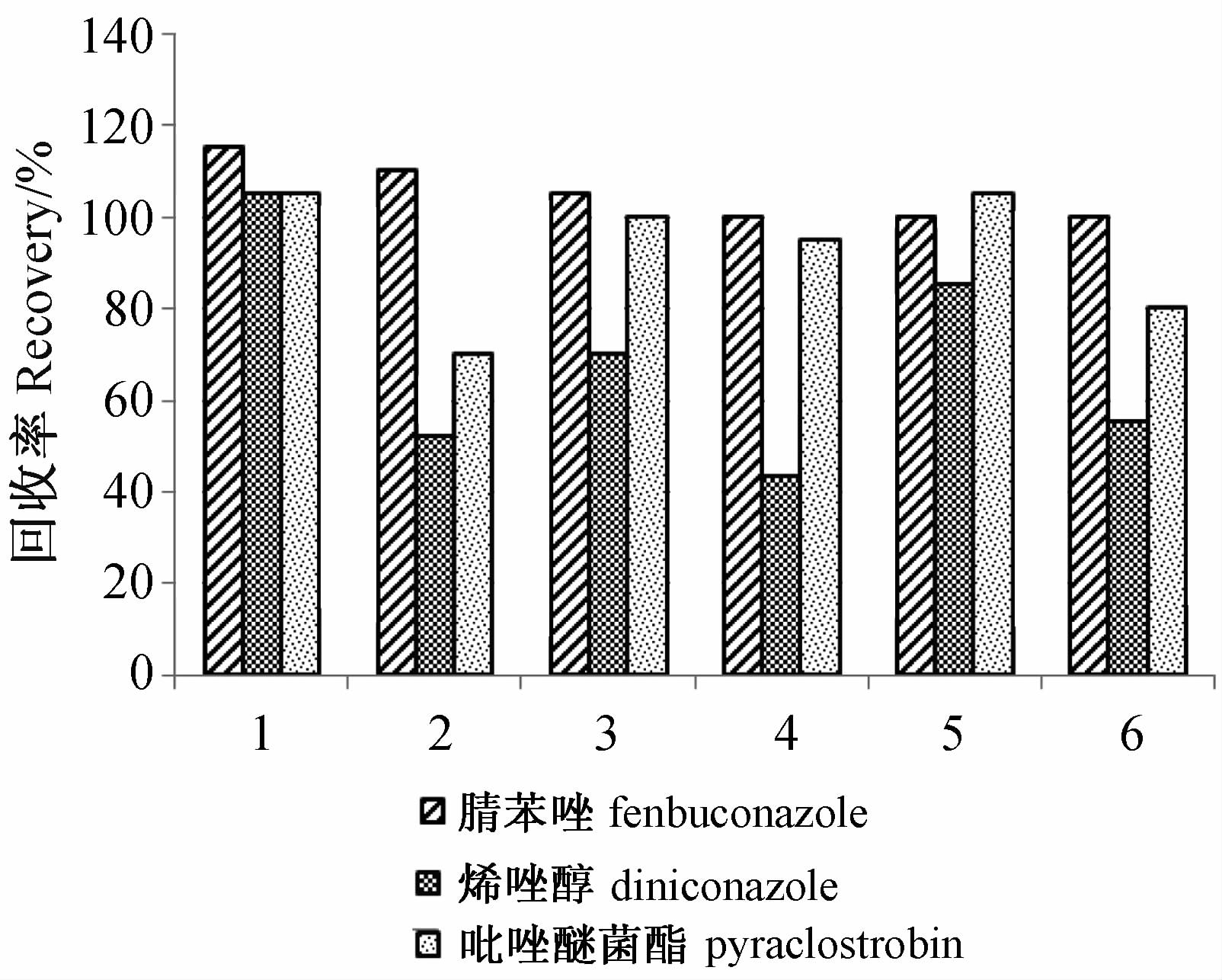
2 结果与讨论 2.1 净化条件的选择本研究考察了PSA、PSA+GCB、C18、C18+GCB、PSA+C18和PSA+C18+GCB等净化芒果提取液。结果(图 1)表明:添加GCB,烯唑醇的回收率低于60%,达不到分析方法的要求;分别添加PSA+C18、PSA和C18,3种农药的回收率在70%~115%之间,其中以C18粉末作为吸附剂时,烯唑醇回收率低于以等当量的PSA和PSA + C18为吸附剂的回收率,其原因可能是C18的净化能力弱于等当量的PSA,导致烯唑醇的基质效应更大;单独使用PSA或C18时,净化液呈黄色,而使用PSA+C18时净化液澄清透明,净化效果较好。故最终选择PSA+C18作为吸附剂来净化芒果提取液。
|
1: 70mg PSA;2: 35mg PSA + 25mg GCB;3: 70mg C18; 4: 35mg C18 + 25mg GCB;5: 35mg PSA + 35mg C18; 6: 35mg PSA + 35mg C18 + 25mg GCB. 图 1 不同净化条件下3种杀菌剂的回收率 Fig. 1 Recoveries of three fungicides under different cleaning conditions |
在电喷雾离子源电离模式下,以流动注射方式分别对吡唑醚菌酯、腈苯唑和烯唑醇的单一标准溶液进行母离子全扫描,再对各自的子离子进行全扫描,每个化合物选择两对响应值高的特征离子对作为定量及定性离子对,并进行MRM参数的优化,优化结果见表 2。在1.4节的色谱条件下,以甲醇和1 mmol/L乙酸铵水溶液作为流动相,吡唑醚菌酯、腈苯唑和烯唑醇可获得较好的分离度及较高的响应值。图 2为标准溶液(质量浓度为100 ng/mL)的总提取离子色谱图。
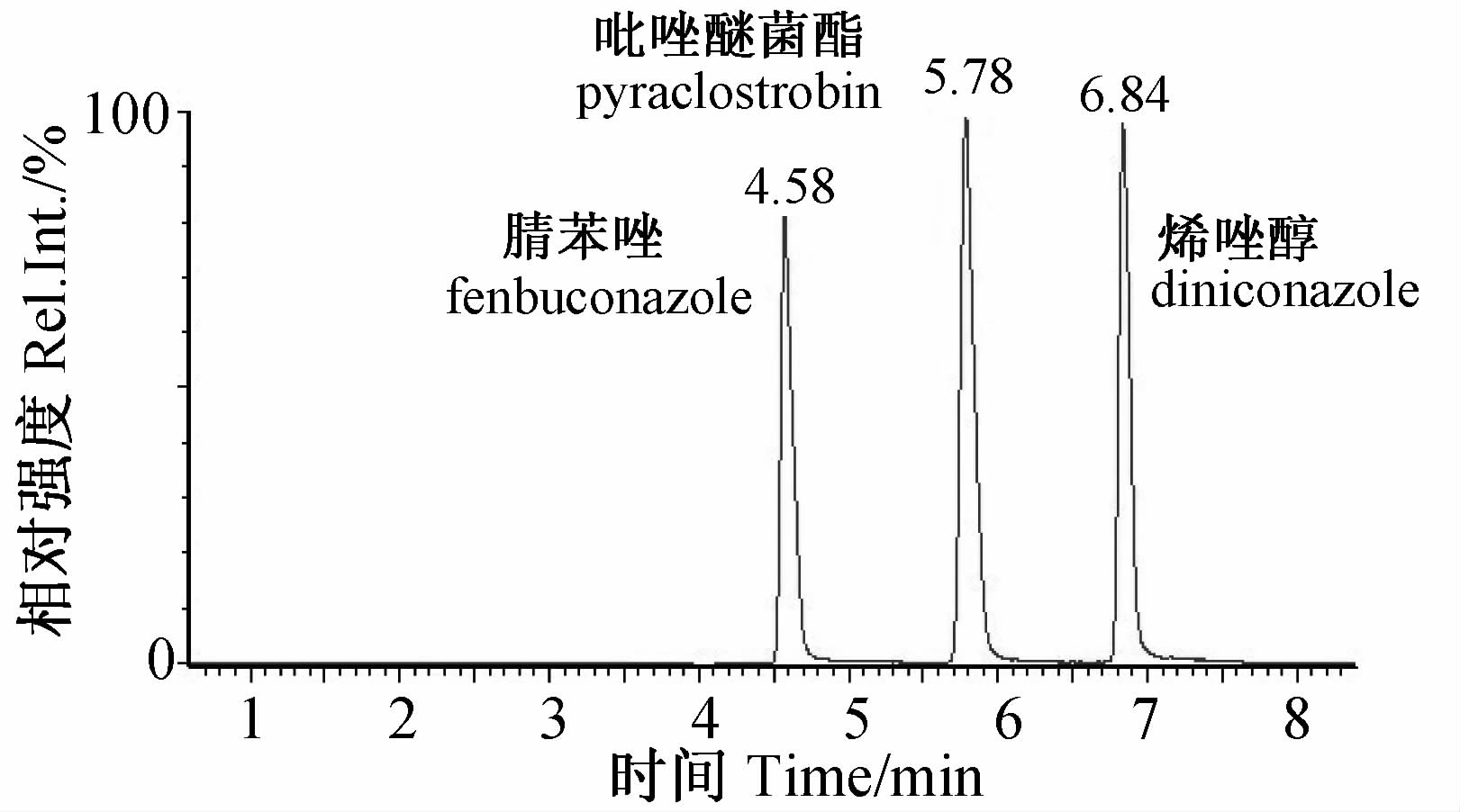 | 图 2 标准溶液的总提取离子色谱图 Fig. 2 Total ion chromatograms of the standard solution |
取1.3.2节中配制的基质匹配标准溶液按1.4节的方法测定,绘制标准曲线。结果(表 3)表明:在5.00 ~ 500 ng/mL 范围内,以仪器响应峰面积对各目标药剂的质量浓度进行线性回归,发现吡唑醚菌酯、腈苯唑和烯唑醇均呈良好线性关系。方法中吡唑醚菌酯、腈苯唑和烯唑醇的检出限(LOD,S/N=3)分别为0.2、0.6和0.3 μg/kg,定量限(LOQ)分别为0.5、1.0和0.5 μg/kg。
|
|
表 3 3种杀菌剂的线性方程、相关系数和线性范围 Table 3 The linear equations,correlation coefficient and linear range for three fungicides |
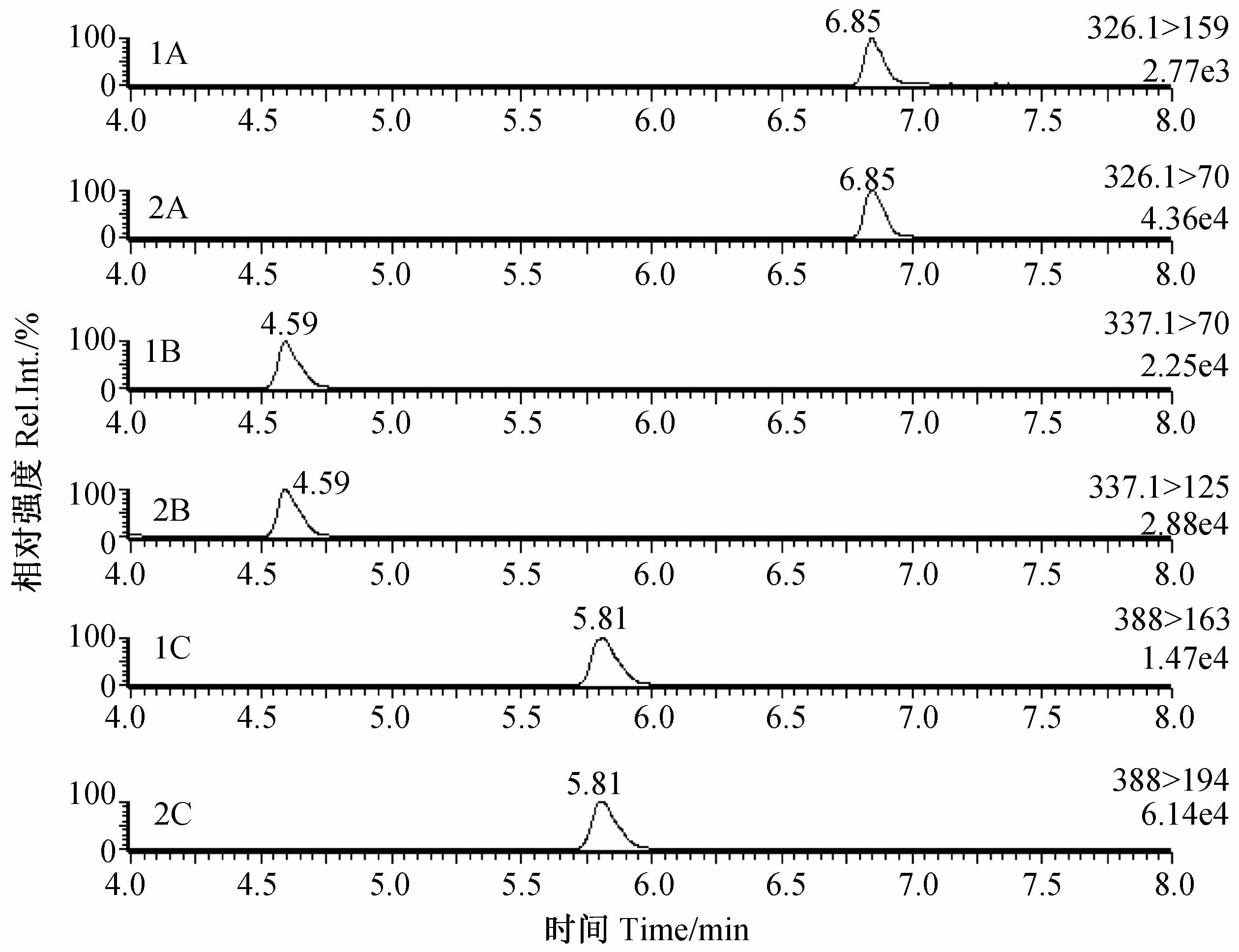
取空白芒果样品,在0.50(腈苯唑为1.0)、2.5、5.0、50 μg/kg 4个添加水平下,按1.2节的方法进行前处理,平行测定5次。结果(表 4)显示:平均添加回收率在70%~105%之间,相对标准偏差(RSD)在0.90% ~ 4.6% 之间,符合方法学要求[19]。图 3为在0.5 μg/kg(腈苯唑为1.0 μg/kg)添加水平下的MRM谱图。
|
|
表 4 样品添加回收率及相对标准偏差(n=5) Table 4 Recovery and relative standard deviation of the method(n=5) |
|
1:定性离子对;2:定量离子对。
A:烯唑醇;B:腈苯唑;C:吡唑醚菌酯。
1: qualitative ion pair; 2:quantitative ion pair. A: diniconazole; B: fenbuconazole; C: pyraclostrobin. 图 3 多反应监测模式下样品添加(吡唑醚菌酯和烯唑醇 为0.5 μg/kg,腈苯唑为1.0 μg/kg)的选择离子色谱图 Fig. 3 Selected ion chromatogram of the spiked sample (spiked level: pyraclostrobin and diniconazole 0.5 μg/kg; fenbuconazole 1.0 μg/kg) under multiple reaction monitoring (MRM) mode |
结果(表 5)表明:在5.00 ~ 100 ng/mL范围内,吡唑醚菌酯的基质效应小于10%,对结果影响较小,可以忽略。腈苯唑和烯唑醇的基质效应在10.1%~30.2%之间,对结果影响较大,需要使用基质标准曲线进行校准。
|
|
表 5 3种杀菌剂在芒果提取液中的基质效应 Table 5 Matrix effects of three fungicides in mango extraction |
在我国芒果中,有注册登记并制定了最大残留限量标准的农药仅有8种,但实际在芒果树上使用的农药却很多。通过对热带水果质量安全普查发现,吡唑醚菌酯、腈苯唑和烯唑醇经常用于防治芒果炭疽病、叶斑病、黑星病、白粉病和霜霉病等,但目前只有吡唑醚菌酯进行了注册登记[6]。采用本研究建立的方法对采集于海口市南北水果批发市场的23份芒果样品进行检测,均未检出吡唑醚菌酯、腈苯唑和烯唑醇残留。
3 结论本研究建立了一种基于QuEChERS原理的前处理方法,结合UPLC-MS/MS的高分辨能力快速检测芒果中吡唑醚菌酯、腈苯唑和烯唑醇3种杀菌剂的残留量。试验优化了超高效液相色谱与质谱的采集参数,确定了吸附剂的种类及用量,并考察了3种杀菌剂的基质效应。方法学考察及实际样品测定证明该方法前处理简单、快速,操作简便易行,且准确度、灵敏度高,重复性好,检出限低,可用于同时检测芒果中吡唑醚菌酯的残留量。
| [1] | 李日旺, 黄国弟, 苏美花, 等. 我国芒果产业现状与发展策略[J]. 南方农业学报, 2013, 44(5):875-878. Li Riwang, Huang Guodi, Su Meihua, et al. Status and developmental strategies of mango industry in China[J]. J South Agric, 2013, 44(5):875-878(in Chinese) |
| [2] | 吴迪, 聂向云, 张希跃, 等. 土壤中吡唑醚菌酯的残留分析方法和消解动态研究[J]. 农药科学与管理, 2012, 33(7):25-28. Wu Di, Nie Xiangyun, Zhang Xiyue, et al. GC determination of pyraclostrobin residues in soil[J]. Pestic Sci Admin, 2012, 33(7):25-28(in Chinese) |
| [3] | 孙扬, 秦旭, 秦冬梅, 等. 水稻中腈苯唑残留量的气相色谱分析[J]. 农药, 2009, 48(11):827-828. Sun Yang, Qin Xu, Qin Dongmei, et al. Analysis of fenbuconazole in rice by GC[J]. Agrochemicals, 2009, 48(11):827-828(in Chinese) |
| [4] | 王文博, 邬元娟, 陈子雷, 等. 气相色谱法测定土壤中腈苯唑残留及其代谢产物[J]. 农药, 2009, 48(1):44-46. Wang Wenbo, Wu Yuanjuan, Chen Zilei, et al. The determination of fenbuconazole residue and metabolize production in soil by GC[J]. Agrochemicals, 2009, 48(1):44-46(in Chinese) |
| [5] | 王卉, 杨金川, 杨森, 等. 气相色谱-质谱法同时测定黄瓜中腈苯唑与联苯三唑醇的残留量[J]. 农药科学与管理, 2012, 33(7):29-33. Wang Hui, Yang Jinchuan, Yang Sen, et al. Simultaneous determination of fenbuconazole and bitertanoi residues in cucumber by gas chromatography-mass spectrometry[J]. Pestic Sci Admin, 2012, 33(7):29-33(in Chinese) |
| [6] | 邹冬梅, 吕岱竹, 王明月, 等. 我国芒果农药最大残留限量制定及农药残留现状分析[J]. 中国热带农业, 2012, 45(2):16-19. Zou Dongmei, Lv Daizhu, Wang Mingyue, et al. The maximum residue limits for pesticide and pesticide residues status of mango in China[J]. China Trop Agric, 2012, 45(2):16-19(in Chinese) |
| [7] | GB 2763-2014, 食品中农药残留最大限量[S]. 北京:中国标准出版社, 2014. GB 2763-2014, Maximum residue limits for pesticides in food[S]. Beijing:Standard Press of China, 2014.(in Chinese) |
| [8] | European Community. Commission Regulation(EC) No 149/2008 of 29 January 2008 Amending Regulation(EC) No 396/2005 of the European Parliament and of the Council by Establishing Annexes II, III and IV Setting Maximum Residue Levels for Products Covered by Annex I thereto[J]. Offic J Eur Union, 2008, 3(1):1-50. |
| [9] | Anastassiades M, Lehotay S J, Stajnbaher D, et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and "dispersive solid-phase extraction" for the determination of pesticide residues in produce[J]. J Aoac Int, 2003, 86(2):412-431. |
| [10] | Valverde A, Piedra L, Aguilera A, et al. Analysis and residue levels of forchlorfenuron(CPPU) in watermelons[J]. J Environ Sci Health B, 2007, 42(7):801-807. |
| [11] | 董静, 潘玉香, 朱莉萍, 等. 果蔬中54种农药残留的QuEChERS/GC-MS快速分析[J]. 分析测试学报, 2008, 27(1):66-69. Dong Jing, Pan Yuxiang, Zhu Liping, et al. Improvements and applications of the QuEChERS method in multi-residue analysis of 54 pesticides in vegetables and fruits[J]. J Instrum Anal, 2008, 27(1):66-69(in Chinese) |
| [12] | Nguyen T D, Yu J E, Lee D M, et al. A multiresidue method for the determination of 107 pesticides in cabbage and radish using QuEChERS sample preparation method and gas chromatography mass spectrometry[J]. Food Chem, 2008, 110(1):207-213. |
| [13] | Yang Gengliang, Liu Haiyan, Wang Manman, et al. Chromatographic characterization and solid-phase extraction on diniconazole-imprinted polymers stationary phase[J]. Rea Funct Polym, 2006, 66(5):579-583. |
| [14] | Esteve-Turrillas F A, Mercader J V, Agulló C, et al. Development of immunoaffinity columns for pyraclostrobin extraction from fruit juices and analysis by liquid chromatography with UV detection[J]. J Chromatogr A, 2011, 1218(30):4902-4909. |
| [15] | Li Yuanbo, Dong Fengshou, Liu Xingang, et al. Simultaneous enantioselective determination of fenbuconazole and its main metabolites in soil and water by chiral liquid chromatography/tandem mass spectrometry[J]. J Chromatogr A, 2011, 1218(38):6667-6674. |
| [16] | Jiang Xiaoxue, Shi Haiyan, Wu Ni, et al. Development of an enzyme-linked immunosorbent assay for diniconazole in agricultural samples[J]. Food Chem, 2011, 125(4):1385-1389. |
| [17] | Wang Huili, Chen Jinhui, Guo BaoYuan, et al. Enantioseletive bioaccumulation and metabolization of diniconazole in earthworms(Eisenia fetida) in an artificial soil[J]. Ecotox Environ Saf, 2014, 99:98-104. |
| [18] | 黄宝勇, 欧阳喜辉, 潘灿平. 色谱法测定农产品中农药残留时的基质效应[J]. 农药学学报, 2005, 7(4):299-305. Huang Baoyong, Ouyang xihui, Pan canping. Matrix effects in the analysis of pesticide residue in agroproducts by chromatographic methods[J]. Chin J Pestic Sci, 2005, 7(4):299-305(in Chinese) |
| [19] | NY/T 788-2004,农药残留试验准则[S]. 北京:中国农业出版社, 2004. NY/T 788-2004, Guideline on pesticide residue trials[S]. Beijing:China Agriculture Press, 2004.(in Chinese) |
 2015, Vol. 17
2015, Vol. 17


