2. 华中科技大学同济医学院药学院, 武汉 430030;
3. 江苏克胜集团股份有限公司, 江苏建湖 224700;
4. 华中科技大学同济医学院附属同济医院, 武汉 430030
2. Tongji School of Pharmacy, Huazhong University of Science and Technology, Wuhan 430030, China;
3. Jiangsu KWIN Group Co., Ltd., Jianhu 224700, Jiangsu Province, China;
4. Department of Pharmacy, Tongji Hospital of Tongji Medical College, Huazhong University of Science and Technology, Wuhan 430030, China
哌虫啶为我国自主研发的高效、低毒、广谱的新烟碱类杀虫剂,主要用于防治同翅目害虫,对稻飞虱的防效高于90%,对蔬菜蚜虫的防效达94%以上,明显优于己产生抗性的吡虫啉,可广泛用于果树、小麦、大豆、蔬菜、水稻和玉米等多种作物害虫的防治[1]。目前,有关该农药的合成、农业应用及残留分析等方面研究已较为深入[2, 3, 4, 5, 6],而关于其在机体内代谢、分布及排泄却鲜有研究报道。人类可能通过呼吸道吸入、皮肤接触或者食用含有该药剂残留的瓜果、蔬菜而摄入哌虫啶,因此,了解其在动物体内的吸收、分布及排泄过程对于阐明其毒性机制及研究解毒方案极为重要。本研究首次建立了血浆、组织、尿样及粪样中哌虫啶含量的分析方法,采用高效液相色谱-串联质谱技术(HPLC-MS/MS),通过测定单次灌胃给药后大鼠血浆、组织(心、肝、脾、肺、肾、脑、骨骼肌、脂肪)、粪便和尿液样品中哌虫啶的浓度,对该药剂在大鼠体内的代谢动力学进行了研究,以期阐明哌虫啶在大鼠体内的吸收、分布及代谢过程,为进一步的毒理学研究提供依据。
1 材料与方法 1.1 药剂及实验动物95.7%的哌虫啶(paichongding)原药,淡黄色粉末,批号20120719001,相对分子质量366.76,江苏克胜集团股份有限公司。内标物非索非那定(fexofenadine)原药,纯度99.6%,白色结晶状粉末,批号20120801,相对分子质量 538.13,湖北恒绿源科技有限公司。Sprague Dawley(SD)大鼠,8~9周龄,SPF级,由湖北省实验动物研究中心提供,动物生产许可证号:SCXK(鄂)2008—0005,动物质量合格证号:No.42000600002602,实验动物设施许可证号:SYXK(鄂)2012—0065。
1.2 主要仪器设备QTRAP 4500质谱仪,AB Sciex 公司;XB-C18色谱柱(50.0 mm×2.1 mm,5.00 μm),月旭Welch公司(中国);LC-20ADXR高效液相色谱泵,SIL-20ACXR自动进样器及CTO-20AC柱温箱,日本岛津公司。
1.3 液相色谱-质谱检测条件 1.3.1 色谱条件流动相A为含0.1%甲酸的水溶液,流动相B为乙腈,梯度洗脱程序见表 1;自动进样器清洗液为甲醇;柱温箱温度40 ℃;流速0.8 mL/min;色谱柱平衡状态时的柱压为11 MPa;自动进样器温度2~8 ℃;进样体积为5.0 μL。
|
|
表 1 流动相梯度洗脱程序 Table 1 Gradient program of mobile phase |
电喷雾离子源ESI+;多重反应监测(MRM)模式;喷雾电压4 500 V;涡旋离子喷雾温度600 ℃;用于监测哌虫啶的离子对为367.3/125.8(碰撞能量54 eV),监测内标非索非那定的离子对为502.5/466.2(碰撞能量39 eV)。
1.4 分组、给药及样本采集供试24只大鼠随机分为3个哌虫啶剂量组(100、400及750 mg/kg),每组8只,雌雄各半。将哌虫啶原药溶于0.5%羧甲基纤维素钠溶液中,分别配制成质量浓度为5、20 及75 mg/mL的混悬液,单次灌胃给药。分别于给药前、给药后15 min及0.5、1、2、4、8、24、48、72、96 h,以颈静脉采血法采集大约0.3 mL全血,取血浆检测其中哌虫啶的浓度。
另设750 mg/kg高剂量组,单次灌胃给药。设4个时间点分别采集大鼠各组织样品,每时间点雌雄各采集4只,共采样32只,其中于96 h时采集组织样品的大鼠同时用于尿液及粪便收集。分别于给药后0.5、2、24及96 h放血处死该高剂量组大鼠,采集其心、肺、肝、脾、肾、脑、骨骼肌及脂肪组织,制备组织匀浆,测定组织内哌虫啶的质量浓度。将96 h时处死组大鼠置于代谢笼内,分别于0~8、8~24、24~48、48~72及72~96 h各时间段采集给药后大鼠的尿样和粪样:尿样记录总体积,混合均匀后留取5 mL(不足5mL的则留取全部样品),置于冻存管内;粪样经干燥后称重,装入塑料瓶内;上述样品均于-80 ℃保存,待测。
1.5 生物样品测定方法 1.5.1 实验溶液配制哌虫啶标准储备液配制:精确称取两份适量的哌虫啶标准品,用甲醇配成质量浓度为2.50 mg/mL的储备液,其中一份用于配制校正标样,另一份用于配制质控样品(QC)。
非索非那定内标储备液配制:精确称取适量非索非那定原药,用甲醇配成质量浓度为0.50 mg/mL的内标储备液。
校正标样和质控样品溶液配制:将 2.50 mg/mL的哌虫啶标准储备液用体积分数为50%的甲醇-水溶液稀释,配制成系列质量浓度的工作溶液。
内标工作溶液配制:将0.50 mg/mL的非索非那定内标储备液用体积分数为50%的甲醇-水溶液进一步稀释,配制质量浓度为100 ng/mL 的内标工作溶液,用于大鼠血浆、组织中哌虫啶分布情况测定;配制200 ng/mL 的内标工作溶液,用于大鼠排泄试验样品(粪便和尿液)的测定。
含内标物纯溶液的配制:精密吸取哌虫啶标准储备液,用体积分数为50%的甲醇-水溶液稀释,配制成 哌虫啶 质量浓度分别为0.175和43.9 ng/mL的纯溶液,其内标物质量浓度均为0.585 ng/mL,用于基质效应检测。
所有实验溶液均于4 ℃下储存。
1.5.2 生物样品处理及检测取50.0 μL 大鼠血浆样品至2.00 mL 离心管中,加入25.0 μL、100 ng/mL的内标工作溶液,加入400 μL 乙腈以沉淀蛋白,涡旋混合5 min,于4 ℃、17 000×g下离心10 min。取上清液50.0 μL 置于96孔深孔板,加入450 μL体积分数为50%的甲醇-水溶液,涡旋混合5 min,待测。进样体积5.00 μL。
将大鼠各组织用生理盐水清洗干净,吸干水分,取适量组织(不超过4.00 g)放入50.0 mL聚丙烯锥形管中并称重。向该管中加入相当于各组织质量值9倍体积的V(乙腈)∶V(水)=20∶80的溶液,匀浆。取50.0 μL各组织(心、肝、脾、肺、肾、脑、骨骼肌、脂肪)匀浆样品溶液至2.00 mL 离心管中,加入25.0 μL 内标工作溶液(非索非那定质量浓度为100 ng/mL),再加入400 μL乙腈以沉淀蛋白,涡旋振荡5 min,17 000×g下离心10 min。取50.0 μL上清液置于96孔深孔板,加入450 μL 体积分数为50%的甲醇-水溶液,涡旋混合5min,待测。进样体积5.00 μL。
根据当日分析批次的标准曲线,计算给药后大鼠组织匀浆样品中哌虫啶的质量浓度,并根据组织称重结果计算哌虫啶的分布情况( μg/g组织)。
取大鼠排泄物(粪便匀浆液和尿液)样品50.0 μL 至 2.00 mL 离心管中,加入25.0 μL 内标工作溶液(非索非那定质量浓度为200 ng/mL),再加入800 μL乙酸乙酯进行萃取,涡旋振荡5 min,于 17 000×g下离心10 min。取上清液100 μL 置于96孔深孔板中,用氮气吹干,加入500 μL 体积分数为50%的甲醇-水溶液,涡旋混合5 min,待测。进样体积5.00 μL。
1.5.3 方法的建立及验证为确保分析结果的可靠性,对所建立的大鼠血浆中哌虫啶浓度测定方法进行了完整验证,对大鼠组织及粪便和尿液中哌虫啶浓度测定方法进行了部分验证[7]。定量线性范围5.00~5 000 ng/mL,质控样品质量浓度分别为5.00 ng/mL(定量下限,LLOQ)、15.0 ng/mL(低浓度质控样品,LQC)、255 ng/mL(中浓度质控样品,MQC)、3 750 ng/mL(高浓度质控样品,HQC)及25 000 ng/mL(稀释可靠性评价质控样品,DQC)。验证指标包括选择性、基质效应、标准曲线和定量范围、精密度和准确度、提取回收率及稳定性等。
1.6 数据统计分析根据所测得各样品中哌虫啶原药的浓度,采用WinNonlin 6.3 中的非房室模型计算药代动力学参数,通过SPSS Statistics 19分析雌、雄大鼠的药代动力学参数统计学差异。主要参数包括:t1/2(半衰期)、Ke(消除速率常数)、Cmax(峰浓度)、Tmax(达峰时间)、Vd(表观分布容积)、CL(清除率)、MRT(平均滞留时间)和 AUC(血浆浓度时间曲线下面积)。
2 结果与分析 2.1 方法验证结果 2.1.1 选择性通过对6 个不同个体来源大鼠空白血浆、组织匀浆、粪便匀浆和尿液样品的测定表明,受试物保留时间干扰峰低于定量下限样品中分析物响应值的20.0%;内标保留时间干扰峰均低于空白样品中内标响应值的5.0%;结果符合国家药典标准[8]。比较不加内标的定量上限样品、空白样品、混合来源的空白基质和试剂空白,以评价受试物和内标之间的相互干扰,结果表明:空白样品、混合来源的空白基质和试剂空白中受试物保留时间处的干扰峰均低于定量下限质控样品中受试物响应值的20.0%;不加内标的定量上限样品、混合来源的空白基质和试剂空白中内标保留时间处的干扰峰均低于空白样品中内标响应值的5.0%;结果符合国家药典标准[8]。相关图谱见图 1~图 5。
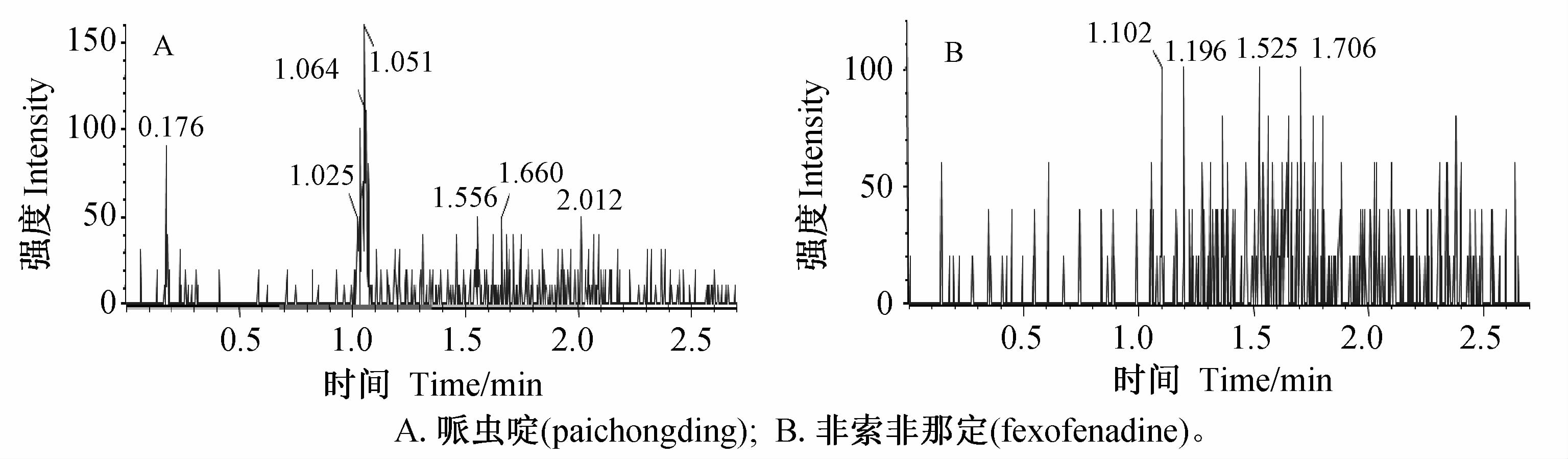 | 图 1 代表性空白大鼠血浆样品的HPLC-MS/MS图(第4分析批11号样本) Fig. 1 Representative HPLC-MS/MS chromatogram of rat blank plasma sample(AG004,sample 11) |
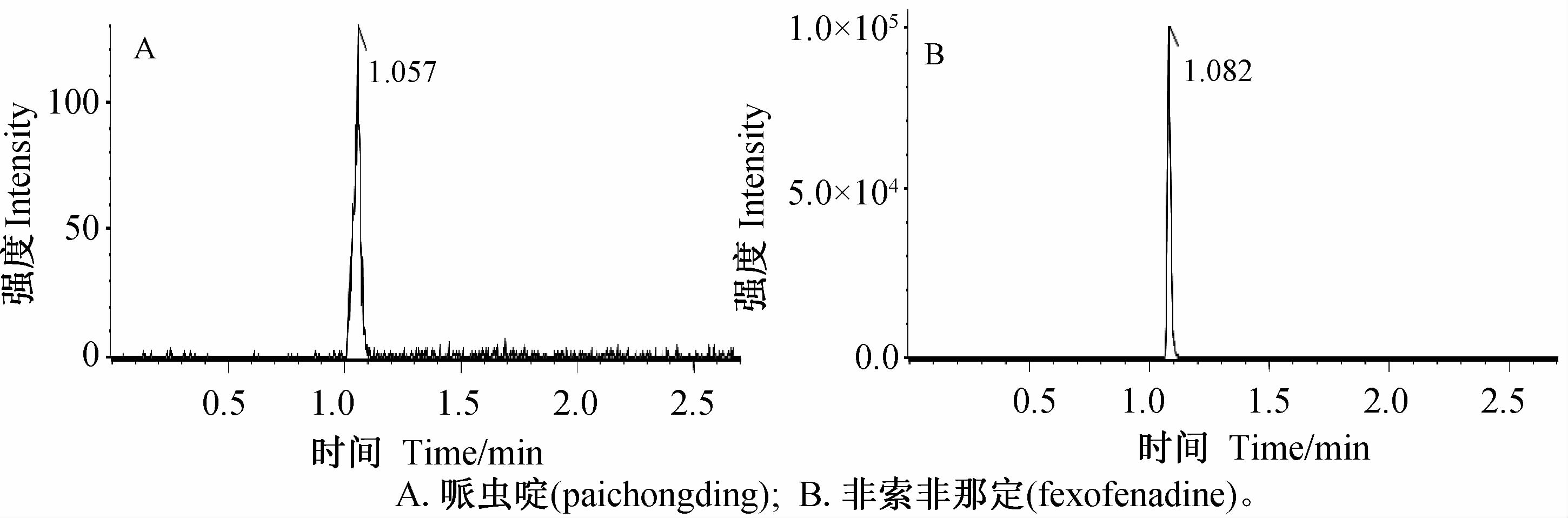 | 图 2 大鼠血浆定量下限样品的HPLC-MS/MS图(第4分析批15号样本) Fig. 2 HPLC-MS/MS chromatogram of LLOQ sample in rat plasma(AG004,sample 15) |
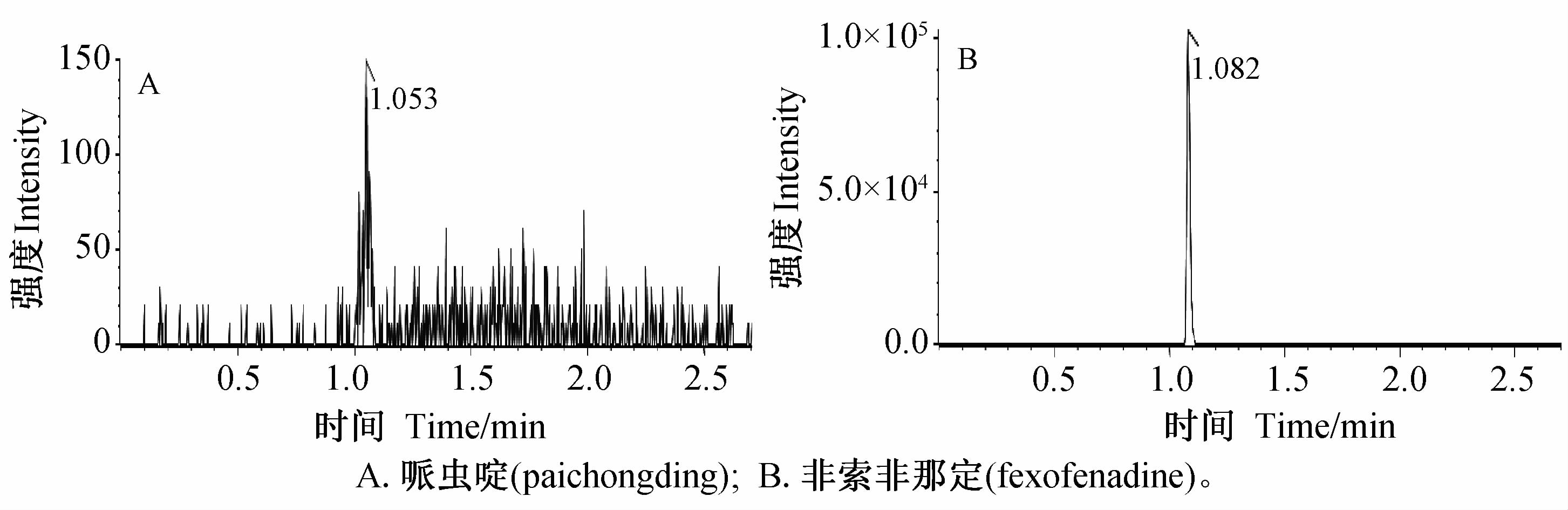 | 图 3 空白大鼠血浆样本的HPLC-MS/MS图(第4分析批44号样本) Fig. 3 HPLC-MS/MS chromatogram of zero concentration sample in rat blank plasma(AG004,sample 44) |
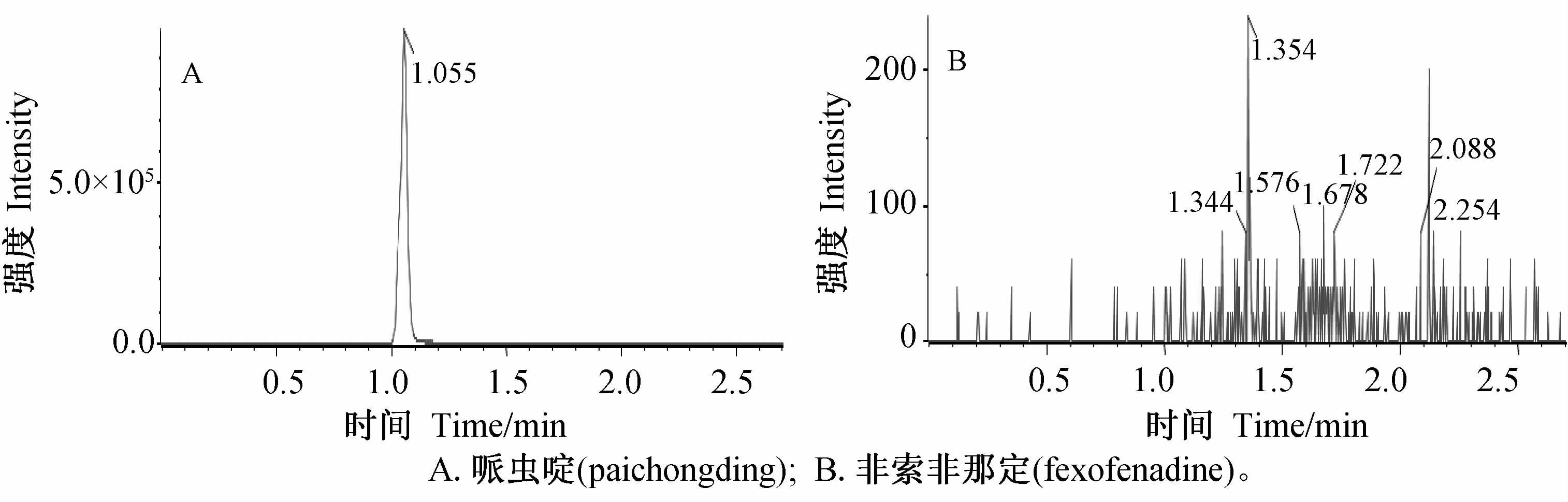 | 图 4 不加内标空白大鼠血浆定量上限样品的HPLC-MS/MS图(第4分析批45号样本) Fig. 4 HPLC-MS/MS chromatogram of ULOQ sample without internal standard in rat blank plasma(AG004,sample 45) |
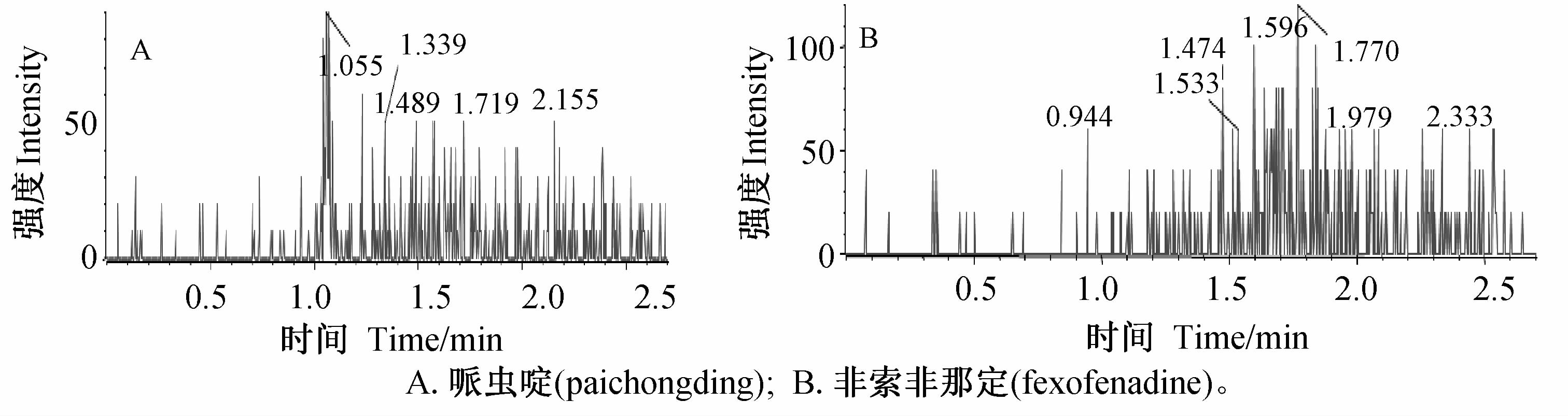 | 图 5 空白试剂样品的HPLC-MS/MS图 (第4分析批48号样本) Fig. 5 HPLC-MS/MS chromatogram of reagent blank sample(AG004,sample 48) |
分别测定了基质样品、纯溶液中分析物和内标的峰面积,并计算内标归一化的基质效应因子[9]。结果显示,待测物哌虫啶经内标归一化所得基质效应因子的相对标准偏差(RSD)均小于15.0%,表明大鼠空白血浆、组织匀浆、粪便匀浆和尿液基质均不影响对受试物的检测。
2.1.3 标准曲线和定量范围准确吸取哌虫啶标准工作溶液至各基质中,配制质量浓度分别为5.00、10.0、50.0、200、500、2 500、4 000和5 000 ng/mL的校正标样,按照1.3.2节条件进样测定。以分析物和内标的峰面积比(area ratio)为纵坐标,进样质量浓度(ng/mL)为横坐标,以1/(x2)为权重系数进行回归,得标准曲线。结果表明,在5.00~5 000 ng/mL范围内,分析物和内标的峰面积比与进样质量浓度之间线性关系良好(R2 >0.995),符合国家药典标准[8],证明该标准曲线适用于本研究的定量分析。
2.1.4 准确度及精密度根据批内及批间精密度和准确度评价分析方法的精密度和准确度,每浓度质控样品平行测定6次。结果显示:低、中、高浓度质控样品的批间及批内精密度相对标准偏差(RSD)均≤15.0%(LLOQ在±20.0%内),各浓度质控样品的准确度均值均在其标示值的±15.0%之内(LLOQ在±20.0%内),结果符合国家药典标准[8]。
2.1.5 提取回收率结果表明:针对血浆及组织匀浆,受试物哌虫啶在低、中、高3个浓度质控样品中的提取回收率为89.4%~117.4%,在尿液及粪便匀浆样品中的提取回收率为69.1%~84.3%,且各浓度质控样品提取回收率的波动均小于30.0%,结果符合要求。
2.1.6 稳定性测定结果显示:室温(25 ℃)下,全血样品中哌虫啶在2 h内可保持稳定,血浆、各组织匀浆、粪便匀浆及尿液样品中哌虫啶放置24 h内稳定;各基质中哌虫啶经冻融循环6次以内可保持稳定;哌虫啶在血浆基质中于-60 ℃至-80 ℃储存94 d内可保持稳定。
上述验证试验结果显示,本研究所建立的哌虫啶含量的HPLC-MS/MS分析方法灵敏有效,所得实验结果稳定可靠。
2.2 大鼠血浆中哌虫啶浓度及代谢动力学参数大鼠单次灌胃给予100、400及750 mg/kg哌虫啶后,其经时过程的血药浓度分别见图 6;采用WinNonlin 6.3中的非房室模型计算所得代谢动力学参数分别见表 2。由图 6可见,灌胃给予大鼠100、400及750 mg/kg哌虫啶后,约0.5 h即可达血浆峰浓度(除高剂量组雌性大鼠外),表明该药物吸收迅速。在上述受试剂量范围内,哌虫啶的平均半衰期为4~8 h,表观分布容积为10~30 L/kg。其血药浓度-时间曲线下面积(AUC)与剂量呈线性相关性,表明在100~750 mg/kg剂量范围内,该药在大鼠体内分布过程呈剂量依赖型药代动力学特征。采用SPSS Statistics 19软件对雌、雄大鼠的药代动力学参数进行单因素方差分析发现:低、中剂量下,哌虫啶原药的代谢动力学结果未显示性别差异;高剂量下,雌性大鼠的AUC明显增加,Tmax明显延长,与雄性动物差异显著,提示在此剂量下,哌虫啶在代谢及毒性效应上可能存在性别差异。
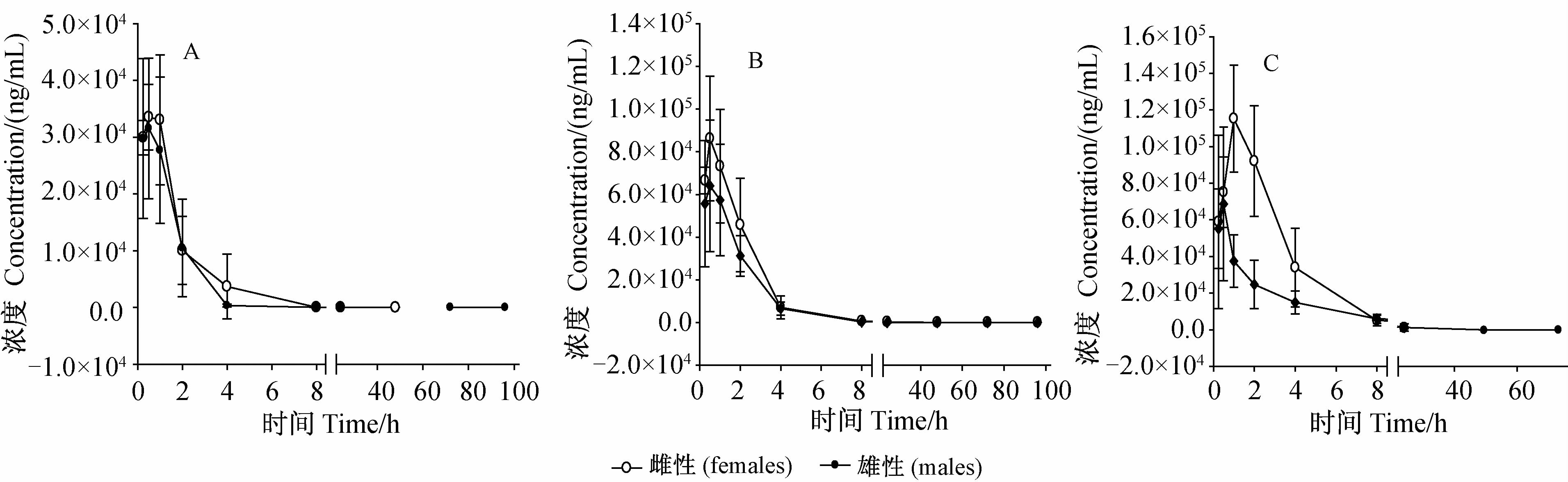 | 图 6 不同剂量哌虫啶对大鼠灌胃后的血药浓度-时间曲线 Fig. 6 Plasma concentration-time curve after oral gavage of paichongding at different dosages for rats |
|
|
表 2 大鼠灌胃给予不同浓度哌虫啶原药后的药代动力学参数(x±s,n=4) Table 2 The pharmacokinetics parameters of rats after a single oral dose with paichongding |
大鼠灌胃给予750 mg/kg哌虫啶原药后,经时过程各组织(心、肝、脾、肺、肾、脑、骨骼肌和脂肪)中哌虫啶的含量见图 7。试验表明:灌胃给药后,哌虫啶迅速向机体的各组织分布,0.5 h后在各组织中即达到峰值,峰值时各组织中哌虫啶含量由高到低依次为:肝脏>肾脏>肺>脾脏>心脏>骨骼肌>脑>脂肪;至给药后96 h,各组织中均未检测出哌虫啶;此外,哌虫啶在各组织中的分布未见明显性别差异。
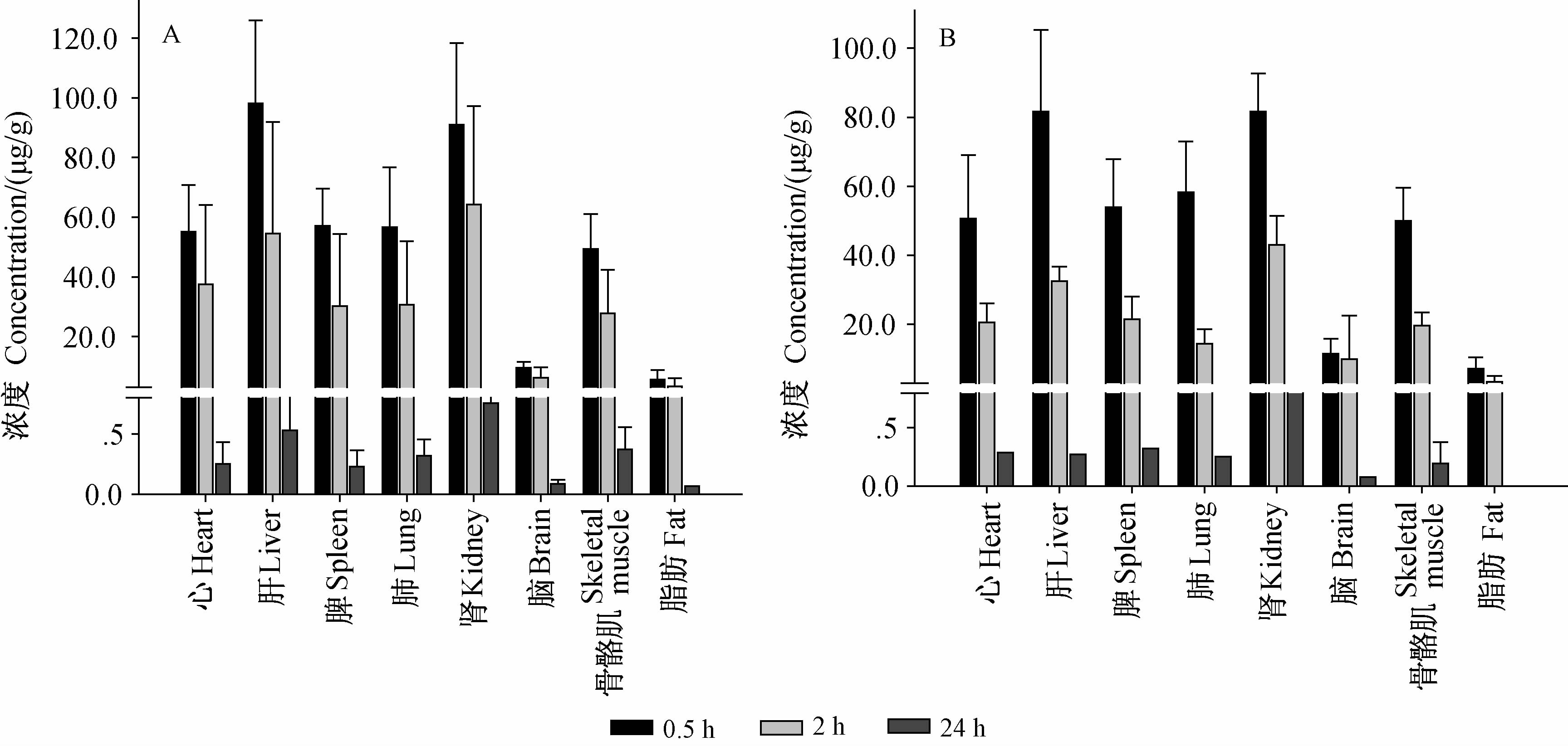 | 图 7 大鼠灌胃给予750 mg/kg哌虫啶原药后药剂在体内各组织中的分布 Fig. 7 Paichongding concentration in different tissues from rats |
粪便及尿液中哌虫啶的累积排泄率结果见图 8。灌胃给予750 mg/kg 哌虫啶原药后,其在大鼠尿液及粪便中均有检出,说明该药可经粪便及尿液排泄。给药后,哌虫啶在雄性和雌性大鼠粪便中的96 h累积排泄百分率(样品中哌虫啶含量×样品总体积/总摄入量×100%)分别为0.119%和0.170%;其在雄性和雌性大鼠尿液中的96 h累积排泄百分率分别为1.15%和2.12%。
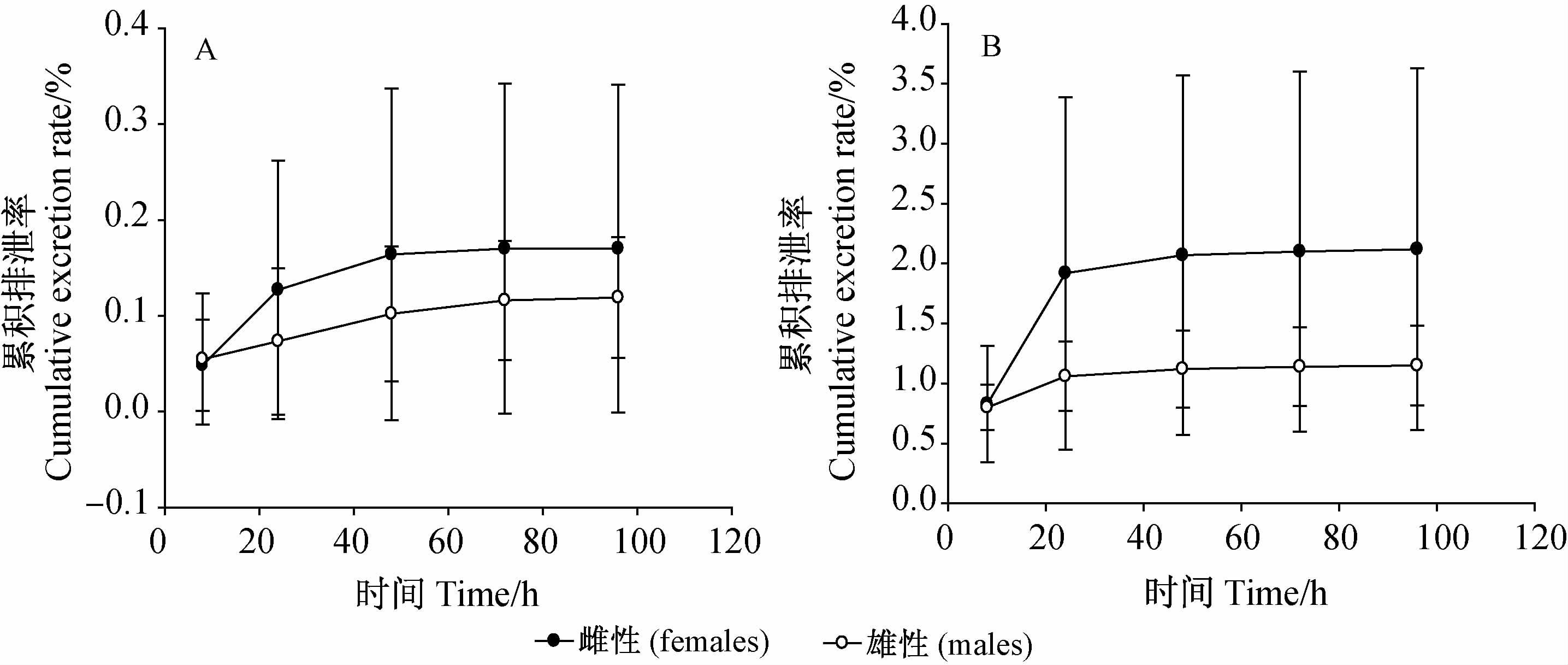 | 图 8 大鼠灌胃给予750 mg/kg 哌虫啶原药后药剂在粪便及尿液中的累积排泄率 Fig. 8 The cumulative excretion rate in feces and urine |
本研究采用新建立的HPLC-MS/MS 方法,分别测定了灌胃给药后哌虫啶在大鼠血浆、组织、粪便和尿液样品中的分布,该方法准确、灵敏、快速(分析时间小于3 min),较之前报道的HPLC分析方法[10]更为优越;大鼠血浆、组织、粪便和尿液中哌虫啶的定量下限均为5.00 ng/mL,线性范围均为5.00~5 000 ng/mL。经方法学验证,该方法符合生物样品定量分析指导原则要求,分析结果真实可靠。
大鼠体内代谢动力学试验结果显示:哌虫啶吸收迅速,给药后约0.5 h在各组织中即可达血药浓度峰值;其消除也较快,给药8 h后血药浓度即接近定量下限值。在100、400及750 mg/kg受试剂量范围内,SD雄鼠和雌鼠体内哌虫啶含量与AUC0-t及AUC0-inf 呈线性相关性(雄:r=0.996 4,雌:r=0.991 3),提示在该剂量范围内其药代动力学特征呈剂量依赖型。低、中剂量下,哌虫啶原药在雄性和雌性大鼠中的代谢动力学结果未显示出显著的性别差异;高剂量下,则雌、雄鼠之间AUC和Tmax值存在显著性差异,提示雌性动物可能对该农药更敏感。
经750 mg/kg剂量哌虫啶灌胃给药后,药物可快速向大鼠机体各组织分布,其中肝、肾中含量最高,心、脾、肺、骨骼肌次之,脑和脂肪中仅有少量分布。不同组织、器官中农药残留量的差异与各组织、器官在代谢中的功能及地位有关,其中肝和肾是动物体内代谢农药的主要器官[11],本研究测得肝、肾中哌虫啶的含量最高,与上述理论一致。排泄物样品测定结果显示,经尿液及粪便排泄的原形哌虫啶原药含量较低,提示哌虫啶原药在大鼠体内可能发生广泛的代谢后再排出体外。
在新烟碱类杀虫剂的生物代谢中,目前研究和报道较多的生物酶主要是细胞色素 P450酶系和醛氧化酶[12],参与哌虫啶同类产品吡虫啉代谢的酶主要为CYP3A4及醛氧化酶[13]。有关哌虫啶的具体代谢途径及参与的代谢酶还有待进一步研究证实,其可能的研究途径包括细胞色素P450酶系、微粒体、细胞液、S9、转基因细胞系、原代肝细胞、肝切片及灌流肝脏等体外代谢体系[14]。
| [1] | 徐晓勇, 邵旭升, 吴重言, 等. 新颖杀虫剂——哌虫啶[J]. 世界农药, 2009, 31(4):52. Xu Xiaoyong, Shao Xusheng, Wu Zhongyan, et al. Novel insecticide-paichongding[J]. World Pestic, 2009, 31(4):52(in Chinese) |
| [2] | 吴重言, 李忠, 吴伟, 等. 哌虫啶及其中间体新合成方法研究[J]. 现代农药, 2012, 11(6):7-11. Wu Zhongyan, Li Zhong, Wu Wei, et al. New synthesis methods of IPP and its intermediate[J]. Modern Agrochem, 2012, 11(6):7-11(in Chinese) |
| [3] | 邓为红, 户和亮, 刘剑青, 等. 不同药剂防治水稻白背飞虱药效试验[J]. 现代农业科技, 2012(3):202-203. Deng Weihong, Hu Heliang, Liu Jianqing, et al. The efficacy study of different pesticides in prevention of Sogatella furcifera[J]. Mod Agric Sci Technol, 2012(3):202-203(in Chinese) |
| [4] | 吴爱国, 吴重言, 孙长锋, 等. 哌虫啶悬浮剂对水稻白背飞虱的防治效果[J]. 植物保护, 2011, 37(4):176-177. Wu Aiguo, Wu Zhongyan, Sun Changfeng, et al. Control effects of Paichongding 10% SC on the white-backed planthoppers in rice fields[J]. Plant Prot, 2011, 37(4):176-177(in Chinese) |
| [5] | 丛路静, 刘纪松, 王美云, 等. 高效液相色谱法检测哌虫啶在稻田水、土壤、稻米和小麦粉中的残留[J]. 食品安全质量检测学报, 2014, 5(3):912-916. Cong Lujing, Liu Jisong, Wang Meiyun, et al. Determination of Paichongding in paddyfield water, soil, rice and wheat by high performance liquid chromatography[J]. J Food Saf Qual, 2014, 5(3):912-916(in Chinese) |
| [6] | Qin X W, Zhang R J, Zhang J, et al. Physiological efects of paichongding applied to rice on the Nilaparvata lugens(STÅL), the brown planthopper[J]. Arch Insect Biochem Physiol, 2014, 87(2):72-84. |
| [7] | U. S. Department of Health and Human Services. Guidance for industry analytical procedures and methods validation for drugs and biologics[EB/OL].(2015-07)[2015-08-20]. http://www.fda.gov/downloads/drugs/guidancecomplianceregulatoryinformation/guidances/ucm386366.pdf |
| [8] | 国家药典委员会. 9012 生物样品定量分析方法验证指导原则[M]//中华人民共和国药典,四部. 北京:中国医药科技出版社, 2015:363-368. National Pharmacopoeia Committee. 9012 Guidance for method validation for quantitative analysis of biological samples[M]//Pharmacopoeia of People's Republic of China, Part 4. Beijing:China Medical Science Press, 2015:363-368.(in Chinese) |
| [9] | 王鹏, 蒋学华, 王凌. LC-MSn应用于生物样品检测中基质效应的评价[J]. 中国新药杂志, 2011, 20(20):1953-1956. Wang Peng, Jiang Xuehua, Wang Ling. Assessment of matrix effect in quantitative bioanalytical methods based on LC-MSn[J]. Chin J New Drugs, 2011, 20(20):1953-1956(in Chinese) |
| [10] | 刘钰, 崔蕊蕊, 庄占兴, 等. 杀虫剂哌虫啶的高效液相色谱分析[J]. 山东化工, 2014, 43(11):110-112. Liu Yu, Cui Ruirui, Zhuang Zhanxing, et al. Determination of pestiside paichongding(IPP) by high performance liquid chromatograph[J]. Shandong Chem Ind, 2014, 43(11):110-112(in Chinese) |
| [11] | 吴慧明, 魏方林, 朱国念, 等. 螺虫乙酯在染毒雄性大鼠体内的分布与代谢[J]. 农药学学报, 2012, 14(4):417-422. Wu Huiming, Wei Fanglin, Zhu Guonian, et al. Study on distribution and metabolism of spirotetramat in rat[J]. Chin J Pestic Sci, 2012, 14(4):417-422(in Chinese) |
| [12] | 范银君, 史雪岩, 高希武. 新烟碱类杀虫剂吡虫啉和噻虫嗪的代谢研究进展[J]. 农药学学报, 2012, 14(6):587-596. Fan Yinjun, Shi Xueyan, Gao Xiwu. Research progresses on the metabolism of neonicotinoids imidacloprid and thiamethoxam[J]. Chin J Pestic Sci, 2012, 14(6):587-596(in Chinese) |
| [13] | Honda H, Tomizawa M, Casida J E. Neonicotinoid metabolic activation and inactivation established with coupled nicotinic receptor-CYP3A4 and-aldehyde oxidase systems[J]. Toxicol Lett, 2006, 161(2):108-114. |
| [14] | Faber H, Vogel M, Karst U. Electrochemistry/mass spectrometry as a tool in metabolism studies-a review[J]. Analytica Chimica Acta,2014, 834:9-21. |
 2015, Vol. 17
2015, Vol. 17


