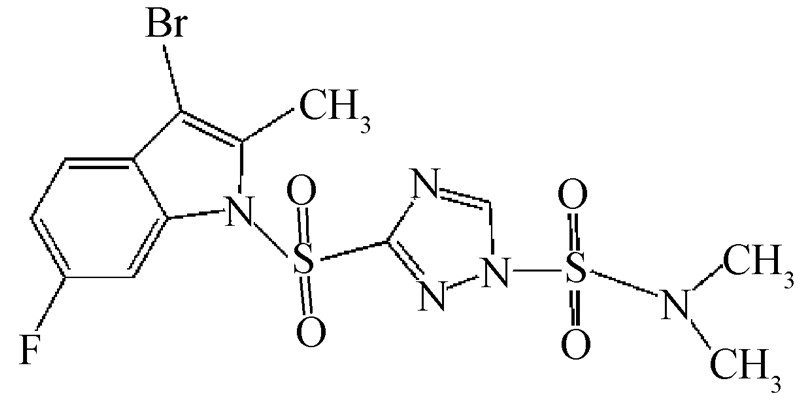
吲唑磺菌胺为日本日产化学公司创制的三唑磺酰胺类杀菌剂[1],化学名称为3-(3-溴-6-氟-2-甲基吲唑-1-基磺酰)-N,N-二甲基-1,2,4,-三唑-1-磺酰胺,分子式为C13H13BrFN5O4S2,相对分子质量466.3,其化学结构式见Scheme 1。
|
Scheme 1 |
吲唑磺菌胺对哺乳动物低毒,对非目标生物安全,具有良好的抗雨淋性[2],杀菌活性高,对黄瓜、葡萄霜霉病,马铃薯、番茄晚疫病以及辣椒疫病等均具有较好的防治效果[3, 4, 5, 6],对于防治由疫霉引起的烟草黑胫病有较广阔的应用前景[7]。
目前,国外对吲唑磺菌胺的残留检测已有报道,Lee等[8]建立了液相色谱-串联质谱(LC-MS/MS)法检测农作物中吲唑磺菌胺等56种农药残留的方法,但尚未见其在烟草上降解规律和残留特征的研究报道。QuEChERS是近年来发展起来的一种新型样品前处理技术[9, 10],可根据样品和目标化合物的特性,选择适合的提取溶剂和净化填料,具有快速、简单、廉价、有效、可靠、安全的特点,已广泛用于食品[11, 12, 13]和环境[14, 15, 16]样品中农药残留的分析研究。本研究建立了QuEChERS前处理与LC-MS/MS检测相结合的测定吲唑磺菌胺在烟草中残留量的方法,并采用所建方法研究了吲唑磺菌胺在烟叶中的残留消解动态和最终残留量,以期为吲唑磺菌胺在烟草上的合理使用准则与最大残留限量(MRL)标准的制定提供参考。
1 材料与方法 1.1 药剂、试剂与仪器99.0%吲唑磺菌胺(amisulbrom)标准品及50%吲唑磺菌胺水分散粒剂,均由日本日产化学工业株式会社提供。N-丙基乙二胺 (PSA),Agela Technologies 公司;甲醇为色谱纯,乙腈为色谱纯和分析纯,其余试剂及有机溶剂均为分析纯;所有用水均为蒸馏水。
Accela高效液相色谱仪和TSQ QUANTUM ULTRA 三重四极杆质谱仪 (美国Thermo公司);BSA323S型千分之一电子天平和BSA323型万分之一电子天平(瑞士Sartorius公司);T-25 basic ULTRA-TURRAX 高速植物组织捣碎机(德国IKA 公司);HYQ-3110涡旋混合振荡器(美国Crystal公司);3K15高速离心机(美国Sigma公司)。
1.2 田间试验田间试验分别于2013和2014年在山东青岛及四川西昌进行,供试烟草品种为中烟100(山东)和云烟87(四川),田间生产过程符合当地良好农业操作规程(GAP)生产要求。试验农药为50%吲唑磺菌胺水分散粒剂,防治对象为烟草黑胫病,推荐施药剂量为有效成分70~105 g/hm2,叶面喷雾,施药次数为3次。参照农业部《农药残留试验准则》[17]和《农药登记残留田间试验标准操作规程》[18],按照不同施药剂量和施药次数,设置4个最终残留量试验及1个消解动态试验,另设对照小区。每小区面积30 m2,重复3次,随机排列,小区间设保护带。
1.2.1 农药残留消解动态试验于烟草旺长后期施药,施药剂量为有效成分157.5 g/hm2,用水量900 L/hm2,叶面均匀喷雾。分别于施药后1 h及1、3、5、7、14、21、28、35和42 d,随机采集1 kg生长正常、无病害烟叶,切碎、混匀,四分法留样200 g,于-20 ℃保存,待测。
1.2.2 最终残留量试验以有效成分105 g/hm2和157.5 g/hm2两个剂量于旺长后期分别喷雾3和4次,用水量900 L/hm2,施药间隔期为7 d。分别于最后一次施药后7、14和21 d,随机采集烟叶样品不少于100片,经三段式烘烤工艺烘烤,粉碎、缩分后取200 g,于-20 ℃保存,待测。
1.3 分析方法 1.3.1 样品的提取与净化提取:称取鲜烟叶样品5.0 g(或干烟叶样品2.0 g,加2 mL蒸馏水,轻摇使样品润湿,静置5 min)于50 mL具盖离心管中,加入10 mL乙腈,涡旋1 min;加入4 g无水硫酸镁,1 g氯化钠,1 g柠檬酸钠和0.5 g柠檬酸氢二钠,立即涡旋2 min,然后在4 000 r/min条件下离心10 min,待净化。
净化:移取1.5 mL上清液置于盛有150 mg无水硫酸镁和25 mg PSA的 2 mL离心管中,涡旋2 min,在13 000 r/min 条件下离心5 min;吸取上清液500 μL,加入500 μL蒸馏水,经0.22 μ m有机相滤膜过滤,待测。
1.3.2 检测条件LC-MS/MS色谱条件:Thermo Hypersil GOLD C18色谱柱 (100 mm×2.1 mm,3.0 μm);流动相为甲醇-0.1%甲酸水,梯度洗脱程序见表 1。柱温25 ℃;进样量10 μL。
|
|
表 1 流动相梯度洗脱程序 Table 1 Gradient program of mobile phase |
质谱条件:电喷雾离子源ESI+;喷雾电压3 000 V;管透镜电压104 V;毛细管温度300 ℃;鞘气压力344.75 kPa;辅助气压力137.90 kPa;多重反应监测(MRM)模式;定性离子对495.96/147.98 (碰撞能量43 eV);定量离子对465.96/226.86 (碰撞能量19 eV)。
1.3.3 标准曲线绘制准确称取0.01 g吲唑磺菌胺标准品,用甲醇定容至100 mL,再用空白基质(鲜烟叶、干烟叶提取液)稀释配制质量浓度为0.001、0.005、0.01、0.05、0.1和0.5 mg/L的系列标准溶液,按1.3.2节的条件测定,重复3次。以进样质量浓度(mg/L)为横坐标、相应的峰面积为纵坐标,绘制标准曲线。
1.3.4 添加回收试验分别在空白鲜烟叶、干烟叶样品中添加0.01、0.1和10 mg/kg 3个水平的吲唑磺菌胺标准溶液,按1.3.1和1.3.2节的方法提取、净化和检测。每个水平重复5次,同时设空白对照。
2 结果与讨论 2.1 方法的线性范围及灵敏度在0.01~0.5 mg/L范围内,吲唑磺菌胺在不同基质中的峰面积(y)与质量浓度(x)间呈良好的线性关系,线性方程为y=9 512 210x+10 461,R2=0.998 3(鲜烟叶);y=10 970 475x+44 236,相关系数R2=0.998(干烟叶)。根据添加回收试验,在选定的样品前处理方法和检测条件下,吲唑磺菌胺在鲜烟叶和干烟叶中的定量限(LOQ)分别为0.01和0.02 mg/kg。
2.2 方法的准确度与精密度结果(表 2)表明:在0.01、0.1和10 mg/kg 3个添加水平下,吲唑磺菌胺在鲜烟叶中的平均回收率为88%~93%,相对标准偏差(RSD)为2.5%~13.9%;在干烟叶中的平均回收率为 93%~107%,RSD为6.7%~7.4%,均符合农药残留检测的要求[19],可用于实际样品的分析与检测。其典型色谱见图 1。
|
|
表 2 吲唑磺菌胺在鲜烟叶、干烟叶中的添加回收率及相对标准偏差 Table 2 Recoveries and RSD of amisulbrom in fresh tobacco leaves and cured tobacco leaves |
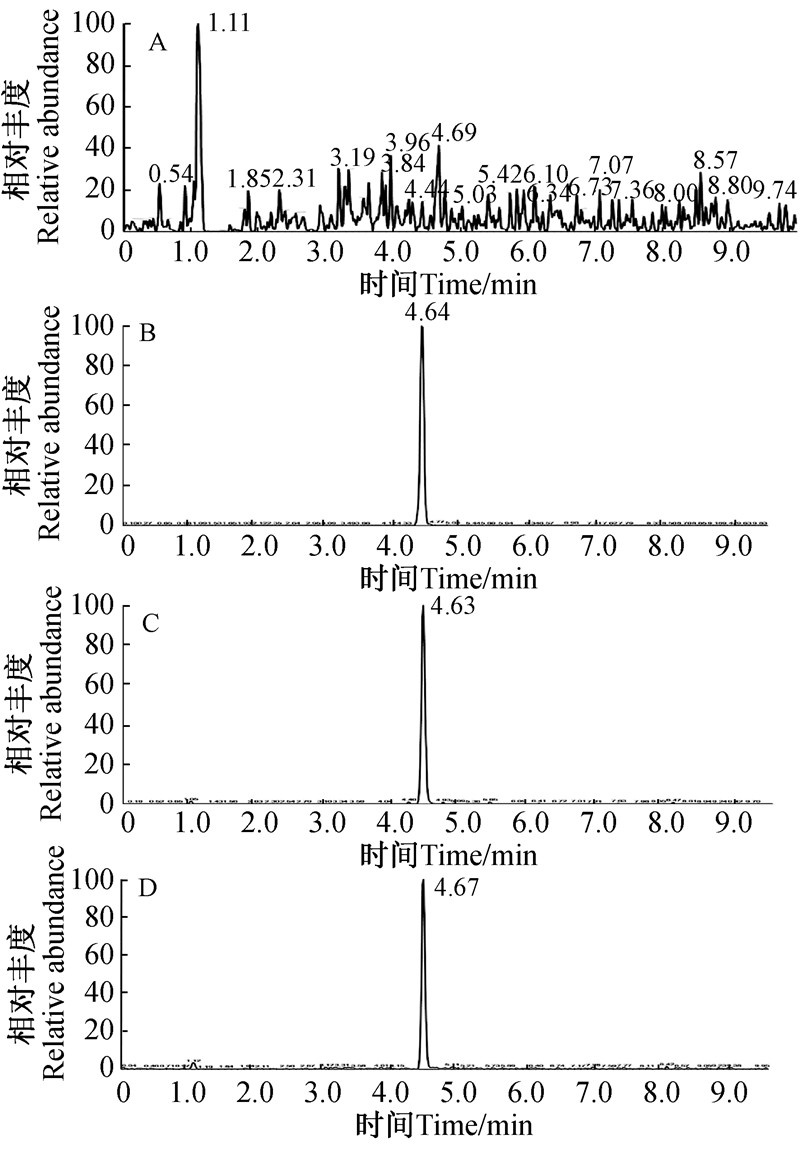 | 图 1 鲜烟叶空白(A),基质匹配标准溶液(0.1 mg/L)(B),鲜烟叶添加(0.1 mg/kg)(C),鲜烟叶样品(D) 典型色谱图(四川,21 d) Fig. 1 Chromatograms of (A) Blank fresh leaf,(B)Matrix matched standard of 0.1 mg/L,(C) Fresh tobacco leaf fortified at 0.1 mg/kg,and (D) Real fresh tobacco leaf sample (Sichuan Province,China,21 d) |
消解动态曲线见图 2,消解动力学方程见表 3。山东试验点,吲唑磺菌胺在烟叶中的原始沉积量为 5.85~7.66 mg/kg,3 d时消解率接近或超过50%,14 d时消解率接近或超过90%,理论半衰期为5.1~9.8 d。四川试验点,吲唑磺菌胺在烟叶中的原始沉积量为5.21~6.30 mg/kg,5 d时消解率超过50%,21 d时消解率超过90%,理论半衰期为7.0~8.4 d。
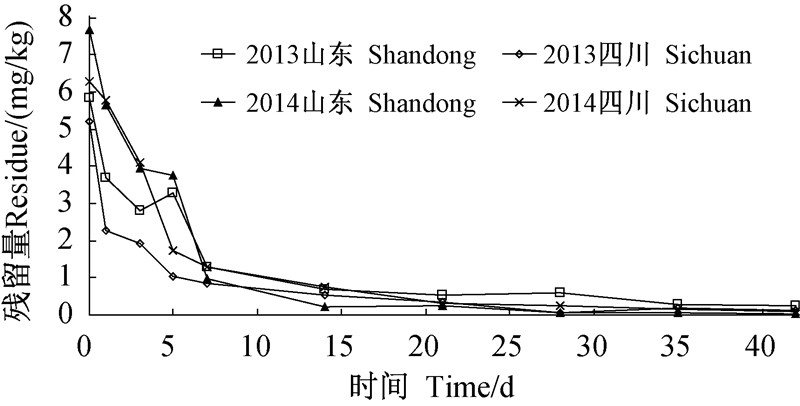 | 图 2 吲唑磺菌胺在鲜烟叶中的消解曲线 Fig. 2 Dissipation curves of amisulbrom in fresh tobacco leaves |
|
|
表 3 吲唑磺菌胺在鲜烟叶中的消解动力学方程及其相关系数 Table 3 Dissipation and correlation parameters of amisulbrom in fresh tobacco leaves |
山东、四川两年两地试验结果(见表 4)表明:距末次施药7 d后吲唑磺菌胺在烟草上的最终残留量<LOQ ~6.40 mg/kg;14 d后残留量<LOQ ~5.95 mg/kg;21 d后残留量<LOQ~6.37 mg/kg。由于我国和国际烟草合作研究中心都未制定吲唑磺菌胺在烟草上的最大残留限量(MRL)值,根据GAP农药残留试验数据和病害发病特征、发生时期,吲唑磺菌胺防治烟草黑胫病,在黑胫病发病初期用药,施药3次,每次间隔7~10 d,施药剂量为有效成分70~105 g/hm2[20]。用OECD农药残留限量计算器计算,7、14和21 d时MRL值均为9 mg/kg,因此建议吲唑磺菌胺在烟叶中残留限量为9 mg/kg,安全间隔期为14 d。
|
|
表 4 吲唑磺菌胺在干烟叶中的最终残留量 Table 4 The terminal residue of amisulbrom in cured tobacco leaves |
建立了采用液相色谱-串联质谱联用检测鲜烟叶及干烟叶中吲唑磺菌胺残留量的分析方法,其精密度、准确度及灵敏度均符合农药残留分析要求。该方法重现性好,前处理方法操作简单,且净化比较彻底,有机溶剂使用少,经济成本低。
山东、四川两年两地烟叶中的消解动态和最终残留试验结果表明:吲唑磺菌胺在烟叶中的残留消解均符合一级动力学方程,在烟叶中的半衰期为5.1~9.8 d,说明吲唑磺菌胺在烟叶中消解较快,属于易降解农药;距末次施药7 d后两年两地吲唑磺菌胺的最终残留量<LOQ ~6.40 mg/kg,建议吲唑磺菌胺在烟叶中残留限量为9 mg/kg,安全间隔期为14 d。
| [1] | 张亦冰. 新颖杀菌剂:amisulbrom[J]. 世界农药, 2009, 31(1): 54. Zhang Yibing. New fungicide:amisulbrom[J]. World Pestic, 2009, 31(1): 54. (in Chinese) |
| [2] | Honda T, Hasunuma N, Nishioka M. Amisulbrom (NC-224): Performance of new fungicide for potato late blight control[R]. PPO-Special Report No.12. Bologna, Italy: EuroBlight Workshop Nissan Chemical Industries, Ltd., 2007: 59-65. |
| [3] | 周振标, 谭耀华, 徐伟松. 新型杀菌剂吲唑磺菌胺对黄瓜霜霉病的防治效果研究[J]. 农药科学与管理, 2014, 35(9): 56-58. Zhou Zhenbiao, Tan Yaohua, Xu Weisong. Study on the control effect of a new fungicide amisulbrom against Pseudoperonospora cubensis[J]. Pestic Sci Admin, 2014, 35(9): 56-58. (in Chinese) |
| [4] | Diehl T, Busse C, Laux P. Canvas. A new product and active ingredient to control potato blight[J]. Kartoffelbau, 2009(6): 258-259. |
| [5] | Brunelli A, Gianati P, Berardi R, et al. Activity of new fungicides on grapevine downy mildew (Plasmopara viticola)[C]//Brunelli A. Giornate Fitopatologiche 2008, Cervia (RA), 12-14 marzo 2008, Volume 2. Università di Bologna, 2008: 283-290. |
| [6] | Davi R, Hasunuma N. Amisulbrom (Leimay©, Shinkon©), a new fungicide for downy mildew control on grape and vegetable crops[C]//Brunelli A. Giornate Fitopatologiche 2008, Cervia (RA), 12-14 marzo 2008, Volume 2. Università di Bologna, 2008: 129-134. |
| [7] | 王静, 孔凡玉. 烟草黑胫病综合防治技术[J]. 烟草科技, 2002(8): 45-47. Wang Jing, Kong Fanyu. The integrated managements of tabacco black shank[J]. Tob Sci Tech, 2002(8): 45-47. (in Chinese) |
| [8] | Lee H, Park S S, Lim M S, et al. Multiresidue analysis of pesticides in agricultural products by a liquid chromatography/tandem mass spectrometry based method[J]. Food Sci Biotechnol, 2013, 22(5): 1-12. |
| [9] | Schenck F J, Hobbs J E. Evaluation of the quick, easy, cheap, effective, rugged, and safe (QuEChERS) approach to pesticide residue analysis[J]. Bull Environ Contam Toxicol, 2004, 73(1): 24-30. |
| [10] | Anastassiades M, Lehotay S J, Štajnbaher D, et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and “dispersive solid-phase extraction” for the determination of pesticide residues in produce[J]. J AOAC Int, 2003, 86(2): 412-431. |
| [11] | Lehotay S J, Son K A, Kwon H, et al. Comparison of QuEChERS sample preparation methods for the analysis of pesticide residues in fruits and vegetables[J]. J Chromatogr A, 2010, 1217(16): 2548-2560. |
| [12] | Wilkowska A, Biziuk M. Determination of pesticide residues in food matrices using the QuEChERS methodology[J]. Food Chem, 2011, 125(3): 803-812. |
| [13] | Koesukwiwat U, Sanguankaew K, Leepipatpiboon N. Rapid determination of phenoxy acid residues in rice by modified QuEChERS extraction and liquid chromatography-tandem mass spectrometry[J]. Anal Chim Acta, 2008, 626(1): 10-20. |
| [14] | Brondi S H G, de Macedo A N, Vicente G H L, et al. Evaluation of the QuEChERS method and gas chromatography-mass spectrometry for the analysis pesticide residues in water and sediment[J]. Bull Environ Contam Toxicol, 2011, 86(1): 18-22. |
| [15] | Shi Chenhui, Gui Wenjun, Chen Jie, et al. Determination of oxadiargyl residues in environmental samples and rice samples[J]. Bull Environ Contam Toxicol, 2010, 84(2): 236-239. |
| [16] | Bragança I, Plácido A, Paíga P, et al. QuEChERS: a new sample preparation approach for the determination of ibuprofen and its metabolites in soils[J]. Sci Total Environ, 2012, 433: 281-289. |
| [17] | NY/T 788—2004, 农药残留试验准则[S]. 北京: 中国农业出版社, 2004. NY/T 788—2004, Guideline on pesticide residue trials[S]. Beijing: China Agriculture Press, 2004. (in Chinese) |
| [18] | 王运浩. 农药登记残留田间试验标准操作规程[M]. 北京: 中国标准出版社, 2007. Wang Yunhao. Standard Operating Procedures on Pesticide Registration Residue Field Trials[M]. Beijing: Standards Press of China, 2007. (in Chinese) |
| [19] | Zhao Pengyue, Wang Lei, Jiang Yaping, et al. Dispersive cleanup of acetonitrile extracts of tea samples by mixed multiwalled carbon nanotubes, primary secondary amine, and graphitized carbon black sorbents[J]. J Agric Food Chem, 2012, 60(16): 4026-4033. |
| [20] | The concept and implementation of agrochemical guidance residue level[S]. CORESTA Guidance No. 1, 2013. |
 2015, Vol. 17
2015, Vol. 17


