2. 浙江省农药检定管理所, 杭州 310004
2. Zhejiang Pesticide Verification Management, Hangzhou 310004, China
炭疽菌属(Colletotrichum spp.)真菌是一类广泛分布于热带、亚热带和温带地区,寄主繁多的植物病原菌,能引起草莓、葡萄、芒果、柑橘、玉米和高粱等农作物炭疽病的发生,造成严重的经济损失[1]。在2012年 Molecular Plant Pathology 杂志组织的投票中,根据科学意义和经济重要性,炭疽菌属病原菌已被推举为世界第八重要的植物病原真菌[2]。胶孢炭疽菌C.gloeosporioides是炭疽菌属内一个重要种,能够侵染470个属、逾1 000种植物[3, 4],引起草莓和葡萄炭疽病的病原菌即主要为胶孢炭疽菌[5, 6, 7]。草莓炭疽病尤以草莓育苗期和移栽存活期发病最重,危害部位以短缩茎、匍匐茎和叶柄为主;葡萄炭疽病可侵染当年生新枝、幼果、叶柄及卷须等组织,待葡萄近成熟期时则危害果实导致果实腐烂。
在草莓和葡萄炭疽病的防治中,目前主要以化学防治为主。20世纪90年代以多菌灵为代表的苯并咪唑类杀菌剂被广泛应用,在浙江葡萄和草莓中已经检测到普遍的高抗药性菌株[8, 9, 10]。因此,寻找新的与已有防治药剂无交互抗药性的杀菌剂用于炭疽病的防治及抗药性治理,是目前我国农业生产的迫切需要。
Qo抑制剂(QoIs)通过与真菌线粒体电子传递链中复合物Ⅲ Cytb的Qo位点结合,阻断电子传递,破坏能量的合成,从而抑制真菌生长或将病菌杀死[11]。该类药剂杀菌谱广、活性高、与环境生物相容性好,且与目前常用的杀菌剂无交互抗药性。由巴斯夫公司开发的吡唑醚菌酯是当前活性较高的QoIs类杀菌剂之一,但病原真菌对该类药剂产生抗药性的突变频率较高,高选择压下在自然界中易形成抗药性群体[12]。
植物病原菌对QoIs类杀菌剂产生抗药性的机理主要是病原菌Cytb基因DNA序列上的G143A、F129L和G137R氨基酸残基发生单点突变或旁路氧化途径被启动[12, 13, 14]。旁路氧化酶(alternative oxidase,AOX)是旁路氧化途径中一个关键的酶,在不同真菌中的表达情况不同,存在固有型和诱导型表达[11]。已有报道表明,旁路氧化途径能减弱病原菌对QoIs类杀菌剂的敏感性[13, 14, 15]。本课题组前期研究了葡萄炭疽病菌对吡唑醚菌酯及吡唑醚菌酯和旁路氧化途径抑制剂水杨肟酸(SHAM)共同作用时的敏感性,结果表明,其旁路氧化贡献值F(F=无SHAM存在时的EC50值/SHAM存在时的EC50值)的平均值为3.78,说明旁路氧化在葡萄炭疽病菌对吡唑醚菌酯的敏感性中可能具有重要作用[9]。金丽华[16]的研究表明,旁路氧化在辣椒炭疽病菌C.capsici 野生菌株中可以提供高达20~35倍的补偿作用,但延长醚菌酯的处理时间,辣椒炭疽病菌对药剂敏感性下降的机理并不是其AOX表达水平增强,而是与cytb的转录水平有关。虽然AOX的作用在高等植物等生物体中已经得到广泛研究[17],但目前对真菌AOX的研究仍很少。
本文拟通过测定草莓炭疽病菌群体对吡唑醚菌酯的敏感性及旁路氧化的贡献值,并结合实时荧光定量PCR(real-time PCR)技术,分析不同敏感性的胶孢炭疽菌在吡唑醚菌酯处理下其AOX基因表达的时间动态。本研究可为探明旁路氧化与胶孢炭疽菌对吡唑醚菌酯敏感性的关系提供依据,为以后的抗药性监测及病害防治提供重要指导。
1 材料与方法 1.1 供试菌株的采集与培养用于敏感性检测研究的65株草莓炭疽病菌C.gloeosporioides 分别采自浙江省临安市、建德市和诸暨市设施草莓上的炭疽病病样,采用组织分离法获得,观察纯化后菌株的培养特征,7 d后用无菌水洗下孢子,显微观察其形态特征。所有菌株于4 ℃下保存于马铃薯葡萄糖琼脂(PDA)斜面上。从本课题组分离得到的葡萄炭疽病菌[9]和草莓炭疽病菌中各随机选择4株对吡唑醚菌酯敏感性差异较大的菌株(分别为GT-32、JH-02、JH-10、GT-17和ZJ2-3、ZJE-3、JD2-2、HX2-10)用于AOX基因表达的研究。本研究所有敏感性测定均在PDA培养基上于25 ℃、黑暗中进行。
1.2 供试药剂及培养基250 g/L吡唑醚菌酯(pyraclostrobin)乳油(EC,制剂商品名:凯润),用无菌水配制成 5 000 μg/mL的母液,于4 ℃下保存,备用。
旁路氧化酶专化性抑制剂:99%水杨肟酸(salicylhydroxamic acid,SHAM)由美国Acros Organics公司生产,溶于丙酮配制成5 000 μg/mL 的母液,4 ℃下保存备用。
AEB培养基:酵母5 g、NaNO3 6 g、KH2PO4 1.5 g、KCl 0.5 g、MgSO4 0.25 g、甘油20 mL,加入去离子水至1 L。将每100 mL分装入锥形瓶中,放入高压灭菌锅中灭菌后,室温保存,备用。
PDA培养基:马铃薯200 g,葡萄糖20 g,琼脂20 g,以蒸馏水定容至1 000 mL。将每200 mL分装入锥形瓶中,放入高压灭菌锅中灭菌后,室温保存,备用。
1.3 主要试剂及仪器设备 小量真菌组织提取采用Total RNA试剂盒(MiniBEST Plant RNA Extraction Kit)及cDNA 合成试剂盒(PrimeScript®Ⅱ 1st strand cDNA Synthesis Kit),实时荧光定量PCR 专用试剂采用SYBR®Premix Ex TaqTMⅡ(Tli RNaseH plus)和 EASY Dilution(均为日本TaKaRa公司产品)。 CFX96TM实时荧光定量PCR仪(美国Bio-Rad公司);超微量蛋白核酸分析仪-柏精BioDrop uLite(英国BioDrop公司)。 1.4 供试菌株对吡唑醚菌酯、SHAM及吡唑醚菌酯+SHAM的敏感性测定 采用菌丝生长速率法[14]测定。将供试菌株在PDA平板上于25 ℃活化培养4 d,在同一圆周上制取直径0.5 cm的菌丝块,分别转移到含0、0.5、1、5和20 μg/mL系列质量浓度吡唑醚菌酯(同时含0或50 μg/mL SHAM )的PDA平板中央。分别以不含任何药剂和仅含50 μg/mL SHAM 者为对照(SHAM对照中含溶剂丙酮),每处理重复4次。培养5 d后测量各处理的菌落直径,取平均值计算抑制率(%)。利用DPS软件,通过药剂浓度对数值(x)与抑制率几率值(Y)之间的线性回归关系,求出毒力回归方程和EC50值。无SHAM时,求得的EC50值为EC50Q,当SHAM 质量浓度为50 μg/mL时,所得EC50值即为EC50(Q+S)。在供试草莓炭疽病菌群体(n=65)对吡唑醚菌酯和吡唑醚菌酯+SHAM的敏感性变化范围内,将EC50值分成不同的区间,统计每个区间出现的菌株个数和频率,以每个区间的EC50值为横坐标,频率为纵坐标,即得到病原菌群体对该种药剂的敏感性分布图。按公式(1)计算旁路氧化贡献值F[18, 19]。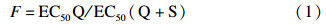
将来自不同寄主和不同敏感性的胶孢炭疽菌株(表 1)预培养4 d,于菌落边缘打取直径5 mm的新鲜菌碟,移入装有100 mL AEB液体培养基的 250 mL 三角瓶中摇培(25 ℃、120 r/min),每瓶6个菌碟,共60瓶。培养36 h后加入终浓度为5 μg/mL 的吡唑醚菌酯,同时设不含药剂对照,分别于2、6、12和48 h取样收集各瓶中的菌丝,每个菌每个取样时间点设3个重复。将收集的菌丝分别提取RNA,并用分光光度计测定浓度。RNA的提取方法按TaKaRa MiniBEST Plant RNA Extraction Kit 试剂盒说明书进行,用DNaseⅠ消化(TaKaRa)进行基因组DNA的去除。取等量各处理菌丝的总RNA(已进行质量控制检测),立即反转录成cDNA。cDNA的反转录方法按TaKaRa 提供的PrimeScriptTMⅡ 1st strand cDNA Synthesis Kit试剂盒说明书进行。
|
|
表 1 不同寄主中对吡唑醚菌酯敏感性存在差异的胶孢炭疽菌菌株 Table 1 Sensitivity of C.gloeosporioides to pyraclostrobin in different host plants |
特异性引物AOX-F:5′-CGAGGAGCACTTCCAGTACA-3′及AOX-R:5′-TGCTGGTCAAACGTCAACTC-3′,用于目标基因的荧光定量PCR;Tub-F:5′-GCTCACCCAGCAGATGTTC-3′及®Tub-R: ATCCTTCATAGCGACCTTGC-3′,用于参照基因的荧光定量PCR。采用Bio-Rad CFX96TM 定量PCR仪进行,每个PCR设置1次重复。反应体系包含SYBR®Premix Ex TaqTMⅡ(Tli RNaseH plus)(2×)12.5 μL,正反向引物各1 μL,各处理的cDNA模板2 μL,加水补足体积至25 μL。反应程序为:95 ℃ 30 s;95 ℃ 5 s,55 ℃ 30 s,72 ℃ 20 s,循环39次。设定于每个循环中的72 ℃、20 s时读取荧光值,最后添加溶解曲线(insert melt curve)分析程序。同时将未知浓度的cDNA稀释成系列浓度梯度进行PCR反应,用未知量样品相应稀释倍数的对数值对每个稀释样品的CT值绘制目标和参照基因的标准曲线,根据标准曲线的线性(R2>0.980)、扩增效率(90%~105%)及重复反应的一致性,判断定量PCR试验的最优化。
1.5.3 实时荧光定量PCR取各处理组样品,用EASY Dilution稀释10倍后,按1.5.2节所确定的反应程序进行实时荧光定量PCR检测。按公式(2)计算扩展效率E与标准曲线斜率的相关性。

理论上,在每个指数扩增循环中,PCR产物的量呈2倍增加,即反应效率为2,则优化的标准曲线斜率为-3.32。参照Bio-Rad荧光定量PCR应用指南,按公式(3)将扩增效率E转换成百分率,即每个循环扩增模板的百分比。
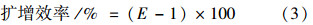
目前普遍采用操作简便的2-△△CT法进行相对基因表达分析,详细步骤见Bio-Rad荧光定量PCR应用指南,所得结果即是通过Tubulin基因表达水平校准的试验样品中AOX基因相对于标准样品(0 h 取样,0 μg/mL吡唑醚菌酯)增加或减少的倍数。
1.6 数据分析处理在Excel中分析、计算各菌株在吡唑醚菌酯各处理浓度下的抑制率,并应用DPS软件,以药剂浓度的对数值为横坐标、抑制率几率值为纵坐标作毒力回归曲线,求得各菌株的EC50值。应用IBM SPSS软件,通过LSD和Duncan法对相同时间不同菌株和同一菌株不同时间的AOX基因表达量进行多重比较方差分析。采用CFX Manager 软件分析目标基因和参照基因的标准曲线和溶解曲线。
2 结果与分析 2.1 SHAM对草莓炭疽病菌菌丝生长速率的影响结果(图 1)表明,50 μg/mL SHAM单独处理对不同菌株菌丝生长的影响不同:抑制率最低为-51.8%,最高为45.6%,平均抑制率为13.7%;对16.9%的菌株表现为促进生长作用,对1.5%的菌株的菌丝生长无影响,对81.5%的菌株表现出不同程度的抑制作用。该结果表明不同菌株中旁路氧化的情况存在较大差异。
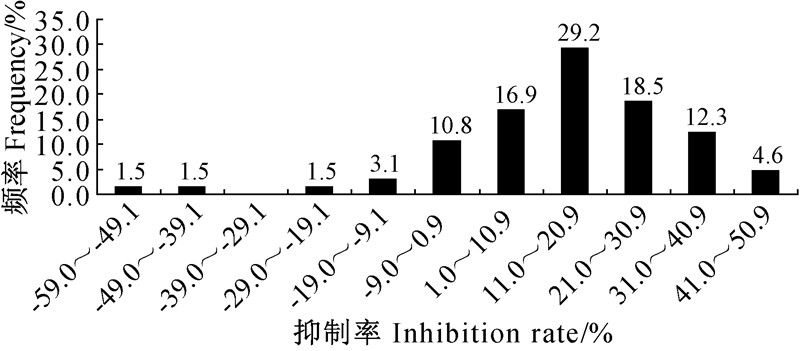 | 图 1 Effect of SHAM at 50 μg/mL on growth rate of C.gloeosporioides population (n=65) Fig. 1 50 μg/mL的水杨肟酸对草莓炭疽病菌群体(n=65)菌丝生长的影响 |
无SHAM 存在时,吡唑醚菌酯抑制草莓炭疽病菌菌丝生长的EC50Q值在0.09~24.26 μg/mL之间(图 2),平均为6.65 μg/mL。当体系中含有50 μg/mL的 SHAM时,吡唑醚菌酯对草莓炭疽病菌菌丝生长的抑制活性并未显著提高,其EC50(Q+S)值在0.06~48.98 μg/mL之间(图 3),平均为10.58 μg/mL。旁路氧化的相对贡献值F最低为0.02,最高为11.17,平均为0.96,其中78.46%的菌株的F值<1 (图 4)。上述研究进一步表明,旁路氧化在不同菌株中的情况差异较大。
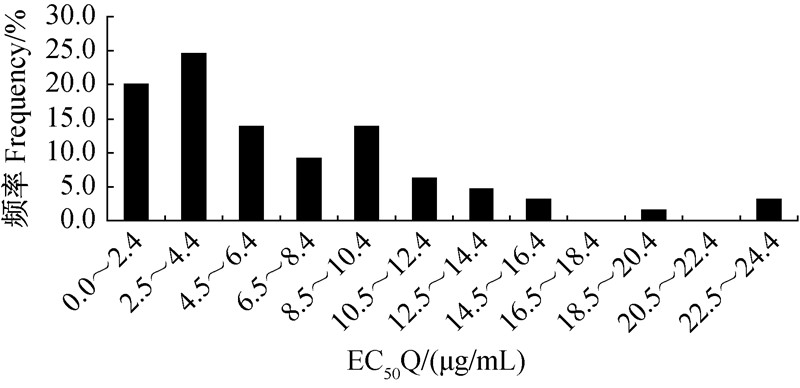 | 图 2 无SHAM存在时草莓炭疽病菌群体(n=65)对吡唑醚菌酯的敏感性 Fig. 2 Sensitivity of C.gloeosporioides population(n=65) to pyraclostrobin in the absence of SHAM |
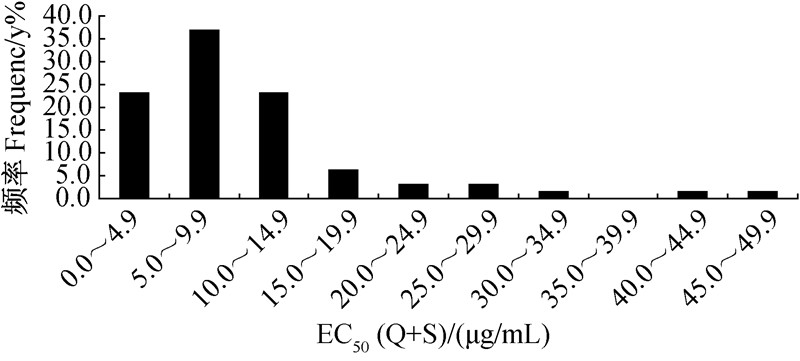 | 图 3 有50 μg/mL SHAM存在时草莓炭疽病菌群体(n=65)对吡唑醚菌酯的敏感性 Fig. 3 Sensitivity of C.gloeosporioides population (n=65) to pyraclostrobin in the presence of SHAM(50 μg/mL) |
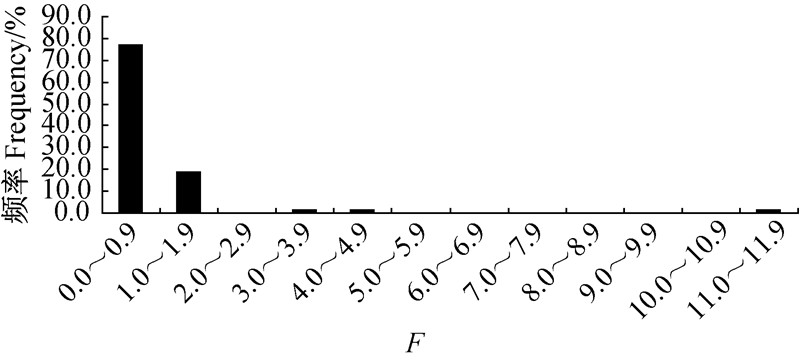 | 图 4 草莓炭疽病菌群体(n=65)对吡唑醚菌酯敏感性中旁路氧化的贡献值(F) Fig. 4 Contribution values F of alternative respiration in sensitivity of C.gloeosporioides population(n=65) to pyraclostrobin |
将未知浓度的cDNA样品稀释为系列浓度梯度,就基因AOX和Tubulin进行荧光定量PCR分析,以样品稀释倍数的对数值对每个稀释样品的CT值作图,发现两者呈递减的线性关系(图 5)。目标基因和参照基因标准曲线的斜率分别为-3.211 7和-3.213 3,两标准曲线的决定系数R2分别为0.987 2和0.986 9,保证了定量PCR反应的R2值>0.980,扩增效率均为104.8%,位于90%~105%高效率扩增范围内。图 6中目标基因和参照基因的溶解曲线均显示为单峰,表明PCR产物为单一产物。
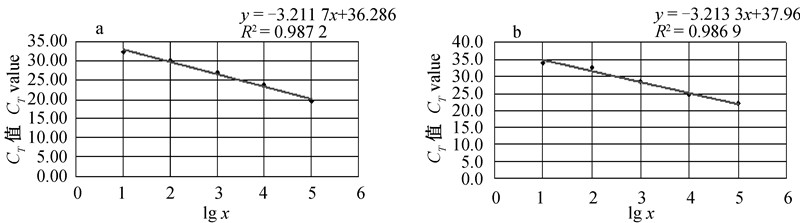 |
a:目标基因(AOX)的标准曲线;b:参照基因(Tubulin)的标准曲线。 a:Standard curve for target genes(AOX);b:Standard curve for refer genes(Tubulin). 图 5 cDNA样品系列稀释倍数对数值与CT值的标准曲线 Fig. 5 Standard curve between CT and cDNA templates with log gradient dilution multiple |
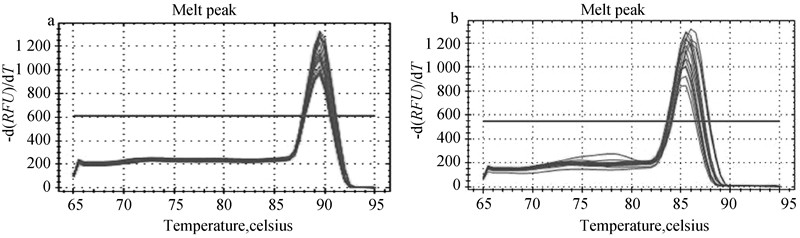 |
a:AOX基因的溶解曲线;b:Tubulin基因的溶解曲线。 a:Dissociation cure of AOX;b:Dissociation cure of Tubulin. 图 6 目标基因AOX和参照基因Tubulin的溶解曲线 Fig. 6 Dissociation curve for AOX and Tubulin |
分别取来自葡萄和草莓两个寄主中对吡唑醚菌酯敏感性差异较大的各4个胶孢炭疽菌菌株(表 1),采用2-△△CT法对目标基因AOX和参照基因Tubulin的相对表达量进行了分析,并分析了5 μg/mL 吡唑醚菌酯处理组胶孢炭疽菌菌丝AOX基因表达量在2、4、12和48 h时相对于校准样品(0 h,0 μg/mL吡唑醚菌酯)增加或减少的倍数(图 7)。PCR分析结果表明,除ZJE-3外,JD2-2和JH-10 AOX基因的表达均在处理12 h时表现出最显著性的增强,而其余菌株则均在6 h时表现为最显著增强。同时比较了同一时间不同菌株间AOX基因表达的差异显著性(P=0.05),结果表明,吡唑醚菌酯处理对不同菌株AOX基因表达的影响存在显著差异,但这种差异与菌株对吡唑醚菌酯的敏感性高、低之间无显著相关性(图 7)。
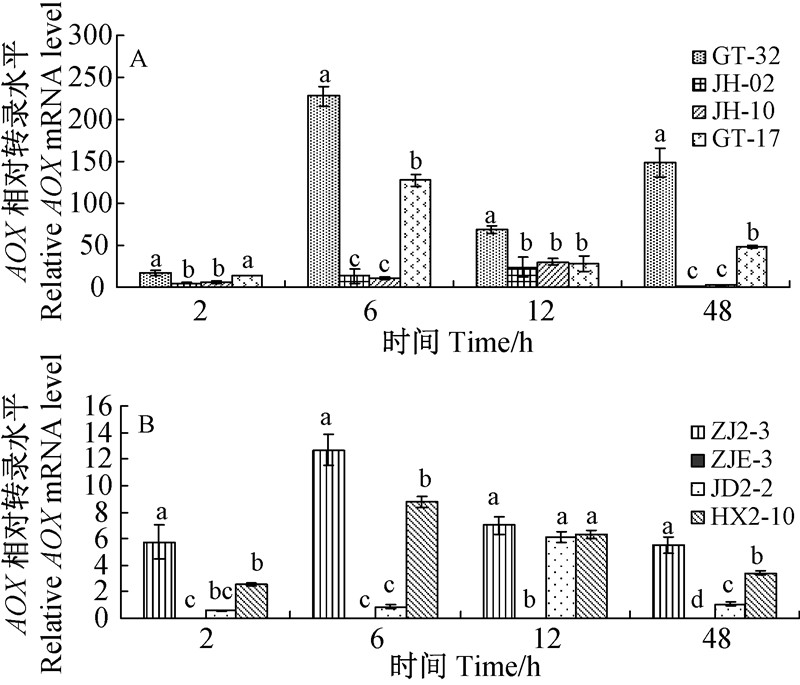 |
A.葡萄炭疽病菌;B.草莓炭疽病菌。A.Isolates from grape;B.Isolates from strawberry.注:数据经Duncan氏新复极差检验,不同字母表示0.05水平差异显著。
Note: Date were tested by Duncan′s multiple range test, the different letters indicated significant difference at 0.05 level. 图 7 吡唑醚菌酯处理不同时间下胶孢炭疽菌AOX基因的表达情况 Fig. 7 Effect of treatment for different time with pyraclostrobin on the transcript levels of alternative oxidase encoding gene, AOX, in mycelia of C.gloeosporioides isolates |
吡唑醚菌酯是一种重要的QoIs类杀菌剂,由于其高选择性及广谱、高效的抗菌活性等特点而使其在杀菌剂中占据了重要地位[20]。本研究结果表明,吡唑醚菌酯对草莓炭疽病菌具有较高的生物活性,有望取代苯并咪唑类等传统杀菌剂用于草莓炭疽病的防治。本研究检测了不同草莓炭疽病菌群体(n=65)对吡唑醚菌酯的敏感性,结果发现,无SHAM 存在时,吡唑醚菌酯抑制草莓炭疽病菌菌丝生长的EC50Q值位于0.09~24.26 μg/mL之间,且其敏感性呈连续性分布;当SHAM质量浓度为50 μg/mL 时,吡唑醚菌酯抑制草莓炭疽病菌菌丝生长的EC50(Q+S)值在0.06~48.98 μg/mL之间,且敏感性呈正态分布,表明该结果能反映出自然情况下病原菌对该杀菌剂的敏感性特征,因此其平均EC50值(10.58±9.27) μg/mL可作为草莓炭疽病菌对吡唑醚菌酯敏感性的参考值,用于后续的抗药性监测。本课题组前期报道了葡萄炭疽病菌对吡唑醚菌酯的敏感性范围在0.91~21.35 μg/mL,其平均EC50值为(4.78±3.72) μg/mL[9]。相比较而言,草莓炭疽病菌的敏感性分布更广。
已有研究表明,旁路氧化途径能降低一些真菌对QoIs药剂的敏感性。陈聃[9]报道,旁路氧化途径能减弱98%的葡萄胶孢炭疽菌菌丝对吡唑醚菌酯的敏感性,该结果与对稻瘟病菌Magnaporthe grisea[18]和灰葡萄孢菌 Botrytis cinerea[13]的研究报道一致。果蔬灰霉病菌中旁路氧化的相对贡献值(F)平均为3.19,其中32.4%的菌株的F值<1[14]。本研究结果表明:旁路氧化在来自不同寄主植物的同种病原菌对QoIs类杀菌剂敏感性中的作用也存在明显差异,虽然SHAM单独处理对81.5%的草莓炭疽病菌菌株表现出了不同程度的抑制作用,但是78.5%的菌株的F值<1,即存在SHAM时吡唑醚菌酯对草莓炭疽病菌菌丝生长的抑制活性反而低于无SHAM时,导致这一结果的原因还有待进一步研究分析。前期研究表明,葡萄炭疽病菌的平均F值为3.78,98%的菌株的F值>1[9];而草莓炭疽病菌的平均F值只有0.96,仅21%菌株的F值>1,其原因也有待进一步研究分析。
进一步采用实时荧光定量PCR方法,分析了处理48 h内胶孢炭疽菌AOX基因的表达情况。结果显示:吡唑醚菌酯处理能诱导胶孢炭疽菌AOX基因的表达,在处理6~12 h内,各菌株AOX基因的表达水平均出现了显著的增强,但AOX基因表达量差异与菌株对吡唑醚菌酯的敏感性之间并无显著的相关性。需要指出的是,由于AEB液体培养基较PDA培养基更不易产生污染,培养效果较好,真菌生长速度快,在各种真菌的液体培养中使用广泛,因此本研究中AOX基因表达分析时采用的培养基是AEB;而本课题组在前期研究葡萄炭疽病菌对吡唑醚菌酯的敏感性时采用的是PDA培养基,因此在草莓炭疽病菌对吡唑醚菌酯的敏感性研究中同样也采用了PDA培养基,以便于对不同寄主中胶孢炭疽菌的比较分析。关于PDA与AEB培养基对敏感性测定结果的影响以及ZJE-3菌株的表达特征等还有待进一步研究分析。
研究结果表明,草莓炭疽病菌对吡唑醚菌酯的敏感性可能还涉及某种未知的途径,菌体的旁路氧化能够抑制该途径激活,但一旦旁路氧化受阻则该途径可发挥较大的作用;当然,也可能是由于旁路氧化在草莓炭疽病菌菌丝生长对吡唑醚菌酯的敏感性中不起关键作用。具体还需进一步研究确定。金丽华[16]也曾报道,延长嘧菌酯对辣椒炭疽病菌的处理时间,则嘧菌酯对菌丝呼吸耗氧的抑制作用将丧失,其原因并非由旁路氧化作用引起,而是存在其他机制。早期的观点认为,由于植物中存在天然的旁路氧化酶抑制剂,因此旁路氧化在离体条件下真菌对QoIs的敏感性中具有一定作用,但在植株活体条件下影响则不大[15, 18, 19, 21]。而Avila-Adame等的研究表明,敲除AOX基因对稻瘟病菌的致病力并无明显影响,但会显著降低植株活体条件下稻瘟病菌对QoIs的抵抗能力[22]。这也证明了病原真菌中的旁路氧化情况是非常复杂的。因此,研究旁路氧化在某一病原菌对杀菌剂敏感性中的作用以及杀菌剂对旁路氧化酶表达的诱导作用,可为QoIs的应用提供重要指导。
| [1] | Cannon P F,Buddie A G, Bridge P D.The typification of Colletotrichum gloeosporioides[J]. Mycotaxon, 2008,104:189-204. |
| [2] | Dean R, Kan J A L V, Pretorius Z A, et al. The top 10 fungal pathogens in molecular plant pathology[J]. Mol Plant Pathol, 2012, 13(4):414-430. |
| [3] | Cannon P F, Damm U, Johnston P R, et al. Colletotrichum-current status and future directions[J]. Stud Mycol, 2012, 73(1):181-213. |
| [4] | Rampersad S N, Perez-Brito D, Torres-Calzada C, et al. Genetic structure and demographic history of Colletotrichum gloeosporioides sensu lato and C.truncatum isolates from Trinidad and Mexico [J]. BMC Evol Biol, 2013,13:130. |
| [5] | 韩国兴. 杭州地区草莓炭疽病病原鉴定及防治研究[D]. 杭州:浙江大学, 2009. Han Guoxing. Etiology of anthracnose of strawberry in Hangzhou and its management [D]. Hangzhou: Zhejiang University, 2009. (in Chinese) |
| [6] | 任海英,蒋桂华,方丽,等.浙江省草莓炭疽病菌鉴定及生物学特性研究[J].浙江农业学报,2011,23(5):937-941. Ren Haiying, Jiang Guihua, Fang Li, et al. Identification and characterization of the pathogen of strawberry anthracnose in Zhejiang province[J]. Acta Agriculturae Zhejiangensis, 2011,23(5):937-941. (in Chinese) |
| [7] | Suzaki K. Improved method to induce sporulation of Colletotrichum gloeosporioides, causal fungus of grape ripe rot[J]. J Gen Plant Pathol, 2011, 77(2):81-84. |
| [8] | 韩国兴, 礼茜, 孙飞洲,等.杭州地区草莓炭疽病病原鉴定及其对多菌灵和乙霉威的抗药性[J].浙江农业科学, 2009(6):1169-1172. Han Guoxing, Li Qian, Sun Feizhou, et al. Etiology of anthracnose of strawberry in Hangzhou and its resistance for carbendazim and diethofencarb[J].J Zhejiang Agric Sci, 2009(6):1169-1172. (in Chinese) |
| [9] | 陈聃.葡萄炭疽病菌的抗药性检测和治理研究[D]. 临安:浙江农林大学,2013. CHEN dan. Resistance detection and management of grape ripe rot causing by Colletotrichum gloeosporioides[D].Lin'an: Zhejiang Agriculture and Forest University, 2013. (in Chinese) |
| [10] | 叶佳,张传清.葡萄炭疽病菌对甲基硫菌灵、戊唑醇和醚菌酯的敏感性检测[J].农药学学报,2012,14(1):111-114. Ye Jia, Zhang Chuanqing. Detection of sensitivity of grape anthracnose to thiophanate methyl,tebuconazole and kresoxim-methyl[J]. Chin J Pestic Sci, 2012,14(1):111-114.(in Chinese) |
| [11] | 徐汉虹. 植物化学保护学[M]. 北京: 中国农业出版社,2007:157-158. Xu Hanhong. Chemical Protection of Plants[M]. Beijing: China Agricultural Press, 2007:157-158. |
| [12] | 贾俊超, 马琳, 范志金, 等. 病原菌对Strobilurin类杀菌剂抗药性机理的研究进展[J]. 农药学学报, 2008, 10(1):1-9. Jia Junchao, Ma Lin, Fan Zhijin, et al. Progress on study of resistance mechanism of strobilurin fungicides[J]. Chin J Pestic Sci, 2008,10(1):1-9. (in Chinese) |
| [13] | Banno S, Yamashita K, Fukumori F, et al. Characterization of QoI resistance in Botrytis cinerea and identification of two types of mitochondrial cytochromeb gene[J]. Plant Pathol, 2009,58(1):120-129. |
| [14] | 张雅,李红叶,张传清,等.旁路氧化与设施蔬菜灰葡萄孢霉菌菌丝生长对嘧菌酯敏感性的关系[J].农药学学报,2006,8(4):306-312. Zhang Ya, Li Hongye, Zhang Chuanqing, et al. Relationship between alternative respiration and sensitivity of growth rate in Botrytis cinerea collected from vegetable greenhouses to azoxystrobin[J].Chin J Pestic Sci, 2006,8(4):306-312. (in Chinese) |
| [15] | Wood P M, Hollomon D W. A critical evaluation of the role of alternative oxidase in the performance of strobilurin and related fungicides acting at the Qo site of complex Ⅲ[J]. Pest Manag Sci, 2003,59(5):499-511. |
| [16] | 金丽华. 嘧菌酯对辣椒炭疽菌(Colletotrichum capsici)的毒力及分子毒理学研究[D].南京:南京农业大学, 2007. Jin Lihua. Bioactivity and molecular toxicology of azoxystrobin against Colletotrichum capsici[D]. Nanjing:Nanjing Agricultural University, 2007. (in Chinese) |
| [17] | McDonald A E. Alternative oxidase: an inter-kingdom perspective on the function and regulation of this broadly distributed'cyanide-resistant'terminal oxidase [J].Funct Plant Biol, 2008,35(7):535-552. |
| [18] | Avila-Adame C, Köller W. Impact of alternative respiration and target-site mutations on responses of germinating conidia of Magnaporthe grisea to Qo-inhibiting fungicides[J]. Pest Manag Sci, 2003,59(3):303-309. |
| [19] | Ziogas B N, Baldwin B C, Young J E. Alternative respiration:a biochemical mechanism of resistance to azoxystrobin(ICIA 5504) in Septoria tritici [J]. Pestic Sci, 1997,50(1): 28-34. |
| [20] | 赵平,严秋旭,李新,等.甲氧基丙烯酸酯类杀菌剂的开发及抗性发展现状[J].农药, 2011, 50(8):547-551. Zhao Ping, Yan Qiuxu, Li Xin, et al. Current status of resistance and development of strobilurin fungicide[J]. Agrochemicals, 2011,50(8):547-551. (in Chinese) |
| [21] | Vanlerberghe G C, Mclntosh L. Alternative oxidase: from gene to function [J]. Annu Rev Plant Physiol Plant Mol Biol,1997,48:703-734. |
| [22] | Avila-Adame C, Köller W. Disruption of the alternative oxidase gene in Magnaporthe grisea and its impact on host infection[J]. MPMI, 2002,15(5):493-500. |
 2015, Vol. 17
2015, Vol. 17


