2. 河南农业大学 理学院, 郑州 450002;
3. 河南省烟草公司, 郑州 450002
2. College of Science, Henan Agricultural University, Zhengzhou 450002, China;
3. Tobacco Leaf Company of Henan Province, Zhengzhou 450002, China
壳寡糖(CS)是一种聚合度在3到10之间,交联度低于5%的低聚β-(1,4)-2-脱氧-2-氨基葡萄糖[1],可诱导植物产生防御反应[2]。研究表明,壳寡糖具有抗真菌[3]和抗病毒活性[4, 5]。对植物或接种过病毒的叶片喷施壳寡糖,可以防治由烟草坏死病毒(TNV)、烟草花叶病毒(TMV)、花生矮化病毒(PSV)、黄瓜花叶病毒(CMC)和马铃薯X病毒引起的植物局部或全身感染[6, 7]。席夫碱(Schiff base)是指由活性羰基和氨基通过缩水形成的含亚氨基或烷亚氨基的有机化合物,席夫碱衍生物及其金属络合物不仅是一种重要的化学分析试剂和有机合成中间体,还具有抗菌、灭菌等生物活性[8]。宋宝安等[9]研究表明,含不同取代基的席夫碱衍生物具有不同的抗TMV活性,其中取代基为2-氯-5-硝基的衍生物活性最强。孟凡德等[10]研究表明,水杨酸与L-氨基酸缩合形成席夫碱后,再与银形成配合物,对TMV具有很好的抑制作用。
烟草花叶病对烟田的危害十分严重,可造成烟草品质下降,等级降低,因此研究一种绿色有效的抗烟草花叶病的药剂十分重要。目前,国内外相继合成的壳寡糖席夫碱、壳寡糖烷基化衍生物的抗病效果明显提高 [11, 12]。随着研究的深入,壳寡糖诱导植物抗病性的作用机理将逐渐被了解,并为植物抗病基因工程奠定理论基础,壳寡糖及其衍生物的应用前景将会更加广阔[13]。笔者以具有季铵盐结构的新型壳寡糖席夫碱季铵盐衍生物为还原剂和稳定剂合成了其纳米银,并研究了经不同浓度的该纳米银溶液处理后烟株中相关生理生化指标的变化,初步探讨了其诱导烟株产生抗TMV活性的机理,旨在为开发高效、环保型抗病毒药剂提供依据。
壳寡糖季铵盐席夫碱衍生物的合成路线见Scheme 1。
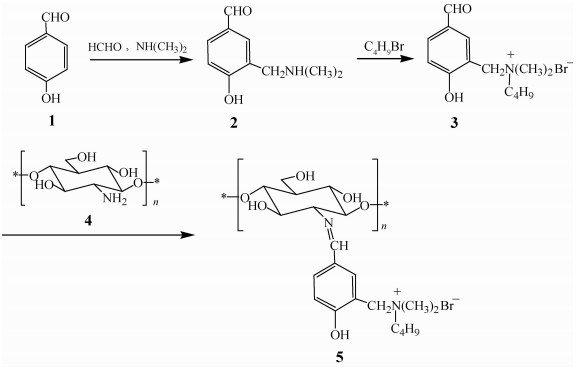 | Scheme 1 |
检测抗TMV活性所用的枯斑寄主为珊西烟Nicotiana tabacum cv. Xanthi-nc;TMV系统侵染寄主为普通烟Nicotiana tabacum K326。 1.1.2 供试病毒
烟草花叶病毒(Tobacco mosaic virus,TMV),由贵州大学提供,采用常规汁液摩擦接种法在普通烟上繁殖。 1.1.3 药剂及试剂
2%宁南霉素水剂(ningnanmycin AS,用蒸馏水稀释260倍),德强生物股份有限公司。壳寡糖(oligochitosan平均相对分子质量约为5 000)及正溴丁烷(98%),上海海曲化工有限公司;甲醛(37%),洛阳市化学试剂厂;二甲胺水溶液(>40%),天津科密欧化学试剂厂;对羟基苯甲醛(98%),阿拉丁试剂;乙腈(HPLC级),天津赛孚瑞有限公司;甲醇,色谱纯,湖北杜文化工科技有限公司;其余试剂均为市售分析纯。 1.1.4 仪器
CL-2型恒温加热磁力搅拌器(郑州国瑞科技仪器有限公司);FEI TECNALG2型透射电子显微镜(荷兰 FEI 公司);GSL-101BI激光颗粒分布测量仪(辽宁仪表研究所有限责任公司);安捷伦1200高效液相色谱仪(安捷伦科技有限公司)。 1.1.5 色谱条件
EclipseXDB-C18色谱柱(150 mm×4.6 mm,5 μm);采用A和B双泵系统,流动相A为甲醇(色谱纯),流动相B为超纯水;流速 1 mL/min;柱温30 ℃;进样量15 μL;检测波长 254 nm。 1.2 试验方法 1.2.1 壳寡糖季铵盐衍生物的合成 1.2.1.1 3-二甲氨甲基-4-羟基苯甲醛(2)的合成
参考文献[14]方法,但略有改进。在100 mL三口瓶中,加入4.50 g(0.05 mol)37%甲醛、3.24 g(0.04 mol) 40%二甲胺水溶液和15 mL乙醇,磁力搅拌下加热回流(约50 ℃)10 min后,加入0.996 g(0.008 mol)对羟基苯甲醛,再加热回流12 h;减压下旋转蒸发除去溶剂,用乙酸乙酯萃取4次(30 mL/次),减压脱溶,所得固体用石油醚重结晶,抽滤得无色针状晶体3.24 g,收率为45.2%。熔点79.5~80.6 ℃(文献值[14]80~81 ℃)。 1.2.1.2 溴化二甲基丁基(5-甲酰-2-羟基)苯甲基铵(3)的合成
在100 mL圆底烧瓶中,加入0.723 g(0.004 mol)化合物2,先用5 mL乙腈溶解,再加入0.006 mol正溴丁烷,磁力搅拌下加热回流5~8 h(回流管上安装干燥管,用高效液相色谱[HPLC,流动相V(甲醇)∶V(水)=0.3∶1]监测至反应结束;冷却至室温,加入大量乙酸乙酯,出现白色固体粉末,抽滤,用乙酸乙酯洗涤3次,于真空干燥箱中干燥,得白色固体0.586 g,收率62.0%。 1.2.1.3 壳寡糖季铵盐衍生物5的合成
在100 mL圆底烧瓶中,加入一定量的化合物3,用15 mL甲醇溶解后,分别加入2 mL冰乙酸和0.483 g(0.003 mol)壳寡糖(4),磁力搅拌下加热回流10~12 h(回流管上安装干燥管);抽滤,以乙醇为溶剂进行索氏提取10~12 h,在50 ℃下真空干燥12 h,得土黄色固体粉末(5),密封保存。 1.2.2 壳寡糖季铵盐衍生物纳米银的合成
向50 mL 烧杯中加入15 mL壳寡糖季铵盐衍生物(5)溶液(1 mg/mL),在80 ℃、搅拌下缓慢加入0.2 mL银氨溶液(其中[Ag(NH3) 2+]=0.0042 mol/L),继续搅拌10 min,得橙红色壳寡糖季铵盐衍生物纳米银溶液15 mL(以下简称纳米银溶液)。 1.2.3 纳米银粒子形貌观察
将稀释后的纳米银溶液滴加于透射电子显微镜覆有碳膜的铜网网格上,室温下真空干燥 30 min,待溶剂挥发后观察纳米银粒子的形貌。加速电压为 200 kV。 1.2.4 枯斑抑制筛选试验
采用枯斑寄主半叶法[15, 16]。TMV病毒汁液质量浓度为3.33 μg/mL,采用常规汁液摩擦接种法。
选取长势一致、具有4~5片真叶的盆栽珊西烟,剪去顶部。将供试药剂与TMV等体积混合1 h后喷洒到带微伤的半片烟叶上;另一半喷施清水与TMV等体积混合的溶液,作为对照。每处理重复3次(即每处理选取一株珊西烟,并选取顶部3片叶子作为3次重复),观察发病情况,计算枯斑抑制率。

选取长势一致、具有7~8片真叶的盆栽K326烟株供试。在喷雾施药24 h后,采用常规汁液摩擦接种法于每株下部第3片真叶上接种TMV(3.33 μg/mL),试验设4个处理:处理1(喷施稀释260倍的2%宁南霉素水剂后接种TMV,Control);处理2(喷施50 μg/mL纳米银溶液后接种TMV,T1);处理3(喷施25 μg/mL纳米银溶液后接种TMV,T2);处理4(喷施10 μg/mL纳米银溶液后接种TMV,T3)。每处理重复3次。分别于接种后1、4、7、10、13和16 d取样装入锡箔纸内,置于-80 ℃冰箱中保存。
采用Gooding等 [17]的方法提纯TMV。采用乙醇提取法[18]测定叶绿素含量;参照李合生的方法[19] 测定超氧物歧化酶(SOD)含量;参照文献[20]方法测定过氧化物酶(POD)含量;参照李靖等的方法[21] 测定多酚氧化酶(PPO)活性;采用考马斯亮蓝G-250染料结合法[22] 测定可溶性蛋白含量;参照赵世杰[23]的方法测定丙二醛(MDA)含量。 2 结果与分析 2.1 壳寡糖季铵盐衍生物5的合成与红外表征
通过Mannich甲基化反应和烷基化反应,先将季铵盐单元引入到对羟基苯甲醛结构中,再通过其与壳寡糖的缩合反应制得了土黄色粉末状的壳寡糖季铵盐希夫碱5,其与壳寡糖比对的红外光谱见图 1。
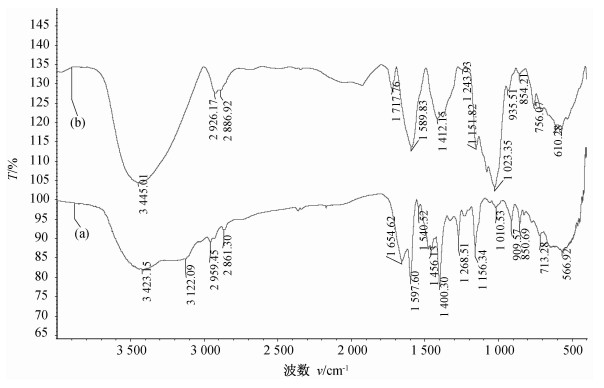 | 图 1 壳寡糖季铵盐衍生物5(a)与壳寡糖(b)的的红外光谱对比 Fig. 1 Infra-red spectra of oligochitosan quaternary ammonium salt derivative 5 (a) and bligochitosan (b) |
从图 1可以看出:与壳寡糖的相比,壳寡糖季铵盐衍生物5的红外光谱发生了明显变化:在3 445 cm-1处的O—H和N—H伸缩振动峰明显减弱,并移至3 423 cm-1处,说明壳寡糖上的氨基发生了缩合反应;在3 122 cm-1出现了苯环氢的特征吸收峰;在2 959 和2 861 cm-1出现了季铵盐基团中甲基和亚甲基中的C—H伸缩振动峰;壳寡糖中1 590 cm-1处氨基的N—H变形振动吸收峰消失,而在1 655 cm-1处出现了CN的伸缩振动吸收峰;此外,在1 598、1 541 和1 456 cm-1出现了苯环的特征骨架峰,1 400 cm-1处是甲基和亚甲基中的C—H变形振动峰。这些特征峰表明壳寡糖季铵盐希夫碱的形成。 2.2 不同浓度的壳寡糖季铵盐衍生物对纳米银溶液生成的影响
固定Ag(NH3)2+溶液的体积为0.5 mL,在80 ℃下,考察加入不同浓度壳寡糖季铵盐衍生物(5)反应30 min后生成其纳米银溶液的紫外光谱。由图 2可看出:化合物5的质量浓度对纳米银的形成影响较大,当其质量浓度为1 和2 mg/mL时,在420 nm处出现了球形纳米银粒子的特征等离子共振吸收峰,表明有纳米银粒子形成,同时可得到
稳定的红色纳米银溶液;而从1 mg/mL增加到 3 mg/mL 的过程中,其吸收峰的强度逐渐下降,在 3 mg/mL 时,420 nm处的吸收峰完全消失,同时反应溶液中出现大量AgBr沉淀。这是由于当化合物5质量浓度增加时,体系中溴负离子浓度也同时增加,其与银离子反应的速率大于Ag(NH3)2+被还原为Ag0 的速率,导致Ag(NH3)2+最终转化为AgBr。因此合适的壳寡糖季铵盐衍生物的质量浓度为 1 mg/mL。
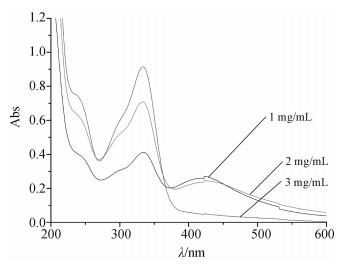 | 图 2 壳寡糖季铵盐衍生物(5)质量浓度对形成的纳米银紫外光谱的影响 Fig. 2 Effects of oligochitosan quaternary ammonium salt derivative concentration on UV-Vis spectra of silver nanoparticles solution |
图 3是银氨溶液[Ag(NH3)2+]的加入量对纳米银溶液UV-Vis光谱的影响,其中反应温度为80 ℃,反应时间为30 min,壳寡糖季铵盐衍生物的质量浓度为1 mg/mL,银氨溶液的加入量分别为0.1、0.5、1.0、1.5、2.0和2.5 mL。随着银氨溶液加入量的增加,纳米银溶液的 Amax (最大吸光度) 不断增大,溶液的颜色逐渐加深,后3组完全成为黑色。从稳定性上看,当银氨溶液的加入量在1.0 mL以上时,均得不到稳定的纳米银溶液。由此说明,随着银氨溶液加入量的增加,还原反应速率加快,溶液中纳米银粒子浓度迅速增加。但当银氨浓度过大时,由于单位时间内形成的晶核数目增加太快,银纳米粒子还来不及被壳寡糖季铵盐衍生物覆盖在其表面形成保护层,就因粒子之间发生碰撞而沉淀。因此适宜的银氨溶液的加入量为1 mL。
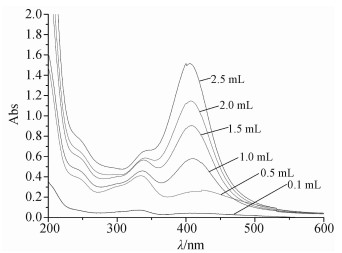 | 图 3 银氨溶液[Ag(NH3)2+]的加入量对纳米银紫外光谱的影响 Fig. 3 Effects of Ag(NH3)2+ concentration on UV-Vis spectra of silver nanoparticles solution |
由4.2×10-3mol/L的银氨溶液与1 mg/mL壳寡糖季铵盐衍生物在80 ℃下反应30 min后制得的纳米银溶液的透射电镜(TEM)(图 4)可以看出:纳米银为规则球形,分散性好,粒径 7~12 nm,且分布均匀。纳米银粒子表面包裹着一层可视度较低的物质,这是由于修饰后的壳寡糖链缠绕在球形纳米银颗粒的表面,对纳米银形成了一种保护作用,证明了壳寡糖季铵盐衍生物的稳定作用。同时由于壳寡糖季铵盐衍生物结构中含有的大量羟基、季铵离子以及还原反应后产生的羰基等亲水基团,促使纳米颗粒具有良好的亲水性能,因此,在这种糖链保护下,合成的纳米银粒子能够很好地分散在水中,形成透明、稳定的溶液。
 | 图 4 壳寡糖季铵盐衍生物纳米银溶液的透射电镜(TEM)分析图 Fig. 4 TEM image of oligochitosan quatemary ammonium salt derivative silver nanoparticles |
不同药剂对珊西烟TMV枯斑的钝化抑制效果见表 1。可以看出,不同浓度的壳寡糖季铵盐衍生物纳米银溶液对枯斑的抑制效果与壳寡糖、宁南霉素和壳寡糖季铵盐衍生物相比有明显提高,其中以25 μg/mL 的纳米银溶液抑制效果最好,为74.0%,分别比50 μg/mL壳寡糖溶液和2%宁南霉素水剂高41.5%和24.4%;50 μg/mL的壳寡糖季铵盐衍生物对枯斑抑制效果稍高于壳寡糖,但无显著差异;与2%宁南霉素水剂相比,除25 μg/mL的纳米银处理和10 μg/mL的纳米银处理差异显著外,其他处理间均无显著差异。可见,壳寡糖季铵盐衍生物纳米银溶液对TMV枯斑的抑制效果较好。
|
|
表 1 供试药剂对珊西烟TMV的钝化抑制效果 Table 1 Inhibition of the test reagent against TMV diseases on Nicotiana tabacum cv. Xanthi-nc |
25 μg/mL的纳米银溶液对珊西烟TMV枯斑的抑制效果见图 5。
 |
注:左半叶为喷施25 μg/mL纳米银溶液与TMV的混合物;右半叶为喷施清水与TMV的混合物。 Note:The left of the leave was sprayed with 25 μg/mL oligochitosan quaternary ammonium salt derivative silver nanoparticles which was mixed with TMV; The right of the leave was sprayed with water that mixing with TMV. 图 5 μg/mL壳寡糖季铵盐衍生物纳米银溶液对珊西烟上由TMV侵染产生枯斑的抑制效果 Fig. 5 Inhibition of necrosis spots on Nicotiana tabacum cv. Xanthi-nc by 25 μg/mL oligochitosan quaternary ammonium salt derivative silver nanoparticles |
不同浓度的药剂处理对烟叶中叶绿素含量的影响见图 6。结果表明:2%宁南霉素水剂处理的叶绿素含量在第4天时明显升高,之后骤然下降,呈现出单峰曲线变化;50 μg/mL 的纳米银溶液(T1处理组)叶绿素含量变化幅度较大,前4 d处于平稳状态,7 d时含量骤增并达到最大值,之后骤降,13 d时又骤增,16 d时又骤降;25 μg/mL 的纳米银溶液(T2处理组)叶绿素含量变化较平稳,仅在10 d时达到最大值;10 μg/mL 的纳米银溶液(T3处理组),除10 d时叶绿素含量下降幅度较大外,其他时间段变化均较平缓。总之,喷施不同浓度的纳米银溶液均可在不同程度上降低被TMV侵染后烟草叶片中叶绿素含量下降的幅度。
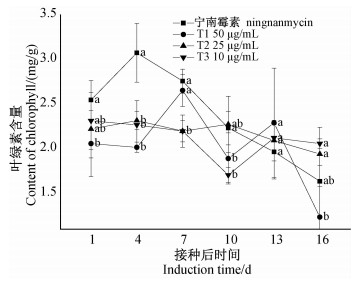 |
注:不同小写字母表示不同处理5%水平下差异显著。 Note:Different small letters are significant difference at 5%. 图 6 不同浓度壳寡糖季铵盐衍生物纳米银溶液(T1~T3)及2%宁南霉素水剂处理下叶绿素的含量变化 Fig. 6 Changes of the contents of chlorophyll under treatment of oligochitosan quaternary ammonium salt derivative silver nanoparticles (T1-T3) and 2% ningnanmycin AS |
结果(图 7)显示:各处理下SOD酶活性整体呈现出倒“V”型动态变化。除T3处理在第10天出现最大酶活性外,其余各处理均在第7天出现最大酶活性。各处理的酶活性曲线变化整体上表现为先升高再降低最后趋于平缓。整体看,各处理与2%宁南霉素水剂处理间几乎无差异。表明喷施不同浓度的纳米银溶液可有效提高烟叶中SOD酶活性。
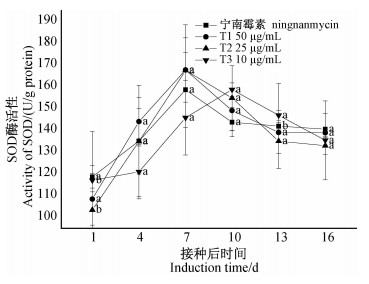 |
注:不同小写字母表示不同处理5%水平下差异显著。 Note:Different small letters are significant difference at 5%. 图 7 不同浓度壳寡糖季铵盐衍生物纳米银溶液(T1~T3)及2%宁南霉素水剂处理下SOD酶的活性变化 Fig. 7 Changes of the activity of SOD under treatment of oligochitosan quaternary ammonium salt derivative silver nanoparticles (T1-T3) and 2% ningnanmycin AS |
喷施一定浓度的纳米银溶液可有效提高烟叶中POD酶活性,4个处理POD酶活性均在第10天达到最大值,其中2%宁南霉素水剂和T2处理下POD酶活性整体高于T1和T3处理,T1处理酶活性最低(图 8)。
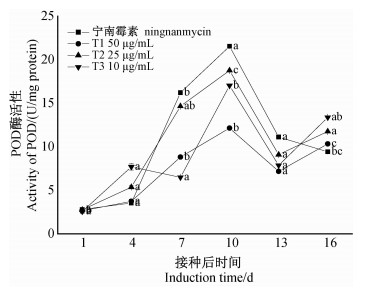 |
注:不同小写字母表示不同处理5%水平下差异显著。 Note:Different small letters are significant difference at 5%. 图 8 不同浓度壳寡糖季铵盐衍生物纳米银溶液(T1~T3)及2%宁南霉素水剂处理下POD酶的活性变化 Fig. 8 Changes of the activity of POD under treatment oligochitosan quaternary ammonium salt derivative silver nanoparticles (T1-T3) and 2% ningnanmycin AS |
结果如图 9所示。4个处理下烟叶中PPO酶活性均随时间的延长而明显升高,表明在一定时间内喷施纳米银溶液可有效的提高烟叶中PPO酶活性。
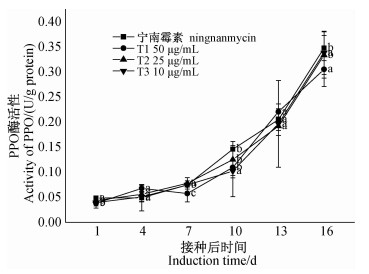 |
注:不同小写字母表示不同处理5%水平下差异显著。 Note:Different small letters are significant difference at 5%. 图 9 不同浓度壳寡糖季铵盐衍生物纳米银溶液(T1~T3)及2%宁南霉素水剂处理下PPO酶的活性变化 Fig. 9 Changes of the activity of PPO under treatment of oligochitosan quaternary ammonium salt derivative silver nanoparticles (T1-T3) and 2% ningnanmycin AS |
结果(图 10)显示:T1、T2和T3处理下烟叶中丙二醛的含量变化与宁南霉素处理相似,均为在第1~7天表现出较为明显的下降趋势,第10天明显上升达最大值,之后趋于下降;虽然4个处理间存在显著差异,但仍表明在一定时间内,喷施一定浓度的纳米银溶液可有效降低烟叶中丙二醛的含量。
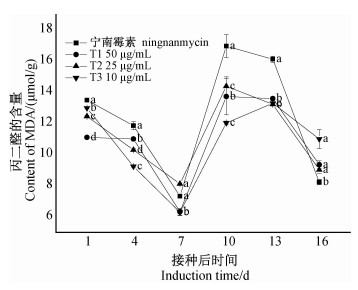 |
注:不同小写字母表示不同处理5%水平下差异显著。 Note:Different small letters are significant difference at 5%. 图 10 不同浓度壳寡糖季铵盐衍生物纳米银溶液处理(T1~T3)下丙二醛的含量变化 Fig. 10 Changes of MDA content under treatment of loligochitosan quaternary ammonium salt derivative silver nanoparticles (T1-T3) |
结果(图 11)表明:喷施纳米银溶液可有效增加烟叶中可溶性蛋白的含量。4个处理下烟叶中可溶性蛋白含量的变化曲线基本一致,均表现为先增后减再增的趋势。
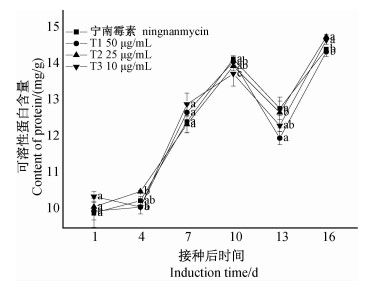 |
注:不同小写字母表示不同处理5%水平下差异显著。 Note:Different small letters are significant difference at 5%. 图 11 不同浓度壳寡糖季铵盐衍生物纳米银溶液处理(T1~T3)下可溶性蛋白的含量变化 Fig. 11 Changes of soluble protein content under treatment of oligochitosan quaternary ammonium salt derivative silver nanoparticles (T1-T3) |
1)以壳寡糖为原料,经氨甲基化、烷基化和缩合3步反应合成了新的壳寡糖季铵盐衍生物,进一步以其作为还原剂和保护剂与银氨溶液反应制备了壳寡糖季铵盐衍生物纳米银溶液。研究发现,当银氨溶液浓度为 4.2×10-3 mol/L、壳寡糖季铵盐衍生物的质量浓度为1 mg/mL,反应温度为 80 ℃,反应时间为30 min时,制得的壳寡糖季铵盐衍生物纳米银的溶液分散性好,粒径在7~12 nm。
2)珊西烟上的盆栽试验结果表明,不同浓度的纳米银溶液对TMV枯斑的抑制效果均较好,其中以25 μg/mL的纳米银溶液抑制效果最好,为74.0%,比50%的壳寡糖溶液和2%宁南霉素水剂分别高41.5%和24.4%;与壳寡糖相比,壳寡糖季铵盐衍生物溶液具有较好的枯斑抑制效果。在由壳寡糖季铵盐衍生物生成纳米银的过程中,壳寡糖季铵盐结构中的酚羟基与银离子作用会被氧化成醌类结构[24],也可能加强其生物活性,包括对病毒的抑制作用。研究表明,一些酚类和醌类物质对番茄黄化曲叶病毒、I型人疱疹病毒等具有较好的抑制作用[25, 26],本课题组合成的具有酚羟基结构的壳寡糖希夫碱纳米银溶液也表现出了较强的抑菌作用[24]。本研究表明,壳寡糖季铵盐衍生物纳米银溶液对TMV枯斑的抑制效果明显优于壳寡糖季铵盐衍生物溶液,这可能与纳米银中所含的酚类或醌类的抗病毒活性有关,也可能与纳米银自身或壳寡糖的抗病毒活性[4, 5, 27]有关,或者跟酚类或醌类的抗病毒活性与纳米银和壳寡糖的抗病毒活性的协同作用有关。
3)通过盆栽试验对壳寡糖季铵盐衍生物纳米银溶液的诱导烟株抗TMV活性进行了初步研究,在普通烟K326上测定了不同浓度的纳米银溶液处理后与抗病性相关的酶SOD、POD、PPO活性的变化规律。活性氧是植物正常代谢过程中的有毒副产物,其积累可导致膜脂过氧化。有研究表明,与活性氧清除有关的防御酶包括SOD、POD、PPO等。杜昱光等[28, 29, 30, 31]发现,感染TMV的烟叶经壳寡糖处理后其防御酶活性得到提高,本研究也得到了类似的结果。与目前国内广泛用来防治TMV的药剂宁南霉素相比,一定浓度的壳寡糖季铵盐衍生物纳米银溶液也可明显提高叶片中SOD、POD和PPO的活性,从而达到对活性氧的有效清除,提高烟草的抗病性。这表明壳寡糖季铵盐衍生物纳米银溶液可诱导烟草对TMV产生抗性。
4)丙二醛是细胞膜膜脂过氧化的最终产物,丙二醛的积累对植物具有毒害作用,其含量的高低反映了细胞膜质的过氧化水平以及植物对逆境条件反映的强弱[32]。本研究结果表明:喷施一定浓度的壳寡糖季铵盐衍生物纳米银溶液在一定时期内可有效降低烟叶中丙二醛的含量。可溶性蛋白属于渗透调节物质,可阻碍氧自由基的产生[33]。研究表明,染病的植物组织细胞内可溶性蛋白质含量降低[34]。王海河等[35]研究发现,受黄瓜花叶病毒(CMV)侵染的烟草(K326)叶片中可溶性蛋白含量在病毒侵染初期到症状出现时明显升高,之后随着症状的加重,含量逐渐降低。本研究表明,一定浓度的壳寡糖季铵盐衍生物纳米银溶液可提高叶片中可溶性蛋白的含量,从而提高烟草的抗病性。
| [1] | Zhang Hu, Du Yuguang, Yu Xingju, et al. Preparation of chitooligosaccharides from chitosan by a complex enzyme[J]. Carbohydr Res, 1999, 320(3-4): 257-260. |
| [2] | Hadwiger L A, Ogawa T, Kuyama H. Chitosan polymer sizes effective in inducing phytoalexin accumulation and fungal suppression are verified with synthesized oligomers[J]. Mol Plant Microbe Interact, 1994, 7(4): 531-533. |
| [3] | Xu Junguang, Zhao Xiaoming, Han Xiuwen, et al. Antifungal activity of oligochitosan against Phytophthora capsici and other plant pathogenic fungi in vitro[J]. Pestic Biochem Physiol, 2007, 87(3): 220-228. |
| [4] | Feng B, Chen Y, Zhao C, et al. Isolation of a novel Ser/Thr protein kinase gene from oligochitosan-induced tobacco and its role in resistance against tobacco mosaic virus[J]. Plant Physiol Biochem, 2006, 44(10): 596-603. |
| [5] | Zhao Xiaoming, She Yuguang, Du Yiaoping, et al. Induction of antiviral resistance and stimulary effect by oligochitosan in tobacco[J]. Pestic Biochem Physiol, 2007, 87(1): 78-84. |
| [6] | Pospieszny H, Chirkov S, Atabekov J. Induction of antiviral resistance in plants by chitosan[J]. Plant Sci, 1991, 79(1): 63-68. |
| [7] | Chircov S N, Il'ina A V, Surgucheva N A, et al. Effect of chitosan on systemic viral infection and some defense responses in potato plants[J]. Russian J Plant Physiol, 2001, 48(6): 774-779. |
| [8] | 朱传方, 吴爱斌, 徐汉虹. 2,4-二羟基苯乙酮席夫碱化合物的合成[J]. 化学试剂, 2001, 23(3): 150-151. Zhu Chuanfang, Wu Aibin, Xu Hanhong. Synthesis of 2,4-dihydroxyacetophotone Schiff base[J]. Chem Reagents, 2001, 23(3): 150-151. (in Chinese) |
| [9] | 高兴文, 蔡学建, 宋宝安, 等. 4(3H)-喹唑啉酮类Schiff碱的合成与抗烟草花叶病毒活性[J]. 有机化学, 2008, 28(10): 1785-1791. Gao Xingwen, Cai Xuejian, Song Bao'an,et al. Synthesis and anti-tobacco mosaic virus activity of 4(3H)-Quinazolinone Schiff base[J]. Chin J Org Chem, 2008, 28(10): 1785-1791. (in Chinese) |
| [10] | 孟凡德, 赵全芹, 李明霞, 等. 银-氨基酸席夫碱配合物的合成、表征及对烟草花叶病毒抑制作用初探[J]. 化学试剂, 2000, 22(3): 176-177. Meng Fande, Zhao Quanqin, Li Mingxia,et al. Synthesis and characterization of Ag(I)-amino acid Schiff base complexes and inhibition to tobaccum mosaic virus[J]. Chem Reagents, 2000, 22(3): 176-177. (in Chinese) |
| [11] | Huang Junmin, Chen Ruyu. An overview of recent advances on the synthesis and biological activity of α-aminophosphonic acid derivatives[J]. Heteroatom Chem, 2000, 11(7): 480-492. |
| [12] | Miao Zhiwei, Fu Cuirong, Wang Bin, et al. Synthesis and electrospray ionization mass spectra of N-(1,3,2-dioxaphosphorinan-2-ylmethyl) thiophosphoramidates[J]. Chin J Chem, 2007, 25(9): 1344-1348. |
| [13] | 赵小明, 尹恒. 寡糖免疫调节剂(疫苗)在作物上的应用[C]. 2011. Zhao Xiaoming, Yin Heng. The application of oligochitosan on crop[C]. 2011. |
| [14] | Fang Xubin, Fang Lei, Gou Shaohua, et al. Design and synthesis of dimethylaminomethyl-substituted curcumin derivatives/analogues: Potent antitumor and antioxidant activity, improved stability and aqueous solubility compared with curcumin[J]. Bioorg Med Chem Lett, 2013, 23(5): 1297-1301. |
| [15] | Hadidi A, Khetarpal R K, Koganezawa H. Plant Virus Disease Control[M]. St Paul, Minnesota: The American Phytopathol Society, 1998: 154-162. |
| [16] | French C J, Towers G H N. Inhibition of infectivity of potato virus X by flavonoids[J]. Phytochemistry, 1992, 31(9): 3017-3020. |
| [17] | Gooding G V Jr, Hebert T T. A simple technique for purification of tobacco mosaic virus in large quantities[J]. Phytopathology, 1967, 57(11): 1285. |
| [18] | 李虎林, 白青竹, 姬文秀, 等. 不同类型烟草叶片叶绿素和类胡萝卜素含量比较分析[J]. 延边大学农学学报, 2008, 30(3): 153-156. Li Hulin, Bai Qingzhu, Ji Wenxiu,et al. Comparison and analysis of chorophyll and carotinoid content in leaves for different kind of tobacco[J]. J Agri Sci Yanbian Univ, 2008, 30(3): 153-156. (in Chinese) |
| [19] | 刘炳辉, 董晓颖, 李志军, 等. 硬肉桃果实成熟前后几种与果实软化相关的生理指标的变化[J]. 植物生理学通讯, 2008, 44(5): 887-890. Liu Binghui, Dong Xiaoying, Li Zhijun,et al. Changes in several physiological indexes related to fruit softening of crisp peach fruits before and after ripening[J]. Plant Physiol J, 2008, 44(5): 887-890. (in Chinese) |
| [20] | Chen Yafei, Zhan Yong, Zhao Xiaoming, et al. Functions of oligochitosan induced protein kinase in tobacco mosaic virus resistance and pathogenesis related proteins in tobacco[J]. Plant Physiol Biochem, 2009, 47(8): 724-731. |
| [21] | 李靖, 利容千, 袁文静. 黄瓜感染霜霉病菌叶片中一些酶活性的变化[J]. 植物病理学报, 1991, 21(4): 277-283. Li Jing, Li Rongqian, Yuan Wenjing. On the change of enzyme activities of cucumber leaf infected by pseudoperonospora cubensis (Berk, ET CTRT) rosws[J]. Acta Phytopathol Sinica, 1991, 21(4): 277-283. (in Chinese) |
| [22] | 张龙翔, 张廷芳, 李令嫒. 生化实验方法和技术[M].2版. 北京: 高等教育出版社, 1997: 312-313. Zhang Longxiang, Zhang Tingfang, Li Lingyuan. Method and Technique of Biochemical Experiment[M].2nd Ed. Beijing: Higher Education Press, 1997: 312-313. (in Chinese) |
| [23] | 赵世杰, 许长成, 邹琦, 等. 植物组织中丙二醛测定方法的改进[J]. 植物生理学通讯, 1991, 30(3): 207-210. Zhao Shijie, Xu Changcheng, Zou Qi,et al. Improvements of method for measurement of malondialdehvde in plant tissues[J]. Plant Physiol Commu, 1991, 30(3): 207-210. (in Chinese) |
| [24] | Wang Zhimin, Xu Cuilian, Zhao Mingqin, et al. One-pot synthesis of narrowly distributed silver nanoparticles using phenolic-hydroxyl modified chitosan and their antimicrobial activity[J]. RSC Adv, 2014, 4(87): 47021-47030. |
| [25] | 王春梅. 丁子香酚和接种番茄黄化曲叶病毒对番茄几丁质酶和β-1,3-葡聚糖酶活性的影响[J]. 江西农业学报, 2013, 25(9): 78-80. Wang Chunmei. Effects of eugenol and TYLCV inoculation on activities of chitinase and β-1,3-glucanase in tomato[J]. Acta Agri Jiangxi, 2013, 25(9): 78-80. (in Chinese) |
| [26] | 杨虹, 邓成国, 张端莲, 等. 虎杖多种醌类化合物对I型人疱疹病毒感染豚鼠皮肤的感染率分析[J]. 数理医药学杂志, 2004, 17(4): 306-307. Yang Hong, Deng Chengguo, Zhang Duanlian,et al. Tissue change of on antiviral effect of ethy acetate extract component of Rhizoma polygong cuspidate on human simplex virus-I[J]. J Math Med, 2004, 17(4): 306-307. (in Chinese) |
| [27] | Lu Lei, Sun R W Y, Chen Rong, et al. Silver nanoparticles inhibit hepatitis B virus replication[J]. Antivir Ther, 2008, 13(2): 253-262. |
| [28] | 惠娜娜, 郭成瑾, 商文静, 等. 壳寡糖诱导和TMV侵染烟草防御酶活性的变化[J]. 西北农林科技大学学报(自然科学版), 2007, 35(3): 213-216. Hui Nana, Guo Chengjin, Shang Wenjing, et al. Changes of activities of defensive enzymes in tobacco leaves treated with chito-oligosaccaride and inoculated with TMV[J]. J Northwest A & F Univ (Natl Sci Ed), 2007, 35(3): 213-216. (in Chinese) |
| [29] | 杜昱光, 白雪芳, 赵小明, 等. 壳寡糖对烟草防御酶活性及同工酶酶谱的影响[J]. 中国生物防治, 2002, 18(2): 83-86. Du Yuguang, Bai Xuefang, Zhao Xiaoming,et al. The effect of oligochitosan on the activity of defensive enzyme and zymogram of isoenzyme in tobacco leaves[J]. Chin J Biol Control, 2002, 18(2): 83-86. (in Chinese) |
| [30] | 马镝, 赵秀香, 吴元华. 壳寡糖对烟草花叶病毒的抑制作用及其对烟草酶活性的影响[J]. 中国生物防治, 2008, 24(2): 154-158. Ma Di, Zhao Xiuxiang, Wu Yuanhua. Inhibition ofchito-oligosaccharide against plant virus diseases[J]. Chin J Biol Control, 2008, 24(2): 154-158. (in Chinese) |
| [31] | 郭卫华, 赵小明, 杜昱光. 壳寡糖对烟草幼苗生长和光合作用及与其相关生理指标的影响[J]. 植物生理学通讯, 2008, 44(6): 1155-1157. Guo Weihua, Zhao Xiaoming, Du Yuguang. Effects of oligochitosan on the growth and photosynthesis and physiological index related to photosynthesis of tobacco seedlings[J]. Plant Physiol Commun, 2008, 44(6): 1155-1157. (in Chinese) |
| [32] | 蒋靓, 庄杰云, 樊叶杨, 等. 与水稻耐逆性相关的叶片丙二醛含量的 QTL分析[J]. 中国水稻科学, 2007, 21(4): 436-438. Jiang Jing, Zhuang Jieyun, Fan Yeyang, et al. QTL mapping for leaf malondialdehyde content associated with stress tolerance in rice[J]. Chinese J Rice Sci, 2007, 21(4): 436-438. (in Chinese) |
| [33] | 彭志红, 彭克勤, 胡家金. 渗透胁迫下植物脯氨酸积累的研究进展[J]. 中国农学通报, 2002, 18(4): 80-83. Peng Zhihong, Peng Keqin, Hu Jiajin. Research progress on accumulation of proline under osmotic stress in plants[J]. Chin Agri Sci Bull, 2002, 18(4): 80-83. (in Chinese) |
| [34] | 景岚, 王丽芳, 康俊. 不同抗性的向日葵品种接种锈菌后叶片中可溶性蛋白、可溶性总糖及叶绿素含量的变化[J]. 临沂师范学院学报, 2008, 30(6): 76-80. Jing Lan, Wang Lifang, Kang Jun. Changes of soluble protein, total sugar and chlorophyll in the leaves of different resistant sunflower varieties[J]. J Linyi Teachers, Univ, 2008, 30(6): 76-80. (in Chinese) |
| [35] | 王海河, 蒋继宏, 吴祖建, 等. 黄瓜花叶病毒M株系RNA3的变异分析及全长克隆的构建[J]. 农业生物技术学报, 2000, 8(2): 180-185. Wang Haihe, Jiang Jihong, Wu Zujian, et al. Diversity analysis of RNA3 of cucumber mosaic virus strain M and construction of its full-length cDNA clone[J]. J Agri Biotechnol, 2000, 8(2): 180-185. (in Chinese) |
 2015, Vol. 17
2015, Vol. 17


