2. 中国科学院 动物研究所, 农业虫害鼠害综合治理国家重点实验室, 北京 100101
2. State Key Lavoratory of Integrated Management of Pest Insects and Rodents, Institute of Zoology, Chinese Academy of Sciences, Beijing 100101, China
叶菌唑(metconazole)又称羟菌唑,化学名称为(1RS,5RS;1RS,5SR)-5-(4-氯苄基)-2,2-二甲基-1-(1H-1,2,4-三唑-1-基甲基)环戊醇,是日本吴羽化学公司于20世纪90年代初开发的新型三唑类广谱内吸性杀菌剂,可有效防治小麦赤霉病、小麦白粉病以及小麦锈病等禾谷类作物病害[1]。目前,叶菌唑在美国、欧盟以及日本等国家和地区已有登记使用,其在小麦上的最大残留限量(MRL)分别为0.15、0.15和0.2 mg/kg,但在我国尚未得到推广,也尚未制定MRL标准。
目前,国内外有关叶菌唑的报道多为其毒力测定及合成工艺研究[2],也有一些关于叶菌唑在肉类[2]、中草药[3]、水果[4]和谷物[5, 6, 7]基质中的残留检测方法的相关报道,主要包括气相色 谱-质谱法(GC-MS)[2, 3, 5]、气相色谱-串联质谱法(GC-MS/MS)[7]以及高效液相色谱-串联质谱法(HPLC-MS/MS)[4, 6]等,但尚未见叶菌唑在小麦中的残留行为及其膳食暴露风险评估方面的研究报道。本研究建立了叶菌唑的气相色谱-氮磷检测器(GC-NPD)分析方法,并基于此方法研究了其在小麦中的残留及消解变化趋势,针对所得残留结果进行了膳食暴露风险评价,以期为我国小麦中叶菌唑的合理使用及MRL标准的制定提供依据。
1 材料与方法
1.1 仪器与药剂
Agilent 7890A气相色谱仪,配有氮磷检测器及自动进样器(美国Agilent公司);KQ-600型超声波清洗器(昆山市超声仪器有限公司);SC-3612台式低速离心机(安徽中佳科学仪器有限公司);EYELA OSB-2000 旋转蒸发仪(上海爱朗仪器有限公司);AL204-IC d=0.001 g天平,SPN202F d=0.01 天平(梅特勒-托利多称重设备系统有限公司);CNW-CA3755弗罗里硅土固相萃取柱(1 g/6 mL,由上海安谱科学仪器有限公司提供)。
叶菌唑(metconazole)标准品(纯度99.5%),由Dr. Ehrenstorfer Gmbh提供;50%叶菌唑水分散粒剂(metconazole 500WDG)。所用试剂均为市售分析纯(石油醚经重蒸后使用)。
1.2 分析方法 1.2.1 样品的提取麦粒:称取10 g经研磨成粉的麦粒样品(精确到0.01 g)于50 mL具塞离心管内,加入20 mL乙腈,振荡1 min后超声提取15 min。加入6 g氯化钠,剧烈摇动1 min,3 000 r/min 离心5 min。取上清液10 mL在100 mL 茄形瓶中,35 ℃下旋转蒸发至近干,待净化。
麦秆:称取5 g经切碎的麦秆样品(精确到0.01 g)于200 mL玻璃瓶内,加入10 mL蒸馏水和40 mL乙腈,摇匀后超声提取15 min。过滤至事先称有6 g氯化钠的50 mL具塞离心管中,剧烈摇动1 min,3 000 r/min 离心5 min。取上清液20 mL于100 mL 茄形瓶中,35 ℃下旋转蒸发至近干,待净化。 1.2.2 样品净化
采用弗罗里硅土固相萃取柱净化,先用5 mL V(丙酮)∶V(石油醚)=10∶90混合溶剂活化萃取柱,弃去;再用10 mL 上述混合溶剂分两次将待净化残渣溶解上样,最后用20 mL 相同混合溶剂分4次洗脱。收集洗脱液共30 mL,35 ℃下旋转蒸发至近干,用2.5 mL丙酮溶解待色谱分析。 1.2.3 GC-NPD检测条件
Agilent HP-5气相色谱柱(30 m×0.32 mm×0.25 μm);升温程序:120 ℃,保持1 min,以25 ℃/min 的速率升温至280 ℃,保持5 min。进样口温度280 ℃;载气为高纯氮气,流速3 mL/min;检测器温度340 ℃;氢气流量3 mL/min,空气流量60 mL/min;进样量2 μL;不分流进样。在此条件下,叶菌唑的保留时间为7.65 min。 1.2.4 标准曲线绘制
采用外标法定量。称取叶菌唑标准品0.027 0 g(精确至0.000 1 g)于25 mL容量瓶中,用丙酮溶解并配制成1 074.6 μg/mL的母液,采用梯度稀释法用丙酮稀释成5、2.5、1、0.5、0.25、0.1和0.04 μg/mL的叶菌唑系列标准工作溶液,在1.2.3节所述色谱条件下测定。以样品质量浓度(x,mg/L)为横坐标,峰面积(y)为纵坐标,绘制标准曲线。 1.2.5 添加回收试验
在空白麦粒和麦秆中添加一定量的叶菌唑标准溶液。添加水平覆盖实际样品中叶菌唑的残留浓度范围:麦粒中为0.02、0.15和1 mg/kg,麦秆中为0.04、0.15、5 和10 mg/kg,每个水平5次重复,按本研究所建立的方法进行提取、净化及GC-NPD分析,计算平均回收率和相对标准偏差(RSD)。
1.3 田间试验
试验地点为北京市通州区、安徽省宿州市及黑龙江省哈尔滨市。小区面积为30 m2,各处理均设3次重复,小区间设置保护行,同时设空白对照区。各小区种植条件一致。50%叶菌唑水分散粒剂在小麦上的推荐使用剂量(有效成分)为45~90 g/hm2。
1.3.1 消解动态试验选择未施用过叶菌唑的小麦田,以推荐使用高剂量的2倍(有效成分180 g/hm2)于麦苗返青至拔节期喷雾施药1次。于施药后2 h及1、3、5、7、10、14、21、30、45 d采集地表以上的全株1 kg以上,切碎后混匀,-20 ℃冰箱中贮存待测。 1.3.2 最终残留试验
以推荐使用高剂量(有效成分90 g/hm2)及其1.5倍剂量(135 g/hm2)于小麦锈病和白粉病发病初期分别施药2次和3次,施药间隔为7 d,分别于末次施药后14、21和28 d随机采集处理组和对照组的小麦植株及麦穗样品。小麦植株切碎后混匀,麦穗脱粒后混匀,-20 ℃冰箱中贮存待测。 1.4 膳食摄入风险评价
膳食暴露量和风险评价结果分别由公式(1)和(2)计算得出。
EED=(CRL×Fi)/bw(1)
RQ=EED/ADI(2)
式中:EED (estimated exposure dose)为估计暴露量,mg/kg bw;CRL (calculated residue level)为理论残留量,mg/kg;Fi (food intake)为食物摄入量,kg;bw为体重,kg;RQ (risk quotient)为风险商值;ADI (acceptable daily intake)为每日允许摄入量,mg/kg bw。当RQ>1时,表示存在不可接受的较大风险,数值越大,风险越大;当RQ<1时,表示风险是可接受的,数值越小,风险越小[8]。
2 结果与讨论
2.1 方法的线性范围、检出限及定量限
外标法定量分析结果表明,在0.04~10 mg/L的范围内,叶菌唑的峰面积(y)与质量浓度(x,mg/L)间呈良好线性关系,回归方程为y=70.721 8x-0.925 3,相关系数r=0.999 6。按照3倍信噪比计算,叶菌唑在麦粒和麦秆中检出限(LOD)分别为0.005 和0.01 mg/kg。其在麦粒和麦秆中的定量限(LOQ)则分别为0.02 和0.04 mg/kg。 2.2 方法的准确度和精密度
添加回收试验结果(表 1)表明:在不同添加水平范围内(添加水平覆盖实际样品中叶菌唑含量范围),叶菌唑在麦粒和麦秆中的平均回收率在81%~101%之间,RSD在 2.1%~9.1%之间。准确度和精密度均符合农药残留分析标准要求。典型色谱图如图 1所示,目标峰附近无杂质峰,净化效果较好
| 表 1 叶菌唑在不同样品中的平均添加回收率(n=5)Table 1 Recoveries of metconazole in different samples at different levels (n=5) |
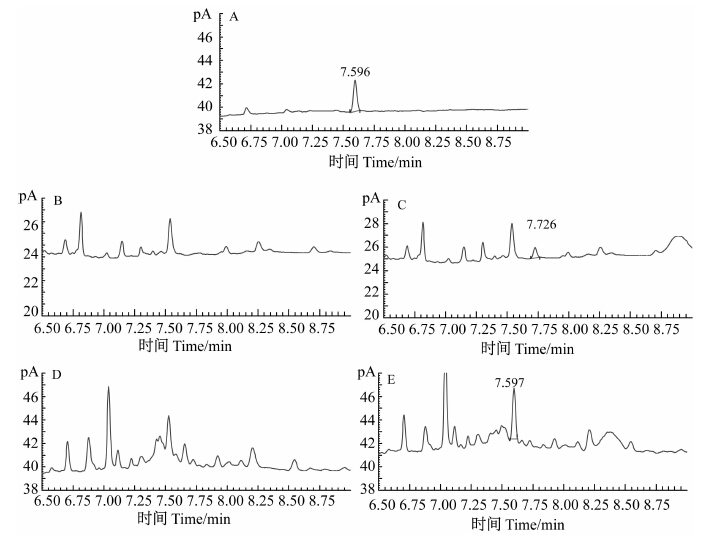 |
A. 叶菌唑标样(0.04 mg/L);B. 麦秆空白样品;C. 麦秆添加样品(0.04 mg/kg); D. 麦粒空白样品;E. 麦粒添加样品(0.02 mg/kg)。 A. Standard of metconazole (0.04 mg/L); B. Blank of wheat straw; C. Wheat straw sample with 0.04 mg/kg metconazole; D. Blank of wheat grain; E. Wheat grain sample with 0.02 mg/kg metconazole. 图 1 叶菌唑标准品和麦秆及麦粒样品色谱图 Fig. 1 Chromatogram of metconazole standard and difference sample of wheat straw and wheat grain |
北京、安徽和黑龙江3地的消解动态试验结果(表 2)表明:叶菌唑在小麦植株中的消解规律符合一级动力学方程,其在小麦植株中的半衰期为 4.9~7.3 d。黑龙江样品药后10 d的消解率为86%,安徽和北京两地样品7 d 消解率达90%以上,3地消解趋势基本一致,消解速率较快。
| 表 2 叶菌唑在小麦植株中的消解动态Table 2 Dissipation of metconazole in wheat straw |
结果见表 3。距最后一次施药间隔14 d采样测定,麦粒中叶菌唑的残留量<0.02~0.037 mg/kg;间隔21 d时,残留量<0.02~0.024 mg/kg;间隔28 d 时,残留量<0.02~0.022 mg/kg。叶菌唑在小麦籽粒中的残留量随采收间隔期的延长而减少,间隔14 d时残留中值(STMR)为0.02 mg/kg。
| 表 3 叶菌唑在麦粒中的最终残留量Table 3 The terminal residues of metconazole in grain |
2.5 膳食暴露和风险评价
根据膳食摄入结构和所得最终残留结果,可计算出不同人群的膳食摄入暴露量,从而进行风险评估[9, 10]。不同国家和不同年龄组成均可导致膳食摄入结构的差异,因此,针对我国膳食结构进行的风险评估是必要的。根据相关标准规定,叶菌唑的ADI为0.048 mg/kg bw[11],理论残留量CRL以残留中值0.02 mg/kg计,根据公式(1)和(2)计算估计暴露量和风险商值。叶菌唑在我国仍未得到登记推广,因此本评价仅针对与小麦相关的面粉及制品。我国不同人群(年龄和性别)中面粉及制品的平均摄入量(Fi)、估计暴露量(EED)和风险商值(RQ)见表 4。
膳食暴露结果显示,对于不同年龄段及性别人群,风险商值为0.001~0.002,远小于1,其膳食暴露风险较低,处于可接受的安全水平。
| 表 4 我国不同人群对面粉及其制品平均摄入量、估计暴露量和风险商值Table 4 Average intake of wheat,EED and RQ for different population in China |
本研究建立了叶菌唑在小麦中的残留分析方法,该方法重现性好、灵敏度高,准确度和精密度符合农药残留分析标准要求。
消解动态试验结果表明,叶菌唑在小麦植株中的消解速率较快,半衰期为4.9~7.3 d。最终残留试验结果表明,采用50%叶菌唑水分散粒剂按推荐使用高剂量(有效成分90 g/hm2)及其1.5倍剂量(有效成分135 g/hm2)处理,收获的小麦籽粒中叶菌唑的最高残留量为0.037 mg/kg,均低于美国及欧盟规定的叶菌唑在小麦上的最大残留限量(0.15 mg/kg)。
膳食摄入风险评价结果表明,叶菌唑在小麦中的残留风险较低,该结果可为我国相关MRL标准的建立提供参考。但值得注意的是,由于叶菌唑在我国尚未得到登记推广,本研究仅考虑了摄入面粉及制品对我国居民健康状况的影响,对蔬菜、水果、油料作物等尚未涉及,因此如果考虑到叶菌唑逐步在中国登记,其风险尚需进一步确定。此外,制定农药MRL标准及进行风险评估需要足够和具有充分代表性试验点的残留数据,而本文数据仅来源于典型代表地区的1年3地试验结果,在数据量上有所不足,因此还需增加不同年度、不同生态环境以及不同生产方式条件下的残留试验数据,方可评估制定出合理的MRL标准。
| [1] | 邬柏春, 冯化成. 三唑类杀菌剂种菌唑和叶菌唑[J]. 世界农药, 2001, 23(3): 52-53. Wu Bochun, Feng Huacheng. Triazole fungicides ipconazole and metconazole [J]. World Pestic, 2001, 23(3): 52-53. (in Chinese) |
| [2] | Konwick B J, Garrison A W, Avants J K, et al. Bioaccumulation and biotransformation of chiral triazole fungicides in rainbow trout (Oncorhynchus mykiss) [J]. Aquatic Toxicology, 2006, 80(4): 372-381. |
| [3] | Nguyen T D, Lee K J, Lee M H, et al. A multiresidue method for the determination 234 pesticides in Korean herbs using gas chromatography mass spectrometry [J]. Microchem J, 2010, 95(1): 43-49. |
| [4] | Nguyen T D, Han E M, Seo M S, et al. A multi-residue method for the determination of 203 pesticides in rice paddies using gas chromatography/mass spectrometry [J]. Analytica Chimica Acta, 2008, 619(1): 67-74. |
| [5] | Lozano A, Rajski L, Uclés S, et al. Evaluation of zirconium dioxide-based sorbents to decrease the matrix effect in avocado and almond multiresidue pesticide analysis followed by gas chromatography tandem mass spectrometry [J]. Talanta, 2014, 118: 68-83. |
| [6] | Pizzutti I R, de Kok A, Zanella R, et al. Method validation for the analysis of 169 pesticides in soya grain, without clean up, by liquid chromatography-tandem mass spectrometry using positive and negative electrospray ionization [J]. J Chromatogr A, 2007, 1142(2): 123-136. |
| [7] | Walorczyk S. Development of a multi-residue method for the determination of pesticides in cereals and dry animal feed using gas chromatography-tandem quadrupole mass spectrometry II. Improvement and extension to new analytes [J]. J Chromatogr A, 2008, 1208(1/2): 202-214. |
| [8] | 中国农业科学院农业产品质量标准与检测技术研究所. 农产品质量安全风险评估:原理、方法和应用[M]. 北京:中国标准出版社, 2007. Institute of Quality Standards and Testing Technology for Agro-products Chinese Academy of Agricultural Science. Risk assessment for quality and safety of agro-foods: principles methodologies and applications [M]. Beijing: Standards Press of China, 2007. (in Chinese) |
| [9] | Tsakiris I N, Goumenou M, Tzatzaraki MN, et al. Risk assessment for children exposed to DDT residues in various milk types from the Greek market [J]. Food Chem Toxicol, 2015, 75, 156-165. |
| [10] | FAO/WHO, Food Standards Programme, Codex Alimentarius Commission. Report of 45th session of the codex committee on pesticides residues[R].2008.. |
| [11] | Tomlin C D S. The e-Pesticide Manual[CP/DK]. Version 5.0, 2009-2010, British Crop Production Council. |
| [12] | 张志恒, 袁玉伟, 郑蔚然, 等. 三唑磷残留的膳食摄入与风险评估[J]. 农药学学报, 2011, 13(5): 485-495. Zhang Zhiheng, Yuan Yuwei, Zheng Weiran, et al. Dietary intake and its risk assessment of triazophos residue [J]. Chin J Pestic Sci, 2011, 13(5): 485-495. (in Chinese) |
| [13] | 金水高. 中国居民营养与健康状况调查报告之十:2002年营养与健康状况数据集[M]. 北京:人民卫生出版社, 2008. Jin Shuigao. The tenth report of nutrition and health status for China residents: nutrition and health status of annual 2002 [M]. Beijing: People's Medical Publishing House, 2008. (in Chinese) |
 2015, Vol. 17
2015, Vol. 17


