苯氧威(fenoxycarb,Scheme 1)是具有保幼激素活性的非萜烯类昆虫生长调节剂,于1982年由瑞士Dr. R. Maag(现属先正达公司)发现并开发。与传统杀虫剂作用于昆虫神经系统的机制不同,苯氧威主要通过影响昆虫体内保幼激素水平而抑制昆虫的生长,其杀虫谱广,具有胃毒、触杀以及杀卵作用,可用于防治林业、果树害虫、仓储害虫以及农田害虫[1, 2, 3],也可在水域中撒施防治蚊类幼虫[4, 5]。
 | Scheme 1 |
苯氧威在生产中应用广泛,但有研究表明其对一些有益生物可产生不良影响。尹素芳等研究发现,苯氧威对天敌异色瓢虫成虫有触杀作用,并且能抑制其产卵及发育[6];朱忠林等发现苯氧威对鲤鱼具有中等毒性[7]。深入研究苯氧威对鱼类不同发育阶段的毒性作用,将有利于指导其安全合理使用,并可为评价该药剂对环境生态系统的影响奠定基础,但目前尚未见相关研究报道。笔者采用半静态方法,研究了苯氧威对斑马鱼胚胎、仔鱼、成鱼的急性毒性及对其胚胎卵黄囊仔鱼阶段的慢性毒性作用,结果报道如下。
1 材料与方法 1.1 供试材料 1.1.1 药剂及主要仪器设备
93.0%苯氧威(fenoxycarb)原药(河南省恒誉商贸有限公司),试验时准确称量一定量原药,用丙酮溶解并加入少量吐温-80助溶,配成系列浓度药液;丙酮(分析纯)、吐温-80(化学纯)(国药集团化学试剂有限公司)。
RXZ型智能光照培养箱(宁波江南仪器厂);GE-5爱国者数码观测王(北京华旗资讯科技发展有限公司);COIC双目显微镜(重庆光电仪器有限公司);HANNA-93735溶解氧分析仪、HANNA-98128 pH/温度计及HANNA-31625硬度仪(意大利哈纳公司);千分之一电子天平;爱生斑马鱼饲养设备、爱生斑马鱼产卵盒、玻璃鱼缸、广口塑料盒、酸度计等。
1.1.2 实验生物斑马鱼Brachydanio rerio:购于北京高峰水族馆,亲鱼体长3.00~4.00 cm,质量0.60~1.20 g,成鱼体长2.00~4.00 cm,质量0.20~0.40 g,在实验室条件下驯养不少于7 d。实验用水经曝气去氯处理,pH值为7.5±0.5,水中溶氧量大于空气饱和值的80%,水质硬度为(205±13) mg/L(以CaCO3计),温度为(27±1) ℃。采用自然光照与白炽灯光照。每天喂食2次搭配的混合饲料(市售成品饵料,含干虾及干红虫)。每天换水量为1/2。驯养期间死亡率小于5%。
斑马鱼胚胎:由亲鱼产卵所得。产卵前至少一周将雌、雄斑马鱼分开饲养,试验前一天上午8:00喂食后,将4条雌鱼、2条雄鱼放入专用产卵盒,用透明隔板隔开,傍晚时用黑布遮挡,于第二天早上7:00~7:30撤走黑布,抽掉隔板,借助微弱的光线刺激雌、雄鱼追逐产卵。收集0.5 h之内的新卵,用重组水迅速清洗鱼卵,去除杂物,获得胚胎。
斑马鱼仔鱼:由胚胎孵化而得。培养条件:实验用水为重组水,温度27~28 ℃,pH 7.5~8.5,14 h∶10 h昼夜光照比。重组水配制:称取2.94 g CaCl2·2H2O、1.23 g MgSO4·7H2O、1.065 g NaHCO3和0.06 g KCl溶解于10 L去离子水中,曝气至空气饱和值的80%以上,pH值在7.0~8.0之间,硬度为(204±6) mg/L(以CaCO3计)。
1.2 试验方法1.2.1 对成鱼和仔鱼的急性毒性试验
参照《化学农药环境安全评价试验准则》[8]中“鱼类毒性试验”和OECD 203准则[9]方法进行。在预试验基础上,分别配制系列质量浓度苯氧威药液:1.50、1.65、1.80、1.95、2.10 mg/L(成鱼),0.50、0.60、0.70、0.80、0.90、1.00 mg/L(孵化12 h仔鱼)和0.60、1.00、1.40、1.80、2.20 mg/L(孵化72 h仔鱼)。将不同发育阶段斑马鱼暴露在盛有相应试验药液的烧杯中,观察24、48、72及96 h时的死亡数和中毒症状。用玻璃棒轻触斑马鱼成鱼尾部,或者用软皮管轻吹仔鱼,无可见运动者视为死亡。每24 h更换3/4 体积药液。设助剂对照及空白对照。每处理设3次重复,每重复10条成鱼(仔鱼)。
1.2.2 对胚胎的毒性试验参照OECD 草案“鱼类胚胎急性毒性试验(FET)”[10]以及OECD 212准则[11]进行。挑选发育正常的斑马鱼受精卵,分别暴露于0.50、0.75、1.13、1.70、2.55、3.83 mg/L(急性毒性试验)或者0.10、0.20、0.40、0.60、0.80、1.00 mg/L(慢性毒性试验)的苯氧威药液中,设助剂对照(含吐温-80和丙酮,用量小于0.1 mL/L)和重组水空白对照。
急性毒性试验:将受精卵转移至24孔板中,其中20个孔为同一浓度的苯氧威药液,另外4个孔为空白对照。每孔2 mL药液、1枚受精卵,每处理含两个24孔板。慢性毒性试验:将10枚受精卵转移到盛有120 mL药液的烧杯中,每浓度设3次重复。将胚胎置于气候箱中,于温度27~28 ℃,14 h∶10 h昼夜光照比条件下培养。试验期间不喂食,每24 h更换3/4体积药液。
按照Nagel[12]的方法,分别于24、48、72及96 h时在显微镜下观察致死(lethal)效应(卵凝结、发育停滞、无心率等)、亚致死(sublethal)效应(孵化延迟、黑色素减弱、心率减缓或停止、自主运动次数减少等)和致畸(teratogenic)效应(脊柱弯曲、尾部畸形等)。
亚致死效应统计方法:每处理随机取10~12粒有活性的胚胎,24 h时在倒置显微镜下观察其自主运动情况,记录20 s内的自主运动次数,每枚胚胎统计两次,取平均值;48 h时观察记录20 s内的心率;于96 h或试验结束时,每处理随机取10~12条存活的孵化仔鱼,在数码观测王下测量其体长。于胚胎孵化后观察仔鱼的形态、行为等是否异常,统计每天孵化的仔鱼数量,计算孵化率与96 h孵化延迟率:孵化延迟率/%=(尚未孵化但仍有活性的胚胎数/暴露胚胎总数)×100。
1.3 数据分析采用机率值法计算药剂对斑马鱼胚胎、仔鱼、成鱼的半数致死浓度(LC50)。数据均以平均值±标准差(mean±SD)表示。用SPSS 16.0软件进行差异显著性分析,P<0.05表明差异显著。根据处理组和对照组的差异显著性,确定最低可观测效应浓度(lowest observed effect concentration,LOEC)和无可观测效应浓度(no observed effect concentration,NOEC)。
2 结果与分析 2.1 苯氧威对斑马鱼的急性毒性 2.1.1 苯氧威对不同发育阶段斑马鱼的急性毒性
试验结果表明:苯氧威对斑马鱼胚胎、仔鱼、成鱼的急性毒性均表现出明显的时间和剂量效应关系,即随着暴露时间延长和剂量增加,药剂毒性增大;不同发育阶段斑马鱼对苯氧威的敏感性不同,96 h-LC50值顺序依次为胚胎>仔鱼(3 d)>成鱼>仔鱼(12 h),表明孵化后12 h的仔鱼对苯氧威最敏感,成鱼次之,而胚胎的敏感性最低(表 1)。根据《化学农药环境安全评价试验准则》[8]中农药对鱼类的毒性等级划分标准,苯氧威对斑马鱼成鱼的急性毒性为中等毒。
| 表 1 苯氧威对不同发育阶段斑马鱼的急性毒性 Table 1 Acute toxicity of fenoxycarb to zebrafish embryos,larvae and adult zebrafish |
2.1.2 苯氧威对斑马鱼的亚致死效应
试验中观察发现:苯氧威处理使斑马鱼成鱼出现身体翻转、体背发黑、游动失衡、冲游等中毒症状;对胚胎和仔鱼则表现为亚致死效应:致使斑马鱼胚胎的自主运动及心率出现异常,胚胎发育停滞,头部不分化,身体及尾部不分节,心包囊肿,无黑色素富集或黑色素明显减弱,尾部发育畸形,孵化仔鱼脊柱弯曲以及鱼体发黑等(图 1)。
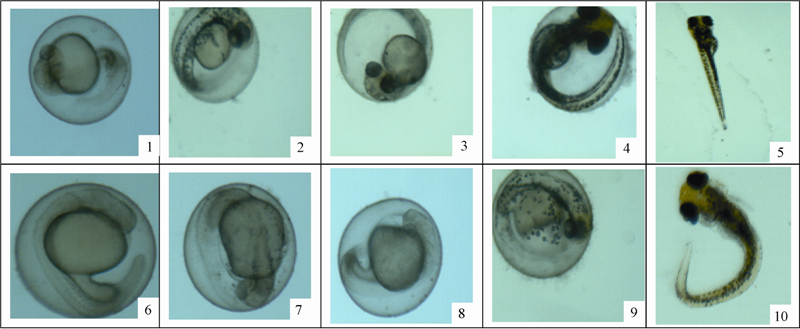 |
1~5为空白对照处理:1. 24 h正常发育胚胎;2和3. 48 h正常发育胚胎;4. 72 h正常发育胚胎;5. 72 h正常孵化的仔鱼。6~10为苯氧威处理:6. 24 h,发育缓慢;7和8. 48 h,心包囊肿; 9. 72 h,心包囊肿与尾部畸形;10. 仔鱼脊柱弯曲。 No.1-5 was control group: 1. normal embryo at 24 h; 2 and 3. normal embryo at 48 h; 4. normal embryo at 72 h;5. normal hatched larva at 72 h. No.6-10 was fenoxycarb-treated group: 6. retarded development of embryo at 24 h; 7 and 8. pericardial edema at 48 h; 9. abnormal tail and pericardial edema at 72 h; 10. axial malformation of larva. 图 1 苯氧威对斑马鱼胚胎和仔鱼的致畸效应(80×) Fig. 1 Teratogenic effects of fenoxycarb on embryos and larvae of zebrafish(80×) |
当苯氧威质量浓度为1.70 mg/L时,处理后24 h,胚胎20 s内自主运动的平均次数为空白对照组的65%,显著低于对照;当其质量浓度达到2.55 mg/L时,20 s内胚胎自主运动的平均次数仅为空白对照的31%,抑制作用更为明显。在上述两个质量浓度下,处理后48 h,胚胎20 s内的平均心率仅分别为空白对照的76%和53%,抑制作用显著。 2.2 苯氧威对斑马鱼胚胎卵黄囊仔鱼阶段的慢性毒性 2.2.1 苯氧威对24 h胚胎自主运动的影响
斑马鱼卵受精后,正常胚胎发育到24 h会出现有规律的自主运动,但暴露在苯氧威系列浓度药液中后,胚胎的自主运动次数减少(图 2),且随着药剂浓度升高,对胚胎自主运动的抑制作用增强,0.6 mg/L苯氧威处理组胚胎的自主运动次数显著低于对照。苯氧威对发育24 h斑马鱼胚胎自主运动的NOEC值为0.4 mg/L,LOEC值为0.6 mg/L。
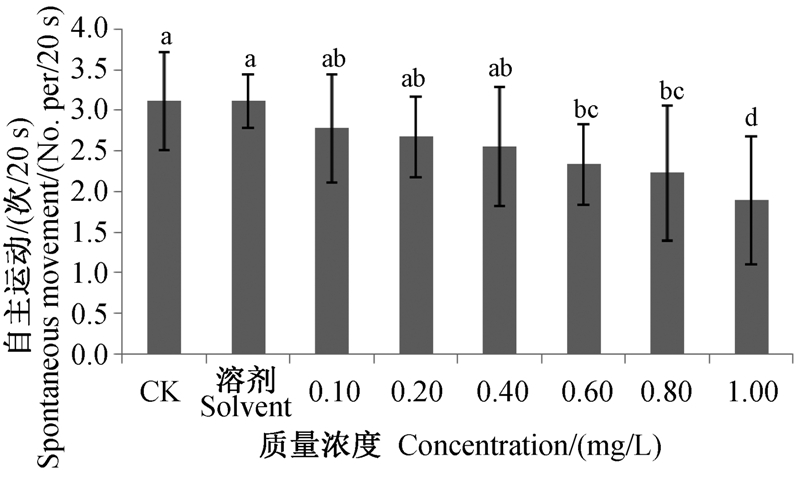 |
图中不同字母表示处理间差异显著(P<0.05)。 Different letters between treatment indicate significant difference(P<0.05). 图 2 苯氧威对发育24 h斑马鱼胚胎自主运动的影响 Fig. 2 Effect of fenoxycarb on the spontaneous movement of zebrafish embryos at 24 h |
斑马鱼胚胎正常发育到48 h会出现稳定的心率,但药剂暴露使得其心率降低,且随着药剂浓度增加,对心率的抑制程度增大(图 3)。苯氧威质量浓度为0.20 mg/L时,胚胎心率与对照组差异显著。苯氧威对斑马鱼48 h胚胎心率的NOEC值为0.10 mg/L,LOEC值为0.20 mg/L。
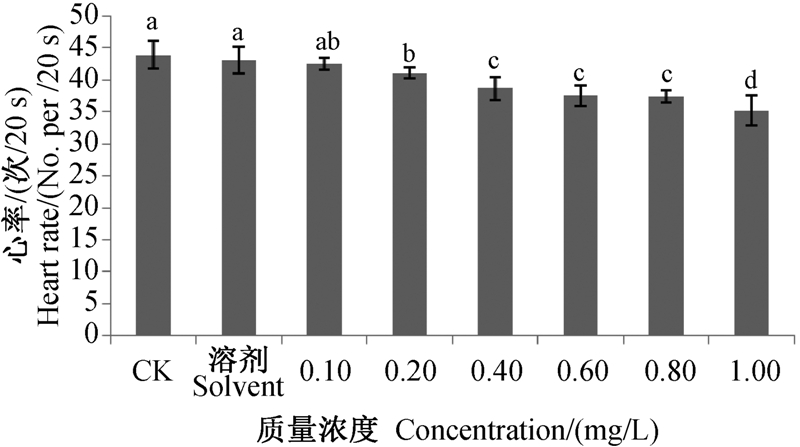 |
图中不同字母表示处理间差异显著(P<0.05)。 Different letters between treatment indicate significant difference(P<0.05). 图 3 苯氧威对斑马鱼48 h胚胎心率的影响 Fig. 3 Effect of fenoxycarb on the heart rate of zebrafish embryos at 48 h |
从图 4中可看出,随着苯氧威处理浓度的增加,仔鱼胚胎出现畸形(以心包囊肿计)的频率明显增大。苯氧威对72 h胚胎造成畸形的NOEC值为0.4 mg/L,LOEC值为0.6 mg/L。
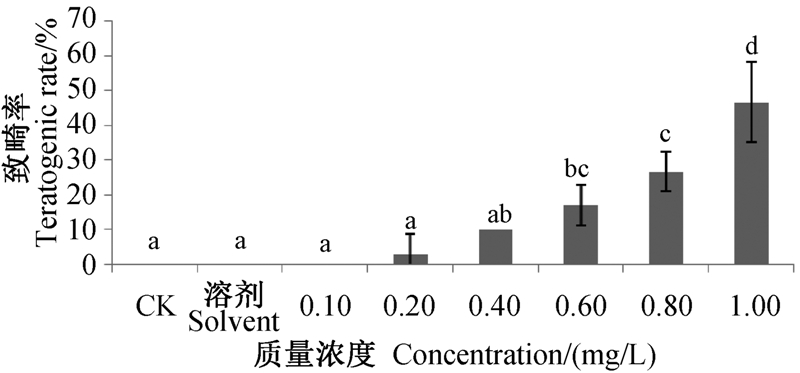 |
图中不同字母表示处理间差异显著(P<0.05)。 Different letters between treatment indicate significant difference(P<0.05). 图 4 苯氧威对斑马鱼72 h胚胎的致畸作用 Fig. 4 Teratogenic rate of zebrafish embryos at 72 h caused by fenoxycarb |
暴露11 d时,胚胎卵黄囊的营养被吸收完,因此结束试验。图 5表明,苯氧威对仔鱼体长有一定的影响,当药剂质量浓度达到0.80 mg/L时,仔鱼体长显著低于对照。苯氧威对仔鱼体长的NOEC值为0.60 mg/L,LOEC值为0.80 mg/L。
2.2.4 苯氧威对试验结束时仔鱼体长的影响
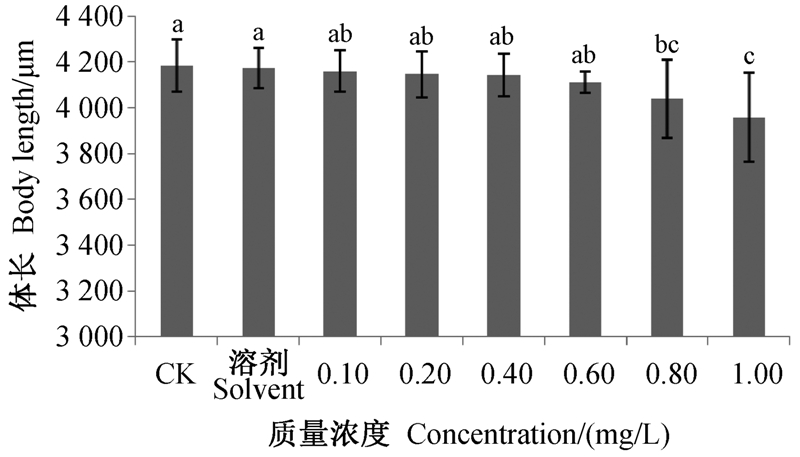 |
图中不同字母表示处理间差异显著(P<0.05)。 Different letters between treatment indicate significant difference(P<0.05). 图 5 苯氧威对孵化斑马鱼体长的影响(11 d) Fig. 5 Effect of fenoxycarb on body length of hatched larvae of zebrafish at the end of experiment(11 d) |
在本试验条件下,空白对照组在54 h左右开始孵化。从图 6中可看出:苯氧威对斑马鱼胚胎孵化有一定抑制作用,且随着药剂浓度的升高,60、72及96 h胚胎孵化率均呈下降趋势,并且出现了不同程度的孵化滞后现象,孵化延迟率呈增大趋势。
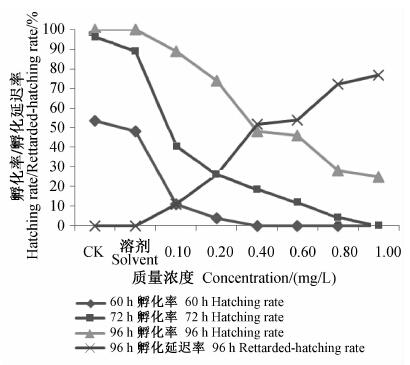 | 图 6 苯氧威对斑马鱼胚胎孵化的影响 Fig. 6 Effect of fenoxycarb on the hatching of zebrafish embryos |
已有研究表明,苯氧威对哺乳动物、鸟类和蜜蜂为低毒,但对鲤鱼的急性毒性为中等毒[7]。本研究中急性毒性试验结果表明,苯氧威对斑马鱼不同发育阶段的96 h-LC50值分别为:胚胎 2.35 mg/L、12 h仔鱼0.98 mg/L、72 h仔鱼1.87 mg/L、成鱼1.67 mg/L,根据《化学农药环境安全评价试验准则》[8]中农药对鱼类的毒性等级划分标准,苯氧威对斑马鱼成鱼的急性毒性等级为中等毒。比较不同发育阶段的96 h-LC50值可以看出,刚孵化的仔鱼是对外部环境最为敏感的阶段,这与三丁基锡对斑马鱼不同阶段的毒性试验结果相一致[13],提醒我们在今后的研究中应该更加关注对环境最为敏感的仔鱼初孵化阶段。胚胎对苯氧威的敏感性最低,可能是由于其外层的受精卵绒毛膜对药剂有抵御作用所致[13, 14],而仔鱼则失去了该层膜的保护,所以对药剂比较敏感。
胚胎卵黄囊仔鱼阶段慢性毒性试验结果表明:苯氧威对斑马鱼胚胎24 h自主运动、48 h心率、72 h畸形率及11 d孵化仔鱼体长均有不同程度的抑制作用,LOEC值分别为0.60、0.20、0.60和0.80 mg/L,而与之对应的NOEC值分别为0.40、0.10、0.40和0.60 mg/L。可以看出,斑马鱼胚胎的自主运动及心率、畸形变化都是比较敏感的毒理学指标,其中心率是斑马鱼胚胎对苯氧威最敏感的观察指标。试验中还发现,苯氧威对斑马鱼胚胎孵化率、试验结束时的仔鱼体长也有明显的抑制作用,而且可导致胚胎出现心包囊肿、尾部畸形、黑色素形成减弱、发育迟缓、脊柱弯曲等现象。
以上结果表明,苯氧威对斑马鱼不同发育阶段的急性和慢性毒性作用均不容忽视,因此在使用中应注意避免药剂对河流、池塘等水域的污染。
| [1] | 柳庆先. 苯醚威的杀虫特点及合成方法[J]. 农药, 2000, 39(3): 13-15. Liu Qingxian. Characteristics and synthesis of fenoxycarb[J]. Pesticides, 2000, 39(3): 13-15.(in Chinese) |
| [2] | 刘长令. 世界农药大全: 杀虫剂卷[M]. 北京: 化学工业出版社, 2012: 193-195. Liu Changling. Encyclopedia of Pesticide in the World: Insecticide[M]. Beijing: Chemical Industry Press, 2012: 193-195.(in Chinese) |
| [3] | 邹立亚, 陈军, 赫巍, 等. 3%高渗苯氧威防治美国白蛾药效筛选试验[J]. 中国森林病虫, 2006, 25(6): 37-39. Zhou Liya, Chen Jun, He Wei, et al. The efficacy tests of 3% high permeation fenoxycarb against Hyphantria cunea[J]. Forest Pest Dis, 2006, 25(6): 37-39.(in Chinese) |
| [4] | Mulla M S, Darwazeh H A, Ede L, et al. Laboratory and field evaluation of the IGR fenoxycarb against mosquitoes[J]. J Am Mosq Control Assoc, 1985, 1(4): 442-448. |
| [5] | Walker E D, Edman J D. Evaluation of fenoxycarb against spring Aedes mosquitoes in Massachusetts[J]. J Am Mosq Control Assoc, 1990, 6(4): 725-726. |
| [6] | 尹素芬, 赵鑫, 王丽晓, 等. 保幼激素类似物苯氧威对异色瓢虫不同发育阶段的影响[J]. 昆虫学报, 2009, 52(11): 1213-1222. Yin Sufen, Zhao Xin, Wang Lixiao, et al. Effects of fenoxycarb, a juvenile hormone analog, on various developmental stages of Harmonia axyridis (Pallas)(Coleoptera: Coccinellidae)[J]. Acta Entomologica Sinica, 2009, 52(11): 1213-1222.(in Chinese) |
| [7] | 朱忠林, 单正军, 蔡道基. 苯氧威对环境生物的安全评价[J]. 农药科学与管理, 2000, 21(6): 12-15. Zhu Zhonglin, Shan Zhengjun, Cai Daoji. Safety evaluation of fenoxycarb on environmental organisms[J]. Pest Sci Admin, 2000, 21(6): 12-15.(in Chinese) |
| [8] | 南京环境科学研究所. 化学农药环境安全评价试验准则(续)[J]. 农药科学与管理, 1990(4): 4-9. Nanjing Institute of Environmental Sciences. Guidelines for testing and assessing environmental safety of chemical pesticides(continue)[J]. Pest Sci Admin, 1990(4): 4-9.(in Chinese) |
| [9] | OECD. OECD guidelines for the testing of chemicals, fish, acute toxicity test [S]. 1992-07-17. |
| [10] | OECD guidelines for the testing of chemicals. Draft proposal for a new guideline, fish embryo toxicity(FET) test[S]. 2006-05-30. |
| [11] | OECD. OECD guidelines for the testing of chemicals, fish, short-term toxicity test on embryo and sac-fry stages[S]. 1998-09-21. |
| [12] | Nagel R. The embryo test with the Zebrafish Danio rerio:a general model in ecotoxicology and toxicology[J]. ALTEX, 2002, 19(Suppl.1): 38-48. |
| [13] | Fent K, Meier W. Tributyltin-induced effects on early life stages of minnows Phoxinus phoxinus[J]. Arch Environ Contam Toxicol, 1992, 22(4): 428-438. |
| [14] | 刘迎, 胡燕, 姜蕾, 等. 5种酰胺类除草剂对斑马鱼胚胎发育的毒性效应[J]. 农药, 2014, 53(11): 806-808. Liu Ying, Hu Yan, Jiang Lei, et al. The toxicity effects of five amide herbicides on embryo development of zebrafish[J]. Agrochemicals, 2014, 53(11): 806-808.(in Chinese) |
 2015, Vol. 17
2015, Vol. 17


