2. 海南师范大学 化学与化工学院, 海口 571100
2. College of Chemistry and Chemical Engineering, Hainan Normal University, Haikou 571100, China
农药水乳剂是指在表面活性剂的作用下,将一种不溶或难溶于水的液体原药或原药的有机溶液分散于水中所形成的分散体系。与乳油相比,水乳剂可大大减少有机溶剂用量,降低农药制剂的毒性及危险性,已成为国际上公认的绿色环保制剂[1]。目前制约水乳剂发展的主要问题是产品的稳定性及货架期[2]。现有水乳剂大多采用小分子表面活性剂作为稳定剂[3, 4],导致体系难以长时间保持稳定。因此,在实际应用中可通过加入一定量的聚合物而提高农药水乳剂的稳定性。吸附型聚合物(蛋白质[5, 6]、嵌段聚合物[7, 8]和疏水改性的多糖[9, 10, 11, 12]等) 可通过空间效应在液滴表面形成界面膜、阻止液滴相互靠近而达到稳定的效果;非吸附型聚合物(如黄原胶[13])则可通过增大连续相的黏度来减缓乳液沉降的速度。虽然通过加入多糖提高农药悬浮剂稳定性[14, 15]的工艺已经很成熟,但由于其黏度一般在500~1 000 mPa ·s,而农药水乳剂黏度只有几十毫帕 ·秒,因此不能直接沿用农药悬浮剂的稳定原理。同时,由于普通聚合物或亲水性太差,或亲油性太差,加入后对提高水乳剂稳定性作用不明显,所以有必要对聚合物进行改性使其具有两亲性。Sovilj 等[9]研究了疏水改性的纤维素衍生物羟丙甲基纤维素(HPMC)对以十二烷基硫酸钠(SDS)为稳定剂的乳液体系稳定性的影响,发现向体系中加入HPMC后,载药的SDS液滴可吸附在HPMC疏水基团上,所形成的较大分子结构可起到空间障碍的作用,从而增强乳液体系的稳定性。
笔者以从海藻中提取的天然可再生多糖聚合物海藻酸钠为原料,通过接枝改性制备了具有两亲性的多糖衍生物,研究了其对以绿色非离子型表面活性剂烷基糖苷为稳定剂的高效氯氟氰菊酯水乳剂的静置稳定性、离心稳定性、分散稳定性、冻融稳定性、液滴粒径、Zeta电位及黏度的影响及其作用机理。同时采用差示扫描量热仪(DSC) 研究了乳液的结晶行为,将其热力学性质与乳液的组成相结合,确定了影响体系冻融稳定性的因素。所得结果还可为差示扫描量热技术在农药水乳剂稳定性表征方面应用提供参考。 1 材料与方法 1.1 试剂及主要仪器
97%高效氯氟氰菊酯(lambda-cyhalothrin)原药(工业级,海南博科科技有限公司);海藻酸(化学纯),胆固醇、氢化钙、二甲基亚砜(DMSO)、N,N′-二环己基碳酰亚胺(DCC)及4-二甲氨基吡啶(DMAP)均为分析纯(阿拉丁试剂公司);三氯甲烷、氢氧化钠、碳酸氢钠、二甲苯及无水乙醇均为分析纯(广州化学试剂厂);烷基糖苷 APG1214(工业级,上海发凯化工有限公司);超纯水。
T25高剪切乳化机(德国IKA公司);JS94H微电泳仪(上海中晨公司);DV-II+PRO黏度计(美国BROOKFIELD公司);Nano ZS 90动态激光散射仪(英国Malvern公司);Turbiscan Lab分散稳定仪(法国Formulaction公司);Q100差式扫描量热仪(美国TA仪器公司);DF-101S集热式磁力加热搅拌器(金坛市医疗仪器厂);BSA124S-CW分析天平(精度为0.01 mg,赛多利斯公司);H-1650台式高速离心机(湘仪离心机仪器有限公司);TENSOR27傅立叶红外光谱仪及DMX500核磁共振波谱仪(瑞士Bruker公司);CS101-1AB电热鼓风干燥箱(重庆银河实验仪器有限公司);769YP-15A粉末压片机(天津市科器高新技术公司)。 1.2 两亲性海藻酸钠衍生物的制备与表征
如图 1所示,胆固醇改性海藻酸钠衍生物(CSAD)是一种在海藻酸钠骨架上通过酯化反应接枝胆固醇分子的两亲性物质。其衍生化方法[16]为:将海藻酸和胆固醇分散于溶剂中,以DCC和DMAP为催化剂,在室温下反应制得。通过傅里叶红外光谱仪、核磁共振波谱仪对产物进行表征。
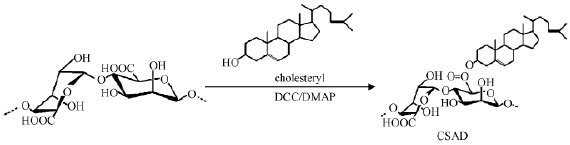 | 图 1 胆固醇改性海藻酸钠衍生物的合成过程Fig. 1 Main process of synthesis of amphiphilic cholesteryl grafted sodium alginate derivative(CSAD) |
将高效氯氟氰菊酯原药先溶解于适量二甲苯中,再加入到一定量的APG中作为油相;将不同含量的CSAD溶解在超纯水中作为水相;将水相和油相混合,在13 000 r/min下乳化20 min制得。制剂中高效氯氟氰菊酯、APG和二甲苯的质量分数分别为2%、4%和6%。 1.4 水乳剂稳定性测定
静置稳定性:通过测定乳液体积分数变化进行表征。将约20 mL新制备的乳液装入玻璃比色管,常温密封存放,记录乳液初始体积,每隔5 d记录乳液体积及外观变化。
离心稳定性:按GB11543—2008中方法[17]测定。将10 mL乳液注入离心管,于4 000 r/min下离心10 min,测量离心分层后乳液体积Vt,以Vr/%=(Vt/10)×100表示水乳剂的离心稳定性。
分散稳定性:取20 mL乳液加入圆柱形平底玻璃瓶中,重复3次,保证每次高度一致(40 mm)。旋紧瓶盖,平移入Turbiscan Lab分散稳定性分析仪进行测试。所有试验均在36 ℃±0.5 ℃下进行,每次测试6 h,扫描间隔3 min。采用Turbiscan Easysoft 软件对数据进行处理,得到水乳剂的稳定性参数(SI)。SI值越小,表明体系越稳定。
冻融稳定性:采用差示扫描量热(DSC)法测定。仪器于20 ℃稳定平衡1 h后,取约25 μ g样品测定。样品从20 ℃以1.5 ℃/min冷却到-30 ℃,之后再逐渐回升至20 ℃,为一个循环。根据扫描谱图分析样品的共晶点和熔点变化。 1.5 Zeta电位测定
采用微电泳仪于室温下测定0.5 mL稀释后乳液的Zeta电位,重复3次,取平均值。 1.6 液滴粒径测定
于25 ℃、633 nm、90°散射角下,取制备 24 h 的乳液0.5 mL,经0.22 μ m滤膜过滤后用超纯水稀释至10 mL,采用激光粒度仪测量其粒径及分布。据文献报道,适度稀释不会影响乳液液滴的粒径[18]。 1.7 水乳剂黏度测定
采用DV-II+PRO黏度计,于乳液发生相分离前在室温下测量其黏度,重复3次,取平均值。
2 结果与讨论
2.1 两亲性海藻酸钠衍生物(CSAD)的结构表征
由于海藻酸分子链上存在大量羟基和羧基,亲水性较强,因此限制了其在药物乳液方面的应用。胆固醇是环戊烷多氢菲衍生物,具有很强的疏水能力。本研究利用海藻酸的羧基与胆固醇的羟基在偶联剂 DCC 与催化剂 DMAP 的脱水和催化作用下发生酯化反应,制备了两亲性多糖聚合物CSAD。
改性前后化合物的红外光谱图见图 2。相对于海藻酸钠,胆固醇改性海藻酸钠(CSAD)在 1 735 cm -1处新出现的峰为酯键的吸收峰,同时其在 2 851 cm-1处出现的峰为亚甲基的碳氢伸缩振动吸收峰。而海藻酸钠自身分子结构中并没有亚甲基的存在,由此可证明海藻酸钠的羧基与胆固醇的羟基发生了酯化反应。
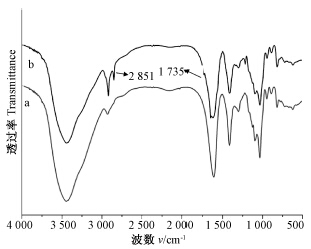 | (a)海藻酸钠 (Sodium alginate); (b)胆固醇改性海藻酸钠(CSAD)。图 2 海藻酸钠和胆固醇改性海藻酸钠的红外光谱图Fig. 2 FTIR spectra of sodium alginate and CSAD |
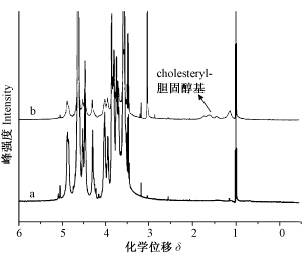
改性前后化合物的核磁共振氢谱比较见图 3。与海藻酸钠相比,CSAD在化学位移(δ)1.1~1.8处新出现的吸收峰为胆固醇分子上的亚甲基质子共振峰,由此进一步证明胆固醇成功接枝到了海藻酸钠分子链上。根据公式(1)可计算改性海藻酸钠中胆固醇的接枝率(DSchol)[19]。
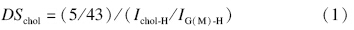
 | (a)海藻酸钠(Sodium alginate);(b)胆固醇改性海藻酸钠(CSAD)图 3 海藻酸钠和胆固醇改性海藻酸钠的核磁共振氢谱图Fig. 3 H NMR spectra of sodium alginate and CSAD |
式中,Ichol-H为胆固醇分子质子峰积分强度,IG(M)\|H为海藻酸钠骨架质子峰积分强度。本研究中改性海藻酸钠的接枝率约为4.56%。 2.2 CSAD对水乳剂稳定性的影响
从图 4可知,不同质量浓度CSAD对乳液体积分数的影响非常显著,当其在0.2~1.0 g/L范围内时,水乳剂体系中乳液的体积分数均保持在90%以上,仅在表面出现很薄的浑浊层,并且在3个 月内可保持稳定不变;当CSAD质量浓度大于2.0 g/L时,水乳剂稳定性逐渐降低,仅几天后即出现油、水分离现象。说明加入较低浓度的CSAD可提高水乳剂的稳定性,但当其浓度过高时反而会加速乳液破乳。
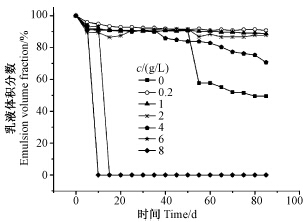 | 图 4 不同胆固醇改性海藻酸钠浓度下高效氯氟氰菊酯水乳剂稳定性随时间变化情况Fig. 4 Variation of stability with storage time for emulsions in the presence of CSAD with different concentrations |
从图 5中可看出:向体系中加入0.2~1.0 g/L的CSAD时,乳液离心系数Vr 增大,水乳剂稳定性提高;而当CSAD质量浓度大于1.0 g/L时,乳液Vr 值逐渐降低,水乳剂稳定性也逐步下降。
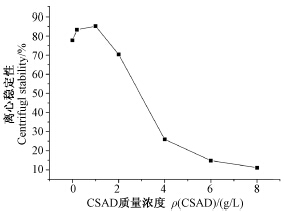 | 图 5 不同浓度胆固醇改性海藻酸钠对高效氯氟氰菊酯水乳剂离心稳定性的影响Fig. 5 Variation of centrifugl stability for emulsions in the presence of CSAD with different concentrations |
随测试时间延长,不同CSAD浓度下乳液的分散稳定性参数(SI)均有所增大,最终趋向平稳(图 6)。但总体来看,CSAD质量浓度在0.2~1.0 g/L范围内时,乳液SI值较空白对照均表现为下降,水乳剂稳定性增强;当CSAD质量浓度继续增大,则SI值明显增大,水乳剂稳定性降低。
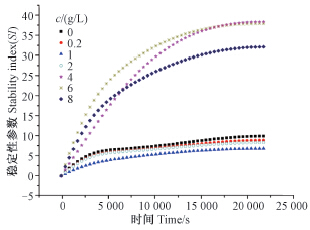 | 图 6 不同胆固醇改性海藻酸钠浓度下高效氯氟氰菊酯水乳剂稳定性参数随时间变化情况Fig. 6 Variation of stability index with storage time for emulsions in the presence of CSAD with different concentrations |
综上所述,分散稳定性分析仪分析结果与静置稳定性和离心稳定性测试结果基本一致,即当CSAD浓度较低时可提高水乳剂的稳定性,其浓度过高则会加速乳液破乳,反而不利于水乳剂稳定。
对低浓度的CSAD而言,由于胆固醇中疏水基团的存在,使得海藻酸衍生物可以固定在液滴表面,同时由于海藻酸盐自身带负电,可增强液滴间的静电作用效果,阻止乳液聚沉;此外因CSAD自身具有亲水骨架,可分散在连续相中,从而增大乳液的空间效应,进一步阻碍了乳液液滴的聚集;因此,低浓度的CSAD可与APG形成混合胶束,通过空间效应和静电效应协同稳定水乳剂体系[20]。当CSAD浓度升高时,液滴排除絮凝作用效应增强,使液滴之间发生桥梁絮凝,乳液稳定性下降。作为一种聚电解质类聚合物,虽然经过疏水改性使其成为了具有高分子表面活性剂性能的衍生物,但由于CSAD的接枝率相对较低,因此当其浓度过高时,聚合物亲水性骨架吸附在乳液液滴表面的作用降低,转而趋向于分散到水相中,并逐步形成微环境的渗透压,进而压缩液滴之间的距离。根据DLVO理论[21]: V=V\-A+V\-R, 随着粒子的靠近,吸引能VA、排斥能VR均有所增大,但当粒子距离很小时,吸引能剧增,使相吸力占优势,总势能V变为负值,液滴发生聚集,从而导致乳液的破坏。Ye等[22]在研究以黄原胶为稳定剂乳液的稳定性时同样发现了排除絮凝的现象。 2.3 CSAD对水乳剂冻融稳定性的影响
在实际应用中,当水乳剂处于低温环境时会出现油相结晶、冰晶形成、界面相转化等过程[23, 24],从而导致乳液破乳。同时,乳液晶点受乳化剂种类、液滴粒径、助表面活性剂等因素的影响,因此可通过差示扫描量热(DSC)法研究乳液的结晶行为,并进一步确定影响乳液冻融稳定性的主要因素,以助于选择合适的水乳剂配方。
图 7和图 8分别为高效氯氟氰菊酯水乳剂的DSC冷冻和加热热力学分析图谱。从图 7中可看出:随CSAD浓度增大,乳液的晶点明显向低温偏移,直到其质量浓度为2.0 g/L时晶点温度才又有所升高,其结晶温度范围为-18.06~-13.25 ℃。分析可能是由于随着CSAD的加入,乳液液滴开始在其疏水基上吸附,并逐渐形成混合胶束,尽管液滴粒径有一定程度的增大,但因其较大的 分子结构可起到空间障碍的作用,阻止液滴聚并,妨碍晶相形成,因而使得乳液结晶温度下降[25]。同时随乳液黏度逐渐变大,空间效应增强,可机械地阻止液滴聚集,阻碍冰晶的形成及扩大,同样也使得结晶温度降低,乳液低温稳定性升高。然而,随着排除絮凝作用的加强,双电层及界面膜厚度被压缩,冰晶易于穿透界面膜,使乳液破乳,结晶温度升高[26]。上述理论可以合理地解释乳液的结晶行为。由图 8可见,乳液的加热DSC曲线只有一个吸热峰,而且不同浓度下的吸热峰几乎未发生偏移,其熔点范围为-1.30~-1.06 ℃,表明CSAD对乳液的熔点几乎没有影响。
 | 图 7 高效氯氟氰菊酯水乳剂的差示扫描量热分析冷冻曲线(20℃~-30℃)Fig. 7 DSC cooling curves of emulsions(20 ℃ to -30 ℃) |
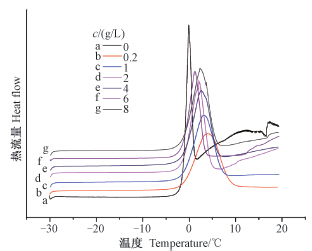 | 图 8 高效氯氟氰菊酯水乳剂的差示扫描量热分析加热曲线(-30℃~20℃)Fig. 8 DSC heating curves of emulsions (-30 ℃ to 20 ℃) |
结晶温度可以反映乳液的冻融稳定性[23]。研究表明,加入CSAD后乳液的冻融稳定性明显提高,尤其是当其质量浓度在1.0~2.0 g/L范围内时。 2.4 CSAD对水乳剂Zeta电位的影响
由图 9可看出,乳液液滴Zeta电位随CSAD质量浓度的增大先升高,到达最大值后再急剧下降,之后缓慢降低。这是因为当CSAD浓度较低时,液滴吸附到其疏水端形成混合胶束,液滴表面所带电荷量变大,使得胶束间的排斥力增大,从而提高了乳液的稳定性;随着CSAD质量浓度继续升高,排除絮凝作用的效应增强,CSAD因静电作用被挤出液滴之间的微环境,不断进入到水相中,导致液滴表面带电量降低,水乳剂发生絮凝,因而稳定性变差。
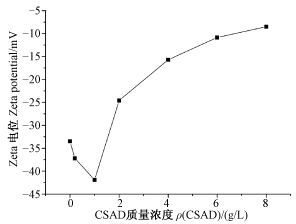 | 图 9 不同浓度胆固醇改性海藻酸钠对高效氯氟氰菊酯水乳剂Zeta电位的影响Fig. 9 Variation of Zeta potential of emulsions in the presence of CSAD with different concentrations |
如图 10所示,乳液液滴粒径随CSAD质量浓度升高先增大,到达最大值后再急剧变小,之后缓慢变小,这与Zeta电位测试结果趋势一致,其原因也类似:当CSAD质量浓度较低时,液滴吸附到其疏水端形成混合胶束,导致粒径增大,在空间位阻效应的影响下,提高了乳液的稳定性;随着CSAD浓度继续增大,排除絮凝作用增强,CSAD因静电作用被挤出液滴之间的微环境,不断进入到水相中,进而形成渗透压,乳液液滴之间的连续相在渗透压作用下被挤出,液滴之间距离被拉近,导致其吸引力进一步增大,液滴双电层被压缩,从而使得粒径降低;当CSAD浓度进一步增大,聚合物在乳液中不断聚集,直至连续相中的聚合物浓度达到一个恒定值,则液滴粒径变化趋于平稳。
 | 图 10 不同浓度胆固醇改性海藻酸钠对高效氯氟氰菊酯水乳剂液滴粒径和黏度的影响Fig. 10 Variation of droplets diameter and viscosity for emulsions in the presence of CSAD with different concentrations |
不同浓度CSAD下乳液的流变学行为研究结果如图 10所示。乳液的黏度随CSAD浓度增加而逐渐变大(15.4~55.7 mPa ·s)。起初黏度增大较 慢,结合粒径分析结果,表明在CSAD浓度较低时形成了混合胶束,该混合胶束受空间位阻效应的影响,机械强度变大,使得乳液黏度增大;同时液滴带电量增大,由于其电黏性效应[22],导致乳液黏度进一步增大。而当CSAD质量浓度大于4.0 g/L时,由于液滴之间的排除絮凝作用以及CSAD开始在乳液中形成弱凝胶,导致体系黏度急剧上升[27],乳液稳定性降低。
图 11为笔者总结归纳的CSAD-APG促进高效氯氟氰菊酯水乳剂稳定的机理:经疏水改性后,CSAD的疏水基团可向APG形成的乳液液滴间渗透,使液滴能够吸附到聚合物分子上形成混合胶束,大大提高乳液的黏度,从而通过空间位阻效应有效地阻止液滴之间的聚结,改善了水乳剂的稳定性。
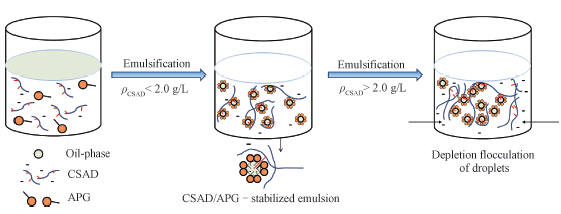 | 图 11 胆固醇改性海藻酸钠/烷基糖稳定水乳剂的机理Fig. 11 Proposed mechanism for CSAD/APG-stabilized emulsion |
本研究通过对海藻酸钠进行疏水接枝改性,成功制备了双亲性CSAD,通过其对以APG为稳定剂的高效氯氟氰菊酯水乳剂液滴粒径、Zeta电位及黏度的影响分析,阐明了CSAD-APG促进乳液稳定的机理,证明了选择合适配比的CSAD-APG体系可以制备长期稳定性较好的高效氯氟氰菊酯水乳剂。所得结果可为制备在常温和低温下稳定性良好的水乳剂提供参考。
| [1] | 张晓光, 刘洁翔, 王海英, 等. 阿维菌素水乳剂的稳定性[J]. 物理化学学报, 2010, 26(3): 617-625. Zhang Xiaoguang, Liu Jiexiang, Wang Haiying, et al. Stability of avermyctin emulsion in water[J]. Acta Phys-Chim Sin, 2010, 26(3): 617-625. (in Chinese) |
| [2] | Zhang Xiaoguang, Liu Jiexiang. Effect of arabic gum and xanthan gum on the stability of pesticide in water emulsion[J]. J Agric Food Chem, 2011, 59(4): 1308-1315. |
| [3] | Casanova H, Araque P, Ortiz C. Nicotine carboxylate insecticide emulsions: effect of the fatty acid chain length[J]. J Agric Food Chem, 2005, 53(26): 9949-9953. |
| [4] | Casanova H, Ortiz C, Peláez C, et al. Insecticide formulations based on nicotine oleate stabilized by sodium caseinate[J]. J Agric Food Chem, 2002, 50(22): 6389-6394. |
| [5] | Benichou A, Aserin A, Garti N. W/O/W double emulsions stabilized with WPI-polysaccharide complexes[J]. Colloids Surf A, 2007, 294(1-3): 20-32. |
| [6] | Sun Changhui, Gunasekaran S, Richards M P. Effects of protein concentration and oil-phase volume fraction on the stability and rheology of menhaden oil-in-water emulsions stabilized by whey protein isolate with xanthan gum[J]. Food Hydrocolloid, 2009, 23(1): 165-174. |
| [7] | Pons R, Solans C, Tadros T F. Rheological behavior of highly concentrated oil-in-water(O/W) emulsions[J]. Langmuir, 1995, 11(6): 1966-1971. |
| [8] | Barnes T J, Prestidge C A. PEO-PPO-PEO block copolymers at the emulsion droplet water interface[J]. Langmuir, 2000, 16(9): 4116-4121. |
| [9] | Sovilj V J, Petrovic L B. Influence of hydroxypropylmethyl cellulose-sodium dodecylsulfate interaction on the solution conductivity and viscosity and emulsion stability[J]. Carbohydr Polym, 2006, 64(1): 41-49. |
| [10] | Sun Wenbin, Sun Dejun, Wei Yunping, et al. Oil-in-water emulsions stabilized by hydrophobically modified hydroxyethyl cellulose: adsorption and thickening effect[J]. J Colloid Interf Sci, 2007, 311(1): 228-236. |
| [11] | Akiyama E, Kashimoto A, Fukuda K, et al. Thickening properties and emulsification me-chanisms of new derivatives of polysaccharides in aqueous solution[J]. J Colloid Interf Sci, 2005, 282(2): 448-457. |
| [12] | Karlberg M, Thuresson K, Lindman B. Hydrophobically modified ethyl(hydroxyethyl) cellulose as stabilizer and emulsifying agent in macroemulsions[J]. Colloids Surf A, 2005, 262(1-3): 158-167. |
| [13] | Sun Changhui, Gunasekaran S, Richards M P. Effect of xanthan gum on physicochemical properties of whey protein isolate stabilized oil-in-water emulsions[J]. Food Hydrocolloid, 2007, 21(4): 555-564. |
| [14] | 沈娟, 黄啟良, 夏建波, 等. 分散剂及黄原胶对多菌灵悬浮剂流变性质的影响[J]. 农药学学报, 2008, 10(3): 354-360. Shen Juan, Huang Qiliang, Xia Jianbo, et al. The effects of dispersant and xanthan gum to rheological property of carbendazim suspension[J]. Chin J Pestic Sci, 2008, 10(3): 354-360. (in Chinese) |
| [15] | 刘月. 20%灭幼脲水悬浮剂的物理稳定性研究[D]. 泰安: 山东农业大学, 2009. Liu Yue. Studing on the physcial of dichlorbenzuron 20% SC[D]. Taian: Shandong Agricultural University, 2009. (in Chinese) |
| [16] | 颜慧琼, 李嘉诚, 冯玉红, 等. 改性海藻酸钠活化SiO2纳米粒子稳定载药Pickering乳液及释药性[J]. 高等学校化学学报, 2013, 34(9): 2164-2179. Yan Huiqiong, Li Jiacheng, Feng Yuhong, et al. Stability and release properties of drug-loaded Pickering emulsions by the modified sodium alginate activated SiO2 nanoparticles[J]. Chem J Chin Univ, 2013, 34(9): 2164-2179. (in Chinese) |
| [17] | GB/T 11534—2008. 表面活性剂中、高粘度乳液的特性测试及其乳化能力的评价方法[S]. 北京: 中国标准出版社, 2008. GB/T 11534—2008. Surface active agents:the identification of emulsion for moderate to high viscosity and the evaluation method of emulsifying capability[S]. Beijing: China Standards Press, 2008. |
| [18] | Zhang Xiaoguang, Liu Jiexiang, Fan Zhijin. Stability of etofenprox in water emulsion induced by block copolymer and surfactant[J]. Colloids Surf A, 2013, 422: 191-198. |
| [19] | Yang Liqun, Zhang Bifang, Wen Liqun, et al. Amphiphilic cholesteryl grafted sodium alginate derivative: synthesis and self-assembly in aqueous solution[J]. Carbohydr Polym, 2007, 68(2): 218-225. |
| [20] | Jayme M L, Dunstan D E, Gee M L. Zeta potentials of gum arabic stabilised oil in water emulsions[J]. Food Hydr, 1999, 13(6): 459-465. |
| [21] | 陈宗淇, 王光信, 徐桂英. 胶体与界面化学[M]. 北京: 高等教育出版社, 2001: 93-104,159-183. Chen Zongqi, Wang Guangxin, Xu Guiying. Colloid and Interface Chemistry[M]. Beijing: High Education Press, 2001: 93-104,159-183. (in Chinese) |
| [22] | Ye A, Hemar Y, Singh H. Enhancement of coalescence by xanthan addition to oil-in-water emulsions formed with extensively hydrolysed whey proteins[J]. Food Hydr, 2004, 18(5): 737-746. |
| [23] | Bamba J, Cavé G, Bensouda Y, et al. Cryoprotection of emulsion in freeze-drying: freezing process analysis[J]. Drug Dev Ind Pharm, 1995, 21(15): 1749-1760. |
| [24] | McClements D J. Protein-stabilized emulsions[J]. Curr Opin Colloid Interface Sci, 2004, 9(5): 305-313. |
| [25] | Palanuwech J, Coupland J N. Effect of surfactant type on the stability of oil-in-water emulsions to dispersed phase crystallization[J]. Colloids Surf A, 2003, 223: 251-262. |
| [26] | Thanasukarn P, Pongsawatmanit R, McClements D J. Influence of emulsifier type on freeze-thaw stability of hydrogenated palm oil-in-water emulsions[J]. Food Hydr, 2004, 18(6): 1033-1043. |
| [27] | Mandala I G, Savvas T P, Kostaropoulos A E. Xanthan and locust bean gum influence on the rheology and structure of a white model-sauce[J]. J Food Eng, 2004, 64(3): 335-342. |
 2015, Vol. 17
2015, Vol. 17


