2. 上海化工研究院, 上海 200062
2. Shanghai Research Institute of Chemical Industry, Shanghai 200062, China
有机磷农药(OPPs)因具有广谱、 高效、 品种多和残留期短等特点[1]而被广泛应用于防治田间害虫,也由此带来了农产品、食品及土壤中的农药残留和环境污染等问题[2, 3]。硫代磷酸酯类杀虫剂(DDPs)是一类重要的有机磷杀虫剂,其活化代谢产物对胆碱酯酶(ChE)能产生很强抑制作用[4],但由于使用浓度低,导致其残留检测非常困难[5];另外,一些中低毒性的 DDPs(如甲基立枯磷、三唑磷和毒死蜱等)作为高毒农药替代品正在农业生产中广泛应用[6, 7]。 因此,开发出及时、快速和准确地测定土壤中此类农药残留的检测方法,可为土壤环境安全评价提供技术支撑,并对监控农药合理使用和保障人类身体健康具有重要意义。
目前,有机磷农药残留检测方法主要有色谱检测法和快速检测法两大类。色谱检测法包括高效液相色谱(HPLC)法、气相色谱(GC)法、薄层色谱(TLC)法、气相色谱-质谱联用(GC-MS)法、液相色谱-质谱联用(LC-MS)法和毛细管电泳法等[8];快速检测法包括免疫分析技术和酶抑制法等[8]。基质固相分散法(MSPD)是一种样品提取方法,具有简便快捷、样品和溶剂用量少等优点[9]。分子印迹聚合物(MIPs)是一类具有较强分子识别能力的新型高分子仿生材料,具有稳定性好、吸附性强、识别性和选择性高等特点,集分离与富集于一体、能够专一性地识别目标分子,材料廉价且可反复使用,适于从复杂基质中分离纯化痕量目标物,以及对基质复杂样品的净化、萃取等前处理过程[10, 11]。但在其制备过程中,多采用以待测物为模板分子的本体聚合技术,得到的聚合物存在模板分子包埋过深、容易渗漏、不利于洗脱和再结合、聚合物后处理繁琐等缺点[12]。目前,国内外尚未见将分子印迹聚合物与固相分散萃取技术相结合用于土壤中4种硫代磷酸酯类有机磷农药残留检测的样品前处理方法的报道,并且多数固相分散萃取的文献均采用乙二胺-N-丙基硅烷(PSA)、活性炭、三氧化二铝、弗罗里硅土和硫酸镁等选择性较差的吸附剂作为分散固相萃取材料[13]。
本研究以代表性结构类似物甲基立枯磷为模板分子,以甲基丙烯酸为功能单体,以乙二醇二甲基丙烯酸酯为交联剂,采用沉淀印迹聚合法合成了分子印迹聚合材料,并以其为固相分散萃取剂, 结合高效液相色谱(HPLC)检测了土壤中4种硫代磷酸酯类杀虫剂的残留量,取得了能满足痕量分析要求的各项参数与结果。所采用的固相分散萃取剂既具有基质固相分散技术简便快捷的特点,又具有分子印迹聚合物选择性高的优势,解决了传统的本体聚合带来的聚合物微粒形状不规则、活性位点不均匀、聚合物后处理繁琐等问题。
1 材料与方法 1.1 主要仪器EYELA N-1100/OSB-2100型旋转蒸发仪(北京五洲东方科技发展有限公司);KQ5200DE型超声波清洗仪(昆山市超声仪器有限公司);Agilent 1260液相色谱仪及色谱工作站(美国Agilent公司);S23000N扫描电镜和CR-21G高速冷冻离心机(日本Hitachi公司)。
1.2 试剂与材料毒死蜱(chlorpyrifos,溶解于甲醇中)、甲基立枯磷(tolclofos-methyl,溶解于甲醇中)、甲基毒死蜱(chlorpyrifos-methyl,溶解于丙酮中)和甲基对硫磷(parathion-methyl,溶解于丙酮中),均为质量浓度为1 000 μg/mL的标准溶液,美国阿拉丁试剂(上海)有限公司);乙酸(分析纯),丙酮、乙腈和甲醇(农残级),Fisher Chemical公司;乙二醇二甲基丙烯酸酯(分析纯),美国 Sigma-Aldrich公司;无水硫酸钠(用前于650 ℃烘5 h)、甲基丙烯酸和偶氮二异丁腈,均为分析纯,国药集团。
土壤样品:从武汉华中农业大学药用植物园采集多年种植培育过不同作物的土壤和对照空白土壤(经检测后不含这4种农药)各 500 g,除去枯枝病叶及草根,晾干后粉碎过40目网筛,备用。
1.3 标准溶液配制及标准曲线绘制先将1 000 μg/mL的各农药标准溶液用乙腈稀释,配制成质量浓度为100 μg/mL的混合标准储备溶液,再逐级稀释成质量浓度为0.05、0.2、0.5、1、2、5、10和20 μg/mL的系列混合标准工作溶液,按1.8节条件测定,绘制峰面积(y)-质量浓度(x)标准曲线。
1.4 高分子印迹聚合微球制备将1.5 mmol甲基立枯磷(模板分子)溶解于120 mL乙腈中,加入6 mmol甲基丙烯酸(功能单体),室温下振荡60 min后置于 4 ℃冰箱冷藏12 h,使甲基立枯磷与甲基丙烯酸充分作用;取出,加入30 mmol乙二醇二甲基丙烯酸酯(交联剂)和30 mg偶氮二异丁腈(引发剂)混匀,通入氮气15 min,以除去溶解氧,密封置于60 ℃烘箱中反应聚合24 h;取出,冷却至室温,于4 ℃、6 000 r/min下离心10 min,得聚合物沉淀;以V(乙酸)∶V(甲醇)=1∶9为溶剂对聚合物沉淀进行索氏提取2次,每次24 h,以去除甲基立枯磷,再用甲醇洗去过量的乙酸至中性,于35 ℃下真空干燥至恒重,得高分子印迹聚合微球(MIPs)。取少量MIPs进行电镜扫描。
按上述方法不加入模板分子甲基立枯磷,制备非印迹聚合微球(NIPs)。
1.5 分子印迹聚合微球的吸附特异性试验与各农药的检出限先将100 μg/mL的混合标准储备溶液用乙腈依次稀释成1.0、5.0、10、25和50 μg/mL的系列混合标准溶液,准确称取10.0 mg MIPs于5 mL试管中,依次加入3 mL甲醇和上述1.0~100 μg/mL的混合标准溶液各200 μL,用甲醇定容至5 mL(药剂质量浓度分别为0.04、0.2、0.4、1、2和4 μg/mL),振荡吸附1 h,过滤,测定吸附液中4种硫代磷酸酯类有机磷杀虫剂的含量,以不同药剂质量浓度下的吸附量绘制等温吸附曲线。
另取10 g空白土壤,加入400 μL 0.5 μg/mL的混合标准工作溶液,按1.6和1.7节的方法处理,计算得到仪器响应信噪比(S/N)及各农药的检出限与定量限。
1.6 样品提取及净化提取:准确称取10 g待测土壤样品,依次加入40 mL丙酮和6 g无水硫酸钠,振荡提取25 min,于40 ℃下旋蒸浓缩至近干,加入2 mL甲醇溶解残余物并定容至2.5 mL,待净化。
净化:取1 mL上述提取物,加入3 mL纯净水,于45 ℃下旋蒸浓缩,除去甲醇,用水定容至4 mL;加入100 mg的MIPs,于25 ℃下振荡30 min后,再于25 ℃、8 000 r/min下离心10 min;弃去上清液,沉淀物用2 mL V(乙酸)∶V(甲醇)=1∶9混合溶液提取,涡旋20 s,振荡20 min;再于25 ℃、6 000 r/min下离心10 min;取上清液于40 ℃下旋蒸浓缩至近干,加入1 mL乙腈溶解残余物,经0.45 μm滤膜过滤后,再用乙腈定容至2 mL,待HPLC检测。
1.7 检测条件Agilent Eclipse XDB-C8色谱柱(150 mm×4.6 mm,5 μm);柱温25 ℃;流动相为V(乙睛)∶V(0.1%乙酸水溶液)=3∶1;流速0.8 mL/min;进样量20 μL;检测波长210 nm;运行时间9 min。
1.8 添加回收与检出限测定试验分别称取空白土壤样品10 g,依次加入不同量的毒死蜱、甲基立枯磷、甲基对硫磷和甲基毒死蜱标准溶液,分别配制成质量浓度为0.50与2.5 mg/kg的含药土样。混合均匀后,按1.6和1.7节的方法处理,计算添加回收率和精密度,每个水平重复5次。
2 结果与分析 2.1 分子印迹聚合微球的吸附特异性及特征
经电镜扫描显示(图 1):MIPs的直径均小于1 μm,微球中有致密的孔隙和凹凸不平的表面,能够有效识别并吸附目标分子。等温吸附曲线结果(图 2)表明:4种杀虫剂在MIPs上的吸附量显著高于在NIPs上的;在杀虫剂质量浓度为2.0 μg/L时,MIPs和NIPs对4种杀虫剂的吸附量趋于饱和;MIPs对毒死蜱(A)和甲基立枯磷(D)的吸附量略高于对甲基对硫磷(B)和甲基毒死蜱(C)的吸附量;在吸附量趋于饱和前,MIPs的吸附等温线分布差异明显,而NIPs的较弱,表明MIPs对4种农药的选择性明显强于NIPs。
 | 图 1 分子印迹聚合微球的扫描电镜图Fig. 1 SEM micrographs of MIPs |
本研究考察了以甲醇、乙醇及乙腈作为流动相进行样品分离洗脱的情况。结果表明:以乙腈为流动相时,所得色谱峰的峰型优于以甲醇和乙醇为流动相时的峰型,并且在乙腈中加入体积分数为0.1%的乙酸水溶液后可优化峰型,提高试验的灵敏度,尤其是可将毒死蜱的灵敏度提高近3倍。因此,最终确定以V(乙腈)∶V(0.1%乙酸水溶液)=3∶1混合溶液为流动相洗脱目标物。
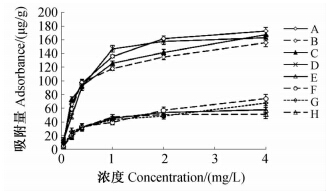 | A~D和E~H分别为MIPs和NIPs对毒死蜱、甲基对硫磷、甲基毒死蜱和甲基立枯磷的等温吸附曲线 Adsorption curves of chlorpyrifos,parathion-methyl,chlorpyrifos-methyl,tolclofos-methyl on MIPs(A,B,C,D)and NIPs(E,F,G,H)图 2 MIPs和NIPs对4种杀虫剂的等温吸附曲线Fig. 2 Adsorption curves of four insecticides on MIPs and NIPs |
结果(见表 1)表明:4种杀虫剂的线性范围均在0.01~5 mg/kg之间,相关系数r均在0.99以上;经MIPs富集纯化后的4种杀虫剂均得到了充分分离(图 3);NIPs的选择性吸附能力明显低于MIPs的(图 3C与图 4B)。
| 表 1 4种杀虫剂的线性范围与标准曲线Table 1 Linear range and standard equations of four insecticides |
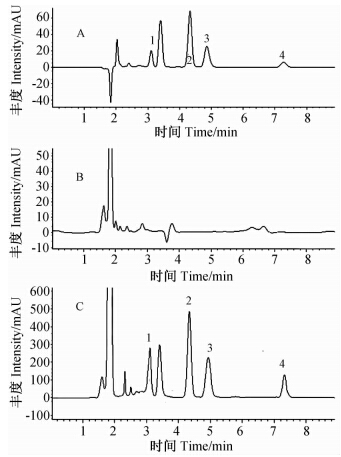 | A.混合标样(0.2 μg/mL); B.空白土样; C.空白土样添加(0.5 mg/kg)。1.甲基对硫磷,2.甲基毒死蜱,3.甲基立枯磷,4:毒死蜱 A. Blended standard substance(0.2 μg/mL); B. Blank soil sample; C. Addition of standard substance in blank soil sample(0.5 mg/kg). 1. parathion-methyl; 2. chlorpyrifos-methyl; 3. tolclofos-methyl; 4. chlorpyrifos图 3 混合标样、经MIPs富集提取后的空白土样及空白土样添加4种农药后的液相色谱图Fig. 3 Chromatograph chart of standard substance,extracted blank sample and addition of standard substance in blank soil sample with MIPs |
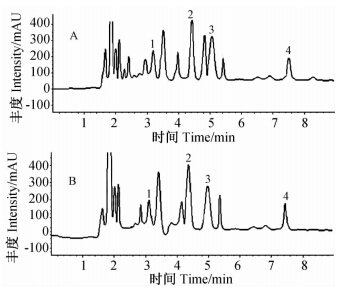 | 1.甲基对硫磷; 2.甲基毒死蜱; 3.甲基立枯磷; 4.毒死蜱 1. parathion-methyl; 2. chlorpyrifos-methyl; 3. tolclofos-methyl; 4. chlorpyrifos图 4 未净化土样(A)与经NIPs净化的空白土样(B)添加4种农药(0.5 mg/kg)后的液相色谱图Fig. 4 Chromatograph chart of no depurative soil sample(A) and purified sample by NIPs of the addition of standard substance(0.5 mg/kg) in blank soil sample(B) |
4种农药的仪器响应信噪比(S /N)分别为11.7、12.5、16.7 和15.2,折算出4种农药的检出限(LOD,S /N ≥3)分别为毒死蜱0.673 μg/kg、甲基立枯磷0.729 μg/kg、甲基对硫磷1.226 μg/kg和甲基毒死蜱0.452 μg/kg,其定量限LOQ(S /N≥10)分别为毒死蜱3.218 μg/kg、甲基立枯磷4.536 μg/kg、甲基对硫磷6.351 μg/kg和甲基毒死蜱3.612 μg/kg。
按照1.7节的检测条件,连续对同一质量浓度为0.2 μg/mL的毒死蜱标样进行测定,进样量为 20 μL,重复6 次。结果(图 3A)表明:峰面积和保留时间的平均值分别为 1.765×102(RSD 0.61%)和 7.3 min(RSD 0.47%),说明该方法重现性好,仪器的精密度高。
2.4 添加回收结果与样品测定添加回收试验结果(表 2)表明:在0.5~2.5 mg/kg的添加水平下,4种农药的添加回收率为76%~96%,其中,甲基立枯磷的添加回收率最高,为92%~96%,而甲基对硫磷的最低,为76%~91%。其相对标准偏差RSD均低于8%。表明该方法具有较高的准确度及精密度,能够适用于土壤中农药多残留的测定。
| 表 2 4种杀虫剂添加平均回收率及相对标准偏差Table 2 Average recovery and RSD of the four pesticides in soil samples(n=5) |
在优化的条件下,对某药用植物园中实际土壤样品进行测定,据调查,该园于年初栽培时曾施用过乐斯本(含毒死蜱有效成分48%)两次。结果显示:仅检出毒死蜱,其平均残留量为(2.38±0.14) μg/kg(n=5),说明在作物栽培中,毒死蜱曾被广泛使用过,其他3种农药使用较少或降解较快。
3 结论及讨论本研究采用高分子印迹聚合微球作为固相分散剂选择性地富集提取了土壤中4种硫代磷酸酯类杀虫剂,使用HPLC进行检测,建立了同时测定土壤中毒死蜱、甲基立枯磷、甲基对硫磷和甲基毒死蜱残留量的检测方法。该方法具有样品前处理方法简便快速、 线性范围宽、 检出限较低、 实用性较强等优点,克服了传统本体分子印迹方法中印迹聚合物后处理繁琐、微球颗粒不规则的问题。其检出限均低于2 μg/kg,能够满足分析要求。
本研究选用V(乙酸)∶V(甲醇)=1∶9的混合溶液为溶剂提取样品,最终样品中难免残留一些极性较强的乙酸、甲基丙烯酸和乙二醇二甲基丙烯酸酯,而这些残留物不仅会对弱极性毛细管柱的理化性质有一定影响,还可能在较高温度下与待测物农药发生副反应,从而影响检测结果,故不宜选用GC-FPD或GC-FID进行检测。本研究选用通用型HPLC-UV仪在常温下进行检测,取得了较好的结果。
古丽娜尔等采用基质固相分散-加速溶剂萃取结合气相色谱法测定土壤中毒死蜱的检出限为1 μg/kg[14];朱将伟等用GC法测定了土壤中有机磷农药残留,毒死蜱和甲基对硫磷的LOD值分别为5和8 μg/kg[15],均高于本研究中毒死蜱LOD值(0.673 μg/kg)。本方法易于普及掌握,且成本低,为土壤中硫代磷酸酯类农药多残留的同时测定提供了一种快速灵敏的方法,可满足大批量样品分析对质量和进度的要求。尤其适合中小型实验室和单位用于土壤中硫代磷酸酯农药的残留量测定和土壤环境安全评价。
| [1] | 朱晓兰, 蔡继宝, 杨俊, 等. 加速溶剂萃取-气相色谱法测定土壤中的有机磷农药残留[J]. 分析化学, 2005, 33(6): 821-824. Zhu Xiaolan, Cai Jibao, Yang Jun, et al. Determination of organophosphate pesticide residues in soil by accelerated solvent extraction-gas chromatography[J]. Chin J Anal Chem, 2005, 33(6): 821-824.(in Chinese) |
| [2] | Lu Chensheng, Barr D B, Pearson M A, et al. Dietary intake and its contribution to longitudinal organophosphorus pesticide exposure in urban/suburban children[J]. Environ Health Persp, 2008, 116(4): 537-542. |
| [3] | Wu Chunxia, Liu Ning, Wu Qinhua, et al. Application of ultrasound-assisted surfactant-enhanced emulsification microextraction for the determination of some organophosphorus pesticides in water samples[J]. Analytica Chimica Acta, 2010, 679(1-2): 56-62. |
| [4] | 李少南, 张莉, 边文杰, 等. 鱼类肝脏微粒体对于硫代磷酸酯类杀虫剂活化代谢率的种间差异[J]. 生态毒理学报, 2010, 5(6): 809-816. Li Shaonan, Zhang Li, Bian Wenjie, et al. Species-related difference of liver microsomes of fish in activation of organothiophosphorus insecticides[J]. Asian J Ecotoxicol, 2010, 5(6): 809-816.(in Chinese) |
| [5] | 吴武杰, 保志娟, 权小菁, 等. 有机磷农药残留检测前处理技术研究进展[J]. 化学分析计量, 2009, 18(4): 88-90. Wu Wujie, Bao Zhijuan, Quan Xiaojing, et al. Advances of preparation technique of organophosphorus pesticides residues detection[J]. Chem Anal Meterage, 2009, 18(4): 88-90.(in Chinese) |
| [6] | Ta Na, Zhou Fang, Gao Zhanqi, et al. The status of pesticide residues in the drinking water sources in Meiliangwan Bay, Taihu Lake of China[J]. Environ Monit Assessm, 2006, 123(1-3): 351-370. |
| [7] | Wang Ligang, Liang Yongchao, Jiang Xin. Analysis of eight organophosphorus pesticide residues in fresh vegetables retailed in agricultural product markets of Nanjing, China[J]. Bull Environ Contam Toxicol, 2008, 81(4): 377-382. |
| [8] | 李垚辛, 董全. 有机磷农药残留检测技术的研究进展[J]. 中国食物与营养, 2010,(4): 12-15. Li Yaoxin, Dong Quan. Detection technical progress of organophosphorus pesticide residue[J]. Food and Nutrition in China, 2010,(4): 12-15.(in Chinese) |
| [9] | 刘茜, 刘晓宇, 邱朝坤, 等. 基质固相分散-高效液相色谱法测定鲫鱼肌肉中残留的辛硫磷[J]. 色谱, 2009, 27(4): 476-479. Liu Qian, Liu Xiaoyu. Qiu Chaokun, et al. Application of matrix solid-phase dispersion for the determination of phoxim in crucian carp samples by high performance liquid chromatography[J]. Chin J Chromatogram, 2009, 27(4): 476-479.(in Chinese) |
| [10] | 徐靖, 刘娟, 金江岚. 分子印迹基质固相分散-超高效液相色谱法测定儿童玩具中双酚A[J]. 理化检验:化学分册, 2011, 47(6): 665-671. Xu Jing, Liu Juan, Jin Jianglan. UPLC determination of bisphenol a in children's toys with molecular imprinted matrix solid phase dispersion[J]. Phys Test Chem Anal(Part B: Chem Anal), 2011, 47(6): 665-671.(in Chinese) |
| [11] | 白文. 分子印迹技术在有机磷农药毒死蜱检测中的应用研究[D]. 长春: 吉林大学, 2011. Bai Wen. Research on molecular imprinting technology in the detection of organophosphorus pesticide chlorpyrifos[D]. Changchun: Jilin University, 2011.(in Chinese) |
| [12] | 陈逃, 姜涵, 邓晨辉, 等. 分子印迹-基质固相分散快速分离分析辣椒制品中的苏丹红[J]. 2014, 35(19): 312-315. Chen Tao, Jiang Han, Deng Chenhui, et al. Fast separation and analysis of Sudan dyes in chili products by molecular imprinted-matrix solid phase dispersion[J]. Sci Technol Food Ind, 2014, 35(19): 312-315.(in Chinese) |
| [13] | 张丹, 王俊红, 曾正宏. 分散固相萃取-气相色谱法测定水果中多种有机磷农药残留[J]. 分析化学, 2009, 37(增): 94-95. Zhang Dan, Wang Junhong, Zeng Zhenghong. Determination of multiple organophosphorus pesticide residue in fruit by solid-phase dispersion-GC chromatogram[J]. Chin J Anal Chem, 2009, 37(Suppl.): 94-95.(in Chinese) |
| [14] | 古丽娜尔 ·艾合坦木, 周梦春. 基质固相分散-加速溶剂萃取ASE-气相色谱法测定土壤中毒死蜱残留量[J]. 干旱环境监测, 2013, 27(1): 20-22. Gulinaer·Aihetanmu, Zhou Mengchun. Determination of chlorpyrifos residues in soil with matrix solid-phase dispersion-accelerated solvent extraction(ASE)-GC chromatogram[J]. Arid Environ Monit, 2013, 27(1): 20-22.(in Chinese) |
| [15] | 朱将伟, 赵燕, 刘军, 等. 气相色谱法测定土壤中有机磷农药残留[J]. 中国卫生检验杂志, 2011, 21(4): 863-867. Zhu Jiangwei, Zhao Yan, Liu Jun, et al. Determination of organophosphorus multi-residues in soil by gas chromatography[J]. Chin J Health Lab Technol, 2011, 21(4): 863-867.(in Chinese) |
 2015, Vol. 17
2015, Vol. 17


