2. 吉林大学 植物科学学院, 吉林省资源微生物功能研究工程中心, 长春 130062
2. College of Natural Resources and Environment, College of Plant Science, Jilin University, Changchun 130062, China
大多数农药原药都需加工成一定形态的制剂才能应用,正确选择剂型并设计合理的配方及加工工艺,在新药研究中占有十分重要的地位。随着大量农药原药的涌现,根据不同原药的特点、防治对象和施用方法,相继出现了多种农药剂型,其中可湿性粉剂(WP)和乳油(EC)是两种主要的传统剂型。可湿性粉剂是以无机载体为主的固体载药微粒,不仅容易飘移和散落到环境中,而且其负载的农药有效成分因无法完全释放而不能充分发挥作用,同时还很难降解;乳油制剂虽然加水稀释后比较方便喷洒施用,但是其产品中的大量有机溶剂容易导致环境污染及危害人体健康。因此,近年来发达国家已经开始限制或禁止农药可湿性粉剂和乳油新品种的登记,转而重视水基化农药制剂的研究开发[1]。根据对国际农药制造协会联合会(GIFAP)推荐的农药主要剂型代码的统计,目前已有60多种农药剂型,而我国已获准登记生产的农药制剂共有4 000多种,归属52种剂型[1]。为提高农药的防治效果,节约施药成本,降低残留污染,保护食品与生态安全,农药剂型正朝着水基化、缓释的方向发展[1]。
在农药制剂发展过程中,提高难溶性药物的分散性是解决农药有效利用率低这一难题的重要途径。虽然医药和农药的应用主体不同,但二者有许多共通之处,因此,许多医药剂型已被借鉴到农药领域并得到了成功的应用,如水乳剂(EW)、悬浮剂(SC)和具有缓释作用的微囊悬浮剂(microcapsule suspension)等[2]。借鉴医药领域的一些新剂型和新技术开发新的农药制剂,是缩短农药剂型研发周期的有效途径。
纳米混悬剂(nanosuspension)是近年来出现的一种纳米医药新剂型,其药物粒子的平均粒径小于1 μm,是一种分散度极好的纳米胶态分散体系。将疏水、疏油的药物制成纳米混悬剂,具有有机溶剂用量少、生物利用率高和稳定性好等优点,目前已在人体口服、注射和肺部给药等药剂制备方面得到广泛应用,如止吐药阿瑞吡坦(aprepitant)和免疫抑制剂西罗莫司(sirolimus) 纳米混悬剂均已商品化。Moeschwitzer等[3]制备了醋酸氢化钠可的松(hydrocortisone acetate)纳米混悬剂,并发现其在溶解度和生物利用率方面均有所提高。在农药制剂领域,陶氏益农公司率先提出纳米尺寸的制剂可以增加农药的生物利用率[2],但目前尚无相关的商品化产品。
农药纳米混悬剂(pesticide nanosuspension)是指农药有效成分以晶体或无定型状态,在表面活性剂的作用下均匀分散在水中而形成的一种平均粒径小于1 μm的农药新剂型[2]。目前市场上广泛应用的农药悬浮剂(SC)是多相分散体系,根据热力学能量降低原理,悬浮剂中的农药颗粒会发生奥氏熟化现象,致使其分散稳定性变差,出现分层、沉降等贮存稳定性问题[4]。与悬浮剂相比,农药纳米混悬剂的粒径明显降低,比表面积增大,农药的溶解速率加快,黏附性增大,渗透性及生物活性增强,可显著提高其有效成分的利用率,并且由于农药纳米混悬剂的粒径分布更窄,因此具有良好的物理稳定性[5]。
采用纳米化高分子材料作载体,可以有效控制农药的释放。Liu等[6]以聚乙烯吡啶和聚乙烯吡啶-苯乙烯为载体,制备了杀菌剂戊唑醇(tebuconazole)和百菌清(chlorothalonil)的纳米微粒(粒径100~250 nm),发现其可有效控制农药的释放,且增加苯乙烯的浓度可以减缓戊唑醇和百菌清的释放速率。郑和堂和尚青等报道,采用纳米高分子材料可制备能控制释放的啶虫脒(acetamiprid)[7]和伊维菌素(lvermectin)[8]纳米微粒。黃啟良等[9]报道了一种将二氧化硅作为载药系统的阿维菌素(abamectin)纳米微粒,发现其具有明显的缓释作用,并可同时减缓阿维菌素的水解和光解。
农药纳米混悬剂是一种高效环保的农药新剂型,给许多疏水、疏油型农药制剂的加工提供了新的发展契机。本文拟就纳米混悬剂的几种主要制备方法以及其在医药、农药等领域的应用进展进行综述,并初步探讨其贮存稳定性。
1 农药纳米混悬剂的制备方法
目前国内外制备农药纳米混悬剂的方法主要有两种:自上而下(top-down)法和自下而上(bottom-up)法(图 1)。另外,在实际应用中也可能会将不同的具体方法结合使用。
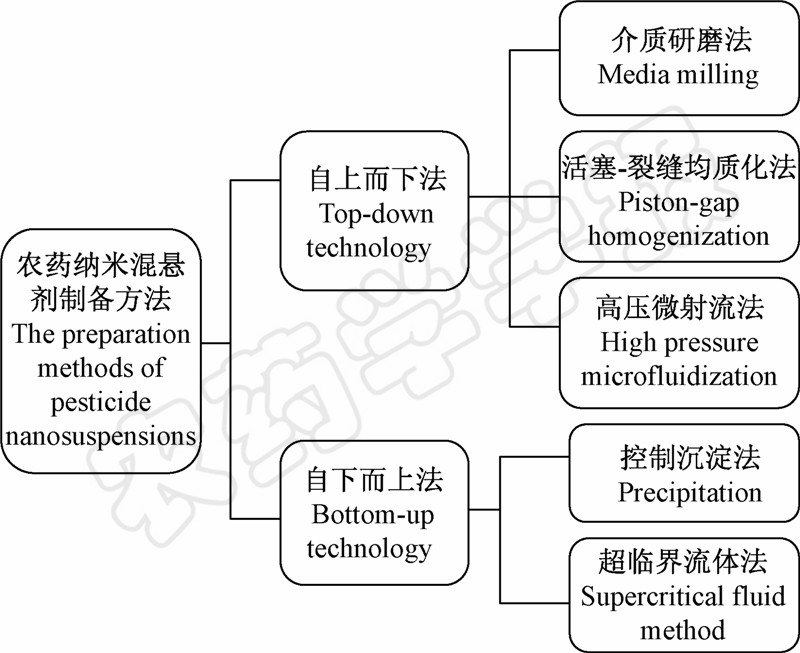 | 图 1 利用自上而下法和自下而上法制备 农药纳米混悬剂的示意图 Fig. 1 Bottom-up and top-down techniques for the preparation of nanosuspensions |
自上而下法又叫“top-down”法,是指利用机械的方法将农药颗粒破碎至纳米级粒子,其常见的方法包括介质研磨法、活塞-裂缝均质化法和高压微射流法等[10, 11]。 1.1.1 介质研磨法
介质研磨法是将农药有效成分和表面活性剂水溶液置于盛有研磨介质的研磨罐内,通过研磨介质运动产生的剪切力和挤压作用而得到纳米级的药物粒子。其研磨介质包括玻璃珠、二氧化锆珠和一些特殊的聚合物,如由硬的聚苯乙烯衍生物包覆的珠子等[12]。研磨时间则取决于药物的硬度、表面活性剂种类及用量、温度、分散介质的黏度以及机器能量的输入和研磨介质的大小等。Ghosh等[13]利用介质研磨法制备了NVS-102纳米混悬剂,并研究了载药量、研磨介质尺寸、研磨时间及不同表面活性剂(泊洛沙姆、羟丙基甲基纤维素和聚乙烯吡咯烷酮)对该纳米混悬剂粒径和稳定性的影响。
介质研磨法又分为干磨法和湿磨法,其不同之处在于湿磨法需在研磨罐中加入助剂水,干磨法则不需要,通常湿磨法的效果更好。陈欣等[14]利用干磨法和湿磨法分别制备了烯效唑(uniconazole)纳米混悬剂,在相同的助剂、研磨介质和时间下,发现干磨法制得的混悬剂粒径主要分布在2 μm左右,未达到纳米尺度,而湿磨法得到的混悬剂粒径主要分布在1 μm以下,且分散性较好。目前,由于机器能量的 提高以及研磨介质粒径的降低,研磨时间已显著缩短,一般研磨30~120 min即可达到纳米级粒径水平,且粒径分布较窄[12]。 Goswami等[15]采用行星球磨仪,可以实现同时制备不同配方的纳米混悬剂。目前在介质研磨技术中,一次研磨的药物量最低是10 mg,因此可用于药物早期配方筛选研究,同时也很容易将研磨仪器由实验室规模放大至生产规模[16]。
介质研磨法的优点是技术成熟、应用广、工艺简单,并且适用于疏水、疏油药物的加工,但同时因研磨介质腐蚀造成样品污染的问题也一直是研究热点。研磨介质的腐蚀与药物硬度、介质材料以及研磨时间相关。Buchmann等[16]报道,利用玻璃珠作为研磨介质时存在腐蚀性问题。有研究者采用一些特殊的聚合物作为研磨介质,如高度交联的聚苯乙烯珠,因其具有弹性形变,可降低研磨介质的磨损腐蚀,减少污染[15]。当前市场上加工纳米晶体(nanocrystal)时通常采用一种特殊的0.5 mm聚苯乙烯珠作为研磨介质,可以显著减少对样品的污染[13]。另外,因产品黏附在研磨系统所引起的产率降低,也是一个持久性的难题。
介质研磨法目前已在农药纳米混悬剂的制备中得到广泛应用。Chin等[17]利用介质研磨法制备了40.64%克百威(carbofuran)纳米混悬剂,其平均粒径为30 nm左右。在0 ℃放置7 d后,该纳米混悬剂中有效成分未发生明显改变,54 ℃放置14 d后,有效成分质量分数仅降低了3.2%,表明该纳米混悬剂较稳定。针对小菜蛾幼虫的毒力试验表明,该纳米混悬剂和微米级混悬剂的LD50值分别是9.42 mg/L和10.69 mg/L,纳米混悬剂的杀虫效率较微米混悬剂提高了13.5%。Storm等[18]利用介质研磨法制备了多种杀虫剂、除草剂和杀菌剂的纳米混悬剂,其平均粒径在150~320 nm之间。 1.1.2 活塞-裂缝均质化法
活塞-裂缝均质化法出现于20世纪90年代中期,最初是将药物在纯水中进行均质,之后发展为药物可以在非水介质或者含水量少的分散介质中均质[11]。空化作用是活塞-裂缝均质化法中降低粒径最重要的因素。该方法采用的设备是活塞-裂缝均质机,由高压柱塞泵、均质阀及外部冲击环组成。柱塞泵将混悬液吸入泵内,经加压后流出,其吸入和压出混悬液的流速相对较稳定;均质阀由一个固定的阀座和一个可调的阀芯组成,二者之间形成一个大小可调的狭缝;外部冲击环则是一个固定大小的出口横截面。三者联合使得高速流动的混悬液受剪切、撞击及空化效应作用,从而使药物达到纳米级粒子。其具体加工过程[19]是:先将药物制备成粗混悬液,当粗混悬液从均质机中相对较宽的气缸高速通过狭缝时,由于横截面减小,液体的动压急速增大,同时静压降低,当静压≤其蒸气压时,液体开始沸腾产生气泡,之后随着液体离开狭缝,气泡破裂产生强大的空化作用,使药物粉碎;经过多次循环即可得到纳米级的粒子。均质化过程中的压力、循环次数、温度及药物的硬度影响着纳米混悬剂的粒径 [11]。
活塞-裂缝均质化法的优点是所制备的纳米混悬剂粒径分布窄,加工比较简单,容易扩大生产,适用于疏水、疏油的药物,也不会对样品产生污染;不足之处是,该方法不适用于制备高浓度和高黏度的药物,以免堵塞机器[19]。
利用活塞-裂缝均质化法制备医药纳米混悬剂的技术已较为成熟,并且将其与其他技术结合还可以有效提高纳米混悬剂的制备效率。Salazar等[20]制备了格列本脲(glibenclamide)纳米混悬剂,先将药物溶解于乙醇中,经喷雾干燥后再通过活塞-裂缝均质机制备成纳米混悬剂。在相同的均质条件下,未经喷雾干燥处理的纳米混悬剂的平均粒径为772 nm、 D50为2.686 μm、 D90为14.423 μm,而经过喷雾干燥预处理的纳米混悬剂的平均粒径为236 nm、D50为0.131 μm、D90为0.285 μm,表明喷雾干燥预处理可以有效提高活塞-裂缝均质化法的均质效率。Talekar等[21]将药物PIK-75、水和泊洛沙姆188混合,先用剪切机预处理制成微混悬液,再置于活塞-裂缝均质机中,分别于7 250 psi(1 psi=6.895 kPa)处理15个循环、15 000 psi处理15个循环、18 000 psi处理15个循环,制得平均粒径为182 nm 的纳米混悬剂,其多分散性指数(PDI)为0.2。PIK-75微混悬液15 min时在水中的溶出度为18%,3 h时的饱和溶出度达到38%,而PIK-75纳米混悬剂 30 min 时在水中的溶出度为56%,3 h时的饱和溶出度达到89%,表明该PIK-75纳米混悬剂在水中的溶出度显著提高。
活塞-裂缝均质化法目前在制备农药纳米混悬剂方面已有应用。孙以文等[22]先将农药原药 [硫双威(thiodicarb)、氟虫腈(fipronil)和嘧菌酯(azoxystrobin)]、助剂和水置于高剪切乳化机中进行乳化剪切,待物料均匀后再通过活塞-裂缝均质机高压均质。与采用传统方法制备的混悬剂相比,该方法制得的纳米混悬剂粒径明显降低,且粒径分布变窄。 1.1.3 高压微射流法
高压微射流法是将大颗粒药物分散于水溶液或其他溶剂中,高速通过一个特别设计(“Z”形或“Y”形)的均化室,利用撞击力、剪切力和气穴来降低药物的粒径。对于“Z”形的均化室,混悬液是在很短的时间内通过几次改变液流的方向,因碰撞而产生剪切力;对于“Y”形的均化室,则是由于两个管道中的混悬液在交叉处高速碰撞而产生剪切力[11]。在运用高压微射流法制备纳米混悬剂时,影响药物粒径大小和分布的主要因素为药物的硬度、处理压力和循环次数。该方法具有操作简单、安全无污染、处理时间短和适用于工业化生产等优点,能制备粒径小且分布均匀的药剂,但同时也存在不适用于硬度较大的药物及仪器较昂贵等不足[23]。
王习魁等[24]研究了高压微射流法超细粉碎的作用机理和微孔流道形状对样品粉碎效果的影响。结果发现,样品在微射流孔道中流速极高,速率梯度极大,从而使得微射流流场内产生极强的作用力,保证了高压微射流对样品的粉碎效果。同时文中给出了微射流流场内3种主要作用力的表达式,指出了影响作用力大小的关键因素,通过对多种形式微孔流道的比较分析,发现带撞击模式的微孔流道更有利于颗粒的粉碎。韩冬辉等[25]利用高压微射流法制备了甘蔗纤维素的纳米混悬剂,并探讨了不同因素对该制剂粒径的影响。Moeschwitzer等[26]利用高压微射流法制备的胃酸分泌抑制剂奥美拉唑纳米混悬剂,在0 ℃下贮存30 d仍具有良好的稳定性。Saheki等[27]采用高压微射流设备制备了蛋卵磷脂-豆油的脂质纳米分散体系,其平均粒径小于100 nm。阎乃珺[28]研究了不同微射流压力对小麦面筋蛋白功能性质的影响,结果发现:微射流处理可增加小麦面筋蛋白的溶出度,并且微射流压力对其溶出度的影响与小麦面筋蛋白浓度有关。 1.2 自下而上法
自下而上法也叫bottom-up法,是将农药由分子状态聚集成为纳米级粒子,其主要制备方法包括控制沉淀法和超临界流体法。 1.2.1 控制沉淀法
控制沉淀法是指将含有农药原药的溶液滴加到反溶剂中,使药物由于过饱和而析出结晶,通过控制析出结晶的条件而形成纳米粒子[29]。将药液与反溶剂混合的方法很多,如液体喷射、多入口涡流混合等。
利用控制沉淀法制备的纳米药物可以是晶体也可以是无定型状态。如NanomorphTM技术是先将药物溶解在能与水混溶的溶剂中,再加入另一种聚合物水溶液,快速混合即可形成无定型的纳米微粒。采用该技术制备的无定型纳米微粒比纳米晶体具有更大的饱和溶出度和更快的溶出速率,但由于无定型的纳米微粒在一定条件下会再结晶,因此需要精确选择沉淀过程中的条件以及稳定剂[30]。咸强强[31]将牛磺酸(taurine)溶于乙醇,在超声波条件下加入含助剂的水溶液中,超声一段时间后静置,体系呈现白色乳光状。通过对牛磺酸的浓度、助剂种类和用量、超声时间等进行优化筛选,所制备的牛磺酸纳米混悬剂平均粒径为50 nm左右,-4 ℃放置 7 d后仍保持白色乳光状,稳定性较好。试验发现,与同浓度的牛磺酸微混悬剂相比,该纳米混悬剂可明显促进小麦幼苗根系及植株的生长,根长和株高分别增加了10.3%和7.8%。巩丽丽[32]利用该方法制备了吲哚丁酸(butanoic)纳米混悬剂:将吲哚丁酸混悬液加入含助剂的水溶液中,超声直至呈现白色乳光状,得到吲哚丁酸纳米混悬剂。通过对吲哚丁酸混悬液浓度、助剂种类和用量、样品注入速率、超声时间等进行优化筛选,所得吲哚丁酸纳米混悬剂的粒径为250~300 nm。与其原药相比,吲哚丁酸纳米混悬剂对大叶黄杨绿枝扦插的促生长效果明显,当纳米混悬剂中吲哚丁酸质量浓度为20 mg/L时,与同浓度原药相比,最长不定根长和根部直径分别增加了29.07%和18.87%。Zeng等[33]以环己酮/N,N-二甲基甲酰胺为溶剂,以含Tween-80和十二烷基硫酸钠(SDS)的水溶液作为反溶剂,制备了高效氯氰菊酯(β-cypermethrin)纳米混悬剂,其平均粒径为160 nm左右,载药量为85%~87%,稳定性较好。Anjali等[34]利用控制沉淀法制备了氯菊酯(permethin)纳米混悬剂,其平均粒径为150 nm左右,经X-射线衍射,证明该纳米混悬剂为无定型状态。相比氯菊酯粗悬浮剂,其纳米混悬剂对至倦库蚊Culex qinquefasciatus幼虫的LC50值明显降低[34]。胡林等[35]利用控制沉淀法制备了鱼藤酮(rotenone)水基纳米混悬剂,其平均粒径为127 nm,对松材线虫的毒力是鱼藤酮丙酮溶液的7.5倍。
将控制沉淀法与冷冻干燥或喷雾干燥技术相结合,可以减缓无定型的纳米微粒的再结晶。Elek等[36]以异丙醇和醋酸异丙酯为溶剂,以含SDS、十二烷基醚硫酸盐(SLES)和Morwet D-425的水溶液为反溶剂,首先制备成氟酰脲(novaluron)微乳剂,再通过喷雾干燥法去除有机溶剂得到粉末(平均粒径为200 nm),极大地提高了制剂的物理稳定性。
利用控制沉淀法制备含有纳米光催化材料的农药纳米混悬剂,可以有效提高农药的降解率。阎建辉等[37]将烯酰吗啉(dimethomorph)和纳米光催化材料TiO2/Ag溶于丙酮,充分搅拌得到均匀油相,之后在高速剪切搅拌下加入到含助剂的水溶液中,形成纳米混悬剂。通过对20%烯酰吗啉乳油和10%烯酰吗啉纳米混悬剂的毒力进行对比测试,得两种制剂的致死中浓度(LC50)分别为232.5和186.5 mg/L,表明10%烯酰吗啉纳米混悬剂的毒力高于乳油[37]。于太阳光下直射5 d,烯酰吗啉纳米混悬剂和乳油的降解率分别是68.0%和28.3%,表明纳米光催化材料TiO2/Ag可以显著提高烯酰吗啉的光降解率,进而提高其环境安全性[37]。周文祥等[38]将溴虫腈(chlorfenapyr)溶于少量有机溶剂,加入经助剂和硬脂酸修饰的纳米Ag/TiO2并混合均匀,高速剪切搅拌下加入去离子水,得到稳定的溴虫腈纳米混悬剂,其平均粒径为100 nm。太阳光下直射3 d后,其与未添加光催化材料的微米级溴虫腈悬浮剂的分解率分别是67.5%和0.64%,表明残留在农作物上的溴虫腈纳米混悬剂可以在较短时间内被降解。孙宏伟、汪学英等[39, 40, 41, 42]的研究也表明,添加改性后的纳米光催化材料可加快农药的降解,降低农药残留。
控制沉淀法的优点是设备简单、耗能低,缺点是药物需至少能溶解于1种溶剂,而且在沉淀过程中很难控制粒径的增长,因而限制了该方法在农药纳米混悬剂制备中的推广应用。 1.2.2 超临界流体法
超临界流体法是近 10 年发展起来的制备超细微粒的新技术,主要包括超临界流体快速膨胀法[43]和气体抗溶剂再结晶法[44]等。超临界流体快速膨胀法利用的是药物的溶解度随超临界流体密度变化而变化的原理。在超临界条件下,超临界流体的密度可以随压力和温度在较大范围内变化,当降低压力或温度时,药物达到过饱和而析出,从而得到纳米微粒[43]。气体抗溶剂再结晶法是指将药物溶液与某种能与其溶剂互溶的超临界流体混合,当两者互溶时,体积膨胀,黏度降低,致使原溶剂对药物的溶解度大大降低,药物以纳米尺度析出[44]。
很多物质都可以作为超临界流体法的溶剂,其中二氧化碳由于无毒无味、临界温度接近室温、临界压力低、化学性质稳定以及来源广而被广泛关注。Yao等[45]采用二甲基亚砜作为溶剂,以二氧化碳为反溶剂,制备了喜树碱(camptothecine)纳米混悬剂,发现当喜树碱在二甲基亚砜中的质量浓度为1.25 mg/mL、溶剂与反溶剂混合的流速为6.6 mL/min、温度为35 ℃、压力为20 MPa时,所得喜树碱纳米混悬剂的平均粒径为250 nm左右。Young等[46]利用超临界流体法制备了环孢素A(ciclosporin A)纳米混悬剂,其平均粒径为400~700 nm。Taki等[47]将敌草隆(diuron)和L-聚乳酸溶解于二氯甲烷,以二氧化碳作为反溶剂,采用气体抗溶剂再结晶法制备了敌草隆纳米混悬剂。
与传统结晶法相比,超临界流体法可减少有机溶剂的使用,更绿色环保;但缺点是需要特殊设备,成本较高[43]。 1.3 结合技术
由于上述各方法均有其优缺点,因此将几种方法结合使用已成为近年来研究的热点,通常可先利用自下而上法制备出沉淀物,再采用自上而下法将热力学不稳定的沉淀物制备成有序晶体结构的纳米微粒。
研究人员将不同制备方法相结合,产生了两种新的技术—— NanoedgeTM技术和Smartcrystal技术[48, 49]。NanoedgeTM技术是先按照自下而上法中的控制沉淀方法,将药物溶解在与水混溶的溶剂中,再加入到水中形成混悬液,之后再将此混悬液经自上而下法中的介质研磨法或者活塞-裂缝均质化法而得到纳米混悬剂。使用这种结合技术,一方面可以防止由于药物颗粒太大造成活塞-裂缝均质机堵塞,同时还可缩短研磨或均质时间,降低能耗。Ma等[50]利用NanoedgeTM技术制备了缬沙坦(valsartan)纳米混悬剂:按照自下而上法中的控制沉淀方法,先将缬沙坦溶于甲醇,再将其加入到泊洛沙姆407水溶液中,最后将该体系经自上而下法中的活塞-裂缝均质化而制得纳米混悬剂。他们同时对沉淀过程的温度、搅拌速率及活塞-裂缝均质化过程的压力、循环圈数进行了优化筛选。所得纳米混悬剂的平均粒径为117 nm,在室温条件下放置7 d,其粒径无明显增长。Quan等[51]同样利用控制沉淀法结合活塞-裂缝均质化法,制备了尼群地平(nitrendipine)纳米混悬剂。Smartcrystal技术则是将自上而下法中的介质研磨法与活塞-裂缝均质化法结合使用,先通过研磨机对混悬液进行预处理,再经活塞-裂缝均质化而制得纳米混悬剂,此种结合技术有利于纳米混悬剂粒径的降低,并可提高生产效率[49]。
2 农药纳米混悬剂的稳定性问题
农药纳米混悬剂的贮存物理稳定性问题主要包括沉降、聚集、晶体增长及晶型改变。当粒子分散不均一时会出现奥氏熟化现象,即随时间推移,小粒子逐渐分散并沉积在大粒子表面[29],该现象会导致纳米药物物理性质的改变,降低其贮存稳定性。
通常可采用以下3种方法 [29]抑制奥氏熟化现象:一是优化加工过程的参数,如均质压力和圈数、研磨时间及速率,以尽可能得到粒径分布较窄的纳米粒子;二是加入离子型和非离子型表面活性剂,通过电荷排斥和空间阻隔作用保持纳米粒子的稳定;三是通过喷雾干燥或冷冻干燥,将纳米混悬液制成粉末。其中将纳米混悬液制成粉末是提高其贮存稳定性最常用的方法,在市场开发方面很有潜力。而目前限制喷雾干燥法广泛应用的原因是其较低的生产效率、溶剂的选择性及药物的热敏感性。
Mauludin等[52]以SDS和Tween-80为助剂,采用活塞-裂缝均质化法制备得到了平均粒径约为500 nm的芸香苷(rutin)纳米混悬剂,发现其理化性质极其稳定。Yue等[53]采用冷冻干燥、喷雾干燥及真空干燥法对黄芩苷(baicalin)纳米混悬剂进行干燥处理,并考察了不同表面活性剂在不同干燥方法中对药物粒径的影响。结果发现:干燥过程会导致药物表面的表面活性剂结晶,从而丧失其抑制纳米微粒聚集的能力;另外,由于干燥过程需要加热,所产生的热应力也会导致纳米微粒的聚集。因此,严格控制干燥过程中的相关参数,对于样品的再分散十分重要。Mahesh等[54]利用控制沉淀法结合活塞-裂缝均质化法制得伊曲康唑(itraconazole)纳米混悬剂,之后再通过喷雾干燥制成粉末,发现在药物表面包覆一些离子型表面活性剂和适量的糖可使之更好地再分散。Cerdeira等[55]以十二烷基硫酸钠(SDS)和羟丙基甲基纤维素(HPMC)为表面活性剂,利用介质研磨法制备了咪康唑(miconazole)纳米混悬剂,其平均粒径为210 nm左右。为提高该纳米混悬剂的稳定性,加入甘露醇作为冷冻保护剂进行冷冻干燥。结果发现,冷冻干燥后的纳米混悬剂粉末与未加工的咪康唑粗粉末在水中20 min时的溶解度分别为52%和28%,60 min时分别为65%和46%,冷冻干燥后溶解度明显提高。赵晓玲[56]将葡萄糖、甘露醇、海藻酸钠、乳糖和蔗糖作为冷冻保护剂,考察了冷冻干燥前后齐墩果酸(oleanolic acid)的粒径变化,证明以蔗糖为冷冻保护剂冷冻干燥后的齐墩果酸粉末再分散效果较好。总之,将纳米混悬剂干燥制成粉末后其能否再分散至纳米级状态,是其固化成败的关键,因此需要严格控制干燥过程中的各参数。
3 总结与展望
农药纳米混悬剂不仅可以解决绝大多数难溶性农药的溶解性问题,而且可以提高其生物利用率,减少农药的使用量,降低残留污染,是一种高效、环保的绿色农药新剂型。
目前有关农药纳米混悬剂稳定性机理的研究尚不够完善,相关的加工技术也还有待开发,而同类医药剂型加工技术的发展为农药剂型开发提供了新的思路和方法。此外,农药纳米混悬剂使用后在作物和环境中的分布及转移也有待进一步探讨。相信在不久的将来,随着农药纳米混悬剂加工技术的进步和表面活性剂高通量筛选方法的建立及优化,必将涌现出更多高效、安全的农药纳米混悬剂新品种。
| [1] | 刘广文. 现代农药剂型加工技术[M]. 北京: 化学工业出版社, 2012: 1-10. LIU Guangwen. Modern Pesticide Formulation Processing Technology[M]. Beijing: Chemical Industry Press, 2012: 1-10(in Chinese) |
| [2] | STROM R M, PRICE D C, LUBETKIN S D. Aqueous dispersions of agricultural chemicals: US, 20010051175[P]. 2001-12-13. |
| [3] | MOESCHWITZER J P, MUELLER R H. Factors influencing the release kinetics of drug nanocrystal-loaded pellet formulations[J]. Drug Development and Industrial Pharmacy, 2013, 39: 762-769. |
| [4] | 冯建国, 路福绥, 李明, 等. 悬浮液的稳定性与农药水悬浮剂研究开发现状[J]. 农药研究与应用, 2009, 13(3): 12-19. FENG Jianguo, LU Fusui, LI Ming, et al. Stability of suspension solution and development of suspension concentrate products[J]. Agrochem Res Appl, 2009, 13(3): 12-19. (in Chinese) |
| [5] | RAI M, INGLE A. Role of nanotechnology in agriculture with special reference to management of insect pests[J]. Appl Microbiol Biotechnol, 2012, 94(2): 287-293. |
| [6] | LIU Y, YAN L, HEIDEN P, et al. Use of nanoparticles for controlled release of biocides in solid wood[J]. J Appl Polym Sci, 2001, 79(3): 458-465. |
| [7] | 郑和堂, 尚青. 啶虫脒水悬纳米胶囊剂及其制备方法: CN, 1491558[P]. 2004-04-28. ZHENG Hetang, SHANG Qing. Acetamiprid capsule nanosuspension and its preparation method: CN, 1491558[P]. 2004-04-28. (in Chinese) |
| [8] | 尚青, 郑和堂, 祁同生. 伊维菌素水悬纳米胶囊剂及其制备方法: CN, 1491551[P]. 2004-04-28. SHANG Qing, ZHENG Hetang, QI Tongsheng. Ivermectin capsule nanosuspension and its preparation method: CN, 1491551[P]. 2004-04-28. (in Chinese) |
| [9] | 黄啟良, 李凤敏, 折冬梅, 等. 具有缓控释作用的阿维菌素纳米载药体系: CN, 101142913[P]. 2008-03-19. HUANG Qiliang, LI Fengmin, SHE Dongmei, et al. Nano-drug carrier system of avermectin with slow releasing effect: CN, 101142913[P]. 2008-03-19. (in Chinese) |
| [10] | GUO Jingjing, YUE Pengfei, LV Junlan, et al. Development and in vivo/in vitro evaluation of novel herpetrione nanosuspension[J]. Int J Pharm, 2010, 441(1-2): 227-233. |
| [11] | KECK C, MULLER R. Drug nanocrystals of poorly soluble drugs produced by high pressure homogenization[J]. Euro J Pharm Biopharm, 2006, 62(1): 3-16. |
| [12] | MERISKOLE E, LIVERSIDGE G G.Nanosizing for oral and parenteral drug delivery: a perspective on formulating poorly-water soluble compounds using wet media milling technology[J]. Adv Drug Deliv Rev, 2011, 63(6): 427-440. |
| [13] | GHOSH I, BOSE S, VIPPAGUNTA R, et al. Nanosuspension for improving the bioavailability of a poorly soluble drug and screening of stabilizing agents to inhibit crystal growth[J]. Int J Pharm, 2011, 409(1-2): 260-268. |
| [14] | 陈欣. 烯效唑纳米颗粒混悬剂的制备、表征及对小麦种苗生长的影响[D]. 大连: 辽宁师范大学, 2010. CHEN Xin. Preparation and characterization of uniconazole nanoparticle suspension and impact on wheat seeding growth[D]. Dalian: Liaoning Normal University, 2009. (in Chinese). |
| [15] | GOSWAMI A, ROY I, SENGUPTA S, et al. Novel applications of solid and liquid formulations of nanoparticles against insect pests and pathogens[J]. Thin Solid Films, 2010, 519(3): 1252-1257. |
| [16] | BUCHMANN S, FISCHLI W, THIEL F P, et al. Aqueous microsuspension, an alternative intravenous formulation for animal studies[C]//42nd annual congress of the International Association for Pharmaceutical Technology (APV), Mainz. 1996: 124. |
| [17] | CHIN C P, WU H S, WANG S S. New approach to pesticide delivery using nanosuspensions: research and applications[J]. Ind Eng Chem Res, 2011, 50(12): 7637-7643. |
| [18] | STORM R M, PRICE C D, LUBETKIN S D. Aqueous dispersions of agricultural chemicals: U.S., Patent 20010051175[P]. 2001-12-13. |
| [19] | 宋扬, 王晶珂, 彭冲. 药物纳米混悬剂制备研究进展[J]. 河北化工, 2013, 36(2): 13-16. SONG Yang, WANG Jingke, PENG Chong. Research progress of preparation methods of drug nano-suspension[J]. Hebei Chem Ind, 2013, 36(2): 13-16. (in Chinese) |
| [20] | SALAZAR J, MVLLER R H, MÜSCHWITZER J P. Application of the combinative particle size reduction technology H42 to produce fast dissolving glibenclamide tablets[J]. Euro J Pharm Sci, 2013, 49(4): 565-577. |
| [21] | TALEKAR M, KENDALL J, DENNY W, et al. Development and evaluation of PIK75 nanosuspension, a phosphatidylinositol-3-kinase inhibitor[J]. Euro J Pharm Sci, 2012, 47(5): 824-833. |
| [22] | 孙以文, 明亮, 陆凡, 等. 一种制备农药悬浮剂的新方法: CN, 103070164 A[P]. 2013-05-01. SUN Yiwen, MING Liang, LU Fan, et al. The new preparation method of pesticide suspensions: CN, 103070164 A[P]. 2013-05-01. (in Chinese) |
| [23] | AlSHAAL M, MULLER R H, SHEGOKAR R. Smartcrystal combination technology scale up from lab to pilot scale and long term stability[J]. Pharmazie, 2010, 65(12): 877-884. |
| [24] | 王习魁. 高压微射流超细粉碎关键技术研究[D]. 无锡: 江南大学, 2005. WANG Xikui. Study on the key technology of ultra-fine grinding based on high-pressure microfluidics[D]. Wuxi: Jiangnan University, 2005. (in Chinese) |
| [25] | 韩冬辉. 动态高压微射流均相制备甘蔗渣纳米纤维素工艺研究[D]. 武汉: 华中农业大学, 2013. HAN Donghui. Homogenerous preparation of bagasee nanocellulose by dynamic high pressure microfluidization[D]. Wuhan: Huazhong Agricultural University, 2013.(in Chinese) |
| [26] | MOESCHWITZER J, ACHLEITNER G, POMPER H, et al. Development of an intravenously injectable chemically stable aqueous omeprazole formulation using nanosuspension technology[J]. Eur J Pharm Biopharm, 2004, 58(3): 615-619. |
| [27] | SAHEKI A, SEKI J, NAKANISHI T, et al. Effect of back pressure on emulsification of lipid nanodispersions in a high-pressure homogenizer[J]. Int J Pharm, 2012, 422(1-2): 489-494. |
| [28] | 阎乃珺. 动态高压微射流对小麦面筋蛋白性质和结构的影响[D]. 广州: 华南理工大学, 2013. YAN Naijun. Effect of dynamic high pressure microfluidization on properties and structures of wheat gluten[D]. Guangzhou: South China University of Technology, 2013. (in Chinese) |
| [29] | 陈充抒, 梁艳, 梁莉, 等. 纳米混悬剂的制备、表征及其应用研究进展[J]. 武警医学, 2013, 24(4): 358-361. CHEN Chongshu, LIANG Yan, LIANG Li, et al. Advances in study on the preparation of nanosuspensions and application[J]. Med J Chinese People's Armed Police Forces, 2013, 24(4): 358-361. (in Chinese) |
| [30] | SUN B, YEO Y. Nanocrystals for the parenteral delivery of poorly water-soluble drugs[J]. Curr Opin Solid State Mater Sci, 2012, 16(6): 295-301. |
| [31] | 咸强强. 海参营养素、牛磺酸纳米制剂的制备及对小麦幼苗生长的影响[D]. 大连: 辽宁师范大学, 2013. XIAN Qiangqiang. The dispose and effection on growth wheat seedings of sea cucumber nutrients nanoparticles and taurine nanoparticles[D]. Dalian: Liaoning Normal University, 2013. (in Chinese) |
| [32] | 巩丽丽. 吲哚丁酸纳米混悬剂促进大叶黄杨绿枝扦插生根效果研究[D]. 大连: 辽宁师范大学, 2011. GONG Lili. Rooting effect study of indoles butyric acid nano-suspension to promote Euonymus japonicus Thunb. Green branch cutting[D]. Dalian: Liaoning Normal University, 2011. (in Chinese) |
| [33] | ZENG Hui, LI Xuefeng, ZHANG Gaoyong, et al. Preparation and characterization of cypermethrin nanosuspensions by diluting O/W microemulsions[J]. J Disper Sci Technol, 2008, 29(3): 358-361. |
| [34] | ANJALI C H, SUDHEER K S, MARGULIS G K, et al. Formulation of water-dispersible nanopermethrin for larvicidal applications[J]. Ecotoxicol Environ Saf, 2010, 73(8): 1932-1936. |
| [35] | 胡林, 徐汉虹, 梁明龙. 鱼藤酮水基纳米悬浮剂的特性及对松材线虫的杀虫作用[J]. 农药学学报, 2005, 7(2): 171-175. HU Lin, XU Hanhong, LIANG Minglong. The characterization of squeous nanosuspension of rotenone and the bioactivity against Bursaphelenchus xylophilus[J]. Chin J Pestic Sci, 2005, 7(2): 171-175. (in Chinese) |
| [36] | ELEK N, HOFFMAN R, RAVIV U, et al. Novaluron nanoparticles: formation and potential use in controlling agricultural insect pests[J]. Coll Surf A: Phys Eng Asp, 2010, 372(1-3): 66-72. |
| [37] | 阎建辉, 黄可龙, 王跃龙, 等. 环保型烯酰吗啉纳米农药的制备及其性能[J]. 科学通报, 2004, 49(23): 2416-2421. YAN Jianhui, HUANG Kelong, WANG Yuelong. Preparation and characterization of uniconazole nanparticle suspension[J]. Chin Sci Bull, 2004, 49(23): 2416-2421. (in Chinese) |
| [38] | 周文祥, 陈灵谦. 环境友好型溴虫腈纳米农药的制备及其光降解活性[J]. 广东化工, 2007, 34(6): 108-111. ZHOU Wenxiang, CHEN Lingqian. Preparation and photo degradation activity of environmental friendly nano-pesticide for chlorfenapyr[J]. Guangdong Chem Ind, 2007, 34(6): 108-111. (in Chinese) |
| [39] | 阎建辉, 易健民, 唐课文, 等. 环保型甲基嘧啶磷纳米农药制剂的光催化降解[J]. 精细化工,2008, 25(3): 277-280. YAN Jianhui, YI Jianmin, TANG Kewen, et al. Photodegradation of nonpolluting pirimiphos-methyl nano-pesticide formulation[J]. Fine Chem, 2008, 25(3): 277-280. (in Chinese) |
| [40] | 孙宏伟. 纳米薄膜光催化剂的制备及光催化降解农药产物或其中间体的电化学检测研究[D]. 哈尔滨: 东北师范大学, 2013. SUN Hongwei. Fabrication of nano-film photocatalysts and electrochemical determination of photocatalytic degradation productions or intermediates of pesticides[D]. Harbin: Northeast Normal University, 2013. (in Chinese) |
| [41] | 汪学英, 崔荣静, 陈阳, 等. 磁性纳米Fe3O4对毒死蜱的增效和催化降解研究[J]. 环境科学与技术, 2013, 36(8): 152-155. WANG Xueying, CUI Rongjing, CHEN Yang, et al. Enhanched effect and photocatalytic degradetion of chlorpyrifos with nano-magnetic ferroso-ferric oxide[J]. Environm Sci Technol, 2013, 36(8): 152-155. (in Chinese) |
| [42] | 李艳霞, 王岩. 高岭石基掺N纳米TiO2 的制备及对农药的降解研究[J]. 环境科技, 2010, 23(5): 12-14. LI Yanxia, WANG Yan. Study on preparation of N-doped TiO2/Kaolinite and degradation to pesticide[J]. Environ Sci Technol, 2010, 23(5): 12-14. (in Chinese) |
| [43] | 周凯利. 超临界流体快速膨胀法制备药物微细粒子及其主要影响因素[D]. 长沙: 中南大学, 2012. ZHOU Kaili. Fine drug particles prepared by rapid expansion of supercritical solutions and the main influence factors[D]. Changsha: Central South University, 2012. (in Chinese) |
| [44] | 刘晓金, 钟国华, 胡美英, 等. 超临界流体技术在农药研究中的应用[J]. 精细化工, 2004, 5(9): 679-683. LIU Xiaojin, ZHONG Guohua, HU Meiying, et al. Application of supercritical fluid technology in pesticide science[J]. Fine Chem, 2004, 5(9): 679-683. (in Chinese) |
| [45] | YAO Liping, ZHAO Xiuhua, LI Qingyong, et al. In vitro and in vivo evaluation of camptothecin nanosuspension: a novel formulation with high antitumor efficacy and low toxicity[J]. Int J Pharm, 2012, 423(2): 586-588. |
| [46] | YOUNG T J, MAWSON S, JOHNSTON K P, et al. Rapid expansion from supercritical to aqueous solution to produce submicron suspensions of water-insoluble drugs[J]. Biotechnol Progr, 2000, 16(3): 402-407. |
| [47] | TAKI S, BADEN E, CHARBIT G. Controlled release system formed by supercritical antsolvent coprecipitation of a herbicide and a biodegrabable polymer[J]. Supercritical Fluids, 2001, 21(1): 61-70. |
| [48] | MÜLLER R H, GOHLA S, KECK C M. State of the art of nanocrystals-special features, production, nanotoxicology aspects and intracellular delivery[J]. Euro J Pharm Biopharm, 2011, 78(1): 1-9. |
| [49] | SHEGOKA R, MVLLER R H. Nanocrystals: industrially feasible multifunctional formulation technology for poorly soluble actives[J]. Int J Pharm, 2010, 399(1-2): 129-39. |
| [50] | MA Qiuping, SUN Hongrui, CHE Erxi, et al. Uniform nano-sized valsartan for dissolution and bioavailability enhancement: Influence of particle size and crystalline state[J]. Int J Pharm, 2013, 441(1-2): 75-81. |
| [51] | QUAN Peng, XIA Dengning, PIAO Hongze, et al. Nitrendipine nanocrystals: its preparation, characterization, and in vitro-in vivo evaluation[J]. AAPS Pharm Sci Tech, 2011, 12(4): 1136-1143. |
| [52] | MAULUDIN R, MÜLLER R H. Preparation and storage stability of rutin nanosuspensions[J]. J Pharm Invest, 2013, 43(5): 395-404. |
| [53] | YUE Pengfei, WAN Jing, WANG Jing, et al. D-alpha-tocopherol acid polyethylene glycol 1000 succinate, an effective stabilizer during solidification transformation of baicalin nanosuspensions[J]. Int J Pharm, 2013, 443(1-2): 279-287. |
| [54] | MAHESH V C, CARMEN P. Conversion of nanosuspensions into dry powders by spray drying: a case study[J]. Pharm Res, 2008, 25(10): 2302-2308. |
| [55] | CERDEIRA A M, MAZZOTTI M, GANDER B. Formulation and drying of miconazole and itraconazole nanosuspensions[J]. Int J Pharm, 2013, 443(1-2): 209-220. |
| [56] | 赵晓玲. 齐墩果酸纳米悬浮液及其冻干粉的制备[D]. 武汉: 华中科技大学, 2006. ZHAO Xiaoling. The prearation of oleanolic acid nanosuspensions and lyphilized powders[D]. Wuhan: Huazhong University of Science and Technology, 2006. (in Chinese) |
 2014, Vol. 16
2014, Vol. 16


