2. 山东农业大学 农药环境毒理研究中心, 山东 泰安 271018
2. Research Center of Pesticide Environmental Toxicology, Shandong Agricultural University, Tai'an 271018, Shandong Province, China
微囊化技术一般指利用物理、化学以及物理化学或生物学的方法将化学物质或生物材料包覆在囊壁材料中,使其缓慢释放甚至控制释放。微囊化具有以下主要优势:1)保护敏感的有效成分[1, 2],减少空气、光等环境因素的影响[3, 4];2)其常见状态为干粉或微囊悬浮剂,溶剂用量相对较少,可降低环境压力及减少资源浪费;3)可显著降低对高等动物、非靶标生物等的毒性[5];4)可延缓芯材释放,延长持效期[6, 7];5)可减少或掩蔽不良气味[8]等。该技术在化工及纳米材料[9, 10]、精油[11]、生物材料[12]、食品[1, 2]、医药[13]、印染[14]等领域应用广泛,但由于掌握农药微囊化技术的人比较少,而且工业化生产工艺相对复杂,所以其在农药领域的应用尚处于起步阶段,研究还不够深入。随着经济的发展及公众环保意识的加强,以及对施药安全性要求的提高,不仅促进了高效低毒药剂的开发,也对配套的农药加工技术提出了更高的要求。此外,农村劳动力的转移也极大地推进了省力化剂型的快速发展,微囊作为省力化剂型的代表品种之一,在我国已逐渐受到研究者和企业的重视。
目前对农药微囊的研究主要可归结为制备研究和应用研究两方面。在制备方面,关于制备方法和制备体系的研究报道很多,并已逐步完善,就大多数农药活性物质来说,理论上都有可能找到合适的微囊化方法,但由于工业生产条件的局限及农药使用环境的复杂性,对于具体的农药有效成分是否有必要包覆或者采用何种材料包覆是农药微囊制剂开发的难点。尽管氯氰菊酯(cypermethrin)、辛硫磷(phoxim)、毒死蜱(chlorpyrifos)和阿维菌素(abamectin)等的微囊已经商品化,但目前农药企业生产微囊的技术还不能满足各种施药场合以及不同防治对象使用的要求。因此,农药微囊化研究应该考虑的问题不仅仅是制备技术,还应该包括药效、食品安全和环境污染等方面,但有关这些方面的研究报道国内外都比较少见。
本文就近年来国内外农药微囊化常规方法的研究进展进行了综述,并介绍了新出现的微流体技术和配位聚合技术等微囊化新技术,探讨了相应壁材的特性。此外,根据本实验室多年从事微囊化技术研究的工作经验,结合农药微囊的登记现状,阐述了对农药微囊化优势的看法,探讨了微囊化研究亟待拓展的方向和急需解决的问题,旨在促进农药微囊技术的发展。
1 农药微囊制备方法研究现状及进展
农药微囊的制备方法很多,主要有物理、化学、物理化学和生物学方法。物理方法主要有喷雾干燥法[3]、冷冻干燥法[15]、包合法[16]、超临界流体法[17]、静电结合法[18]、溶剂蒸发法[19]和旋转分离法[20]等。但物理方法普遍生产能力低,且粒径很难做到小于100 μm,其中应用比较广泛的是喷雾干燥法和溶剂蒸发法。物理化学方法主要有相分离法、干燥浴法、熔化分散冷凝法和囊芯交换法等[21],其中相分离法最为常用,但由于受到工艺和载药量的限制,很难获得可重复的相分离条件[5]。根据原料和聚合方式,可将化学微囊化方法分为界面聚合法、原位聚合法和锐孔-凝固浴法等[22],其中界面聚合法和原位聚合法是目前农药微囊制备最常用的方法。有关采用生物学方法进行微囊化的研究相对较少,主要是利用酵母菌等真菌微生物细胞壁的半透性,使芯材进入细胞内,得到粒径为几十微米的微囊产品[23]。近年来也有学者探索提出了微流体技术[24]和配位聚合技术[25]等微囊化新技术。
1.1 常规微囊化方法 1.1.1 喷雾干燥法喷雾干燥法(spray drying)是先将芯材分散于含囊壁材料的溶液中,形成悬浮液或乳浊液,之后将物料雾化成小液滴,在干燥器中液滴所含溶剂迅速蒸发,壁材随之析出成囊。该法多以可食用的蛋白质或多糖等为囊壁材料,在食品领域应用最广。Aghbashlo等[3]采用响应面法(RSM)和遗传算法(GA),以脱脂奶粉(SMP)为囊壁材料,制备了鱼油微囊。结果表明,水相含量、总固含量中油相比例和乳化时间对包覆率和能耗利用效率影响较大。Wang等[2]以聚乙烯吡咯烷酮和海藻酸钠为囊壁材料,采用超声波细胞研磨同步乳化技术均质,经喷雾干燥制备了叶黄素微囊。微囊化后叶黄素的光、热和氧降解半衰期分别延长了5.6、1.9和7.7倍,且发现将脂溶性的叶黄素包覆后,其水溶性明显提高。Torres等[26]以[WTBX]β-环糊精包覆甲氨基阿维菌素苯甲酸盐,所制备的微囊为缩水的球形且粒径分布较窄。喷雾干燥法制备成本低,操作简单,适宜连续生产,但由于在喷雾干燥过程中水分和溶剂的挥发速率过快,囊壁上容易产生缝隙,导致微囊的包覆率普遍偏低[27],因而制约了该方法在农药领域的应用。多层包覆或选择包覆性能更好的囊壁材料可能是解决该问题最有效的方法。吕静等[28]以聚乳酸为囊壁材料制备了尿素微囊,并用石蜡二次包覆,土壤淋溶试验表明,经2次包覆后,芯材尿素的溶出速率显著降低。
1.1.2 溶剂蒸发法所谓溶剂蒸发法(solvent evaporation)是先将芯材和壁材分散到有机相中,之后将有机相转移至与壁材不相溶的溶液中,加热使溶剂蒸发,进而壁材析出成囊[19]。其常用的囊壁材料主要包括丙烯酸甲酯、壳聚糖、聚己内酯和聚乳酸等[29, 30]。Carreras等[31]将聚己内酯和布洛芬分别溶于二氯甲烷和异丙醇中,制备了O1/O2/W双重乳液,室温下搅拌,待溶剂蒸发后得到布洛芬微囊,并发现微囊粒径可通过控制水相的体积和黏度来调节。聚乳酸由于其具有可降解特性,已成为农药微囊化领域最受关注的囊壁材料。郭瑞峰等[30]以聚乳酸为囊壁材料制备了毒死蜱微囊。结果表明:当聚乳酸浓度增大时,微囊的载药量、包覆率和粒径均随之增加;当芯/壁材质量比由1∶2 减小至1∶5 时,微囊的粒径和载药量也随之减小。该毒死蜱微囊在水中的消解速率比乳油慢,有效成分半衰期比乳油的长。室内毒力测定结果表明,1.2 mg/L的毒死蜱微囊水解85 d后用于处理白纹伊蚊3龄幼虫,致死率仍高达76.6%,高于同浓度毒死蜱乳油处理组(53.3%)[32]。孟锐等[33]以聚碳酸亚丙酯包覆毒死蜱,发现当芯/壁材质量比为1∶2 时,所得微囊为规则的球形,载药量16.75%,包覆率高达89.34%。采用溶剂蒸发法制备微囊时,由于其溶剂挥发比喷雾干燥法慢,因此包覆率相对较高。但由于溶剂挥发不均匀,微囊形状一般不规则,粒径也不均匀[26]。此外,二氯甲烷是该方法中最常用的溶剂,若想将芯材完全溶解,其用量一般需为芯材的几倍到几十倍,因而溶剂回收也是需要考虑的问题,但目前尚未见系统报道。
1.1.3 界面聚合法界面聚合法(interfacial poly-merization)是将2种含有双(多)官能团的单体分别溶于不相混溶的两相液体中,用乳化剂将油相(水相)乳化至一定粒度后,添加扩链剂,使之在两相界面上发生缩聚反应,生成具有一定硬度的囊壳,将油相(水相)包覆于囊中。其常见类型见表 1。
| 表 1 界面聚合法制备微囊时常用的聚合物材料 Table 1 Common polymer materials used by interfacial polycondensation |
界面聚合法制备工艺简单,反应速率快,适宜连续化生产,且对生产设备和反应单体的纯度要求不高,对原材料配比要求不严。但要求单体具有较高的反应活性,利于进行缩聚反应。利用该方法既可包覆亲油性芯材,也可包覆亲水性芯材[34, 35],是目前农药微囊工业化生产中最常用的方法之一。笔者等[36]以4,4′-二苯基甲烷二异氰酸酯(MDI)和乙二胺为反应单体,制备了500 g/L的二甲戊灵(pendimethalin)微囊悬浮剂,阐述了囊壁材料用量、平均粒径、固化温度、分散剂和黏度调节剂用量等对微囊形貌和高含量微囊悬浮剂物理稳定性的影响。傅桂华等[37]将多异氰酸酯与丙三醇混合后再进行缩聚反应,降低了多异氰酸酯的活性,进而减少了副反应(异氰酸酯易与水反应)的发生,有效提高了包覆率和芯材的热稳定性。陶晡等[38]通过流变学手段,证明了硅酸镁铝与黄原胶协同使用可显著改善辛硫磷微囊悬浮剂的贮存物理稳定性。
研究不同配方及工艺条件对微囊性能的影响,对微囊的应用具有重要意义。但现阶段有关农药微囊的研究主要集中在贮存物理稳定性及表面形貌等方面,而对聚合反应速率和芯材的释放特性等研究报道较少。由于部分农药的表面性能与其他芯材,如医药和染料等有一定的相似性,因此,了解微囊化技术在医学等领域的研究应用进展,对农药微囊的研究具有较大的参考价值。
Hickey等[39]以MDI分别与二乙烯三胺和四乙烯五胺反应,制备了聚脲微囊,但得到的囊壳机械强度小。之后他们采用在聚脲囊壳表面吸附纳米蒙脱土的方法,增加了囊壳的厚度,机械强度得以增强;此外,选择合适的溶剂使微囊处于膨胀状态也有助于胺向内扩散,从而增大囊壳的厚度。Hong等[40]分别以乙二胺、1,6-己二胺与2,4′-甲苯二异氰酸酯(TDI)反应,制备了以一种芳香精油(migrin oil)为芯材的聚脲微囊。结果发现,以乙二胺为单体制备的微囊比以己二胺为单体制备的微囊粒度分布更广,表面更粗糙,载药量更高,囊壳更厚且释放速率更慢。表明单体胺分子越小,所制备的微囊越致密。Takasu等[41]的研究表明,不同聚合物单体的反应活性差异较大,3种亲油性单体的反应活性依次为异佛尔酮二异氰酸酯(IPDI)<己二异氰酸酯(HMDI)<甲代亚苯基-2,4′-二异氰酸酯(TDI),3种亲水性单体的反应活性顺序为异佛尔酮二胺(IPDA)<己二胺(HMDA)<乙二胺(EDA)。其中选择IPDI和IPDA进行聚合可以降低反应速率,减小囊间的团聚风险,而采用TDI时,团聚不可避免。但在包覆不同的芯材时,聚合反应的敏感性也有较大的差异。笔者等[36]在以高反应活性的4,4′- 二苯基甲烷二异氰酸酯和乙二胺为单体,制备二甲戊灵微囊时未发生粘连或团聚。此外,在选择单体时也应均衡时耗和后续反应,在不造成明显粘连或团聚的情况下,应尽可能缩短反应时间。Xie等[9]以2,4′-甲苯二异氰酸酯与二亚乙基三胺制备了油包水型聚脲微囊。结果表明,随着搅拌速率升高,微囊粒径减小,释放速率加快,但搅拌速率对交联程度的影响很小;同时还证明,高黏度对破碎或变形有较强的抵抗能力,可使微囊的乳液更稳定。Gaudin等[42]以超声破碎取代常规的搅拌,制备了直径为70 nm的纳米微囊。结果表明:当平均粒径为70~200 nm时,粒子大小对囊壳的化学结构和性能影响很小;而油相/水相比是控制平均粒径的关键,当油/水比减小时,粒径也明显减小;超声振幅为80%~100%时,随超声频率增大,粒径反而增大,但其对多分散指数无显著影响。Zhu等[43]将壳聚糖改性,得到了具有良好两亲性的马来酸酐酰化壳聚糖,其在水中的溶解度增大,可形成亲水性囊壁。该研究表明,采用聚乳酸(PLA)+ 酰化壳聚糖制备的微囊的包覆率大于单用酰化壳聚糖制备的微囊,且随聚乳酸含量增多,包覆率增大。Zeta电位测定表明,酰化壳聚糖微囊表面电荷为负电荷,而未洗涤的聚乳酸-马来酸酐酰化壳聚糖微囊表面电荷接近中性。Tsuda等[44]以环己烷二异氰酸酯和乙二醇为反应单体,于75 ℃下固化48 h,得到了吡丙醚(pyriproxyfen)聚氨酯微囊。该微囊悬浮于水中时稳定,可保持良好囊形,而一旦水分蒸发后囊壳即迅速破裂,芯材得以快速释放。该研究为快速释放型农药微囊的发展提供了新思路。他们认为,囊壁厚度和异氰酸酯的结构是影响微囊自发破裂的主要因素,选择脂肪族异氰酸酯可制备较柔软的囊壁,而囊壁厚度小、平均粒径与壁厚的比值大则有助于囊壳破裂。Jabbari等[45]先将MDI、PEG400和 1,4-丁二醇(扩链剂)以质量比2∶1∶1混合,之后通过缩聚反应制备了多孔的二嗪磷聚氨酯微囊。结果表明,囊壁的多孔性受扩链剂(1,4-丁二醇)用量影响很大,当扩链剂用量增大时,孔隙减小。当1,4-丁二醇的质量分数为0~50%时,囊壁为有孔膜,且随其用量增加孔隙减少,粒径也减小;当其质量分数为60%~67%时,囊壁为无孔膜。Wang等[46]以异丙基丙烯酰胺和聚异丙基丙烯酰胺为亲水性单体,以二乙烯基苯为亲油性单体,利用反相乳液聚合法制备了复合微囊。结果表明,该微囊粒径可由纳米粒子的浓度调节,囊壁厚度可由二乙烯基苯的浓度调节。且该微囊对温度有良好的响应,相变温度为27 ℃。释放特性研究表明,芯材罗丹明的释放速率受介质温度影响较大,45 ℃下35 h的累积释放量约为25 ℃时的3倍。
1.1.4 原位聚合法原位聚合法(in situ polymerization)的原理是先在弱碱条件下将可溶性单体预聚,之后在酸催化下预聚物分子间不断交联,最终沉积于芯材表面,形成不溶的聚合物囊壳[47]。该方法使用的单体价廉,生产设备也比较简单,但制备工艺较复杂且工业化生产需要专业的工人。其常用的囊壁材料主要有3种:1)尿素和甲醛反应生成脲醛树脂[48];2)苯酚和甲醛反应生成酚醛树脂[49];3)三聚氰胺和甲醛反应生成密胺树脂[50]。由于苯酚有较强的腐蚀性和刺激性气味,因此酚醛树脂微囊相对较少见。原位聚合法也是农药微囊化最常用的方法之一,多以脲醛树脂为囊壁材料。该方法的关键在于预聚物的沉积,而pH条件则决定了该聚合反应的速率,进而影响微囊的形貌。赵德等[51]通过延缓调酸时间,使脲醛树脂均匀沉积在油/水界面上,制备了大小均匀、形貌良好的毒死蜱微囊。Sukhorukov等[52]以三聚氰胺和甲醛反应生成的密胺树脂,用其包覆荧光化合物,得到粒径为5.2 μm的微囊,并研究了不同pH条件下的荧光反应,以确定包覆情况。结果表明:pH=10时,微囊处于关闭状态,此时包覆率较低;pH=3时,微囊处于开放状态,在该条件下包覆芯材后再将pH升高至10,可极大提高包覆率。此外,囊壁材料用量也是制备成功的关键:壁材用量低时,包覆厚度小,囊壁强度小;但壁材用量过高时,体系黏度增大,脲醛在溶液中形成纳米微粒而吸附在囊的表面或交联成网,易引起团聚[51]。优化制备工艺、提高微囊的热稳定性、调节释放特性和囊壁材料改性等依旧是近年来原位聚合法研究的重点。Fan等[48]制备了尿素-甲醛(UF)微囊,该微囊的囊壁为无孔膜。结果表明,添加无机电解质可增大离子强度,使UF更易沉积到颗粒表面,而高pH值和高搅拌速率则有利于制备表面平滑的微囊。此外,增大油相比例可降低疏水性芯材与亲水相间的界面张力,进而最大限度地提高囊壁的厚度。
近年来,微囊的机械性能也已受到广泛关注。Zhang等[10]研究发现,甲醛/尿素物质的量之比会影响预聚体的组成,进而影响微囊的形貌。且聚合物分子链越长,支链越多则分子排列越紧密,分子间隙越小,囊壁越致密、光滑[53]。Su等[54]以甲醇改性的三聚氰胺-甲醛(MMF)为预聚物,制备了含沥青更新剂的新型微囊,并成功应用两步凝聚(TSC)法,明显提高了MMF囊壁的刚性和韧性。同时他们发现:增加预聚物用量可使囊壁变厚;增大囊壁密度,可使微囊的杨氏模量增大,从而提高囊壁抵抗变形的能力;降低预聚物滴加速率可显著提高微囊的热稳定性[54]。此外,由于囊壳的形成是凝聚过程,壁材用量决定其厚度,因此降低芯/壁材质量比可增加囊壁厚度[55],但壁材用量也不宜过多,以避免团聚现象发生。他们在研究温度对微囊形变影响的过程中,以屈服点评价微囊的强度时发现[56]:在同一粒径及壁厚的情况下,密胺树脂囊壁的强度比脲醛树脂的大;温度是影响囊壁机械性能的重要因素,包覆的相变材料在吸热和放热的过程中膨胀或收缩,均会导致囊壳破裂。因此在包覆毒死蜱、二甲戊灵等固体原药时,为了降低溶剂用量,多采用加热的方法暂时提高有效成分在溶剂中的溶解度[36]。此类产品在贮存时,部分原药在微囊中以晶体的形式存在,也会对囊壁造成机械压力,当贮存于寒冷地区时,原药在溶剂中的溶解度下降,囊壳破裂的风险更大。因此考察和改善农药微囊的机械性能对于扩大其使用地域具有极高的实用价值。
1.1.5 相分离法相分离法(phase separation)主要包括复凝聚法和单凝聚法。复凝聚法是将两种或多种等电点差异较大的高分子材料与芯材混合形成溶液,调节溶液pH值,进而使带异种电荷的高分子间相互交联形成聚电解质复合物,并沉积于芯材表面而制得微囊。复凝聚法主要受pH 值和壁材浓度两个因素的影响,且当壁材高分子所带的异种电荷相等时,微囊产率最高。黄彬彬等[57]以明胶和阿拉伯胶为壁材,用乙酸调节溶液pH=4,得到甲氨基阿维菌素微囊。该法制备工艺简单,可直接包覆固体芯材,无需添加有机溶剂,但其包覆率仅为62%。Nakagawa等[58]以明胶和阿拉伯胶为壁材,采用冷冻诱导的方法制备了[WTBX]β-胡萝卜素微囊。结果表明,冷冻速率为-1 ℃/min时包覆率最大,而冷冻速率为-2 ℃/min时可有效控制芯材释放,但该方法的能耗较高。单凝聚法是通过向含有芯材的某种聚合物溶液中加入非溶剂或不良溶剂、凝聚剂、凝聚诱导剂等而使该聚合物的溶解性降低,从溶液中析出并沉积于芯材表面形成微囊。Shimokawa等[59]绘制了明胶-水-甲醇、明胶-水-乙醇和明胶-水-丙醇的三元相图,以探索理想的凝聚方法。结果表明,随不良溶剂疏水性增大(甲醇<乙醇<1-丙醇<2-丙醇),凝聚区域增大。疏水性强的溶剂体系其持续释放效果更明显,以明胶-水-丙醇制备的非那西丁微囊 24 h 的释放速率比用明胶-水-乙醇制备的低34%。微囊悬浮剂是农药领域最常见的微囊化剂型[36],而采用相分离法制备的微囊不仅有效成分含量偏低[5],也很难得到稳定的微囊悬浮剂,因而阻碍了其在农药领域的应用。
1.1.6 自组装微囊自组装(self-assembly)一般指利用分子间的静电、氢键或共价键等相互作用,使两种或多种物质沉积于芯材表面,以达到包覆的目的。利用该方法可制备多层复合膜,具有操作简便、囊壁厚度可控等优点。经典的自组装技术是以静电作用为驱动力,将带有正、负电荷的物质交替沉积于芯材表面[60, 61]。海藻酸含有两种糖醛酸,可与二价金属离子(如Ca2+)发生反应,生成不溶于水的海藻酸盐凝胶物。Pongjanyakul等[62]和Yeh等[11]通过Ca2+与海藻酸钠相互作用,分别包覆了美沙芬和茶树油。该类微囊的制备主要受壁材用量影响,随海藻酸钠浓度提高或氯化钙浓度降低,微囊的粒径增大,尤其是当氯化钙浓度较低时,溶液中海藻酸钠的浓度对微囊粒径有显著影响[62]。此外,微囊的释放也受海藻酸钠浓度、氯化钙浓度和交联时间的影响,囊壁越厚,壁材交联越彻底则释放速率越慢[62]。Wichchukit等[63]以乳清蛋白/藻酸盐和氯化钙为反应单体,包覆了核黄素和维生素B2。流变学特性研究表明,向藻酸盐溶液中添加乳清蛋白形成的胶体溶液具有假塑性和粘弹性;而核黄素复合体微球的释放规律符合零级动力学模型。Shulkin等[64]以苯乙烯马来酸酐共聚物和水溶性的多胺反应生成交联的聚合盐,包覆了昆虫性信息素十二烷基乙酸盐和十二烷醇。结果表明:以不同分子质量的共聚物制备的微囊,其释放性能无明显差异;快速滴加胺的微囊多孔,但释放速率反而比缓慢滴加胺的微囊慢;干燥条件下,壁厚的微囊释放速率加快,而壁薄的微囊变化不明显。Teng等[65]发现,与羧甲基壳聚糖相比,以羧甲基壳聚糖-大豆蛋白复合物为壁材时,对Ca2+浓度和pH范围的要求降低,其载药量达到6.06%,包覆率高达96.8%;傅里叶变换红外光谱(FTIR)表明,该微囊结构致密,且氢键缔合明显;与单用大豆蛋白相比,复合壁材微囊在人工胃液中的释放速率明显减慢,而在人工肠环境中释放速率明显加快。Hui等[66]利用壳聚糖质子化的氨基与藻酸盐的羧基产生的同步静电作用,形成聚合电解质复合体,并用其包覆牡丹皮。正交试验表明,影响包覆率的因素排序为壁材浓度>芯/壁材比>交联时间>搅拌速率。他们发现,随壁材浓度增大,溶液黏度也增大,有助于获得更厚的囊壳,且壁材浓度越大包覆率越高。Dinsmore等[67]通过自组装胶体颗粒在液滴表面沉积,制备了可精准控制粒径、渗透性及机械强度的固体胶囊。其研究表明,高吸附量可提高胶体颗粒的弹性,通过囊壁上的孔洞控制释放速率是最直接的方法,对于弹性囊壳则可通过调节剪切应力控制释放。以聚赖氨酸连接的胶体颗粒可变形性更大,是提高机械强度的有效方法。贾进伟等[68]以戊唑醇(tebuconazole)为芯材,在壳聚糖上引入疏水性甲基丙烯酸甲酯链,制备了平均粒径为220 nm的纳米微囊,其载药量为21.8%,包覆率为85.7%。按戊唑醇质量浓度48.2 mg/L处理40 d后,对木霉和黑曲霉菌的抑制率仍可达70.6%和89.1%。周斌等[69]以木质素磺酸钠和壳聚糖为壁材,包覆了阿维菌素。扫描电子显微镜(SEM)观察显示:该微囊表面粗糙且无明显孔隙。释放结果表明,采用层层自组装方式制备的阿维菌素微囊具有一定的缓释能力,且随组装层数 (0~32层 )的增加,微囊的释放速率显著降低。
自组装多采用价廉的囊壁材料,制备工艺也比较简便,但该方法目前在农药领域研究应用仍很少。究其原因,可能是由于自组装最常用的单体壁材是海藻酸盐、壳聚糖和改性的壳聚糖等,这些物质多微溶于水,而易溶于酸,因此很难得到含量较高的微囊悬浮剂。未来可考虑通过抽滤、浓缩或喷雾干燥等手段制备微囊粉剂或微囊粒剂。
1.2 微囊化新方法 1.2.1 微流体技术微流体法(microfluidic tech-nique)是利用微流体装置制备大小均一微囊的有效方法,其粒径可由微流体装置的孔径来调节。该方法在材料科学和药剂学领域多有研究。Lee等[70]通过玻璃毛细管微流体装置制备了W/O/W双重乳液,溶剂为甲苯和氯仿,壁材为丙交酯和乙交酯(PLGA)的混合物,溶剂挥发后形成全吞没型微囊(芯材被完全包覆于囊内)。结果表明,当不考虑溶剂的影响时,丙交酯的含量越高,微囊的包覆率越高。Zhang等[24]利用微流体技术,一步法制备了具有高度单分散性的超分子多孔微囊,其微液滴前体脱水后可立即形成稳定的单个微囊,且随油相流动速率与水相流动速率比值的增大,初始液滴和微囊的粒径反而减小。该法的优点是微囊大小均一可控,缺点是很难实现批量化生产,在农药领域可能只适用于将价格特别昂贵的原药微囊化。
1.2.2 配位法配位法(coordination)制备微囊的原理是:以Fe2+和Cu2+等金属离子为中心离子,使其与含孤对电子的配体通过配位键合得到配位化合物,当配体为分子较大的有机物时,可得到配位聚合物,其沉积于芯材颗粒表面即可形成微囊。但只有当配位化合物在水中的溶解度很小时,才能采用该方法制备微囊。Ejima等[25]分别以天然多元酚单宁酸和Fe3+为有机配位体和离子交联剂,一步组装制备了通用膜,进而包覆得到聚苯乙烯等微囊。所得微囊对pH值较敏感,随pH值增大,囊壳的稳定性呈指数型增加;当pH<6时则囊壳容易降解。这为高安全性微囊制剂的开发提供了新思路。Bentley等[71]报道了其他天然的自组装配位体,包括酚类物质(咖啡酸)、没食子酸、邻苯二酚和黄酮等。Mal等[72]首先通过2-甲酰吡啶与4,4′-联苯胺-2,2′-二磺酸反应得到有机配位体(亚胺),之后与Fe2+自组装得到稳定的中空四面体,将对空气敏感的白磷包覆其中,可使疏水性的白磷分子在空气中保持稳定,而白磷的释放则可通过添加配位竞争剂苯来实现。广义上,配位法也是自组装的一种,可制备多层复合膜,但与1.1.6节不同的是其利用了分子间的配位作用。该法所采用的壁材如单宁酸等在水中溶解度较大,在多种微粒表面均吸附性能良好,且其在较低用量下与Fe3+配位即具有良好的包覆性能[25],本实验室初步研究也发现,单宁酸-Fe3+配位复合体可在多种农药表面沉积(待发表)。总之,由于配位法对设备要求不高,囊壁延展性好,壁材价格也比较低廉[25],因此有望在农药领域推广应用。但目前尚未见相关报道。 2 我国农药微囊的登记及应用现状
近年来我国登记生产的农药剂型结构发生了明显变化,特别是2013年,乳油和可湿性粉剂的比例明显下降,而悬浮剂和微囊的比例显著提高(表 2),表明我国农药剂型整体正逐渐向水基化及缓释化方向发展。
国内农药微囊产品登记始见于1998年,截至2014年1月共计165例(含过期和有效登记)。1998年至2006年间,每年新增的微囊产品登记数较少,从2006年开始逐年增加,特别是2009年以后增速明显加快(图 1)。涉及的有效成分主要有毒死蜱、辛硫磷、高效氯氟氰菊酯(lambda-cyhalothrin)、阿维菌素、噻虫啉(thiacloprid)和1-甲基环丙烯(1-methylcyclopropene)。登记的主要剂型为微囊悬浮剂(CS,高达135例),有效成分含量多在30%以下,其余剂型有微囊粉剂(CJF,4例),微囊粒剂(CG,9例),种子处理微囊悬浮剂(CF,8例),微囊悬浮-悬浮剂(ZC,8例)和微囊悬乳剂(ZW,1例)。目前的农药微囊多是在液体环境下制得,芯材被高分子材料包覆后,形成大量的类似固体的颗粒,再进一步制备成水基化的微囊悬浮剂,生产工艺简便且成本较低,若添加固体填料或进行喷雾干燥则可制备成微囊粒剂或粉剂,但会增加生产工序及成本。此外,由于对水喷雾是最常用的施药方式,也决定了微囊产品以微囊悬浮剂为主[36]。根据不同的施药方式及防治需要,今后需研究开发不同剂型的微囊产品。如将适宜在水田使用的农药开发为微囊粒剂,通过撒施方式施药,不仅可达到“轻简化”的目的,且对施药者安全性较高,但目前登记品种较少。为了有效防治森林重要害虫松材线虫,吴学民等[74]研发了噻虫啉微囊粉剂,通过改善药剂对叶面的粘附性而提高了防治效果。
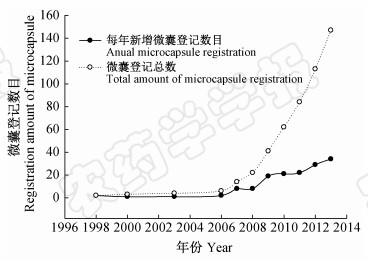 | 图 1 我国微囊制剂登记数量变化曲线 Fig. 1 Change curves of microcapsule registration amount in China |
不同类别的农药微囊适用于不同的防治对象及应用领域。将有机磷类杀虫剂制备成微囊,可主要用于地下害虫的防治。毒死蜱微囊悬浮剂花生拌种或喷穴防治蛴螬等地下害虫,具有省时省力的作用,目前已在山东、河南、河北、江苏和安徽等省花生产区得到广泛应用[75]。拟除虫菊酯类如联苯菊酯(bifenthrin)和高效氯氟氰菊酯微囊主要用于防治卫生害虫,具有降低溶剂用量、减少刺激性气味等特点,适宜在室内应用,同时可有效解决以滞留喷洒方式施药时,乳油或悬浮剂中有效成分易光解、水解或被微生物降解的问题[76]。由于农药防治对象种类多、差异大,因此应根据具体靶标和施药环境,选择不同的壁材和微囊化技术。如在叶面施用微囊制剂防治病虫害时,鉴于农民一般在病虫害发生前期施药,所以适宜选择降解速率快的壁材,如聚乳酸[30]和配位聚合物[25],或多孔的壁材;地下害虫在作物的整个生长季均有发生,因此适宜选择降解速率较慢的聚脲、聚氨酯或脲醛树脂等壁材;而当微囊产品主要用于果蔬保鲜时,以生物相容性良好的明胶和阿拉伯胶等作为壁材无疑是最理想的选择[77]。自然,选定壁材的同时也就决定了相应的微囊化技术。
从能被微囊化的有效成分的理化性质看,目前可被包覆的主要是液体原药[如辛硫磷、异丙甲草胺(metolachlor)、乙草胺(acetochlor)等],或者是在常规溶剂中溶解度大的固体原药[如毒死蜱、二甲戊灵、异口恶草松(clomazone)等]。在工业上,这些有效成分的微囊化主要采用原位聚合法和界面聚合法,制备工艺相对简单,产品性能也比较稳定,其中原位聚合法主要以脲醛树脂或密胺树脂为壁材,而界面聚合法主要选择聚脲或聚氨酯。对于原药是固体且在常见有机溶剂中溶解度较小的农药,如嘧菌酯(azoxystrobin)、甲氨基阿维菌素苯甲酸盐(emamectin benzoate)等,由于包覆率低或受制备工艺限制,目前尚无商品化的品种。但该类有效成分的小试工艺已有报道,一般采用复凝聚法或溶剂蒸发法在原药颗粒表面沉积成膜[57, 78],其中溶剂蒸发法制备的微囊包覆率略高于复凝聚法制备的微囊[77, 78]。也有研究表明,先将原药颗粒均匀分散于白油中,再乳化得到S/O/W(水包油包固)型双重乳液,最终在油水界面成膜,可制得包覆率大于85%的吡虫啉(imidacloprid)微囊[79]。
微囊化赋予了农药有效成分新的特性。目前农药的微囊化主要是为了延长其持效期,避免敏感有效成分的光解,如阿维菌素[80]和辛硫磷[38]的微囊化。但是微囊的其他特性也值得关注和开发利用:1)有机磷类农药和一些熏蒸剂等普遍具有刺激性气味,将这些药剂微囊化可明显减少不良气味[8],如噻唑膦(fosthiazate)、脱叶磷(tribuphos)等药剂的微囊化;2)二甲戊灵、异丙甲草胺等除草剂施到土壤表面后易被淋溶[81, 82],从而对作物种子发芽造成威胁,将其制备成微囊可降低药剂的淋溶性,减少药害的发生;3)异 NFDA1 草松和 2,4-D-丁酯(2,4-D-butylate)等药剂挥发性强、易飘移,在使用过程中易对邻近作物造成药害[83, 84],将此类有效成分微囊化,由于微囊颗粒自身质量增加和囊壁阻碍了药剂的挥发,可有效减少对周围作物的药害[85]。
从农药类别分析,目前已登记的微囊产品大多是杀虫剂,除草剂微囊品种较少,仅有乙草胺、异 NFDA1 草松和精异丙甲草胺(s-metolachlor)等几种,尚未见有关杀菌功能微囊产品的登记,仅有阿维菌素微囊登记用于防治线虫病害。
总之,在开发农药微囊制剂时,应结合原药的理化特性、防治对象、用药环境、施药方式、实际需要和最终的防治效果等因素,综合考虑决定是否应该将某农药开发成微囊产品,并选择适宜的壁材、微囊化技术和剂型。
近年来,关于乳油中有害溶剂限量使用的呼声越来越高,我国工业和信息化部现已颁布HG/T 4576—2013“农药乳油中有害溶剂限量”标准[86],并已于2014年3月1日开始实施,涉及的溶剂包括甲苯、二甲苯、N,N-二甲基甲酰胺(DMF)和甲醇等。随着相关管理政策的出台,预计乳油在农药剂型中的比例将会逐步下降,水基化剂型比重会大幅度增加。微囊悬浮剂兼有水基化和缓释的特点,因此将是农药剂型发展的一个重要方向。根据以上对我国微囊制剂产品登记情况的分析,笔者认为,我国农药的微囊化在以下领域正在或有待进一步研究和开发。
1)种子处理剂微囊。种子处理对操作和使用者安全,环境污染小,且因为其直接包覆在种子表面,有效成分利用率高,药剂损失率低于1%[87]。杀菌剂拌种防治多种土传和种传病害具有明显优势,但部分杀菌剂,如三唑类,采用种子处理时对作物的安全性较差,常导致出苗延迟或出苗率降低[88]。王娜等[89]将戊唑醇微囊化后,有效缓解了其对玉米出苗和生长发育的抑制作用。因此,此类具有杀菌作用的微囊种子处理剂应得到重视。
2)果蔬保鲜剂微囊。常规保鲜手段如低温和气调贮藏成本较高且操作难度大,为化学保鲜剂的推广应用带来了机遇。1-甲基环丙烯原药为气体,美国罗门哈斯公司将其开发成了方便使用的微囊粒剂[90],是目前国内仅有的商品化保鲜剂微囊产品,已广泛用于果品和花卉的保鲜。而水果、蔬菜的长期贮藏需要持效期更长的微囊产品,能否将常规保鲜剂如咪鲜胺(prochloraz)、噻菌灵(thiabendazole)和抑霉唑(imazalil)等开发为微囊缓释产品应用于果蔬保鲜,尚需进一步研究。
3)植物精油微囊。植物精油是一类挥发性较强的化合物,将具有毒杀或驱避活性的植物精油微囊化可拓宽其应用范围,对开发环境友好型农药产品具有重要意义。Zhao等[91]的研究表明,香茅醇、1-辛烯-3-醇等挥发性化合物对多种病、虫、草害具有一定的防效,但由于挥发性太强而难以实际应用,微囊化则可降低其挥发性,为其成功应用于生产实践提供了可能。周一万等[92]制备了冬青油微囊,在有效成分300 g/hm2的剂量下喷雾处理,药后11 d对菊小长管蚜的防效仍保持在90%以上。
4)昆虫性信息素微囊。昆虫性信息素挥发性较强,多作为迷向剂广泛用于果园害虫防治,被包覆后可显著延长其持效期[93, 94]。虽然该类化合物微囊化的配方和工艺并不复杂[95],但目前推广应用也较少。微囊化既可延长性信息素的作用时间,也可提高其与其他化合物的相容性,将昆虫性信息素与杀虫剂、化学不育剂、细菌和病毒等联合使用,将有效促进性信息素在农业生产中的应用[96]。
5)土壤处理剂微囊。1,3-二氯丙烯(1,3-dichloropropene)、氯化苦(chloropicrin)、威百亩(metham-sodium,甲基二硫代氨基甲酸钠)和硫酰氯等均是高效、广谱的土壤处理剂,可有效杀灭土壤中的线虫、真菌及细菌等[97, 98]农业病虫害,是溴甲烷(methyl bromide)理想的替代品种。但是,1,3-二氯丙烯和氯化苦施用时对操作者的毒性很大,威百亩遇水后分解产生的熏蒸活性物质异硫氰酸甲酯的毒性也很大[97],将这些化合物微囊化则有望解决上述问题。Wang等[8]以明胶为壁材,将1,3-二氯丙烯和氯化苦微囊化后,发现并未影响其对镰孢菌属、疫霉属和腐霉属真菌的活性,为该类化合物的微囊化研究提供了很好的思路。 3 农药微囊化亟待解决的几个问题
农药微囊剂型符合环保化和缓释化的发展方向,但是微囊技术在被进一步开发和利用之前,仍有一些问题亟待解决。
3.1 壁材特性与应用性能的关系目前可作为微囊壁材的高分子材料有明胶-阿拉伯胶[58]、脲醛树脂[10]、密胺树脂[50]、聚脲[9]、聚酰胺[29, 32]、聚氨酯[44, 45]和聚酯等。这些高分子材料本身的性质,如亲水性、抗光性、强度、降解特性,以及芯材在高分子壁材中的扩散系数等,均会影响到微囊的特性以至其应用范围[45, 54]。但目前关于农药微囊的研究主要集中于配方、工艺优化及释放特性等方面,在不同壁材及其特性与应用性能的关系方面还有很多问题需要明确。
3.2 农药微囊使用环境与药效的关系与许多医药、食品及化妆品微囊所处的单一环境不同,农药微囊的施用环境要复杂得多,涉及作物表面、土壤、空气及水体等不同介质及环境,而且针对害虫、病原菌和杂草等防治对象的不同,对药剂释放形式的要求也存在较大差异,微囊化后的芯材在上述环境中的释放特性,直接影响其防治病虫草害的速效性和持效性。因此,微囊在不同环境中的释放动态,包括释放速率、释放程度(是否完全释放),温度、湿度等环境因子对芯材释放的影响以及与药效的关系等,将是今后微囊开发时不可回避和亟待研究的重要课题。
3.3 药剂残留芯材被包覆后,由于缓慢释放而延长了其持效期,但同时也可能会造成更长时间的农药残留,所以微囊化后的农药在土壤、水体以及作物上的残留风险也是必须重点关注的问题。
3.4 壁材的降解有些用作壁材的高分子物质(如聚脲、聚氨酯等)本身比较稳定、降解慢,将这些高分子材料释放到环境中后,可能会给环境带来压力,造成新的污染[99]。近年来,采用可降解材料制备微囊已受到越来越多研究人员的青睐,在各领域均有报道,使用的壁材包括聚乳酸、聚己内酯[29, 30, 31, 32, 33]等。国内也有关于伊维菌素[29]和毒死蜱聚乳酸微球的研究报道[30],但载药量低一直是这类可降解壁材微囊发展的巨大障碍[29, 30],有待深入研究。
3.5 速效性与持效性的矛盾如果纯粹追求微囊的持效性,可能导致其前期释放过慢或者释放量不够,从而影响防治效果,所以为了兼顾速效性和持效性,微囊的包覆率不能太高,或者可考虑将其与其他药剂或剂型复配使用。相关问题也有待于深入开展研究。
3.6 微囊的释放机制现有的微囊制剂多是靠芯材缓慢渗透囊壁而进行释放的,即无论虫、草、菌等有害生物是否为害,芯材都会一直释放。我们是否可以研制出具有控释效果的微囊呢?如在防治森林害虫天牛时,最理想的释放方式是:将微囊施于植物表面后,药剂基本不释放,而当其取食或者踩踏到微囊时,药剂迅速释放,达到杀灭害虫的目的;在防治作物病害时,当微囊施于植物表面或土壤中后,药剂何时释放取决于是否存在目标病原菌,如果能在病原菌生长和侵染时释放某种特定物质,将该种物质作为启动微囊内药剂释放的触发剂,就有可能开发出防治某种特定病害的特异性微囊。如上文所述,Tsuda等[44]研制了吡丙醚聚氨酯微囊,该微囊悬浮于水中时稳定,可保持良好囊形,使用时待水分蒸发后囊壳即迅速破裂。此种技术可用于包覆易水解或与其他药剂物理相容性差的农药。因此,可赋予药剂特定功能的特异性微囊化技术将是未来农药微囊研究与开发的主要方向。
| [1] | XU Jin, ZHAO Wenxiu, NING Yawei, et al. Improved stability and controlled release of ω3/ ω6 polyunsaturated fatty acids by spring dextrin encapsulation[J]. Carbohydr Polym, 2013, 92(2): 1633-1640. |
| [2] | WANG Guoying, CHEN Juan, SHI Yanping. Preparation of microencapsulated xanthophyll for improving solubility and stability by nanoencapsulation[J]. J Food Eng, 2013, 117(1): 82-88. |
| [3] | AGHBASHLO M, MOBLI H, RAFIEE S, et al. Optimization of emulsification procedure for mutual maximizing the encapsulation and exergy efficiencies of fish oil microencapsulation[J]. Powder Technol, 2012, 225: 107-117. |
| [4] | AGHBASHLO M, MOBLI H, RAFIEE S, et al. Energy and exergy analyses of the spray drying process of fish oil microencapsulation[J]. Biosyst Eng, 2012, 111(2): 229-241. |
| [5] | SCHER H B, RODSON M, LEE K S. Microencapsulation of pesticides by interfacial polymerization utilizing isocyanate or aminoplast chemistry[J]. Pestic Sci, 1998, 54(4): 394-400. |
| [6] | FRIEDMAN-RUDOVSKY J. With novel paint, chemist aims to vanquish the Vinchuca[J]. Science, 2012, 336(6082): 666-667. |
| [7] | STOJAKOVC D, BUGARSKI B, RAJIC N. A kinetic study of the release of vanillin encapsulated in Carnauba wax microcapsules[J]. J Food Eng, 2012, 109(3): 640-642. |
| [8] | WANG Qiuxia, YAN Dongdong, MAO Liangang, et al. Efficacy of 1, 3-dichloropropene plus chloropicrin gelatin capsule formulation for the control of soilborne pests[J]. Crop Prot, 2013, 48: 24-28. |
| [9] | XIE Zhiyi, CHEN Nengchang, LIU Chengshuai, et al. Synthesis and characterization of ethylenediamine tetraacetic acid tetrasodium salt loaded in microcapsules with slow release properties[J]. Chin J Chem Eng, 2010, 18(1): 149-155. |
| [10] | ZHANG Ting, ZHANG Min, TONG Xiaomei, et al. Optimal preparation and characterization of poly(urea-formaldehyde) microcapsules[J]. J Appl Polym Sci, 2010, 115(4): 2162-2169. |
| [11] | YEH K W, CHANG C P, YAMAMOTO T, et al. Release behavior of capsules loaded by volatile liquid in multicores[J]. Colloid Polyme Sci, 2012, 290(15): 1583-1591. |
| [12] | MA Ying, ZHANG Ying, WANG Yu, et al. Study of the effect of membrane thickness on microcapsule strength, permeability, and cell proliferation[J]. J Biomed Mater Res, Part A, 2013, 101A(4): 1007-1015. |
| [13] | ZHANG Maojie, WANG Wei, XIE Rui, et al. Microfluidic fabrication of monodisperse microcapsules for glucose-response at physiological temperature[J]. Soft Matter, 2013, 9(16): 4150-4159. |
| [14] | COMISKEY B, ALBERT J D, YOSHIZAWA H, et al. An electrophoretic ink for all-printed reflective electronic displays[J]. Nature, 1998, 394(6690): 253-255. |
| [15] | SUTTER S C, BUERA M P, ELIZALDE B E. β-Carotene encapsulation in a mannitol matrix as affected by divalent cations and phosphate anion[J]. Int J Pharm, 2007, 332(1–2): 45-54. |
| [16] | 郑立辉. 尿素包合法制取低熔点石蜡的研究[J]. 精细石油化工, 2002(6): 11-13. ZHENG Lihui. Preparation of low melting point paraffin by urea-adduct method[J]. Spec Petrochem, 2002(6): 11-13.(in Chinese) |
| [17] | 林书乐, 王坤, 程江, 等. 微胶囊技术新进展[J]. 高分子材料科学与工程, 2012, 28(5): 179-182. LIN Shule, WANG Kun, CHENG Jiang, et al. Recent progress in microencapsulation technology[J]. Polym Mater Sci Eng, 2012, 28(5): 179-182.(in Chinese) |
| [18] | 张武杰, 李保国, 张超, 等. 静电喷雾法制备海藻酸钙-羧甲基纤维素钠液芯微胶囊的工艺选优[J]. 上海理工大学学报, 2007, 29(4): 349-352. ZHANG Wujie, LI Baoguo, ZHANG Chao, et al. Optimizing lecnological parameters for preparing calcium alginate-sodium carboxymethyl cellulose liquid core microcapsules by using electrostatic spray method[J]. J Univ Shanghai Sci Technol, 2007, 29(4): 349-352.(in Chinese) |
| [19] | O'DONNELL P B, MC-GINITY J W. Preparation of microspheres by the solvent evaporation technique[J]. Adv Drug Delivery Rev, 1997, 28(1): 25-42. |
| [20] | 李志强, 任彦荣. 微胶囊技术及其应用研究进展[J]. 化学推进剂与高分子材料, 2004, 2(6): 19-23. LI Zhiqiang, REN Yanrong. Microencapsulation technology and research progress of its application[J]. Chem Propellants Polym Mater, 2004, 2(6): 19-23.(in Chinese) |
| [21] | NIXON J R. Preparation of microcapsules with possible pharmaceutical use[J]. Endeavour, 1985, 9(3): 123-128. |
| [22] | SOPPIMATH K S, KULKARNI A R, AMINABHAVI T M, et al. Cellulose acetate microspheres prepared by O/W emulsification and solventevaporation method[J]. J Microencapsulation, 2001, 18(6): 811-817. |
| [23] | 付颖, 叶非, 王常波. 微胶囊剂农药发展概述[J]. 农药科学与管理, 2001, 22(4): 39-41. FU Ying, YE Fei, WANG Changbo. The development of microencapsulation of pesticide[J]. Pestic Sci Admin, 2001, 22(4): 39-41.(in Chinese) |
| [24] | ZHANG Jing, COULSTON R J, JONES S T, et al. One-step fabrication of supramolecular microcapsules from microfluidic droplets[J]. Science, 2012, 335(6069): 690-694. |
| [25] | EJIMA H, RICHARDSON J J, LIANG K, et al. One-step assembly of coordination complexes for versatile film and particle engineering[J]. Science, 2013, 341(6142): 154-157. |
| [26] | TORRES P, VILLA F, GONZÁLEZ J, et al. Preparation and characterization of the emamectin benzoate/hydroxypropyl-b-cyclodextrin inclusion complex[J]. J Chil Chem Soc, 2011, 56(4): 951-954. |
| [27] | 张可达, 徐冬梅, 王平. 微胶囊化方法[J]. 功能高分子学报, 2001, 14(4): 474-480. ZHANG Keda, XU Dongmei, WANG Ping. Microencapsulation method[J]. J Funct Polym, 2001, 14(4): 474-480. (in Chinese) |
| [28] | 吕静, 李丹, 孙建兵, 等. 低分子量聚乳酸包膜尿素的缓释特性及其减少氨挥发的作用[J]. 中国农业科学, 2012, 45(2): 283-291. LÜ Jing, LI Dan, SUN Jianbing, et al. Slow release characteristics of the low molecular weight polylactic acid-coated urea and its reduction effects on soil ammonia volatilization[J]. Scientia Agricultura Sinica, 2012, 45(2): 283-291. (in Chinese) |
| [29] | 夏晓静, 周建平, 王翔, 等. 伊维菌素聚乳酸微球的制备[J]. 中国药科大学学报, 2004, 35(5): 429-432. XIA Xiaojing, ZHOU Jianping, WANG Xiang, et al. Preparation of polylactic acid microspheres loading ivermectin[J]. J China Pharm Univ, 2004, 35(5): 429-432. (in Chinese) |
| [30] | 郭瑞峰, 黄彬彬, 杨晓伟, 等. 毒死蜱-聚乳酸微球的制备及其性能评价[J]. 农药学学报, 2011, 13(4): 409-414. GUO Ruifeng, HUANG Binbin, YANG Xiaowei, et al. Preparation and characteristics analysis of microspheres of chlorpyrifos and polylactic acid[J]. Chin J Pestic Sci, 2011, 13(4): 409-414. (in Chinese) |
| [31] | CARRERAS N, ACUÑA V, MARTÍ M, et al. Drug release system of ibuprofen in PCL-microspheres[J]. Colloid Polym Sci, 2013, 291(1): 157-165. |
| [32] | 杨石有, 刘德坤, 张翠, 等. 毒死蜱微球和乳油在水中的消解动态及其对白纹伊蚊幼虫的毒力[J]. 农药学学报, 2013, 15(4): 464-468. YANG Shiyou, LIU Dekun, ZHANG Cui, et al. Decline dynamics of chlorpyrifos microspheres and emulsifiable concentrate in water and its toxicity to the larvae of Aedes albopictus[J]. Chin J Pestic Sci, 2013, 15(4): 464-468. (in Chinese) |
| [33] | 孟锐, 刘双清, 朱锐, 等. 可降解聚碳酸亚丙酯-毒死蜱微胶囊的制备及缓释性能评价[J]. 农药学学报, 2012, 14(5): 565-573. MENG Rui, LIU Shuangqing, ZHU Rui, et al. Preparation of degradable poly(propylene carbonate)-chlorpyrifos microcapsule and performance evaluation on its controlled release[J]. Chin J Pestic Sci, 2012, 14(5): 565-573. (in Chinese) |
| [34] | MATSUNAMI Y, ICHIKAWA K. Characterization of the structures of poly(urea-urethane) microcapsules[J]. Int J Pharm, 2002, 242(1-2): 147-153. |
| [35] | SOTO-PORTAS M L, ARGILLIER J F, MECHIN F, et al. Preparation of oily core polyamide microcapsules via interfacial polycondensation[J]. Polym Int, 2003, 52(4): 522-527. |
| [36] | 李北兴, 王凯, 张大侠, 等. 高含量二甲戊灵微囊悬浮剂物理稳定性的影响因素及优化[J]. 农药学学报, 2013, 15(6): 692-698. LI Beixing, WANG Kai, ZHANG Daxia, et al. Factors that affecting physical stability of high content pendimethalin capsule suspension and its optimization[J]. Chin J Pestic Sci, 2013, 15(6): 692-698. (in Chinese) |
| [37] | 傅桂华, 钟滨, 陈建宇, 等. 界面聚合法制备农药微胶囊剂的研究[J]. 农药, 2005, 44(2): 66-68. FU Guihua, ZHONG Bin, CHEN Jianyu, et al. Pesticide microcapsules prepared by an interfacial polymerization method[J]. Chin J Pestic, 2005, 44(2): 66-68. (in Chinese) |
| [38] | 陶晡, 康占海, 张金林. 硅酸镁铝及其与黄原胶协同使用对30% 辛硫磷微囊悬浮剂贮存物理稳定性的影响[J]. 农药学学报, 2012, 14(5): 574-578. TAO Bu, KANG Zhanhai, ZHANG Jinlin. Study on influence of veegum and the coordination of veegum with xanthan gum to physical stability of phoxim 300 capsule suspension[J]. Chin J Pestic Sci, 2012, 14(5): 574-578. (in Chinese) |
| [39] | HICKEY J, BURKE N A D, STÖVER H D H. Layer-by-layer deposition of clay and a polycation to control diffusive release from polyurea microcapsules[J]. J Membr Sci, 2011, 369(1-2): 68-76. |
| [40] | HONG K J, PARK S M. Preparation and characterization of polyurea microcapsules with different diamines[J]. Mater Res Bull, 1999, 34(6): 963-969. |
| [41] | TAKASU M, KAWAGUCHI H. Preparation of colored latex with polyurea shell by miniemulsion polymerization[J]. Colloid Polym Sci, 2005, 283(7): 805-811. |
| [42] | GAUDIN F, SINTES-ZYDOWICZ N. Poly(urethane-urea) nanocapsules prepared by interfacial step polymerisation in miniemulsion: the droplet size: a key-factor for the molecular and thermal characteristics of the polymeric membrane of the nanocapsules?[J]. Colloids Surf A, 2011, 384(1-3): 698-712. |
| [43] | ZHU Aiping, LI Fengjuan, JI Lijun. Poly(lactic acid)/N-maleoylchitosan core-shell capsules: preparation and drug release properties[J]. Colloids Surf B, 2012, 91: 162-167. |
| [44] | TSUDA N, OHTSUBO T, FUJI M. Preparation of self-bursting microcapsules by interfacial polymerization[J]. Adv Powder Technol, 2012, 23(6): 724-730. |
| [45] | JABBARI E, KHAKPOUR M. Morphology of and release behavior from porous polyurethane microspheres[J]. Biomaterials, 2000, 21(20): 2073-2079. |
| [46] | WANG Mian, ZHANG Kui, WU Wei, et al. Synthesis of temperature-responsive hybrid capsules and their controlled release property[J]. Colloids Surf A, 2011, 385(1-3): 126-133. |
| [47] | KIM K S, LEE J Y, PARK B J, et al. Synthesis and characteristics of microcapsules containing electrophoretic particle suspensions[J]. Colloid Polym Sci, 2006, 284(7): 813-816. |
| [48] | FAN Chuangjie, ZHOU Xiaodong. Influence of operating conditions on the surface morphology of microcapsules prepared by in situ polymerization[J]. Colloids Surf A, 2010, 363(1-3): 49-55. |
| [49] | 常怀春, 吕通建, 郭轶超, 等. 酚醛树脂为囊壁的微胶囊红磷的制备及其在电缆料中的阻燃应用[J]. 塑料工业, 2011, 39(增刊1): 89-92. CHANG Huaichun, LÜ Tongjian, GUO Yichao, et al. Preparation of microencapsulated red phosphorus with phenol-formaldehyde resin as shell and its flame-retardant application in cable compound[J]. China Plast Ind, 2011, 39(Suppl.1): 89-92.(in Chinese) |
| [50] | KAGE H, KAWAHARA H, HAMADA N, et al. Operating conditions and microcapsules generated by in situ polymerization[J]. Adv Powder Technol, 2002, 13(3): 265-285. |
| [51] | 赵德, 刘峰, 慕卫, 等. 毒死蜱微囊悬浮剂的制备及微囊化条件的优化[J]. 农药学学报, 2006, 8(1): 77-82. ZHAO De, LIU Feng, MU Wei, et al. Preparation of chlorpyrifos aqueous capsule suspension and optimization of encapsulation conditions[J]. Chin J Pestic Sci, 2006, 8(1): 77-82. (in Chinese) |
| [52] | SUKHORUKOV G B, ANTIPOV A A, VOIGT A, et al. pH-controlled macromolecule encapsulation in and release from polyelectrolyte multilayer nanocapsules[J]. Macromol Rapid Commun, 2001, 22(1): 44-46. |
| [53] | ATKKIN R, DAVIES P, HARDY J, et al. Preparation of aqueous core/polymer shell microcapsules by internal phase separation[J]. Macromolecules, 2004, 37(21): 7979-7985. |
| [54] | SU Junfeng, SCHLANGEN E. Synthesis and physicochemical properties of high compact microcapsules containing rejuvenator applied in asphalt[J]. Chem Eng J, 2012, 198-199: 289-300. |
| [55] | SU Junfeng, SCHLANGEN E, QIU Jian. Design and construction of microcapsules containing rejuvenator for asphalt[J]. Powder Technol, 2013, 235: 563-571. |
| [56] | SU Junfeng, WANG Xinyu, DONG Hua. Influence of temperature on the deformation behaviors of melamine-formaldehyde microcapsules containing phase change material[J]. Mater Lett, 2012, 84: 158-161. |
| [57] | 黄彬彬, 骆桂红, 童小钰, 等. 复凝聚法制备甲氨基阿维菌素苯甲酸盐微囊[J]. 农药学学报, 2009, 11(4): 493-498. HUANG Binbin, LUO Guihong, TONG Xiaoyu, et al. Preparation of emamectin-benzoate microcapsules by complex coacervation[J]. Chin J Pestic Sci, 2009, 11(4): 493-498. (in Chinese) |
| [58] | NAKAGAWA K, NAGAO H. Microencapsulation of oil droplets using freezing-induced gelatin-acacia complex coacervation[J]. Colloids Surf A, 2012, 411: 129-139. |
| [59] | SHIMOKAWA K I, SAEGUSA K, WADA Y, et al. Physicochemical properties and controlled drug release of microcapsules prepared by simple coacervation[J]. Colloids Surf B, 2013, 104: 1-4. |
| [60] | 关英, 张拥军, 张文静, 等. 层层自组装膜的研究: 从基础到生物医学领域中的应用[J]. 高分子通报, 2013(1): 40-52. GUAN Ying, ZHANG Yongjun, ZHANG Wenjing, et al. Layer-by-layer assembled films: from fundamentals to biomedical applications[J]. Polym Bull, 2013(1): 40-52. (in Chinese) |
| [61] | 仝维鋆, 高长有. 层层组装微胶囊的制备及其智能响应与物质包埋释放性能[J]. 高等学校化学学报, 2008, 29(7): 1285-1298. TONG Weijun, GAO Changyou. Layer-by-layer assembled microcapsules: fabrication, stimuli-responsivity, loading and release[J]. Chem J Chin Univ, 2008, 29(7): 1285-1298. (in Chinese) |
| [62] | PONGJANYAKUL T, PUTTIPIPATKHACHORN S. Modulating drug release and matrix erosion of alginate matrix capsules by microenvironmental interaction with calcium ion[J]. Eur J Pharm Biopharm, 2007, 67(1): 187-195. |
| [63] | WICHCHUKIT S, OZTOP M H, MC-CARTHY M J, et al. Whey protein/alginate beads as carriers of a bioactive component[J]. Food Hydrocolloids, 2013, 33(1): 66-73. |
| [64] | SHULKIN A, STÖVER H D H. Microcapsules from styrene-maleic anhydride copolymers: study of morphology and release behavior[J]. J Membr Sci, 2002, 209(2): 433-444. |
| [65] | TENG Zi, LUO Yangchao, WANG Qin. Carboxymethyl chitosan-soy protein complex nanoparticles for the encapsulation and controlled release of vitamin D3[J]. Food Chem, 2013, 141(1): 524-532. |
| [66] | HUI P C L, WANG Wenyi, KAN Chiwai, et al. Preparation and characterization of chitosan/sodium alginate (CSA) microcapsule containing cortex moutan[J]. Colloids Surf A, 2013, 434: 95-101. |
| [67] | DINSMORE A D, HSU M F, NIKOLAIDES M G, et al. Colloidosomes: selectively permeable capsules composed of colloidal particles[J]. Science, 2002, 298(5595): 1006-1009. |
| [68] | 贾进伟, 张绍勇, 张爽, 等. 负载戊唑醇的壳聚糖纳米胶囊的制备与性能研究[J]. 农药学学报, 2013, 15(5): 582-586. JIA Jinwei, ZHANG Shaoyong, ZHANG Shuang, et al. Preparation and properties of chitosan nanocapsules loaded with tebuconazole[J]. Chin J Pestic Sci, 2013, 15(5): 582-586. (in Chinese) |
| [69] | 周斌, 赵静. 层层自组装制备阿维菌素微胶囊及其释药行为[J]. 精细化工, 2008, 25(7): 625-627. ZHOU Bin, ZHAO Jing. Microencapsulation and release kinetics of abamectin by layer-by-layer polyelectrolyte self-assembly[J]. Fine Chem, 2008, 25(7): 625-627. (in Chinese) |
| [70] | LEE M H, HRIBAR K C, BRUGAROLAS T, et al. Harnessing interfacial phenomena to program the release properties of hollow microcapsules[J]. Adv Funct Mater, 2012, 22(1): 131-138. |
| [71] | BENTLEY W E, PAYNE G F. Natures other self-assemblers[J]. Science, 2013, 341(6142): 136-137. |
| [72] | MAL P, BREINER B, RISSANEN K, et al. White phosphorus is air-stable within a self-assembled tetrahedral capsule[J]. Science, 2009, 324(5935): 1697-1699. |
| [73] | 中华人民共和国农业部农药检定所. 农药电子手册单机企业版[CP]. (2014-01). ICAMA of China. The e-pesticide manual (stand-alone edition) [CP]. (2014-01). |
| [74] | 吴学民, 徐妍. 噻虫啉微囊粉剂和悬浮剂及其制备方法和用途: 中国,201010103001 [P]. 2010-06-23. WU Xuemin, XU Yan. Preparation method and uses of thiacloprid CJF and suspension concentrate: CN, 201010103001 [P]. 2010-06-23. |
| [75] | 孙培章. 30% 毒死蜱微囊悬浮剂防治花生蛴螬田间药效试验[J]. 安徽农业科学, 2008, 36(27): 11839, 11863. SUN Peizhang. Field efficacy trials of 30% microcapsule suspension of chlorpyrifos against peanut white grub[J]. J Anhui Agri Sci, 2008, 36(27): 11839, 11863.(in Chinese) |
| [76] | 陆年宏, 谭伟龙, 钱趋程, 等. JWX-Ⅲ型微胶囊悬浮剂滞留喷洒对蚊蝇的灭效研究[J]. 中华卫生杀虫药械, 2013, 19(2): 108-110. LU Nianhong, TAN Weilong, QIAN Qucheng, et al. Effect observation on JWX-Ⅲ in residual spraying against mosquitoes and flies[J]. Chin J Hyg Insect Equip Apr, 2013, 19(2): 108-110. (in Chinese) |
| [77] | 马春娟, 陶丽华. 复凝聚法制备嘧菌酯微囊剂工艺研究[J]. 安徽农业科学, 2008, 36(9): 3496, 3508. MA Chunjuan, TAO Lihua. Study on the technology of preparing azoxystrobin microcapsules by complex coacervation[J]. J Anhui Agric, 2008, 36(9): 3496, 3508. (in Chinese) |
| [78] | 周训卿, 曹立冬, 刘亚静, 等. 嘧菌酯微囊的制备及其性能表征[J]. 农药学学报, 2014, 16(2): 213-219. ZHOU Xunqing, CAO Lidong, LIU Yajing, et al. Preparation and performance characteristics of azoxystrobin microcapsules[J]. Chin J Pestic Sci, 2014, 16(2): 213-219. (in Chinese) |
| [79] | 焦永康, 康占海, 庞民好, 等. 10%吡虫啉微胶囊悬浮剂的研制及其对棉蚜的防治效果[J]. 河北农业大学学报, 2011, 34(6): 83-86. JIAO Yongkang, KANG Zhanhai, PANG Minhao, et al. The preparation of 10% imidacloprid CS and the control efficacy on cotton aphids[J]. J Agric Univ Hebei, 2011, 34(6): 83-86. (in Chinese) |
| [80] | 韩志任, 杜有辰, 李刚, 等. 阿维菌素脲醛树脂微胶囊的制备及其缓释性能[J]. 农药学学报, 2007, 9(4): 405-410. HAN Zhiren, DU Youchen, LI Gang, et al. Preparation and sustained-release behavior of abamectin urea-formaldehyde resin microcapsules[J]. Chin J Pestic Sci, 2007, 9(4): 405-410. (in Chinese) |
| [81] | KJÆR J, ERNSTSEN V, JACOBSEN O H, et al. Transport modes and pathways of the strongly sorbing pesticides glyphosate and pendimethalin through structured drained soils[J]. Chemosphere, 2011, 84(4): 471-479. |
| [82] | UTULU S N, AKOBUNDU I O, FAYEMI A A A. Persistence and downward movement of some selected herbicides in the humid and subhumid tropics[J]. Crop Prot, 1986, 5(2): 129-136. |
| [83] | 葛艳蕊, 冯薇, 吕均超, 等. 除草剂广灭灵脲醛树脂微胶囊剂的研制[J]. 河北科技大学学报, 2010, 31(1): 48-51. GE Yanrui, FENG Wei, LÜ Junchao, et al. Study on preparation of urea-formaldehyde resin microcapsules of clomazone herbicide[J]. J Hebei Univ Sci Technol, 2010, 31(1): 48-51. (in Chinese) |
| [84] | 徐春红, 张维东. 除草剂 2, 4-D丁酯药害产生的原因及预防措施[J]. 上海蔬菜, 2010(2): 73-74. XU Chunhong, ZHANG Weidong. The causes and preventive measures of phytotoxicity of the herbicide 2, 4-D-butyl ester[J]. Shanghai Veg, 2010(2): 73-74. (in Chinese) |
| [85] | ELBAHRI Z, TAVERDET J L. Optimization of an herbicide release from ethylcellulose microspheres[J]. Polym Bull, 2005, 54(4-5): 353-363. |
| [86] | 中华人民共和国工业和信息化部. 中华人民共和国工业和信息化部公告(2013年第52号) [EB/OL]. (2013-10-17)[2013-10-23]. http://www.miit.gov.cn/n11293472/n11293832/n12845605/n13916898/15670646.html MIIT PR-China. Announcement of the Ministry of Industry and Information Technology of the Peoples Republic of China (No.52, 2013) [EB/OL]. (2013-10-17)[2013-10-23]. http://www.miit.gov.cn/n11293472/n11293832/n12845605/n13916898/15670646.html (in Chinese) |
| [87] | 华乃震. 农药剂型的进展和动向(中)[J]. 农药, 2008, 47(3): 157-160. HUA Naizhen. Advance and trend of pesticide formulation development[J]. Agrichemicals, 2008, 47(3): 157-160. (in Chinese) |
| [88] | 王雅玲, 杨代斌, 袁会珠, 等. 低温胁迫下戊唑醇和苯醚甲环唑种子包衣对玉米种子出苗和幼苗的影响[J]. 农药学学报, 2009, 11(1): 59-64. WANG Yaling, YANG Daibin, YUAN Huizhu, et al. Effects of seed-coating tebuconazole and difenoconazole on emergence of maize seeds and response of seedling at chilling stress[J]. Chin J Pestic Sci, 2009, 11(1): 59-64. (in Chinese) |
| [89] | 王娜. 戊唑醇微囊种衣剂的制备及其对玉米安全性机理[D]. 雅安: 四川农业大学, 2011: 16-35. WANG Na. The preparation of microcapsuled tebuconazole seed coatings formulation and its safety mechanism on maize [D]. Ya'an: Sichuan Agricultural University, 2011: 16-35. (in Chinese) |
| [90] | 孙竹波, 孔繁华, 刘震, 等. 3.3% 1-甲基环丙烯微胶囊剂(聪明鲜)对柿子保鲜效果的影响[J]. 山东农业科学, 2007(4): 107-108. KONG Zhubo, KONG Fanhua, LIU Zhen, et al. Effect of 1-methylcyclopropene capsule on the freshness of persimmon[J]. Shandong Agric Sci, 2007(4): 107-108. (in Chinese) |
| [91] | ZHAO L J, YANG X N, LI X Y, et al. Antifungal, insecticidal and herbicidal properties of volatile components from paenibacillus polymyxa strain BMP-11[J]. Agric Sci China, 2011, 10(5): 728-736. |
| [92] | 周一万, 冯俊涛, 张兴. 冬青油微囊悬浮剂的制备及其杀蚜活性研究[J]. 农药学学报, 2013, 15(2): 228-233. ZHOU Yiwan, FENG Juntao, ZHANG Xing. Preparation of wintergreen oil capsule suspension and control efficacy on Macrosiphoniella sanborni[J]. Chin J Pestic Sci, 2013, 15(2): 228-233. (in Chinese) |
| [93] | 朱晓丽, 顾相伶, 张志国, 等. 单凝聚与复凝聚法制备昆虫激素十二醇微胶囊及其释放行为[J]. 高分子学报, 2007(5): 491-496. ZHU Xiaoli, GU Xiangling, ZHANG Zhiguo, et al. Preparation of insect sex pheromone dodecanol containing microcapsules by simple and complex coacervations and their release behavior[J]. Acta Polym Sin, 2007(5): 491-496. (in Chinese) |
| [94] | ATTERHOLT C A, DELWICHE M J, RICE R E, et al. Controlled release of insect sex pheromones from paraffin wax and emulsions[J]. J Controlled Release, 1999, 57(3): 233-247. |
| [95] | 徐妍, 吴国林, 吴学民, 等. 梨小食心虫性信息素微囊化及释放特性[J]. 农药学学报, 2009, 11(1): 65-71. XU Yan, WU Guolin, WU Xuemin, et al. Microcapsulating and controlled release characteristics of sex pheromone of Grapholitha molesta[J]. Chin J Pestic Sci, 2009, 11(1): 65-71. (in Chinese) |
| [96] | KNIGHT A L, LIGHT D M. Adding microencapsulated pear ester to insecticides for control of Cydia pomonella (Lepidoptera: Tortricidae) in apple[J]. Pest Manag Sci, 2013, 69: 66-74. |
| [97] | 曹坳程, 张文吉, 刘建华. 溴甲烷土壤消毒替代技术研究进展[J]. 植物保护, 2007, 33(1): 15-20. CAO Aocheng, ZHANG Wenji, LIU Jianhua. Progress in the alternatives to methyl bromide in soil disinfestation[J]. Plant Prot, 2007, 33(1): 15-20. (in Chinese) |
| [98] | 曹坳程, 褚世海, 郭美霞, 等. 硫酰氟——溴甲烷土壤消毒潜在的替代品[J]. 农药学学报, 2002, 4(3): 91-93. CAO Aocheng, CHU Shihai, GUO Meixia, et al. Sulfuryl fluoride—a potential alternative to methyl bromide in soil fumigation[J]. Chin J Pestic Sci, 2002, 4(3): 91-93. (in Chinese) |
| [99] | 张贵森. 不同壁材高效氯氰菊酯微囊悬浮剂应用及环境特性的影响 [D]. 泰安: 山东农业大学, 2012: 29-30. ZHANG Guisen. Effect of different wall material of Beta-cypermethrin microcapsule suspension on the differences of application environment characteristics [D]. Tai'an: Shandong Agricultural University, 2012: 29-30. (in Chinese) |
 2014, Vol. 16
2014, Vol. 16


