2. 青岛市农业环保能源工作站, 山东 青岛 266000;
3. 湖南中烟工业有限责任公司, 长沙 471000;
4. 山东省烟草专卖局, 济南 250100
2. Qingdao Workstation for Rural Energy & Environmental Protection, Qingdao 266000, Shandong Province, China;
3. China Tobacco Hunan Industrial Co., Ltd., Changsha 471000, China;
4. Shandong Tobacco Monopoly Administration, Ji'nan 250100, China
噻虫嗪(thiamethoxam)属于第二代新烟碱类-硫烟碱杀虫剂[1],相对分子质量为291.7,结构式见Scheme 1,由瑞士诺华(现先正达)公司1991年开发并于1997年上市。它是一种结构新颖的高效、低毒、广谱型烟碱类杀虫剂,具有良好的胃毒和触杀活性[2, 3]。该药用于防治水稻、小麦、棉花及果树、蔬菜作物上的刺吸式口器害虫,如稻飞虱、蚜虫、叶蝉、蓟马、白粉虱以及马铃薯甲虫等,防治效果良好[4],是有机磷、氨基甲酸酯类农药较好的替代品。
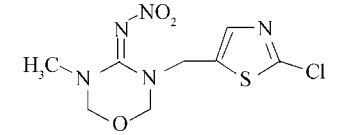 | Scheme 1 |
目前,关于噻虫嗪在不同介质中的残留检测方法已有报道。黄伟等[5]采用Pesticarb NH2-SPE净化柱,V(甲苯)∶V(乙腈)=7∶3溶液洗脱,对马铃薯中噻虫嗪的残留进行了检测,效果较好;Singh等[6]采用微波辅助萃取(microwave aided extraction,MAE)前处理方法提取5种蔬菜(甘蓝、番茄、马铃薯、辣椒、胡椒)样品中的噻虫嗪残留,其添加回收率较高;刘宾等[7]采用甲醇提取,氯化钠水溶液洗涤,二氯甲烷萃取,高效液相色谱法测定了噻虫嗪在菠菜中的消解动态和最终残留;Obana等[8]以甲醇作提取剂,以石墨化碳柱净化,采用液相色谱-质谱联用(LC-MS)法分析了噻虫嗪在12种不同水果和蔬菜样品中的残留,其回收率为70%~95%。目前有关噻虫嗪在烟草上的残留检测技术和消解行为尚未见报道,且烟草中含色素、烟碱、多酚等杂质较多,采用传统的提取、净化方法效果较差。鉴于此,本研究建立了噻虫嗪在烟草和土壤中残留及消解动态的HPLC-UV检测方法,以期为噻虫嗪在烟草上的检测技术研究、最大残留限量(MRL)标准的制定及其合理使用提供参考。
1 材料与方法 1.1 主要仪器及试剂
Waters Alliance 2695/2487高效液相色谱-紫外检测器(HPLC-UV)和Waters Sun Fire RP-18色谱柱(250 mm ×4.6 mm,5.0 μm),美国Waters公司;RSQ-60AS超声波振荡机,宁波荣顺公司;Cleanert NH2-SPE净化柱(500 mg/6 mL),天津博纳艾杰尔科技有限公司。
99.5%噻虫嗪(thiamethoxam)标准品(德国Dr.E公司);22%高效氯氟氰菊酯·噻虫嗪微囊悬浮剂[噻虫嗪含量为12.6%,先正达(中国)公司];乙腈、甲醇、二氯甲烷(经重蒸馏处理)、无水硫酸钠(于600 ℃烘5 h,冷却后备用)、去离子水、氯化钠,均为分析纯,甲醇为色谱纯。
1.2 分析方法 1.2.1 样品的提取与净化提取:准确称取20.0 g鲜烟叶样品置于三角瓶中(或干烟叶样品8.0 g,使用前用10 mL去离子水浸润),加入80 mL乙腈,振荡提取1 h后加入适量氯化钠,再振荡10 min,静置;经加有10 g无水硫酸钠的筒形漏斗过滤;准确量取20 mL滤液于100 mL浓缩瓶中,旋蒸浓缩至近干;加入3 mL V(二氯甲烷)∶ V(甲醇)=99∶1的混合溶液溶解提取物,待净化。
净化:用5 mLV(二氯甲烷)∶ V(甲醇)=99∶1的混合溶液预淋洗Cleanert NH2-SPE净化柱,将上述提取物转入柱中,再用12 mL此混合溶液分3次洗瓶、淋洗,收集淋洗液,浓缩至近干,用甲醇定容至2 mL,经0.22 μm滤膜过滤后待测。
1.2.2 检测条件流动相为V(甲醇)∶V(水)=20∶80;流速为0.8 mL/min;柱温30 ℃;测定波长254 nm;进样量10 μL。在此条件下,噻虫嗪的保留时间为15.4 min。
1.2.3 标准曲线的绘制采用外标法定量。准确称取0.01 g噻虫嗪标准品,用甲醇溶解并定容至100 mL,配制成100 mg/L的噻虫嗪母液;再用甲醇逐级稀释成质量浓度分别为0.01、0.05、0.1、0.5、1.0、5.0和10.0 mg/L的标准曲线工作液,按1.2.2节条件进行检测。以进样质量浓度为横坐标,所对应的色谱峰面积为纵坐标绘制标准曲线。
1.2.4 添加回收试验在鲜烟叶和干烟叶空白样品中,分别添加噻虫嗪标准溶液,添加水平鲜烟叶为0.01、0.5和5 mg/kg,干烟叶为0.05、0.5和5 mg/kg,按照1.2.1和1.2.2节条件进行样品处理和测定。每个水平重复5次。
1.3 田间试验参照《农药残留试验准则》[9]和《农药登记残留田间试验标准操作规程》[10],于2011年及2012年分别在山东青岛和湖南长沙进行田间试验,供试烟草品种分别为中烟100(山东青岛)和云烟87(湖南长沙)。试验设空白对照区、低剂量2次施药、低剂量3次施药、高剂量2次施药、高剂量3次施药和消解动态试验区,每个小区面积为30 m2,3次重复。小区之间设保护行,按照用药量由低到高排列。
1.3.1 消解动态试验于烟草现蕾期,按22%高效氯氟氰菊酯·噻虫嗪微囊悬浮剂制剂用量225 mL/hm2(噻虫嗪有效成分含量28.4 g/hm2)对水喷雾施药1次,分别于施药后1 h及1、3、5、7、14、21、28、35、42 d随机采集烟叶,每小区每次采集烟叶不少于50片,切碎缩分,留样200 g,备用。
1.3.2 最终残留试验按照制剂推荐低剂量150 mL/hm2(噻虫嗪有效成分含量18.9 g/hm2)和推荐高剂量225 mL/hm2(噻虫嗪有效成分含量28.4 g/hm2),于烟草现蕾初期-成熟期对水喷雾,分别施药2~3次,施药间隔期为7 d,每处理3次重复。分别于末次施药后7、14、21 d随机采集上、中和下部烟叶,采用三段式工艺烘烤,粉碎后过10目筛,所有样品于-20 ℃保存,待测。
2 结果与讨论 2.1 前处理条件的优化
烟草中含有较多的烟碱、多酚、色素等杂质,对前处理要求比较高,按文献[4, 5, 6, 7, 8]进行前处理的方法,不适合烟草中噻虫嗪的测定和分析。闫晓阳等[11]采用乙腈提取,C18柱、V(丙酮)∶V(正己烷)=1∶9 淋洗液净化,检测烟草中吡唑醚菌酯残留,净化效果较好,能有效去除烟草中的烟碱、多酚、色素等多种物质;王秀国等[12]采用乙腈提取,PSA(N-丙基乙二胺)柱、V(丙酮)∶V(正己烷)=1∶9淋洗液净化,检测烟草中氯溴异氰尿酸残留,净化效果较好。鉴于此,本研究分别考察了PSA柱、Florisil柱和NH2柱3种净化柱及V(二氯甲烷)∶V(甲醇)=99∶1、95∶5、90 ∶10),V(正己烷)∶V(甲醇)=99∶1、95∶5、90∶10淋洗液对净化效果的影响。结果表明:不同组合间净化效果差别较大,其中采用NH2柱且以V(二氯甲烷)∶V(甲醇)=99∶1为淋洗液时净化效果较好,目标峰附近无杂质干扰且回收率符合残留试验标准的要求。故选此组合去除烟草中的杂质。
2.2 方法的线性范围及检出限结果表明:在0.01~10 mg/L范围内,噻虫嗪的峰面积(y)与质量浓度(x)间呈良好线性关系,回归方程为y=932.292 7+42 367.87x,相关系数r=0.999 7。按照3倍信噪比(S/N)计算,仪器检出限(LOD)为0.05 ng;通过添加回收率确认,噻虫嗪在鲜烟叶中的定量限(LOQ)为0.01 mg/kg,干烟叶中的LOQ为0.05 mg/kg。
2.3 方法的准确度及精密度添加回收试验结果见表 1。在0.01~5 mg/kg添加水平下,鲜烟叶中噻虫嗪的平均回收率为92%~95%,相对标准偏差(RSD)为4.5%~9.2%;在0.05~5 mg/kg添加水平下,干烟叶中噻虫嗪的平均回收率为91%~94%,RSD为5.9%~6.8%,均符合农药残留试验准则要求。典型色谱图如图 1所示,图中杂质峰相对较少,且在目标峰附近无杂质干扰,净化效果好。
| 表 1 噻虫嗪在鲜烟叶和干烟叶中的添加回收率及相对标准偏差Table 1 Recoveries and RSDs of thiamethoxam in fresh tobacco leaves and cured tobacco leaves at different levels |
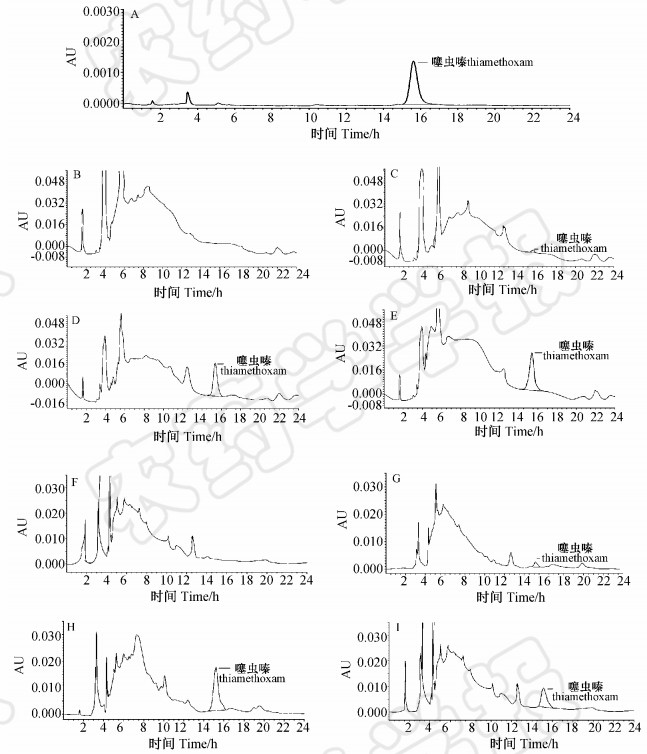 | A.噻虫嗪标样(1.0 mg/L);B.鲜烟叶空白;C.鲜烟叶添加(0.01 mg/kg);D.鲜烟叶添加(0.5 mg/kg);E.鲜烟叶样品;F.干烟叶空白;G.干烟叶添加(0.05 mg/kg);H.干烟叶添加(0.5 mg/kg);I.干烟叶样品。 A. Standard chromatogram at 1.0 mg/L; B. Blank green leaf; C. Green leaf spiked at 0.01 mg/kg; D. Green leaf spiked at 0.5 mg/kg; E. Green leaf sample; F. Blank dry leaf; G. Dry leaf spiked at 0.05 mg/kg; H. Dry leaf spiked at 0.5 mg/kg; I. Dry leaf sample. 图 1 噻虫嗪的典型色谱图Fig. 1 Typical HPLC chromatogram of thiamethoxam |
2.4 噻虫嗪在烟叶中的消解动态
结果(见图 2和表 2)表明:在噻虫嗪有效成分28.4 g/hm2施药剂量下,山东2年鲜烟叶样品中,施药1 h后噻虫嗪的原始沉积量为7.51~7.98 mg/kg,5 d时消解率均超过65%,28 d时消解率均超过90%,理论半衰期为4.6~8.1 d。湖南2年烟叶样品中,施药1 h后噻虫嗪的原始沉积量为1.82~4.96 mg/kg,5 d时消解率均超过70%,14 d时消解率均超过90%,到42 d时其残留量均低于检出限,理论半衰期为1.3~5.5 d。
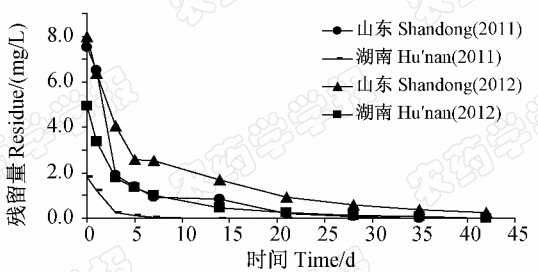 | 图 2 噻虫嗪在鲜烟叶中的消解动态Fig. 2 Decline curves of thiamethoxam in fresh tobacco leaves |
| 表 2 噻虫嗪在鲜烟叶中的消解动力学方程及其相关系数Table 2 Dissipation and correlation parameters of thiamethoxam in fresh tobacco leaves |
结果(见表 3)表明:在噻虫嗪有效成分18.9和28.4 g/hm2 2个剂量下,分别施用22%高效氯氟氰菊酯·噻虫嗪微囊 悬浮剂 2~3次,施药间隔7 d,距末次施药7 d后山东、湖南2年2地烟叶样品中噻虫嗪残留量为0.05~0.80 mg/kg,均低于国际烟草合作研究中心(CORESTA)指导性残留限量标准规定的MRL值(5.0 mg/kg)[13]。表明该制剂中噻虫嗪农药残留降解较快,对大田环境较为安全。
| 表 3 噻虫嗪在干烟叶中的最终残留量Table 3 The final residue of thiamethoxam in cured tobacco leaves |
3 结论
建立了采用高效液相色谱-紫外检测器法检测鲜烟叶和干烟叶中噻虫嗪残留量的分析方法,该方法重现性好,前处理方法操作简单,净化比较彻底,精密性、准确度及检出限均符合农药残留分析要求。采用该方法可以实现烟叶中噻虫嗪残留的检测。
噻虫嗪在烟叶中的理论半衰期为1.27~8.11 d,为易降解农药。按照推荐剂量和次数规范施药,距末次施药7 d后,烟叶中噻虫嗪的残留量远低于CORESTA指导性残留限量规定的限量值5.0 mg/kg,烤后烟叶中农药残留超标风险低,对人体安全。在目前氯氟氰菊酯等拟除虫菊酯类农药、吡虫啉等新烟碱类农药抗药性较严重、农药残留风险较大的情况下,噻虫嗪可以作为防治烟蚜和烟青虫的较有效的农药,具有较高的推广应用价值。
| [1] | 程霞. 第二代新烟碱类杀虫剂噻虫嗪的开发[J]. 世界农药, 2001, 23(4): 17-25.CHENG Xia. Development of the second generation new nicotinoid insecticide thiamethoxam[J]. World Pestic, 2001, 23(4): 17-25. (in Chinese) |
| [2] | 陶贤鉴, 黄超群, 罗亮明. 新一代烟碱类杀虫剂——噻虫嗪的合成研究[J]. 现代农药, 2006, 5(1): 11-13.TAO Xianjian, HUANG Chaoqun, LUO Liangming. Research on synthesis methods of thiamethoxam[J]. Modern Agrochem, 2006, 5(1): 11-13. (in Chinese) |
| [3] | 王险峰. 进口农药应用手册[M]. 北京: 中国农业出版社, 2000: 61-63.WANG Xianfeng. Application Manual of Import Pesticide[M]. Beijing: China Agricultural Press, 2000: 61-63. (in Chinese) |
| [4] | 张国生, 侯广新. 烟碱类杀虫剂的应用、开发现状及展望[J]. 农药科学与管理, 2004, 25(3): 22-26.ZHANG Guosheng, HOU Guangxin. Present status of development and prospect of nicotinoid insecticides[J]. Pestic Sci Admin, 2004, 25(3): 22-26. (in Chinese) |
| [5] | 黄伟,李建中,王会利,等. 噻虫嗪在马铃薯中的残留分析[J]. 环境化学,2010, 29(5): 970-973.HUANG Wei, LI Jianzhong, WANG Huili, et al. Analysis of the residue of thiamethoxam on potato[J]. Environm Chem, 2010, 29(5): 970-973.(in Chinese) |
| [6] | SINGH S B, FOSTER G D, KHAN S U. Microwave-assisted extraction for the simultaneous determination of thiamethoxam, imidacloprid, and carbendazim residues in fresh and cooked vegetable samples[J]. J Agric Food Chem, 2004, 52(1): 105-109. |
| [7] | 刘宾, 郭栋梁, 毛江胜, 等. 菠菜中噻虫嗪的残留检测与消解动态[J]. 农药, 2009, 48(9): 667-674.LIU Bin, GUO Dongliang, MAO Jiangsheng, et al. Residue detection and degradation of thiamethoxam in spinach[J]. Agrochemicals, 2009, 48(9): 667-674. (in Chinese) |
| [8] | OBANA H, OKIHASHI M, AKUTSU K, et al. Determination of neonicotinoid pesticide residues in vegetables and fruits with solid phase extraction and liquid chromatography mass spectrometry[J]. J Agric Food Chem, 2003, 51(9): 2501-2505. |
| [9] | NY/T 788—2004, 农药残留试验准则[S]. 北京: 中国农业出版社, 2004.NY/T 788—2004, Guideline on pesticide residue trials [S]. Beijing: China Agricultural Press, 2004. (in Chinese) |
| [10] | 农业部农药检定所. 农药登记残留田间试验标准操作规程[S]. 北京: 中国标准出版社, 2007.Institute for the Control of Agrochemicals, Ministry of Agriculture, P. R. China. Standard operating procedures on pesticide residue field trials [S]. Beijing: Standards Press of China, 2007. (in Chinese) |
| [11] | 闫晓阳, 王秀国, 李义强, 等. 高效液相色谱法检测吡唑醚菌酯在烟叶和土壤中的残留及消解动态[J]. 农药学学报, 2013, 15(5): 528-533.YAN Xiaoyang, WANG Xiuguo, LI Yiqiang, et al. Residue and dissipation of pyraclostrobin by high performance liquid chromatography in tobacco and soil[J]. Chin J Pestic Sci, 2013, 15(5): 528-533.(in Chinese) |
| [12] | 王秀国, 李义强, 孙惠青, 等. 氯溴异氰尿酸在烟叶及其土壤中的残留分析及消解动态[J]. 农药学学报, 2012, 14(2): 191-197.WANG Xiuguo, LI Yiqiang, SUN Huiqing, et al. Residues and decline dynamics of chloroisobromine cyanuric acid in tobacco and soil[J]. Chin J Pestic Sci, 2012, 14(2): 191-197.(in Chinese) |
| [13] | CORESTA.CORESTA Guidance No. 1, 2013. The concept and implementation of agrochemical guidance residue levels[EB/OL].[2014-03-15]. http://www.coresta.org/ |
 2014, Vol. 16
2014, Vol. 16


