2. 上海市青浦区食用农产品检测中心, 上海 201799
2. Qingpu Edible Agricultural Products Testing Center, Shanghai City, Shanghai 201799, China
噻虫嗪(thiamethoxam),化学名称为3-(2-氯-1,3-噻唑-5-基甲基)-5-甲基-1,3,5- NFDA2 二嗪-4-基叉(硝基)胺(结构式见Scheme 1),原药为白色结晶粉末,易溶于丙酮、甲醇、二氯甲烷等有机溶剂,低毒,对眼睛和皮肤无刺激性。噻虫嗪是第2代新烟碱类杀虫剂的第1个代表化合物[1],不仅具有触杀、胃毒、内吸活性,而且高效、低毒、杀虫谱广,已广泛用于水稻、小麦、棉花、果树及蔬菜等作物上防治刺吸式害虫[2,3]。关于噻虫嗪在作物及土壤中的残留检测方法已有较多报道[4,5,6,7,8,9,10],多采用高效液相色谱法,以甲醇提取、二氯甲烷液-液分配、层析柱或SPE梯度淋洗净化进行样品前处理,存在提取时间长、过程繁琐,不易操控等不足。为此,本研究建立了一种简单、快速检测菠菜中噻虫嗪残留量的方法,并用该法研究了保护地和露地菠菜中噻虫嗪的残留消解规律及安全使用技术。
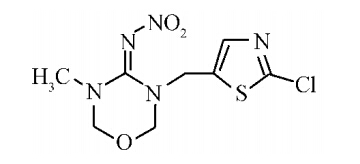 | Scheme 1 |
API 3200液相色谱-串联质谱仪(带岛津LC-20AB检测器,美国AB SCIEX公司);AUY120万分之一电子天平(日本岛津公司);MP1000B百分之一天平(上海舜宇恒平科学仪器有限公司);精密移液枪(Eppendorf 50~200 μL,100~1 000 μL,德国Eppendorf公司);SHA-C振荡器(常州国华电器有限公司);K600粉碎机(德国博朗电器公司);Milli-Q Advantage A10超纯水仪(美国Millipore公司);N-EVAPTM 111氮吹仪(美国Organomation Associates Inc.公司)。
98.6%噻虫嗪标准品(上海市农药研究所);25%噻虫嗪水分散粒剂(上海禾本药业有限公司);甲醇和乙腈均为色谱纯,甲苯和氯化钠均为分析纯。 1.2 田间试验
按照《农药残留试验准则》[11]进行。供试药剂为25%噻虫嗪水分散粒剂。试验小区面积15 m2,每处理3个重复,小区间设保护带,另设不施药空白对照区,用水量为750 kg/hm2。 1.2.1 消解动态试验
25%噻虫嗪水分散粒剂按照推荐剂量的1.5倍(有效成分45 g/hm2),于菠菜生长至4~5叶期时对水稀释后均匀喷洒在菠菜植株上,施药1次,分别于施药后2 h和1、3、5、7、10、14 d,在每个处理小区内对角线法随机选择6~12个点共12棵以上(不少于1 kg)生长正常、无病害、成熟的菠菜植株,切成长1 cm的小段,粉碎后至少留样100 g,于-18 ℃以下贮存,待测。 1.2.2 最终残留试验
25%噻虫嗪水分散粒剂按照推荐剂量(有效成分30 g/hm2)和推荐剂量的1.5倍(有效成分45 g/hm2),于菠菜生长至2~3叶期时对水稀释后首次施药,分别施2次和3次,施药间隔期7 d。分别于距末次施药后3、5、7 d取样。取样及样品预处理同1.2.1节。 1.3 样品前处理方法 1.3.1 提取
称取20 g(精确到0.01g)预处理好的样品于250 mL具塞三角烧瓶中,加入40 mL乙腈,振荡30 min,抽滤至装有6~7 g氯化钠的具塞量筒中。具塞后剧烈振荡1 min,在室温下静置30 min。 1.3.2 净化
吸取20 mL有机相于50 mL试管中,于45 ℃下氮吹至近干。用2 mL乙腈溶解后转移至用5 mL V(乙腈)∶ V(甲苯)=3∶1 的淋洗液预淋洗过的PC-NH2柱中,再用25 mL V(乙腈)∶ V(甲苯)=3∶1 的淋洗液淋洗。收集淋出液,于45 ℃下氮吹至近干,用流动相(VA∶ VB=2∶8,见表 1)定容至1 mL,过0.4 μm有机滤膜,待测。
由于液相色谱-串联质谱仪进样时的线性范围过窄,因此在进行添加回收率和残留量检测时,均用流动相(VA∶VB=2∶8)将样品稀释至线性范围内的浓度再进样。外标法定量,通过标准曲线计算样品中噻虫嗪的浓度。
| 表 1 流动相梯度洗脱条件 Table 1 Gradient elution conditions of mobile phase |
C18不锈钢色谱柱(150 mm×2.1 mm,3 μm);柱温50 ℃;流动相A为V(甲醇)∶V(2 mmol/L乙酸铵+0.1%乙酸水溶液)=5∶95,流动相B为V(甲醇)∶V(2 mmol/L乙酸铵+0.1%乙酸水溶液)=95∶5,梯度洗脱条件见表 1。进样体积20 μL。 1.3.3.2 质谱条件
电喷雾离子源ESI;扫描方式:正离子ESI+;喷雾电压5 500 V;雾化气压力225.8 kPa;气帘气压力137.9 kPa;辅助气压力344.75 kPa;离子源温度550 ℃;去簇电压(DP)40 V;碰撞能量(CE)17/23 eV;检测方式:多反应监测模式(MRM);定性离子对(m/z):292.1/211.2,292.1/132.0;定量离子对(m/z):292.1/211.2。 1.3.4 标准曲线绘制
准确称取25.4 mg噻虫嗪标准品,用甲醇溶解并配制成100 mg/L的标准储备液,再用甲醇稀释成10 mg/L的标准工作溶液。用菠菜空白样品溶液稀释标准工作溶液,配制成噻虫嗪质量浓度分别为0.01、0.02、0.05、0.1和0.2 mg/L 的系列基质匹配标准工作溶液,按1.3.3节条件检测。以噻虫嗪质量浓度为横坐标,相应的峰面积为纵坐标,绘制标准曲线。 1.3.5 添加回收试验
在对照区采集的空白菠菜样品中添加噻虫嗪标准溶液,添加水平分别为0.02、0.2和1.0 mg/kg,每个水平5次重复,按上述方法进行提取、净化和测定。 2 结果与分析 2.1 方法的线性范围和检出限
在0.01~0.2 mg/L范围内,噻虫嗪的质量浓度与峰面积之间存在显著的正相关关系,其线性回归方程为y=1.62×107x,r=0.997。通过添加回收试验确定方法的定量限(LOQ)为0.02 mg/kg,最小检出量为0.2 ng。 2.2 方法的准确度和精密度
结果(见表 2)表明:在0.02~1 mg/kg添加水平下,噻虫嗪的平均回收率在78%~101%之间,相对标准偏差(RSD)在3.1%~4.1%之间,其准确度和精密度均能满足农药残留量检测的要求。
| 表 2 噻虫嗪在菠菜中的添加回收率和相对标准偏差(n=5) Table 2 The spiked recoveries and RSD of thiamethoxam in spinach(n=5) |
消解动态结果(见图 1)显示:施药后1 d,噻虫嗪在露地菠菜中的降解率达50%左右,3 d时达到90%以上;而在保护地菠菜中,5 d的降解率才到50%左右,14 d降解率为90%左右。2种栽培条件下的消解动态均符合一级动力学模型,其在保护地和露地菠菜中的消解动态方程分别为ct=1.26e-0.17t(r=0.980 8)和ct=0.857e-0.54t(r=0.974 6),半衰期分别为4.08和1.28 d。
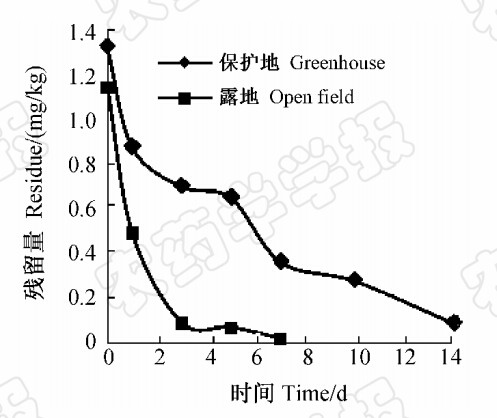 | 图 1 噻虫嗪在菠菜上的消解动态曲线 Fig. 1 Decline dynamic curve of thiamethoxam in spinach |
结果(见表 3)表明:距末次施药后3 d采样测定,保护地和露地菠菜中噻虫嗪的残留量分别为0.39~1.79 mg/kg和0.021~0.098 mg/kg;间隔5 d时,残留量分别为0.36~1.15 mg/kg和<0.02~0.024 mg/kg;间隔7 d时,残留量分别为0.28~0.64 mg/kg和<0.02~0.03 mg/kg。
| 表 3 噻虫嗪在菠菜中的最终残留量 Table 3 Final residues of thiamethoxam in spinach |
建立了液相色谱-串联质谱仪测定菠菜中噻虫嗪残留的分析方法。采用振荡法提取,易于批量样品操作;不需要经液-液萃取,既可减少溶剂的用量,又可缩短样品前处理时间,提高工作效率。方法的定量限为0.02 mg/kg,比在甘蓝上的最大残留限量(MRL)值0.2 mg/kg[14]低一个数量级。添加回收试验证明,该方法选择性强,准确性和精密度均达到农药残留分析要求[11]。
噻虫嗪在保护地菠菜中的半衰期较长,说明其在保护地菠菜中的降解速率比在露地菠菜中的慢,其原因可能与降雨、光照强度以及温度等的差异有关。本次田间试验于3月28日开始,4月29日结束,试验期间以晴到多云天气为主,累计降雨量不超过3 mm,露地平均气温10.8~19.8 ℃,保护地平均气温13.6~23.4 ℃。有研究表明,温度对噻虫嗪在水中的光解速率影响不大[12],但保护地中透光率只有自然光的50%~70%[13]。由此推断,光照强度是影响噻虫嗪降解的主要原因。
最终残留试验结果显示:无论是保护地还是露地栽培,噻虫嗪在菠菜中的最终残留量均随着施药剂量和施药次数的增加而增加,随着采收间隔期的延长逐渐降低;但相同条件下,保护地菠菜中噻虫嗪的残留量均明显高于露地菠菜。因此在菠菜种植过程中,不同的栽培条件下使用噻虫嗪,应设置不同的采收间隔期,以确保农产品的食用安全。
由于我国暂未制定噻虫嗪在菠菜上的MRL值,参照其在结球甘蓝上的MRL值(0.2 mg/kg)[14],建议:25%噻虫嗪水分散粒剂用于露地菠菜上防治蚜虫时,其最高施药剂量为有效成分30 g/hm2,每季最多施药2次,采收安全间隔期为3 d,如果用于保护地菠菜,则安全采收间隔期应在7 d以上。
| [1] | 杨吉春, 李淼, 柴宝山, 等. 新烟碱类杀虫剂最新研究进展[J]. 农药, 2007, 46(7): 433-438. YANG Jichun, LI Miao, CHAI Baoshan, et al. Recent research advances in new neonicotinoids insecticides[J]. Agrochemicals, 2007, 46(7): 433-438. (in Chinese) |
| [2] | 程霞, 亦冰. 第二代新烟碱类杀虫剂噻虫嗪的开发[J]. 世界农药, 2001, 23(4): 17-25. CHENG Xia, YI Bing. Development of the second generation new nicotinoid insecticide thiamethoxam[J]. World Pestic, 2001, 23(4): 17-25. (in Chinese) |
| [3] | 张国生, 侯广新. 烟碱类杀虫剂的应用、开发现状及展望[J]. 农药科学与管理, 2004, 25(3): 22-26. ZHANG Guosheng, HOU Guangxin. Present status of development and prospect of nicotinoid insecticide[J]. Pestici Sci Admin, 2004, 25(3): 22-26. (in Chinese) |
| [4] | 相金, 杨俊柱, 张胜义. 噻虫嗪在水稻中的消解动态及风险评估[J]. 安徽大学学报, 2013, 37(4): 88-92. XIANG Jin, YANG Junzhu, ZHANG Shengyi. Dissipation dynamic and risk assessment of thiamethoxam in rice[J]. J Anhui Univ, 2013, 37(4): 88-92. (in Chinese) |
| [5] | 邓立刚, 赵善仓, 毛江胜. 番茄中噻虫嗪残留量的高效液相色谱法测定[J]. 现代农药, 2007, 6(1): 40-41. DENG Ligang, ZHAO Shancang, MAO Jiangsheng. Determination of thiamethoxam insecticide in tomatoes by high performance liquid chromatography with photodiode array detection[J]. Mod Agrochem, 2007, 6(1): 40-41. (in Chinese) |
| [6] | 汤富彬, 陈宗懋, 罗逢健, 等. HPLC法测定黄瓜和土壤中噻虫嗪的残留量[J]. 农药, 2007, 46(5): 335-337. TANG Fubin, CHEN Zongmao, LUO Fengjian, et al. Determination of thiamethoxam residues in cucumbers and soil by HPLC[J]. Agrochemicals, 2007, 46(5): 335-337. (in Chinese) |
| [7] | 李维, 刘国光, 郑立庆, 等. 土壤中噻虫嗪农药残留分析方法[J]. 农业环境科学学报, 2007, 26(2): 739-742. LI Wei, LIU Guoguang, ZHENG Liqing, et al. Determination of thiamethoxam residues in soil[J]. J Agric Sci, 2007, 26(2): 739-742. (in Chinese) |
| [8] | 黄伟, 李建中, 王会利, 等. 噻虫嗪在马铃薯中的残留分析[J]. 环境化学, 2010, 29(5): 970-973. HUANG Wei, LI Jianzhong, WANG Huili, et al. Analysis of thiamethoxam residues in potato[J]. Environ Chem, 2010, 29(5): 970-973. (in Chinese) |
| [9] | 刘宾, 郭栋梁, 毛江胜, 等. 菠菜中噻虫嗪的残留检测与消解动态[J]. 农药, 2009, 48(9): 667-668. LIU Bin, GUO Dongliang, MAO Jiangsheng, et al. Residue detection and degradation of thiamethoxam in spinach[J]. Agrochemicals, 2009, 48(9): 667-668. (in Chinese) |
| [10] | 楼正云, 汤富彬, 陈宗懋, 等. 高效液相色谱法检测茶叶中噻虫嗪残留量[J]. 分析试验室, 2009, 28(增刊1): 76-78. LOU Zhengyun, TANG Fubin, CHEN Zongmao, et al. Determination of thiamethoxam residues in tea by HPLC[J]. Chin J Anal Lab, 2009, 28(Suppl.1): 76-78. (in Chinese) |
| [11] | NY/T 788—2004. 农药残留试验准则[S]. 北京: 中国农业出版社, 2004. NY/T 788—2004. Guideline on pesticide residue trials[S]. Beijing: China Agriculture Press, 2004. (in Chinese) |
| [12] | 郑立庆, 刘国光, 孙德智. 新型农药噻虫嗪的水解与光解研究[J]. 哈尔滨工业大学学报, 2006, 38(6): 1005-1008. ZHENG Liqing, LIU Guoguang, SUN Dezhi. Study on the hydrolysis and photolysis of thimethoxam[J]. J Harbin Inst Technol, 2006, 38(6): 1005-1008. (in Chinese) |
| [13] | 杨伟红, 郭晋平. 温室花卉栽培中光照强度调控研究进展[J]. 北方园艺, 2006(6): 70-72. YANG Weihong, GUO Jinping. An overview on the study of the light-intensity regulation of flowers culture in greenhouse[J]. North Hort, 2006(6): 70-72. (in Chinese) |
| [14] | GB 2763—2012, 食品安全国家标准—食品中农药最大残留限量[S]. 北京: 中华人民共和国卫生部和农业部, 2012. GB 2763—2012, National food safety standard—Maximum residue limits for pesticides in food[S]. Beijing: MOHC and MOA, 2012. (in Chinese) |
 2014, Vol. 16
2014, Vol. 16


