黄瓜靶斑病又名黄瓜褐斑病或黄点病,是由多主棒孢霉Corynespora cassiicola Wei引起的世界性病害[1,2]。随着蔬菜保护地种植规模的不断扩大,该病害蔓延趋势明显,尤其自2008年以后,辽宁、山东、河北及甘肃等地黄瓜产区普遍发生,已成为保护地黄瓜生产中亟待解决的叶部主要病害之一[3,4,5,6]。
苯醚甲环唑和戊唑醇均为三唑类杀菌剂,近年来辽宁省已在黄瓜靶斑病的防治上推广应用,且2013年苯醚甲环唑已获准登记用于该病害的防治。但至今尚未见有关黄瓜靶斑病病原菌群体对苯醚甲环唑和戊唑醇敏感性的研究报道。笔者从辽宁省8个区、市采集分离了101株黄瓜靶斑病菌,测定了其对苯醚甲环唑和戊唑醇的敏感性,以期为这2种药剂在防治黄瓜靶斑病上的合理使用及其抗药性监测提供参考。
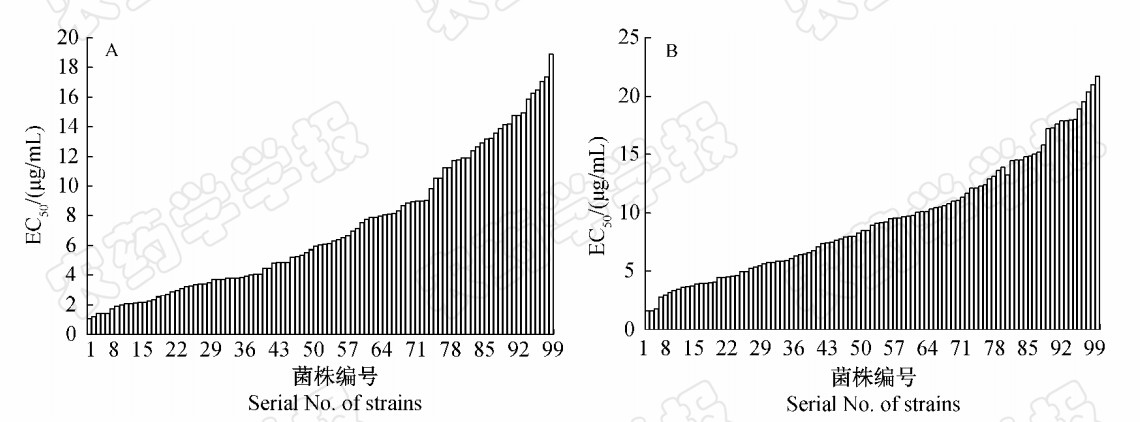 | 图 1 黄瓜靶斑病菌对苯醚甲环唑(A)和戊唑醇(B)的敏感性 Fig. 1 EC50 values of C.cassiicola populations to difenoconazole (A) and tebuconazole (B) |
多主棒孢霉Corynespora cassiicola Wei:于2013年从辽宁省沈阳、普兰店、凌源、铁岭、鞍山、锦州、盘锦、抚顺8个区、市采集黄瓜靶斑病病叶,采用组织分离法成功分离得到101株黄瓜靶斑病菌,其中普兰店(PLD)27株、凌源(LY)23株、铁岭(TL)17株、沈阳(SY)15株、盘锦(PJ)7株、鞍山(AS)5株、锦州(JZ)3株、抚顺(FS)4株。 1.2 药剂
97.3%的苯醚甲环唑(difenoconazole)和98%的戊唑醇(tebuconazole)原药,均为常州市丰登农药厂产品,用丙酮配制成10 000 μg/mL的母液备用。 1.3 黄瓜靶斑病菌对苯醚甲环唑和戊唑醇的敏感性测定
采用菌丝生长速率法[6]。将药剂与PDA培养基混匀,配制成质量浓度分别为1、2、4、8及16 μg/mL 的PDA含药培养基平板。将预培养好的黄瓜靶斑病菌制成直径5 mm的菌饼,接种于含药平板中央,25 ℃恒温培养。以不加药剂的PDA培养基为对照。每处理重复3次。5 d后用十字交叉法测量各处理的菌落直径。 1.4 数据统计分析
通过测定不同质量浓度含药平板上黄瓜靶斑病菌的菌丝直径(mm),按(1)式计算药剂对菌丝生长的抑制率。所得数据经SPSS软件处理,求得EC50值、毒力回归方程和相关系数(r);根据其敏感性频率分布建立病原菌对苯醚甲环唑和戊唑醇的敏感基线;分析不同地区菌株对药剂的敏感性差异以及菌株地理来源与其敏感性的关系。

结果(图 1)表明, 苯醚甲环唑对供试101株黄瓜靶斑病菌的EC50值最小为1.062 μg/mL,最大为18.918 μg/mL,相差16.814倍;戊唑醇对上述菌株的EC50值最小为1.624 μg/mL,最大为21.708 μg/mL,相差12.367倍。在病原菌对杀菌剂的敏感性范围内,将EC50值等分为几个阶段,以每阶段EC50的中值为横坐标,统计每阶段菌株的频率,绘制黄瓜靶斑病菌的敏感性频率分布图(图 2)。101株菌株对苯醚甲环唑和戊唑醇的敏感性频率分布均为连续单峰曲线,呈近似正态分布,苯醚甲环唑的平均EC50值为(7.109±4.578) μg/mL,戊唑醇的平均EC50值为(9.398±4.944) μg/mL。根据野生敏感型病原菌群体对药剂敏感性呈正态分布的原理,可将该平均EC50值7.109 μg/mL及9.398 μg/mL分别定为辽宁省黄瓜靶斑病菌对苯醚甲环唑及戊唑醇的敏感基线。
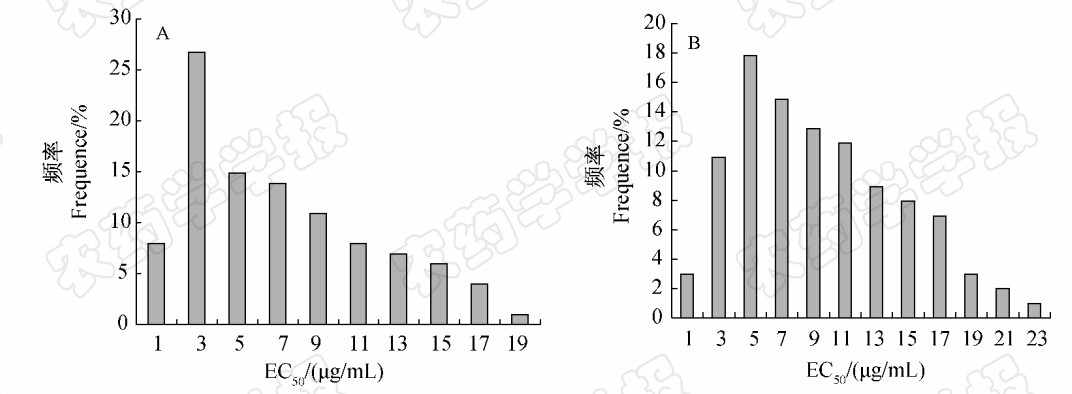 | 图 2 黄瓜靶斑病菌对苯醚甲环唑(A)和戊唑醇(B)的敏感性频率分布 Fig. 2 Frequency distribution of EC50 values of C. cassiicola populations to difenoconazole (A) and tebuconazole (B) |
采用SPSS软件分析了采自辽宁省8个区、市的黄瓜靶斑病原菌群体对2种杀菌剂的敏感性。结果(表 1)表明,不同地区病原菌群体间对苯醚甲环唑和戊唑醇的敏感性均无显著差异。苯醚甲环唑的EC50平均值变化范围为4.916~ 12.044 μg/mL,其中普兰店地区的菌株最敏感,其平均EC50值为4.916 μg/mL,抚顺地区的菌株最不敏感,其平均EC50值为12.044 μg/mL,敏感性相差1.448倍;戊唑醇的EC50平均值变化范围为6.774~13.408 μg/mL,其中盘锦地区的菌株最敏感,其平均EC50值为6.774 μg/mL,铁岭地区的菌株最不敏感,其平均EC50值为13.408 μg/mL,敏感性相差近1倍。由表 1还可发现,黄瓜靶斑病菌对2种杀菌剂的敏感性菌株并非来自同一地区。
| 表 1 辽宁省不同地区黄瓜靶斑病菌对苯醚甲环唑及戊唑醇的敏感性比较 Table 1 Sensitivity (EC50 value) of C.cassiicola to difenoconazole and tebuconazole from different areas in Liaoning Province |
每个地区随机选取3株,共选取24株黄瓜靶斑病菌,采用SPSS软件对苯醚甲环唑和戊唑醇抑制病原菌的EC50值进行系统聚类分析。结果(图 3)表明,苯醚甲环唑对24个菌株的EC50值共分在3个聚类组,第1组包括15个菌株(JZ2,AS2,FS2,LY16,SY17,TL5,PJ7,PLD9,TL3,SY16,PJ15,PLD14,JZ3,AS3和 AS5),第2组包括4个菌株(PJ1,LY13,PLD10和SY18),第3组包括5个菌株(LY17,JZ1,TL13,FS1和 FS4);戊唑醇对24个菌株的EC50值也分在3个聚类组,第1组包括3个菌株(PLD10,FS4和TL13),第2组包括10个菌株(PLD9,TL3,AS3,PJ1,LY13,JZ1,FS1,SY18,LY17和TL5),第3组包括11个菌株(PJ15,SY17,JZ3,AS2,SY16,PLD14,JZ2,FS2,AS5,LY16和PJ7)。不同来源的菌株系列出现在同一聚类组中,表明黄瓜靶斑病菌对每种杀菌剂的敏感性差异与菌株来源地理位置无明显相关性,这与Duncan氏新复极差法的分析结果相对应。尽管每种杀菌剂对菌株的EC50值均可分成3个聚类组,但2种杀菌剂的聚类组所包含的菌株并无相似之处。
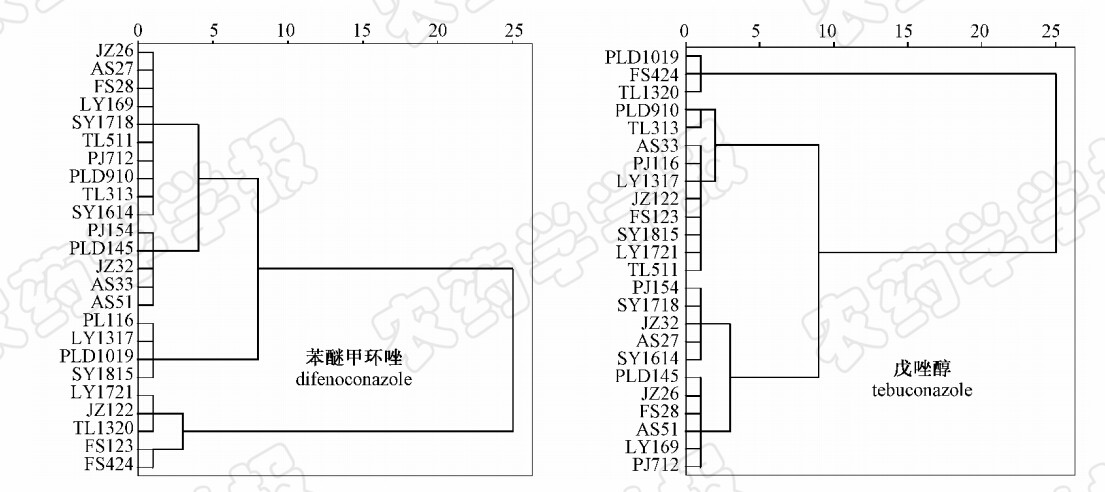 | 图 3 苯醚甲环唑和戊唑醇对黄瓜靶斑病菌EC50值的系统聚类分析 Fig. 3 Hierarchical cluster analysis on EC50 values of difenoconazole and tebuconazole to C.cassiicola |
苯醚甲环唑和戊唑醇是当前防治黄瓜靶斑病的主要杀菌剂[7]。研究表明,苯醚甲环唑对黄瓜靶斑病菌的抑制效果略优于戊唑醇;尽管病原菌不同菌株之间对药剂的敏感性相差较大,但田间尚未出现其抗药性菌株。菌株之间敏感性的差异可能源自病原菌本身存在的生理差异以及病原菌群体组成的复杂多样性,也可能与生产中使用的药剂间存在微弱的交互抗性有关。不同来源地区的黄瓜靶斑病菌对苯醚甲环唑和戊唑醇的敏感性存在差异,但差异均不显著;聚类分析结果也表明,病原菌对药剂的敏感性与其来源地区无关。研究结果表明,目前不同地区或地块的用药水平仍不足以引起病原菌对苯醚甲环唑和戊唑醇敏感性的显著变化。
苯醚甲环唑与戊唑醇同属三唑类杀菌剂,作用于病原菌的C-14脱甲基反应而影响麦角甾醇的生物合成[8]。范昆等[9]研究发现,三唑类杀菌剂戊唑醇、苯醚甲环唑、丙环唑和氟硅唑对苹果轮纹病菌Botryosphaeria berengeriana f.sp.piricola具有不同程度的交互抗药性。刘英华等[10]利用戊唑醇对禾谷丝核菌Rhizoctonia cerealis进行多代汰选,获得了抗性倍数达33.4的抗性菌株,且发现抗戊唑醇的禾谷丝核菌对三唑酮、丙环唑也存在交互抗药性。苯醚甲环唑和戊唑醇对黄瓜靶斑病菌是否也存在交互抗药性,还有待于通过抗性菌株的诱导进一步研究确定。
根据本研究结果及三唑类杀菌剂的相关研究报道,建议生产上不宜同时使用或交替使用苯醚甲环唑、戊唑醇及其他三唑类杀菌剂,以阻止或延缓黄瓜靶斑病菌对该类药剂的抗药性,延长其使用寿命。
| [1] | ISHⅡ H. Impact of fungicide resistance in plant pathogens on crop disease control and agricultural environment[J]. Japan Agricultural Research Quarterly, 2006, 40(3): 205-211. |
| [2] | PETERSON P D, CAMPBELL C L. Prevalence and ecological association of foliar pathogens of cucumber in North Carolina, 1996-1998[J]. J Plant Dis, 2002, 86(10): 1094-1100. |
| [3] | 岳宏忠. 黄瓜褐斑病的识别与防治[J]. 甘肃农业科技, 2010(2): 50-51. YUE Hongzhong. Diagnosis and control of cucumber brown spot[J]. Gansu Agric Sci Tech, 2010(2): 50-51. (in Chinese) |
| [4] | 郝永娟, 王万立, 刘春艳, 等. 保护地黄瓜褐斑病的诊治[J]. 天津农业科学, 2010, 16(1): 39-41. HAO Yongjuan, WANG Wanli, LIU Chunyan, et al. Diagnosis and control of Corynespora cassiicola in cucumber[J]. Tianjin Agric Sci, 2010, 16(1): 39-41. (in Chinese) |
| [5] | 李长松, 张眉, 李林, 等. 山东省黄瓜棒孢叶斑病(褐斑病) 病原菌鉴定和防治[J]. 中国蔬菜, 2009(18): 29-33. LI Changsong, ZHANG Mei, LI Lin, et al. Identification of cucumber target leaf spot (brown spot) pathogen and its control[J]. China Vegetables, 2009(18): 29-33. (in Chinese) |
| [6] | 祁之秋, 纪明山, 陆田, 等. 黄瓜褐斑病防治药剂的离体活性筛选[J]. 植物保护, 2009, 35(2): 140-143. QI Zhiqiu, JI Mingshan, LU Tian, et al. In vitro screening effective fungicides against Corynespora cassiicola[J]. Plant Protection, 2009, 35(2): 140-143. (in Chinese) |
| [7] | 纪军建, 张小风, 王文桥, 等. 黄瓜褐斑病化学药剂防治研究进展[J]. 河北农业科学, 2010, 14(8): 28-31. JI Junjian, ZHANG Xiaofeng, WANG Wenqiao, et al. Research progress on chemical control of cucumber Corynespora leaf spot[J]. J Hebei Agric Sci, 2010, 14(8): 28-31. (in Chinese) |
| [8] | 吴文君. 农药学原理[M]. 北京: 中国农业出版社, 2000: 207-208. WU Wenjun. Theory of Pesticide[M]. Beijing: China Agriculture Press, 2000: 207-208. (in Chinese) |
| [9] | 范昆, 曲健禄, 李林光, 等. 苹果轮纹病菌对戊唑醇的敏感基线及其室内抗药突变体研究[J]. 果树学报, 2013, 30(4): 650-656. FAN Kun, QU Jianlu, LI Linguan, et al. Study on baseline-sensitivity of Botryosphaeria dothidea to tebuconazole and the biological characteristics of tebuconazole-resistant mutants[J]. J Fruit Sci, 2013, 30(4): 650-656. (in Chinese) |
| [10] | 刘英华, 王开运, 姜兴印, 等. 禾谷丝核菌对戊唑醇的抗性及抗药性菌系生物学特性[J]. 植物保护学报, 2003, 30(4): 423-428. LIU Yinghua, WANG Kaiyun, JIANG Xingyin, et al. Resistance of Rhizoctonia cerealis to tebuconazole and the biological characters of tebuconazole-resistant strains[J]. J Plant Protect, 2003, 30(4): 423-428. (in Chinese) |
 2014, Vol. 16
2014, Vol. 16


