光化学降解是农药在环境中的主要降解途径之一,且农药的光解特性对生态环境及农药残留、药效、毒性均有重要影响[1],因此,光解特性是评价农药生态环境安全性的重要指标之一[2],近年来已日益成为农药环境行为研究的热点。朴秀英等[3]以氙灯为光源,研究了单嘧磺酯在水中的光化学降解;Kamiya 等[4]研究了光照条件下环糊精对腐殖质水溶液中有机磷类农药的影响;孙晓燕等[5]研究了高压汞灯光源下溴虫腈在不同溶剂中的光化学降解特性及其影响因素。
嘧菌酯(azoxystrobin)是甲氧基丙烯酸酯类杀菌剂,具有保护、治疗、铲除和抗产孢作用,以及广谱、高效、安全等特点[6]。自嘧菌酯问世以来,已在全世界60余种作物上进行了田间试验,成为了杀菌剂市场上广泛应用的品种[7]。Boudina等[8]研究了嘧菌酯在水相中的光解及光解产物,推测了其光解途径;许静等[9]研究得到嘧菌酯在水中的光解半衰期为1.24 h,表明其在自然水体中易光解。但有关嘧菌酯在水中光解的影响因素则尚未见报道。笔者通过研究嘧菌酯在不同溶液中的光化学降解,以期明确其光解特性及影响因素,旨在为嘧菌酯的合理使用及其环境安全性评价提供参考。
1 材料与方法 1.1 仪器及试剂Agilent 1200 高效液相色谱仪(配UV检测器,美国Agilent公司);N-EVAP111 型氮吹仪(美国Organomation公司);R-200旋转蒸发仪(瑞士BUCHI公司);BL-GHX-V 型光化学反应仪(配500 W 氙灯,上海比朗仪器有限公司)。
嘧菌酯(azoxystrobin)标准品(纯度97.5%,由农业部农药检定所提供) ,用乙腈配成1 000 mg/L的标准母液 ;乙腈(色谱纯);正己烷、甲醇、丙酮、十二烷基硫酸钠(SDS)、硝酸钠、亚硝酸钠、七水合硫酸亚铁、三氯化铁、腐殖酸(均为分析纯);超纯水。
1.2 试验方法 1.2.1 光解试验取50 mL反应液于具塞石英试管 (长200 mm,内径25 mm) 中,待光解仪稳定后进行光解试验。光源为500 W氙灯,照度30 000 lx,石英管距光源10 cm,启动转动电机使反应液均匀受光,光化学反应仪内温度为(25±1)℃。于不同光照时间分别取样测定嘧菌酯的质量浓度。每处理设3次重复,同时设黑暗对照。
1.2.2 初始浓度对光解速率的影响用纯水将嘧菌酯标准母液稀释成质量浓度分别为2、5、10和20 mg/L的反应液,进行光解试验。每处理设3 次重复,同时设空白光照及黑暗对照。
1.2.3 嘧菌酯在不同溶剂中的光解分别用正己烷、丙酮、乙腈、甲醇和水将嘧菌酯标准母液稀释成5 mg/L的反应液,进行光解试验。每处理设3 次重复,同时设空白光照及黑暗对照。
1.2.4 环境共存物质对嘧菌酯光解的影响分别在1、2、10和20 mg/L的硝酸钠、亚硝酸钠和腐殖酸水溶液中,在0.1、1、2和5 mmol/L的三氯化铁和硫酸亚铁水溶液中,在0.5、5、10和50 mg/L的SDS水溶液中添加嘧菌酯标准母液,使其质量浓度为5 mg/L,搅拌及超声混匀后进行光解试验。每处理设3 次重复,同时设空白光照及黑暗对照。
1.3 分析方法取1 mL乙腈反应液,直接进行高效液相色谱(HPLC)分析;分别取1 mL正己烷、丙酮及甲醇反应液,经氮吹仪吹干后用乙腈定容至1 mL,待HPLC检测;水样过0.22 μm滤膜后进行HPLC检测。
HPLC测定条件:Agilent Eclipse XDB-C18色谱柱(250 mm×4.6 mm×5 μm);流动相:V(乙腈)∶ V(水)=65∶35;柱温30℃;流速0.8 mL/min;检测波长240 nm;进样量20 μL。在此条件下,嘧菌酯的保留时间为6.7 min。外标法定量,在0.05~5 mg/L 范围内,嘧菌酯进样质量浓度与峰面积之间呈良好线性关系,线性回归方程为y=68.725x-1.679 1 (R2=0.999 5)。嘧菌酯的最小检出量为0.025 ng,定量限为0.017 mg/kg。
1.4 数据处理农药在环境中的光解可用一级动力学方程[式(1)]进行描述,光解半衰期按式(2)计算;光解残存率和光敏化(淬灭)率分别按式(3)[10]和式(4)[11]计算。

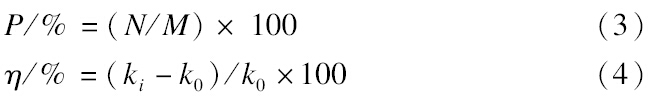
式中:c0为嘧菌酯的初始质量浓度(mg/L);ct为t时刻嘧菌酯的质量浓度(mg/L);k为光解速率常数(h-1);t1/2为光解半衰期(h);P为光解残存率(%);N为光照后残存嘧菌酯的质量浓度(mg/L);M为黑暗对照残存嘧菌酯的质量浓度(mg/L);η为光解的光敏化(淬灭)率(%);k0为嘧菌酯单独光解时的速率常数(h-1);ki为含氮化合物存在时的光解速率常数(h-1)。 2 结果与讨论 2.1 不同初始浓度嘧菌酯在纯水中的光解动力学
当初始质量浓度从2 mg/L升高至20 mg/L时,嘧菌酯在纯水中的光解半衰期延长了1.44倍(表 1)。嘧菌酯在纯水中的光解速率随初始质量浓度的增大而降低,推测是由于在光能一定的条件下,初始浓度增加使得单位分子平均接受到的光能减少,发生降解的机会相应减少。这与王敏欣等[12]的研究结果一致。
| 表 1 不同初始质量浓度下嘧菌酯的光解动力学参数
Table 1 Photo-degradation kinetics parameters of azoxystrobin with
different initial concentrations
|
在植物叶片和水果的外表皮中通常存在着由一些长链非极性物质(如烃、酮、酯、醇、醛和脂肪酸等)组成的蜡质层。绝大部分农药是亲脂性的,故可穿透蜡质层而在植物外表皮中展布。由于蜡质层中的部分功能团会影响农药分子的光化学转化,因此通常用有机溶剂来模拟植物表皮环境进行农药在植物表面的光解研究[13, 14, 15, 16]。嘧菌酯在5种溶剂中的光解结果见图 1,其在不同溶剂中的光解速率存在显著差异,但与溶剂极性无直接关系,光解速率从大到小依次为乙腈>水>甲醇>正己烷>丙酮,半衰期分别为4.8、5.8、11.5、12.1和23.5 h。这和沈佳君等[17]对丙酯草醚在有机溶剂中光解的研究结果一致。推测嘧菌酯在不同溶剂中光解速率产生差异的原因可能跟溶剂性质、溶剂与嘧菌酯分子间的相互作用以及溶剂本身对光的吸收有关。
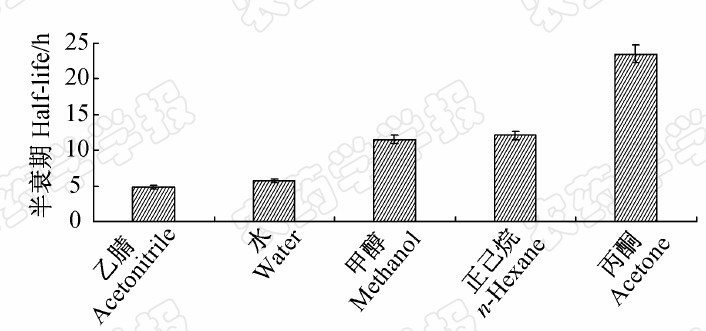 | 图 1 嘧菌酯在不同溶剂中的光解半衰期 Fig. 1 Half-lives for photo-degradation of azoxystrobin in different solvents |
硝酸钠和亚硝酸钠对嘧菌酯光解的影响见表 2和图 2。由表 2可见,NO-3质量浓度分别为0、1、2、10和20 mg/L时,嘧菌酯的光解半衰期分别为5.8、5.5、5.1、4.5和3.9 h。即随着NO-3浓度的增大,其对嘧菌酯光解的光敏化作用增强。
NO-3广泛存在于水环境中,具有光化学活性,可光解生成氮氧自由基(·NO2)和羟基自由基(·OH) 等活性中间体,引发芳香族有机物的硝化、亚硝化和氧化反应[18, 19],从而对水体中的污染物产生间接的光敏化作用。据此推测,加入硝酸钠和亚硝酸钠后嘧菌酯的光解速率加快,可能是由于NO-3在光照条件下产生的·OH与嘧菌酯分子发生了氧化反应,而·NO2与嘧菌酯分子发生了硝化反应所致。
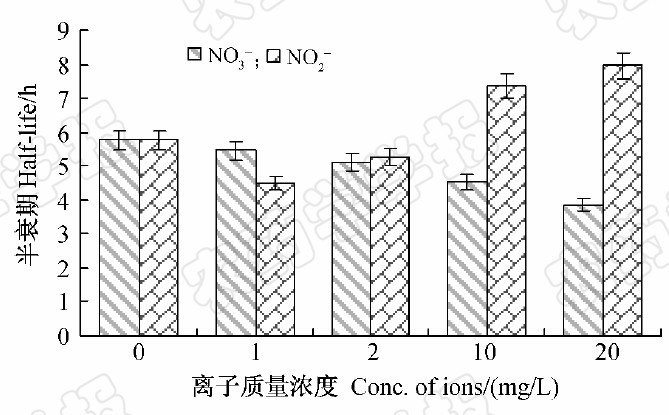 | 图 2 NO-3和NO-2对嘧菌酯光解的影响 Fig. 2 The effects of NO-3and NO-2 on photo-degradation of azoxystrobin |
当NO-2质量浓度在1~2 mg/L之间变化时,其对嘧菌酯光解的促进率从27.99%降到9.72%;当其质量浓度在10~20 mg/L 之间时,则对嘧菌酯的光解表现为光淬灭作用,淬灭率由21.84%提高到27.57%。表明NO-2浓度较低时对嘧菌酯的光解具有光敏化作用,随其浓度增大,光敏化作用逐渐减弱并转为光淬灭作用,且随NO-2浓度的继续增大其淬灭作用逐渐增强。
母昌立等[20]的研究表明,亚硝酸盐对啶虫脒的
光解具有光淬灭作用,且随NO-2浓度的增大光淬灭作用增强。Srensen等[21]认为这可能是由于存在惰性滤层作用,亚硝酸盐部分阻止了有机物分子对光辐射的吸收,进而抑制了有机物的光解。Mack等[22]研究发现,当光照波长在200~400 nm区域时,NO-2光解产生· OH,以提高反应体系的氧化效率,但所产生的NO·和·OH也可重新结合,从而消耗了体系中的部分·OH。因此当NO-2浓度较低时,所产生的·OH与嘧菌酯分子反应,可促进嘧菌酯的光解;随着NO-2浓度增大,其产生的NO·消耗·OH增多,再加上其惰性滤层作用,因而使得嘧菌酯的光解速率随着NO-2浓度的增大表现为先升高后降低的趋势。
| 表 2 NO-3和NO-2对嘧菌酯光解的影响 Table 2 Effects of NO-3and NO-2on photo-degradation of azoxystrobin |
SDS是一种常用的阴离子表面活性剂,常用作农药助剂。不同浓度SDS对嘧菌酯光解的影响结果见表 3。从中可看出,当SDS质量浓度为0.5~50 mg/L 时,嘧菌酯的光解速率常数从0.134 0提高到 0.178 5,半衰期从5.8 h降为3.9 h,说明SDS对嘧菌酯的光解具有光敏化作用,且其光敏化作用随添加浓度的升高而增强。这与李学德等[23]研究SDS对百菌清光解影响的结果一致。加入表面活性剂后,嘧菌酯溶液的紫外吸收光谱可能发生了变化,这或许是导致其光解速率发生变化的主要原因。
2.3.3 腐殖酸的影响腐殖酸是一种广泛存在于水体和土壤中的高分子聚合物,是动植物残体通过微生物分解或合成后的产物[24]。腐殖酸对嘧菌酯光解的影响见表 4,从中可知,当其质量浓度为1~20 mg/L时,嘧菌酯的光解速率常数从0.104 7降低到0.065 9,表现为光淬灭作用,且淬灭作用随腐殖酸浓度的升高而加强。这与花日茂等[25]研究高压汞灯与氙灯光照下腐殖酸对丁草胺光解影响的结果一致。腐殖酸的加入使嘧菌酯溶液的吸收光谱发生了红移,虽然氙灯是模拟太阳光,但其发射光谱集中在短波部分,因此使得嘧菌酯溶液不能吸收足够的能量而快速降解[25]。另外由于腐殖酸对嘧菌酯的吸附作用,导致嘧菌酯的能量和电子向腐殖酸转移,加上腐殖酸中胡敏酸的光掩蔽作用,最终导致嘧菌酯的光解速率下降。
| 表 3 十二烷基硫酸钠对嘧菌酯在水中光解的影响 Table 3 Effects of surfactant (SDS) on photo- degradation of azoxystrobin in water |
| 表 4 腐殖酸对嘧菌酯在水中光解的影响 Table 4 Effects of humic acid on photo-degradation of azoxystrobin in water |
结果见图 3。在浓度为0.1~5 mmol/L 时,Fe3+对嘧菌酯的光解表现为光敏化作用,半衰期从5.6 h降低到2.7 h,光解速率常数从0.128 8提高到0.256 2;而在该浓度下,Fe2+对嘧菌酯光解具有淬灭作用,半衰期从6.7 h增加到10.1 h,光解速率常数从0.102 9降低到0.069 0。
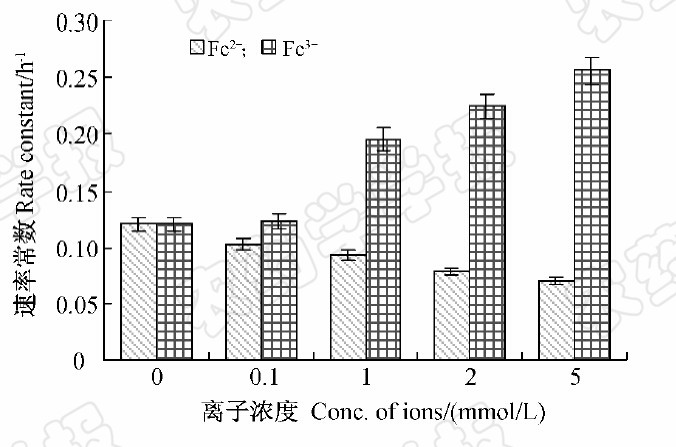 | 图 3 Fe3+和Fe2+对嘧菌酯在水中光解的影响 Fig. 3 Effect of Fe3+ and Fe2+ on the photo-degradation of azoxystrobin |
Fe3+的光敏化作用可能是由于其在氙灯辐射下可产生激发态Fe3+,激发态Fe3+通过与基态或激发态的农药分子形成复合物,进而诱导农药分子的氧化作用[26-27]。同时Fe3+在氙灯照射下与水反应也可生成氧化性较强的·OH,其可催化农药分子发生羟基化反应[27]。而Fe2+ 的光淬灭作用可能是因为在光照条件下,其与光解产生的水不溶性物质一起对光照产生了屏蔽作用,从而降低了嘧菌酯对光的吸收。 3 结论
1)在氙灯照射下,嘧菌酯在纯水中的光解速率随其初始浓度的增大而降低;嘧菌酯在不同溶剂中的光解速率从大到小依次为乙腈>水>甲醇>正己烷>丙酮,其光解速率与有机溶剂极性无关。
2)NO-3对嘧菌酯在水中的光解具有光敏化作用,且随着NO-3浓度的增大,其光敏化作用增强。质量浓度在1~2 mg/L之间时,NO-2对嘧菌酯在水中的光解表现为光敏化作用,但当其添加浓度增大到10~20 mg/L时,则表现为光淬灭作用。
3)SDS对嘧菌酯在水中的光解具有光敏化作用;腐殖酸则表现为光淬灭作用。
4)在0.1~5 mmol/L浓度范围内,Fe3+ 能显著提高嘧菌酯在水中的光解速率,表现为光敏化作用,而Fe2+则会抑制嘧菌酯在水溶液中的光解速率,表现为光淬灭作用。
| [1] | 张晓清, 石利利, 单正军. 农药在液相中的光解研究进展[J]. 农药科学与管理, 2007, 28(7): 41-46. ZHANG Xiaoqing, SHI Lili, SHAN Zhengjun. Studies on the photochemical degradation of pesticides in liquid solution[J]. Pestic Sci Admin, 2007, 28(7): 41-46. (in Chinese) |
| [2] | MATHENE R, KHAN S U. Photodegradation of metolachlor in water in the presence of soil mineral and organic constituents[J]. J Agric Food Chem, 1996, 44(12): 3996-4000. |
| [3] | 朴秀英, 姜辉, 陶传江, 等. 单嘧磺酯水解及在水中的光解研究[J]. 农药学学报, 2012, 14(3): 315-320. PIAO Xiuying, JIANG Hui, TAO Chuanjiang, et al. Study on hydrolysis and photolysis of monosulfuron-ester in water[J]. Chin J Pestic Sci, 2012, 14(3): 315-320. (in Chinese) |
| [4] | KAMIYA M, KAMEYAMA K, ISHIWATA S. Effects of cyclodextrins on photodegradation of organophosphorus pesticides in humic water[J]. Chemosphere, 2001, 42(3): 251-255. |
| [5] | 孙晓燕, 赵百萍, 王鸣华. 溴虫腈在不同溶剂中的光化学降解[J]. 农药学学报, 2013, 15(4): 469-474. SUN Xiaoyan, ZHAO Baiping, WANG Minghua. Study on photochemical degradation of chlorfenapyr in different solvents[J]. Chin J Pestic Sci, 2013, 15(4): 469-474. (in Chinese) |
| [6] | 闫晓静, 金淑惠, 陈馥衡, 等. Strobilurin类杀菌剂作用靶标的研究进展[J]. 农药学学报, 2006, 8(4): 299-305. YAN Xiaojing, JIN Shuhui, CHEN Fuheng, et al. Advance in research of the target of action of strobilurin fungicides[J]. Chin J Pestic Sci, 2006, 8(4): 299-305. (in Chinese) |
| [7] | 张舒亚, 周明国. 甲氧丙烯酸酯类杀菌剂的生物学及应用技术研究[M]//中国植物病害化学防治研究, 第三卷. 北京: 中国农业科技出版社, 2002: 1-10. ZHANG Shuya, ZHOU Mingguo. Biology and Application Technology Research of Strobilurin Fungicides[M]// Chemical Control of Plant Diseases in China (The Third Volume). Beijing: China Agriculture Science & Technology Press, 2002: 1-10. (in Chinese) |
| [8] | BOUDINA A, EMMELIN C, BAALIOUAMER A, et al. Photochemical transformation of azoxystrobin in aqueous solutions[J]. Chemosphere, 2007, 68(7): 1280-1288. |
| [9] | 许静, 孔德洋, 宋宁慧, 等. 甲氧丙烯酸酯类杀菌剂的环境降解特性研究[J]. 农业环境科学学报, 2013, 32(10): 2005-2011. XU Jing, KONG Deyang, SONG Ninghui, et al. Degradability of strobilurin fungicides in water and soils[J]. J Agro-Environ Sci, 2013, 32(10): 2005-2011. (in Chinese) |
| [10] | 褚明杰, 岳永德, 花日茂, 等. 苯噻草胺在不同水质中的光化学降解研究[J]. 环境科学学报, 2005, 25(12): 1647-1652. ZHU Mingjie, YUE Yongde, HUA Rimao, et al. Studies on the photodegradation of mefenacet in different water samples[J]. Acta Scientiae Circumstantiae, 2005, 25(12): 1647-1652. (in Chinese) |
| [11] | 张祥丹, 刘国光, 马杜鹃, 等. 硝酸根和亚硝酸根对水溶液中氯虫苯甲酰胺光解的影响[J]. 北京农业, 2011(6): 24-25. ZHANG Xiangdan, LIU Guoguang, MA Dujuan, et al. NO3/NO2 effection of chlorantraniliprole photolysis to aqueous solution[J]. Beijing Agric, 2011(6): 24-25. (in Chinese) |
| [12] | 王敏欣, 李发生, 韩梅, 等. 异丙草胺在水溶液中的光解动力学[J]. 环境科学, 2003, 24(5): 125-130. WANG Minxin, LI Fasheng, HAN Mei, et al. Photolysis kinetics of propisochlor in water[J]. Environ Sci, 2003, 24(5): 125-130.(in Chinese) |
| [13] | SCHWACK W, BOURGEOIS B, WALKER F. Fungicides and photochemistry: photodegradation of the dicarboximide fungicide iprodione[J]. Chemosphere, 1995, 31(4): 2993-3000. |
| [14] | SCHWACK W, BOURGEOIS B, WALKER F. Fungicides and photochemistry: photodegradation of the dicarboximide fungicide procymidone[J]. Chemosphere, 1995, 31(9): 4033-4040. |
| [15] | KABASHIMA T, YU Z, TANG C, et al. A selective fluorescence reaction for peptides and chromatographic analysis[J]. Peptides, 2008, 29(3): 356-363. |
| [16] | SCHWACK W, WALKER F, BOURGEOIS B. Fungicides and photo chemistry: photodegradation of the dicarboximide fungicide vinclozolin[J]. J Agric Food Chem, 1995, 43(12): 3088-3092. |
| [17] | 沈佳君, 吴刚, 王伟, 等. 除草剂丙酯草醚在有机溶剂中的光化学降解[J]. 核农学报, 2013, 27(8): 1227-1233. SHEN Jiajun, WU Gang, WANG Wei, et al. Photolysis of herbicide zj0273 in organic solvents under ultraviolet light[J]. J Nucl Agric Sci, 2013, 27(8): 1227-1233. (in Chinese) |
| [18] | ZEEP R G, HOLGNE J, BADER H. Nitrate-induced photooxidation of trace organic chemicals in water[J]. Environ Sci Tech, 1987, 21(5): 443-450. |
| [19] | 展满军, 杨曦, 孔令仁. 天然水体中亚硝酸根和硝酸根的光化学研究进展[J]. 环境污染治理技术与设备, 2004, 5(10): 14-19. ZHAN Manjun, YANG Xi, KONG Lingren. A critical review of photochemistry of nitrite and nitrate ions in natural waters[J]. Techn Equip Environ Pollut Control, 2004, 5(10): 14-19. (in Chinese) |
| [20] | 母昌立, 余向阳, 刘贤进, 等. 硝酸根、亚硝酸根对水体中啶虫脒光解的影响[J]. 江苏农业科学, 2011, 39(2): 428-430. MU Changli, YU Xiangyang, LIU Xianjin, et al. NO3/NO2 effection of acetamiprid photolysis to aqueous solution[J]. Jiangsu Agric Sci, 2011, 39(2): 428-430. (in Chinese) |
| [21] | SRENSEN M, TANNER U, SAGAWE G, et al. Photochemical degradation of hydrophilic xenobiotics in the UV/H2O2 process: influence of nitrate on the degradation rate of EDTA, 2-amino-1-naphthalen esulfonate, diphenyl-4-sulfonate and 4,4-diaminostilbene-2,2-disulfonate[J]. Water Res, 1997, 31(11): 2885-2991. |
| [22] | MACK J, BOLTON J R. Photochemistry of nitrite and nitrate in aqueous solution: a review[J]. J Photochem Photobio (A: Chem), 1999, 128(1-3): 1-13. |
| [23] | 李学德, 岳永德, 花日茂, 等. 表面活性剂对水中百菌清光解的影响[J]. 农业环境科学学报, 2007, 26(5): 1729-1732. LI Xuede, YUE Yongde, HUA Rimao, et al. Effects of surfactants on photolysis of chlorothalonil in aqueous solution[J]. J Agro-Environ Sci, 2007, 26(5): 1729-1732. (in Chinese) |
| [24] | 卢静, 朱琨, 赵艳锋, 等. 腐殖酸在去除水体和土壤中有机污染物的作用[J]. 环境科学与管理, 2006, 31(8): 151-154. LU Jing, ZHU Kun, ZHAO Yanfeng, et al. Humic acid in the removal of organic pollutants in water and soil[J]. Environ Sci Manag, 2006, 31(8): 151-154. (in Chinese) |
| [25] | 花日茂, 岳永德, 潘学冬, 等. 腐殖质对丁草胺在水中的光解效应研究[J]. 安徽农业大学学报, 1999, 26(1): 63-67. HUA Rimao, YUE Yongde, PAN Xuedong, et al. Effects of humic acid on photolysis of butachlor in aqueous solution[J]. J Anhui Agric Univ, 1999, 26(1): 63-67. (in Chinese) |
| [26] | MAZELLIER P, JIRKOVSKY J, BOLTE M. Degradation of diuron photoinduced by iron(ⅡI) in aqueous solution[J]. Pestic Sci, 1997, 49(3): 259-267. |
| [27] | MEUNIER L, BOULE P. Direct and induced phototransformation of mecoprop in aqueous solution[J]. Pest Manage Sci, 2000, 56(12): 1077-1085. |
 2014, Vol.16
2014, Vol.16 


