2-嘧啶氧基-N-芳基苄胺类化合物是中国科学院上海有机化学研究所和浙江省化工研究院有限公司共同发现的具有我国自主知识产权和高效除草活性的农药先导化合物[1],现已获得中国发明专利(ZL 00130735.5)、美国发明专利(US 6800590 B2)、韩国发明专利(KR 0511489)、墨西哥发明专利(MX 234202)、欧盟发明专利(EP 1327629)、日本发明专利(JP 4052942)和加拿大发明专利(CA 2425984)授权。基于该先导化合物,现已成功开发出2个新型高效油菜田除草剂——丙酯草醚和异丙酯草醚,并对其代谢过程、作用机理和环境行为等进行了深入研究[2,3,4,5,6,7]。溴嘧氯草醚(开发代号:SIOC0426,化学名称为N-[2-氯-6-(4,6-二甲氧基-2-嘧啶氧基)苄基]-4-溴苯胺)是近年来在此类先导化合物中第一个以棉花田为作用对象实施开发的高活性化合物,具有除草活性高、杀草谱较广、对棉花和棉田主要杂草具有良好的选择性,作为棉田除草剂候选品种具有良好的市场开发前景[8]。
开展农药候选品种的中试合成工艺研究,提高原药含量,提高产品收率,降低成本,开展“三废”排放与治理研究,为进行工业化生产的可行性评估提供依据,是农药候选品种在研究开发阶段必不可少的环节。农药原药中的杂质可能引发原药的药害增加、毒性增强、剂型加工困难和稳定性降低等一系列问题,因而研究农药中试产品中的杂质也是农药候选品种在研究开发阶段必须解决的问题[9]。鉴于此,笔者对除草剂候选品种溴嘧氯草醚开展了公斤级规模上的中试合成工艺研究,并以高效液相色谱(HPLC)外标法测定了中试产品中原药的含量,借助于三维高效液相色谱-质谱联用技术(HPLC-DAD-MS)鉴定出原药中2种主要杂质, 旨在为溴嘧氯草醚后续的工业生产、产品质量分析和剂型加工、田间药效试验等研究奠定基础。笔者对于2-嘧啶氧基-N-芳基苄胺类化合物的合成曾设计了2条合成路线(图 1),实验发现采用Scheme 1会产生多种杂质,且杂质与目标产品的分离困难,因而本研究采用Scheme 2研究了溴嘧氯草醚的中试合成工艺。
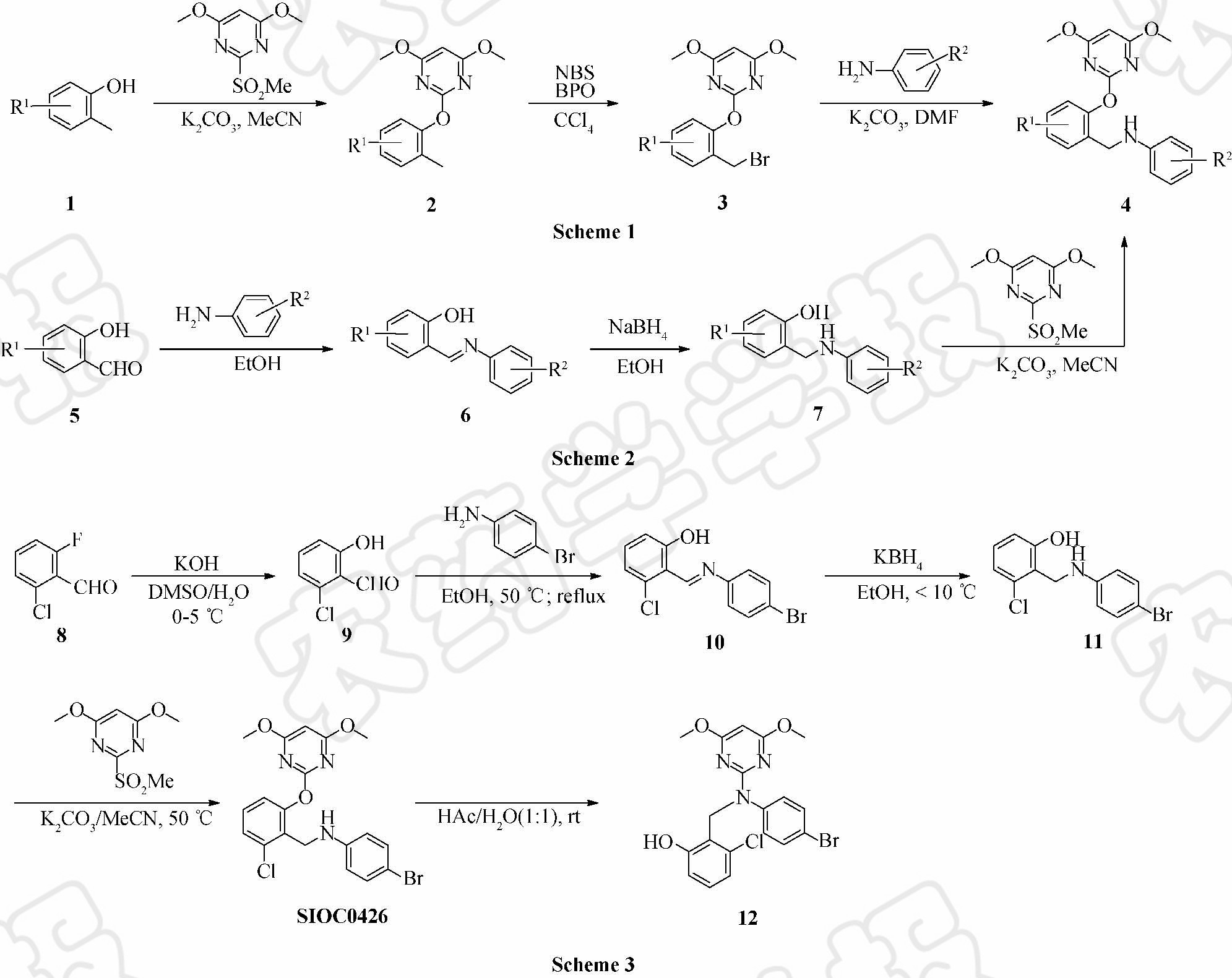 | 图 1 2-嘧啶氧基-N-芳基苄胺类除草剂和杂质推测物标样(12)的合成路线 Fig. 1 Synthetic routes of 2-pyrimidinyloxy-N-aryl-benzylamines and impurity reference standard (12) |
由于中试产品溴嘧氯草醚中杂质含量很低,难以分离获得杂质纯品并通过核磁和质谱等方法鉴定其结构,故笔者通过对Scheme 2中试合成工艺进行分析后推测了杂质的结构,并对推测杂质物标样进行了合成,通过高效液相色谱、紫外光谱和质谱等手段将中试产品溴嘧氯草醚中的杂质与杂质推测物进行了比对,以确定杂质结构。溴嘧氯草醚及杂质推测物标样(12)的合成路线见 Scheme 3。 1 原药的中试合成 1.1 仪器和试剂
Varian INOVA-400MHz低温超导核磁共振仪;Agilent 5975C质谱仪;Agilent 6120 Quadrupole LC/MS系统(配1260 Infinity二极管阵列检测器);Shimadzu LC-20AD高效液相色谱仪(配SPD-M20A二极管阵列检测器);SGW X-4显微熔点仪(温度未校正)。
2-氟-6-氯苯甲醛、对溴苯胺、硼氢化钾、4,6-二甲氧基-2-甲砜基嘧啶、氢氧化钾、浓盐酸、乙醇、乙腈、无水碳酸钾等为工业品。溴嘧氯草醚标准品(纯度99.99%)是由工业级溴嘧氯草醚用乙醇、乙腈多次重结晶自行制备。三氟乙酸、甲酸为色谱纯,购自Tedia公司;乙腈、甲醇为色谱纯,购自百灵威公司;水为超纯水;其他试剂均为市售化学纯。
1.2 合成工艺 1.2.1 6-氯水杨醛(9)的合成在0 ℃下,将质量分数为40%的氢氧化钾水溶液(19.2 kg,136.87 mol)滴入剧烈搅拌的2-氯-6-氟苯甲醛(8,3.01 kg,18.98 mol)的二甲亚砜(4.56 kg)溶液中,控制滴加过程中体系内温度低于10 ℃。滴加完毕搅拌2 h。向反应液中加水(4.50 kg),在体系内温度低于5 ℃条件下滴加质量分数为37%的浓盐酸,调节pH至3~4 [耗用盐酸2.75 kg(27.91 mol)]。搅拌0.5 h后过滤,滤饼充分水洗,得浅黄色固体。粗品用少量乙醇洗涤,过滤,减压烘干得浅黄色固体6-氯水杨醛(9,2.76 kg,收率93.1%)[10]。HPLC检测纯度为98.4%。1H NMR (400 MHz,CDCl3),δ:11.90 (s,1H),10.41 (s,1H),7.40 (t,J=8.0 Hz,1H),6.94 (dd,J=8.0,8.0 Hz,1H),6.89 (d,J=8.0 Hz,1H)。
1.2.2 2-[(4-溴苯基亚氨基)甲基]-3-氯苯酚(10)的合成在50 ℃下,将4-溴苯胺(3.05 kg,17.73 mol)的乙醇(10 kg)溶液滴入含6-氯水杨醛(2.76 kg,17.63 mol)的乙醇(15 kg)溶液中,滴加完毕升温回流2 h。停止加热,搅拌过夜,次日析出大量黄色固体(10),过滤后产品无需纯化直接用于下一步反应。
1.2.3 2-[(4-溴苯氨基)甲基]-3-氯苯酚(11)的合成在温度低于10 ℃下,将硼氢化钾(325 g,6.03 mol)分批加入中间体亚胺(10,5.39 kg,17.34 mol)与乙醇(25 kg)的悬浮液中,加料完毕搅拌30 min,至原料转化完全。减压蒸馏回收大部分乙醇,残余物趁热倾入水(16 kg)中,充分搅拌后过滤,滤饼用乙醇洗涤,减压烘干后得白色固体(11,5.35 kg,97.0%)。m.p. 128.3~130.1 ℃;HPLC检测纯度为98.7%。1H NMR (400 MHz,CDCl3),δ: 7.34 (d,J=8.8 Hz,2H),7.12 (t,J=8.1 Hz,1H),6.94 (d,J=8.0 Hz,1H),6.78 (d,J=8.2 Hz,1H),6.73 (d,J=8.8 Hz,2H),4.61 (s,2H); MS (EI,70 eV),m/z (%): 171 (100),173 (96),77 (36),65 (24),313 (24),141 (23),92 (20),311 (M+,19)。
1.2.4 目标化合物溴嘧氯草醚(SIOC0426)的合成将无水碳酸钾(6.50 kg,47.03 mol)加入中间体11(5.35 kg,17.16 mol)和4,6-二甲氧基-2-甲砜基嘧啶(3.74 kg,17.14 mol)的乙腈(30.3 kg)溶液中,在50 ℃下剧烈搅拌5 h。将反应混合物冷却至室温,抽滤,滤饼用少量乙腈洗涤,滤液浓缩后得黄色粗品,用乙醇(用量为固体质量的3倍)重结晶,得白色固体溴嘧氯草醚(7.04 kg,91.2%)。HPLC 检测纯度为98.2%;m.p. 153~154 ℃;1H NMR (400 MHz,CDCl3),δ:7.31~7.22 (m,2H),7.14 (d,J=8.0 Hz,2H),7.07 (d,J=7.9 Hz,1H),6.45 (d,J=8.0 Hz,2H),5.76 (s,1H),4.41 (s,2H),3.77 (s,6H);13C NMR (75 MHz,DMSO-d6),δ:173.35,164.27,152.91,148.32,135.30,131.83,130.09,129.68,127.33,122.77,114.59,84.71,54.98; ESI-MS,m/z:279,450[M+H]+,452[M+2+H]+,472[M+Na]+,474[M+2+Na]+;MS (EI,70 eV),m/z (%): 279 (100),163 (100),281(35),451 (35),294 (30),250 (29),449 (M+,26),295 (23); UV (MeOH,λmax):205,250 nm。
按照上述合成路线,在同等规模上将中试合成重复6次。以2-氯-6-氟苯甲醛计,6次反应的总收率均可稳定在80%以上。
1.2.5 杂质推测物标样(12)的合成在室温下,将溴嘧氯草醚(901 mg,2 mmol)的丙酮溶液与质量分数为50%的醋酸水溶液等体积混合搅拌12 h,减压脱除溶剂得白色固体(870 mg,96.5%)[11]。HPLC检测纯度为98.0%;m.p. 58.3~59.9 ℃。1H NMR (400 MHz,DMSO-d6),δ:10.08 (s,1H),7.42 (dd,J=8.6,1.9 Hz,2H),7.15 (dd,J=8.6,1.9 Hz,2H),7.03 (td,J=8.1,2.0 Hz,1H),6.78 (d,J=8.0 Hz,1H),6.69 (d,J=8.2 Hz,1H),5.56 (s,1H),5.35 (s,2H),3.72 (s,6H); ESI-MS(+),m/z : 452[M+2+H]+,450[M+H]+ ,474[M+2+Na] +,472[M+Na] +; UV (MeOH,λmax): 225,275 nm。
1.3 中试产品溴嘧氯草醚的含量分析采用HPLC外标法测定。准确称取10.0 mg中试产品溴嘧氯草醚,用乙腈溶解、稀释并定容至100.00 mL;溴嘧氯草醚标准品用同法处理。以溴嘧氯草醚标准品为外标,参考丙酯草醚的HPLC外标定量法[12],使用Shimadzu LC-20AD高效液相色谱仪测定中试产品中溴嘧氯草醚的含量。色谱条件:流速1.00 mL/min;进样量5 μL;检测波长254 nm;柱温40 ℃。采用2种方法洗脱:1)梯度洗脱:洗脱梯度(min/%A)控制为0/10、25/100(A为含0.1%TFA的乙腈,B为含0.1%TFA的水);Dikma Diamonsil C18(2) 色谱柱(150 mm×4.6 mm,5 μm)。溴嘧氯草醚保留时间为 17.543 min(图 2)。2)等度洗脱:流动相为V(甲醇)∶V(水)=80 ∶20;Wondasil C18色谱柱(250 mm×4.6 mm,5 μm)。溴嘧氯草醚保留时间为17.260 min。根据标准样品的质量浓度与积分面积关系的校正曲线及中试产品溴嘧氯草醚的HPLC分析结果计算其含量。两种分析方法结果均表明,中试产品溴嘧氯草醚的含量均大于98%。
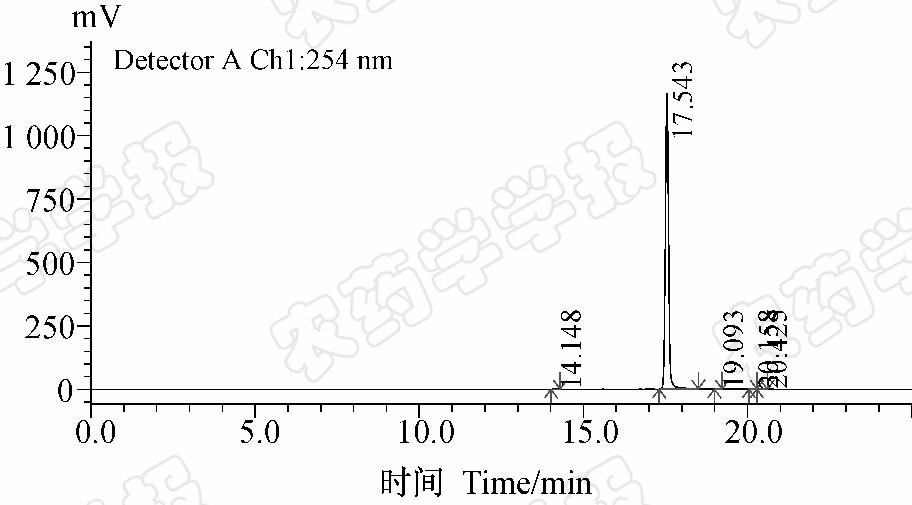 | 图 2 溴嘧氯草醚的高效液相色谱图 Fig. 2 HPLC chromatogram of SIOC0426 |
采用Agilent 6120 Quadrupole LC/MS系统与1260 Infinity二极管阵列检测器联用(HPLC-DAD-MS),对中试产品溴嘧氯草醚的乙腈溶液(15 μg/mL)中的杂质进行分析。色谱条件:Dikma Diamonsil C18(2) 色谱柱(250 mm×4.6 mm,5 μm);洗脱梯度(min/%B)控制:0/10,15/95,25/95(A为含0.1%甲酸的乙腈,B为含0.08%甲酸的水);流速1.00 mL/min;进样量20 μL;柱温40 ℃;波长250 nm。质谱条件:电离方式为ESI;检测方式为正离子全扫描模式;扫描范围100~1 000 amu;碎裂电压70 V;气体均为高纯氮气;雾化气流速11 L/min;雾化气压力35 Psi(241.325 kPa);干燥气温度300 ℃;去溶剂辅助加热温度400 ℃;毛细管电压3 000 V;四极杆温度280 ℃;离子源温度280 ℃。首先通过三维高效液相色谱(HPLC-DAD)确定中试产品溴嘧氯草醚中的主要杂质种类数,然后通过优化质谱条件来确定杂质的相对分子质量及其碎片离子的质核比,进而推测杂质可能的分子结构。通过比较杂质和推测物标样HPLC保留时间、UV光谱和质谱特征(加合离子和碎片离子)以确认中试产品溴嘧氯草醚中杂质的分子结构。
2 结果与讨论 2.1 溴嘧氯草醚的中试合成
在溴嘧氯草醚小试合成中,笔者曾选用Scheme 1路线:即以邻甲酚类衍生物1为起始原料,通过2步亲核取代和1步溴化反应获得目标物4。由于在该路线的溴化反应中会产生少量与中间体3难以分离的嘧啶环溴化副产物13,导致目标物中夹杂有杂质14;同时在中间体3参与的亲核取代反应中不可避免地产生少量二取代的杂质15。这2种杂质均很难从目标物中分离出来,故中试合成时放弃该路线。通过小试合成试验发现,Scheme 2的反应条件温和,反应过程容易控制,产品收率及纯度均较高,因而以此路线为基础开展溴嘧氯草醚的中试合成工艺研究。
在6-氯水杨醛(9)的合成中,通过控制反应温度和氢氧化钾溶液的滴加速度,可尽可能地避免2-氯-6氟苯甲醛的歧化反应,同时延长晶体析出时间,可使反应收率稳定在90%,产品纯度达98%以上。对溴苯胺和6-氯水杨醛均易溶于乙醇,但二者反应产物亚胺(10)却不溶于乙醇,因而通过析晶很容易将亚胺(10)纯化。下一步亚胺的还原几乎是定量反应。在最后一步反应中,若反应配比控制不当,目标产品中往往会夹杂少量难以除去的4,6-二甲氧基-2-甲砜基嘧啶。在本工艺中,用稍过量的中间体11可使4,6-二甲氧基-2-甲砜基嘧啶完全反应;而过量的中间体11在后处理中可被乙腈、乙醇等溶剂洗除,有效地提高了目标产品的纯度。这步反应也可以DMF为溶剂在室温下进行反应,但副产物较多;另外相对于乙腈,DMF回收难度大,成本高,不适合工业化生产。在室温下溴嘧氯草醚微溶于乙腈和乙醇。将黄色溴嘧氯草醚粗品与乙腈(固体质量0.8倍量)在室温下混合打浆30 min后过滤,或者利用乙醇加热重结晶,可有效除去粗品中的副产物,易获得纯度超过98%的溴嘧氯草醚。此工艺反应条件温和,反应收率高,原药纯度高。在生产中,乙醇和乙腈均可回收再利用,因而“三废”排放少,生产成本低,适合于工业化生产。
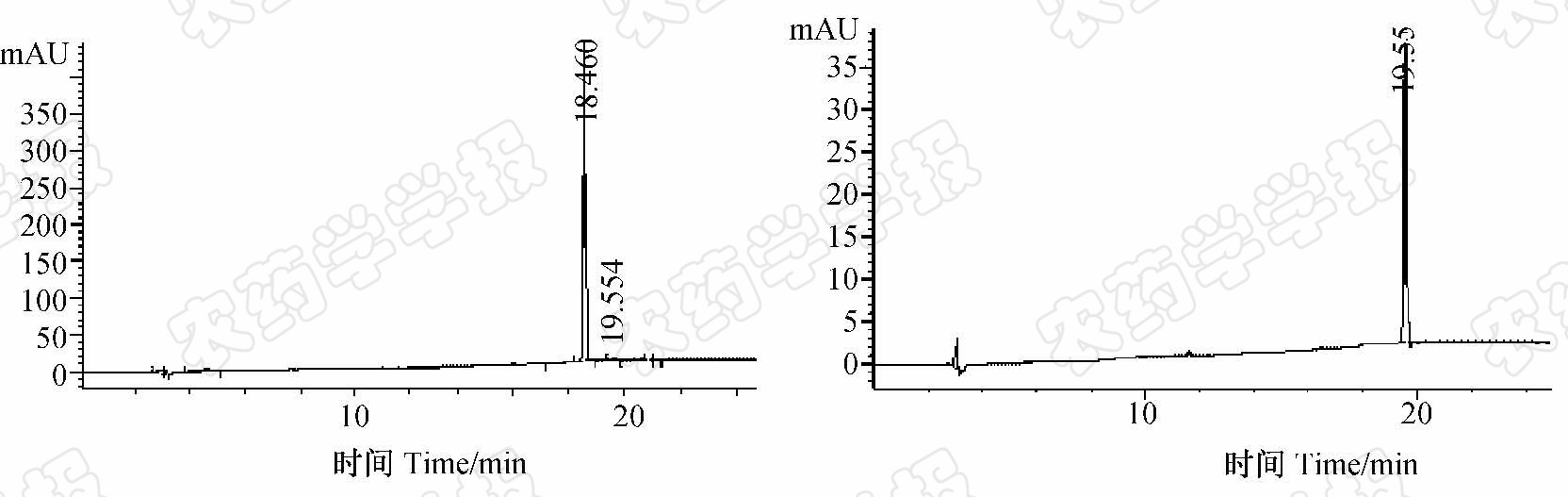 | 图 3 中试产品溴嘧氯草醚(左图)和杂质推测物标样(12,右图)的高效液相色谱图(254 nm) Fig. 3 HPLC chromatogram of SIOC0426 (left) and impurity reference standard (12,right)(254 nm) |
农药原药中的杂质主要来源于农药生产过程中产生的反应副产物、未完全反应的原料和原药分解或重排的产物等。HPLC-DAD分析结果表明,中试产品溴嘧氯草醚中包含2种主要杂质,其HPLC保留时间分别为12.258和19.554 min(见图 3,254 nm)。经HPLC-MS分析及与标样比对确认,HPLC保留时间为12.258 min的杂质为未完全反应的原料2-[(4-溴苯氨基)甲基]-3-氯苯酚(11)。
在中试产品溴嘧氯草醚HPLC色谱图中,保留时间为19.554 min杂质的紫外吸收峰分别位于波长225和275 nm处。通过增加进样量,获得该杂质的质谱数据:ESI-MS(+),m/z : 452[M+H+2]+,450[M+H]+,474[M+Na+2]+,472[M+Na]+。据此推测该杂质的相对分子质量应为449,与溴嘧氯草醚的相对分子质量相同。通过优化质谱碎裂器电压(由默认70 V升至180 V,此时碎片离子最强峰丰度是分子加合离子最强峰丰度的3倍)获得杂质的典型离子碎片(m/z: 310,312; 230,231; 141)。在相同色谱条件下,测得杂质推测物标样(12)的保留时间为19.550 min,紫外吸收峰位于225和275 nm处,这与杂质的HPLC-DAD分析结果一致。在优化的质谱条件下,化合物12的质谱峰对应的质核比和丰度均与中试产品溴嘧氯草醚所含杂质一致,进一步证实中试产品溴嘧氯草醚中保留时间为19.554 min的杂质与化合物12的结构一致。文献报道,2-嘧啶氧基-N-芳基苄胺类化合物可在酸催化下发生N-O型Smiles重排[11],而化合物12则正是溴嘧氯草醚发生N-O型Smiles重排的产物。可见,该杂质源于溴嘧氯草醚的重排反应。试验证实,当最后一步反应温度高于50 ℃或者反应时间过长时,溴嘧氯草醚中该杂质的含量显著增加。
3 结论
以2-氟-6-氯苯甲醛为原料,通过水解、缩合、还原和亲核取代4步反应在公斤级规模上合成了溴嘧氯草醚,反应总收率大于80%,溴嘧氯草醚含量(质量分数)大于98%,其主要杂质为未反应完全的中间体2-[(4-溴苯氨基)甲基]-3-氯苯酚(11)和溴嘧氯草醚发生N-O型Smiles重排的产物(12)。
| [1] | LU Long, CHEN Jie, WU Jun, et al. New 2-pyrimidinyloxy-N-aryl-benzylamine derivatives, their processes and uses:WO 2002034724 . 2002-05-02. |
| [2] | YANG Zhengmin, YE Qingfu, LU Long. Synthesis of herbicidal ZJ0273 labeled with tritium and carbon-14[J]. J Label Compd Radiopharm, 2008, 51(4): 182-186. |
| [3] | YANG Zhengmin, WANG Wei, HAN Ailiang, et al. Determination of herbicide ZJ0273 residue in rapeseed by radioisotopic tracing method[J]. Food Chem, 2009, 114(1): 300-305. |
| [4] | WANG Haiyan, YE Qingfu, YUE Ling, et al. Fate characterization of a novel herbicide ZJ0273 in aerobic soils using multi-position C labeling[J]. Sci Total Environ, 2009, 407(13): 4134-4139. |
| [5] | HAN Ailiang, YUE Ling, LI Zheng, et al. Plant availability and phytotoxicity of soil bound residues of herbicide ZJ0273, a novel acetolactate synthase potential inhibitor[J]. Chemosphere, 2009, 77(7): 955-961. |
| [6] | WANG Haiyan, YE Qingfu, YUE Ling, et al. Kinetics of extractable residue, bound residue and mineralization of a novel herbicide[J]. Chemosphere, 2010, 76(8): 1036-1040. |
| [7] | WANG Haiyan, YU Zhiyang, YUE Ling, et al. Transformation of C-pyrimidinyloxybenzoic herbicide ZJ0273 in aerobic soils[J]. Sci Total Environ, 2010, 408(10): 2239-2244. |
| [8] | 台文俊, 陈杰, 徐小燕, 等. 棉田除草活性化合物SIOC0426生物活性初步评价[J]. 农药学学报, 2009, 11(1): 87-91. TAI Wenjun, CHEN Jie, XU Xiaoyan, et al. Bioactivity assessment on the novel herbicidal compound SIOC0426 in cotton[J]. Chin J Pestic Sci, 2009, 11(1): 87-91. (in Chinese) |
| [9] | 刘聪云, 刘丰茂, 陈铁春, 等. 农药原药中杂质的危害及其管理[J].农药,2010,49(5):385-389. LIU Congyun, LIU Fengmao, CHEN Tiechun, et al. The harm and management of relevant impurities in pesticide technical[J]. Agrochemicals, 2010, 49(5):385-389.(in Chinese) |
| [10] | GYBAECK H, MALMSTROEM J, TERP E G. 2-Carboxamide-4-piperazinyl-benzofuran derivative:WO 2012087229 . 2012-06-28. |
| [11] | WANG Haoyang, LIAO Yuanxi, GUO Yinlong, et al. Interesting acid-catalyzed O-N type smiles rearrangement reactions of 2-pyrimidinyloxy-N-arylbenzylamine derivatives[J]. Synlett, 2005(8): 1239-1242. |
| [12] | 杨征敏, 叶庆富, 唐庆红, 等. 新型除草剂丙酯草醚A 环 C 均标记合成和鉴定[J]. 化学学报, 2005, 63(21): 1999-2003. YANG Zhengmin, YE Qingfu, TANG Qinghong, et al. Radiolabeled synthesis and identification of a novel herbicide, propyl 4- benzoate with all six benzoic ring carbons labeled by C[J]. Acta Chimica Sinica, 2005, 63(21): 1999-2003. |
 2014, Vol. 16
2014, Vol. 16


