以天然或合成的高分子材料为壁材,将固体或液体药物(通称芯材)包裹成的药库型微小胶囊称微囊(microcapsules);而使芯材溶解或均匀分散在成球材料中,形成骨架型微小球状实体则称为微球(microspheres);微囊及微球的制备过程统称为微囊化[1]。目前以脂肪族聚酯、聚乳酸及其共聚物及天然高分子聚合物等生物可降解物质为壁材的农药微球的研究正逐渐成为农药缓释剂研究的热点[2, 3, 4, 5, 6, 7, 8, 9, 10]。
多杀菌素(spinosad)是一种应用前景广阔的新型生物源农药[11],而甲氨基阿维菌素苯甲酸盐(emamectin benzoate,以下简称甲维盐)是一种高效、广谱、无公害的生物源杀虫剂[12, 13]。二者具有不同的作用方式,将其复配使用,可明显提高其对靶标害虫的防治效果,有效延缓鳞翅目害虫抗药性的产生,并能缓解环境压力[14]。但二者在田间易发生光解 [15, 16],导致其在田间叶面施用时持效期较短。目前二者的复配制剂主要为乳油[17]及水分散粒剂[14],若将二者加工成农药微球,可有效降低光解速率,延长持效期。
在农药配方筛选过程中,目前应用较为广泛的试验工艺优化方法是正交设计和均匀设计[18, 19, 20, 21, 22]。这两种方法试验次数均较少,但其更多的是用于对线性模型的预测,对非线性模型的预测精度相对较弱,某些设计表如正交L9(34)不适于二次以上多项式模型[23, 24],而在农药制剂工艺和配方筛选过程中,各影响因素与结果之间关系往往并非简单的线性关系。中心多点等距设计(central composite design,CCD)是在二水平析因设计的基础上加极值点、中心点组成的一种试验设计,已在医药领域有较多应用[25, 26, 27, 28]。在相关试验设计中,若仅有析因设计点,则只能用作线性拟合,但加入极值点后,即可增强其对非线性模型的拟合能力,一定量的中心点重复可保证试验设计的均一精密性及正交性[29]。与正交设计和均匀设计相比,CCD设计能建立拟合度、相关性、预测性更好的非线性回归模型[23],因此可作为农药微球制备工艺优化的工具[30, 31]。
农药配方筛选过程中,往往需要对多个技术指标进行考察。各指标间往往互相影响,对某一项指标有利的因素条件可能不利于另一指标,最终选择条件往往依据这些指标的综合效应。通过“归一化”法,将各个指标均标准化为0~1 间的“归一值” (desirability),由各指标“归一值”求算几何平均数,得总评“归一值”(overall desirability,OD)[32],可实现对各指标综合效应的客观量化。通过中心多点等距设计法建立数学模型,通过优化与预测分析筛选出对多个指标均有利的因素水平。本研究首次制备了多杀菌素·甲氨基阿维菌素苯甲酸盐聚乳酸微球(以下简称多杀菌素·甲维盐微球),并采用中心多点等距设计法,应用总评“归一值”对其制备工艺进行多指标优化,以期为该农药剂型的配方优化提供借鉴。
1 材料与方法 1.1 主要仪器及试剂XHF-I高速内切式匀浆器(宁波新芝生物科技股份有限公司);LS-POP(7)型激光粒度分析仪、SCF-106循环进样系统(珠海欧美克科技有限公司);Eppendorf 5804R高速冷冻离心机(德国艾本德股份公司);FA2004电子分析天平(上海舜宇恒平科学仪器有限公司);Acme9000高效液相色谱仪(HPLC,韩国英麟机器有限公司);88-1大功率双数显磁力搅拌器(常州国华电器有限公司);DHG-9140A型恒温鼓风干燥箱(上海精宏实验设备有限公司)。
95.8%甲氨基阿维菌素苯甲酸盐原药(emamectin benzoate,TC,佳木斯兴宇生物技术开发有限公司);84.97%多杀菌素原药 [spinosad,TC,由陶氏益农48%多杀菌素悬浮剂(催杀)提取纯化];聚乳酸(PLA,注塑级,相对分子质量约为8万,深圳光华伟业实业有限公司);PVA-1788(醇解度88%,阿拉丁试剂有限公司);透析袋(相对分子质量 7 000,美国Viskase公司);其他试剂均为市售分析纯、化学纯或色谱纯。
1.2 试验方法 1.2.1 多杀菌素·甲维盐微球的制备方法及性能表征 1.2.1.1 微球的制备采用溶剂蒸发法[6, 9]。分别称取一定量按比例混配好的多杀菌素·甲维盐原药和 0.4~1.2 g聚乳酸,溶于10 mL二氯甲烷中,保鲜膜密封后置于冰水浴中;待二者充分溶解后,以注射器将药液注入100 mL 质量分数为2.0% 的PVA-1788水溶液中,用高速内切式匀浆器以3 600 r/min乳化0.5 min,制得初乳液。加入约0.3 mL有机硅消泡剂,保持反应温度30 ℃,在避光及 360~1 200 r/min条件下高速搅拌,待二氯甲烷挥发完全后(约3~4 h)离心,抽滤,分离固形物并置于恒温干燥箱中,40 ℃下烘干,即得多杀菌素·甲维盐微球。
1.2.1.2 载药量及包封率测定精确称取20 mg微球,用少量二氯甲烷溶解。待二氯甲烷完全挥发后加入1.5 mL 甲醇,超声萃取5 min,转移至10 mL棕色容量瓶中,重复萃取5次,用甲醇定容至10 mL;经0.22 μm滤膜过滤,高效液相色谱法(HPLC)测定样品中多杀菌素及甲维盐的含量。
HPLC检测条件[17]为:Amemyst C18-H色谱柱 (250 mm×4.6 mm),紫外检测器,柱温为室温(25 ℃),流速1.0 mL/min,检测波长250 nm,进样体积20 μL,流动相为V(甲醇)∶V(乙腈)∶V[水(含0.5%乙酸钠)]=45∶45∶10。分别按(1)、(2)和(3)式计算微球载药量和包封率。


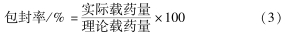
称取0.3 g微球样品和0.03 g磷酸钠(分散剂)于50 mL量杯中,加入超纯水约40 mL,超声波处理5 min,采用循环进样法用激光粒度仪测定微球粒径。按(4)式计算跨距(Sp)。

以磷酸盐缓冲液(PBS,pH 7,含20%甲醇)为释放介质,采用透析膜扩散法[33]测定微球的释药性能。称取75 mg微球,置于含2 mL释放介质的透析袋内,两端扎紧后投入到含150 mL释放介质的锥形瓶中,保鲜膜封口,避光条件下置于25 ℃恒温摇床上,以120 r/min的转速振荡。每隔24 h取2 mL释放介质,经0.22 μm 滤膜过滤后用HPLC测定释放介质中多杀菌素与甲维盐含量,计算农药释放率。每次取样后需补足2 mL释放介质。
1.2.1.5 DSC法验证微球的形成分别称取10 mg左右的多杀菌素·甲维盐微球、按一定比例混配好的多杀菌素·甲维盐原药与空白PLA微球的物理混合物、以及空白PLA微球,置于热分析仪中,以氩气为保护气,从室温开始以10 K/min的速率升温至1 000 K,记录数据并作图。
1.3 试验设计在预试验的基础上,选取对微球性质影响较显著的3个因素作为考察对象,即聚乳酸质量浓度(mg/mL)、理论载药量(%)和搅拌速率 (r/min)。根据CCD 的原理,每个因素设5水平,各因素的极大和极小水平根据预试验结果和制备的实际需要而定。各因素及水平见表 1,试验安排见表 2(1~4列)。
| 表 1 CCD设计的因素、水平表 Tab 1 Independents variables and their levels in coded and physical form in the central composite design |
| 表 2 CCD设计试验表及各项指标值Tab 2 Experimental designs with experimentally determined values of different dependent variables |
按配方制备微球,测定载药量、包封率、平均粒径、跨距及5 d 释放率。参考文献[32]方法,每个指标均标准化为0~1 之间的归一值(desirability),由各指标归一值求算几何平均数,得总评“归一值”(overall desirability)。
对取值越小越好的因素(粒径、跨距及5 d释放率),分别按(5)式计算归一值;对取值越大越好的因素(包封率和载药量),分别按(6)式计算归一值。
d=(Ymax-Y )/(Ymax-Ymin )(5)
d=(Y-Ymin)/(Ymax-Ymin )(6)
OD=(d1d2d3d4d5 ) 1/5(7)
其中d 为各指标的归一值;d1~d5分别表示5个指标的归一值;OD为总评“归一值”;Y为该指标的测定值;Ymax与Ymin分别为所有试验方案中该指标的最大值与最小值。
2 结果与分析微球的各项指标——包封率、粒径、跨距、5 d释放率及总评“归一值”的试验结果见表 2 。经Design-expert.V8.0.6软件拟合,微球的聚乳酸质量浓度、理论载药量及搅拌速率对微球包封率的影响符合线性关系,对微球平均粒径、跨距、5 d释放率及总评“归一值”的影响符合多元二次方程;分别固定3个因素中的一个为中值,绘制其余2个因素对粒径、跨距、5 d释放率及总评“归一值”的三维空间曲面图,对各因素的影响及各因素间存在的交互作用进行分析的结果如下(图 1~2)。
 | 图 1 三维因变量效应图
Fig. 1. 3D response surface graphs of dependent variables
X1、X2、X3分别为聚乳酸的质量浓度(mg/mL)、理论载药量(%)和搅拌速率(r/min)
X1,X2,X3 represent content of polylactic acid(mg/mL),theoretical pesticide loading(%) and stirring speed(r/min),respectively |
 |
图 2 三维因变量效应图
Fig.2 3D response surface graphs of dependent variables
X1,X2,X3分别为聚乳酸质量浓度(mg/mL)、理论载药量(%)和搅拌速率(r/min)
X1,X2,X3represent content of polylactic acid(mg/mL),theoretical pesticide loading(%) and stirring speed(r/min),respectively |
随着聚乳酸质量浓度、理论载药量及搅拌速率的升高,微球的包封率均出现不同程度的增加。经拟合,微球的包封率与聚乳酸质量浓度、理论载药量及搅拌速率在所选区间内符合一级动力学方程为:Y1=74.11+3.55X1+9.47X2+0.74X3, R2=0.871 8,P<0.05,表明线性关系良好,且3个因素在各自区间内并不存在交互作用。本研究结果表明,随着聚乳酸质量浓度、理论载药量和搅拌速率的增大,微球包封率逐渐增大,最高可达95.42%。
2.2 微球平均粒径、跨距、5 d释放率的拟合聚乳酸质量浓度、理论载药量及搅拌速率对微球平均粒径的影响符合二项分布式:Y2=8.25+0.95X1+0.10X2+0.41X3+0.087X1X2+0.020X1X3+0.11X2X3-0.19X12-0.39X22-0.20X32,R2=0.955 6,P<0.05,呈显著相关性。在所选区间内,微球的粒径随聚乳酸质量浓度及搅拌速率的增加而增大;较高或较低的理论载药量均会减小微球粒径,理论载药量在中值(35%)附近取值时,微球粒径达到最大值(见图1a)。3个因素间存在一定的交互作用,其中理论载药量与搅拌速率之间的交互作用更为明显。
聚乳酸质量浓度、理论载药量及搅拌速率对微球跨距的影响符合二项分布式:Y3=1.15+0.18X1-0.023X2-0.040X3-0.046X1X2-0.042X1X3+0.003 47X2X3+0.055X12+0.10X22+0.016X3 2,R2=0.879 4,P<0.05,呈显著相关性。在所选区间内,聚乳酸质量浓度越高,搅拌速率越低,微球的跨距越大;在所选区间接近中值(40%)附近,微球跨距最小(见图1b),较高与较低的理论载药量均会造成跨距增大。3个因素间存在一定的交互作用,其中理论载药量与搅拌速率之间的交互作用较小。 聚乳酸质量浓度、理论载药量及搅拌速率对微球5 d释放率的影响符合二项分布式:Y4=35.57+0.23X1+13.93X2+8.15X3+5.07X1X2+3.34X1X3-4.36X2X3+5.98X12-0.031X22+5.48X32,R2=0.9318,P<0.05,呈显著相关性。随着理论载药量及搅拌速率的增加,微球5 d释放率增加,而当聚乳酸质量浓度在80 mg/mL附近时,微球5 d释放率最小(见图2a)。
2.3 总评“归一值”(OD)的拟合聚乳酸质量浓度、理论载药量及搅拌速率对微球总评“归一值”的影响符合二项分布式:OD=0.49-0.14X1+0.12X2-0.021X3-0.048X1X2-0.003 35X1X3-0.074X2X3-0.096X12-0.054X22-0.019X32,R2=0.832 5,P<0.05,呈显著相关性。随着聚乳酸质量浓度及搅拌速率越大,总评“归一值”有减小的趋势,但其中搅拌速率的影响不显著;随着理论载药量增大,总评“归一值”明显增大(见图2b)。
2.4 微球配方优化及预测由图2b可知,当X1、X2、X3分别在60~80 mg/mL、45%~50%、500~600 r/min区间取值时,总评“归一值”可达到最大。微球粒径是影响微球理化性质的重要因素。粒径越小,越容易配制成悬浮率较高的农药悬浮剂,但过小的微球粒径将增加微球在形成过程中有效成分流失的概率,造成载药量降低,释药速率加快[34, 35]。因此,农药微球的粒径应控制在一定范围内。
本研究根据实际情况,将微球平均粒径控制在7~10 μm。经Design-expert V8.06软件优化,当X1、X2、X3分别取77.79 mg/mL、51.06%、560.91 r/min时,总评“归一值”可达到最大值0.681 1。较优条件下制备的多杀菌素·甲维盐微球表面较为圆整光滑(图 3),粒度分布较为均匀(图 4);差示量热扫描结果(图 5)表明,微球玻璃转化温度较之未包裹多杀菌素及甲维盐的空白聚乳酸微球减小约 10 ℃,说明原药已与聚乳酸框架结构以非定型态结合,而并非简单的物理吸附。经测定,总评“归一值”预测值与实测值偏差较小(见表 3),表明本研究所建立的数学模型可用来预测多杀菌素·甲维盐微球的较优配方。
 | 图 3 微球电子扫描图 Fig.3 Scanning electron microscope photographs of microspheres |
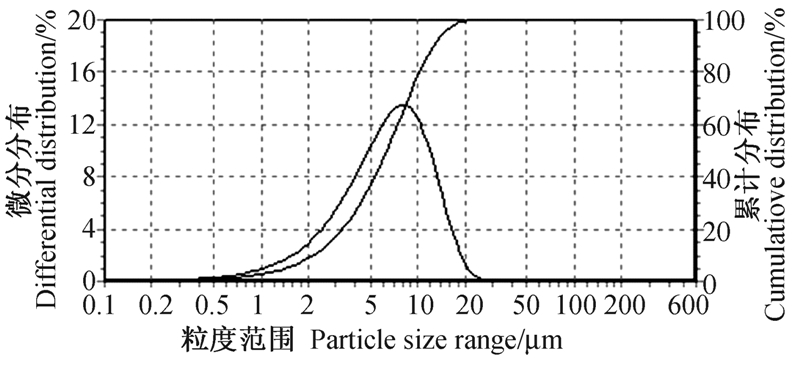 | 图 4 微球粒径分布图 Fig.4 Size distribution of microspheres |
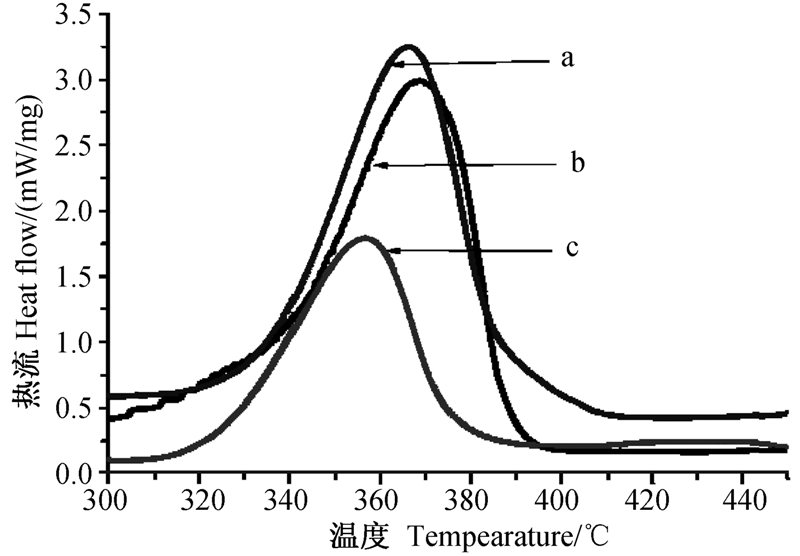 | 图 5 差示量热扫描示意图
Fig.5 Differential scanning calorimetry curve
a,b,c分别为空白聚乳酸微球、空白聚乳酸微球与原药混合物、多杀菌素·甲维盐微球
a,b,c represented blank PLA microspheres,mixture of blank PLA microspheres and pesticides technical,microspheres containing spinosad and emamectin benzoate,respectively. |
| 表 3 预测值及实测值 Table 3 Predicted and observed values |
本研究考察了聚乳酸质量浓度、理论载药量及搅拌速率3个因素对微球理化性质的影响。研究发现,随着聚乳酸质量浓度的增加,微球粒径、理论载药量及包封率均增加,这与郭瑞峰等[8]的研究结果符合。当聚乳酸质量浓度增加时,有机相的黏度增大,乳化形成的有机液滴体积增大,导致固化形成的微球粒径变大;同时,有机液滴增大,会导致有机相与外水相的接触面积减小,致使有效成分流失减小,包封率增大。
本研究表明,随着理论载药量的增大,微球的包封率及5 d 释放率均呈现增大的趋势。原因可能是随着理论载药量的升高,体系中农药的有效成分总量增加,随之流失于外水相的农药占总量的相对比例较小,因而包封率升高;同时,微球理论载药量越高,聚合物骨架材料在处方中所占的比例越小,微球分解时间变短,释药速度加快[35]。
本研究表明,随着搅拌速率增大,微球的粒径、包封率及5 d 释放率均逐渐增大,只有微球跨距呈现减小的趋势。这是因为较快的搅拌速率可加快有机溶剂的蒸发速度,微球形成过程缩短,微球的包封率提高[36, 37];有机溶剂蒸发速度加快还会导致聚合物固化剧烈,乳滴聚结的机率增加,导致微球粒径增大[38];此外,聚合物固化过于激烈,不利于农药包埋,微球控释能力下降,突释现象严重[35, 36]。
吴伟等[32]的研究表明,提高药物微球的理论载药量可使微球各指标的总评“归一值”增大,聚合物质量浓度对总评“归一值”的影响不明显。本研究中,提高理论载药量,减小聚乳酸质量浓度可使总评“归一值”增大;而搅拌速率对总评“归一值”的影响不明显,其原因可能是各指标之间的作用相互抵消了。
本研究结果表明,微球的包封率、粒径、跨距、5 d 释放率等指标最优条件各不相同,各指标之间也相互影响,因此在配方筛选过程中应考虑各指标的综合效应。本研究应用总评“归一值”法,较直观地反映了微球载药量、包封率、平均粒径、跨距及5 d释放率等指标的综合效应。经中心多点等距设计优化预测,筛选出了各项指标均较为适宜的农药微球制备配方。经测定,真实值与预测值偏差较小,模型准确度较好。表明采用中心多点等距设计结合总评“归一值”法,能筛选并优化得到性能较佳的农药微球制备配方,这也为其他类型农药制剂配方的筛选与优化提供了新的思路,具有较好的推广前景。
| [1] | 陆彬. 药物新剂型与新技术 [M]. 北京: 人民卫生出版社, 2005: 187-190. LU Bin. New Technology and New Dosage Forms of Drugs[M]. Beijing: People's Medical Publishing House, 2005: 187-190. (in Chinese) |
| [2] | TAKAYUKI T, MASAHIRO Y, YASUO H, et al. Preparation of polylactide/poly( ε -caprolactone) microspheres enclosing acetamiprid and evaluation of release behavior[J]. Polym Bull, 2008, 61(3): 391-397. |
| [3] | FERNANDEZ R, GINES M, MORILLO E. Development of controlled release formulations of alachlor in ethylcellulose[J]. J Microencapsul, 2000, 17(3): 331-342. |
| [4] | KOEK N, WILKINS M, CAIN B, et al. Controlled release of aldicarb from lignin loaded ionotropic hydrogel microspheres[J]. J Microencapsul, 1999, 16(5): 613-623. |
| [5] | SUAVE J, DALL E C, PEZZIN A P T, et al. Biodegradable microspheres of poly(3-hydroxybutyrate)/poly(E-caprolactone) loaded with malathion pesticide: preparation, characterization, and in vitro controlled release testing[J]. Appl Polym Sci, 2010, 117(6): 3419-3427. |
| [6] | 黄彬彬, 黄榕, 蔡晓娟, 等. 多杀菌素微球制备关键工艺研究Ⅰ[J]. 农药学学报, 2011, 13(3): 314-318. HUANG Binbin, HUANG Rong, CAI Xiaojuan, et al. Study on key process of preparation of spinosad microsphere: I[J]. Chin J Pestic Sci, 2011, 13(3): 314-318. ( in Chinese) |
| [7] | 黄彬彬, 杨丰梅, 张旭溪, 等. 多杀菌素微球制备关键工艺研究II[J]. 农药学学报, 2011, 13(4): 402-408. HUANG Binbin, YANG Fengmei, ZHANG Xuxi, et al. Study on key process of preparation of spinosad microsphere: Ⅱ[J]. Chin J Pestic Sci, 2011, 13(4): 402-408. ( in Chinese) |
| [8] | 郭瑞峰, 黄彬彬, 杨晓伟, 等. 毒死蜱-聚乳酸微球的制备及其性能评价[J]. 农药学学报, 2011, 13(4): 409-414. GUO Ruifeng, HUANG Binbin, YANG Xiaowei, et al. Preparation and characteristics analysis of microspheres of chlorpyrifos and polylactic acid[J]. Chin J Pestic Sci, 2011, 13(4): 409-414. (in Chinese) |
| [9] | 刘德坤, 张少飞, 张翠, 等. 多杀菌素 ·毒死蜱的微囊化及其性能评价[J]. 农药, 2013, 52(1): 19-23. LIU Dekun, ZHANG Shaofei, ZHANG Cui, et al. Preparation of spinosad-chlorpyrifos microsphere and its characteristics analysis[J]. Agrochemicals, 2013, 52(1): 19-23. (in Chinese) |
| [10] | 孟锐, 刘双清, 朱锐, 等. 可降解聚碳酸亚丙酯-毒死蜱微胶囊的制备及缓释性能评价[J]. 农药学学报, 2012, 14(5): 565-573. MENG Rui, LIU Shuangqing, ZHU Rui, et al. Preparation of degradable poly(propylene carbonate)-chlorpyrifos micocapsule and performance evaluation on its controlled release[J]. Chin J Pestic Sci, 2012, 14(5): 565-573. (in Chinese) |
| [11] | 杜顺堂, 朱明军, 梁世中. 生物农药多杀菌素的研究进展[J]. 农药, 2005, 44(10): 441-444. DU Shuntang, ZHU Mingjun, LIANG Shizhong. Research progress on the biopesticide spinosad[J]. Agrochemical, 2005, 44(10): 441-444. (in Chinese) |
| [12] | 毕富春, 徐凤波. 甲氨基阿维菌素苯甲酸盐研究概述[J]. 农药科学与管理, 2002, 23(3): 31-33. Bi Fuchun, Xu Fengbo. Outline of the studies on emamectin benzoate[J]. Pestic Sci Admin, 2002, 23(3): 31-33. (in Chinese) |
| [13] | 张侃侃, 胡德禹, 张钰萍, 等. 甲氨基阿维菌素苯甲酸盐在水稻环境中的残留及消解动态[J]. 农药学学报, 2010, 12(2): 190-194. ZHANG Kankan, HU Deyu, ZHANG Yuping, et al. Residue and decline study of emamectin benzoate in rice field[J]. Chin J Pestic Sci, 2010, 12(2): 190-194. (in Chinese) |
| [14] | 杨会营, 王占娣, 曹冬磊, 等. 10%多杀霉素 ·甲维盐水分散粒剂防治3代水稻二化螟田间药效试验[J]. 农药, 2012, 51(1): 60-61. YANG Huiying, WANG Zhandi, CAO Donglei, et al. Field trial of spinosad ·emamectin benzoate 10% WG against the 3 generation of rice stem borer[J]. Agrochemicals, 2012, 51(1): 60-61. (in Chinese) |
| [15] | 杨成对, 宋莉晖. 多杀菌素及其光照降解产物分析[J]. 高等学校化学学报, 2007, 28(11): 2056-2059. YANG Chengdui, SONG Lihui. Analyses of spinosad and its degradates from light irradiation[J]. Chem J Chin Univ, 2007, 28(11): 2056-2059. (in Chinese) |
| [16] | 钱婧, 花日茂, 汤锋, 等. 甲氨基阿维菌素苯甲酸盐在水中的光解研究[J]. 安徽农业科学, 2009, 37(27): 13211-13213. QIAN Jing, HUA Rimao, TANG Feng, et al. Study on photochemical degradation of emamectin benzoate[J]. J Anhui Agric Sci, 2009, 37(27): 13211- 13213. (in Chinese) |
| [17] | 任晓静. 甲维盐 ·多杀菌素3%乳油高效液相色谱分析[J]. 农药科学与管理, 2010, 31(2): 40-42. REN Xiaojing. HPLC analysis research of 3% emamectin benzoate pleocidin EC[J]. Pestic Sci Admin, 2010, 31(12): 40-42. (in Chinese) |
| [18] | 魏方林, 吴慧明, 程敬丽, 等. 多因素试验设计方法在农药微乳剂配方研制中的应用研究[J]. 农药学学报, 2009, 11(3): 373-380. WEI Fanglin, WU Huiming, CHENG Jingli, et al. Study on the application of multifactor experimental designs in pesticide microemulation development[J]. Chin J Pestic Sci, 2009, 11(3): 373-380. (in Chinese) |
| [19] | 朱丽云, 马良进, 孙培龙, 等. 苏云金杆菌微胶囊剂的研制[J]. 农业环境科学学报, 2005, 24(5): 966-969. ZHU Liyun, MA Liangjin, SUN Peilong, et al. Fomulation of microcapsulation of Bacillus thuringiensis[J]. J Agro-Environ Sci, 2005, 24(5): 966-969. (in Chinese) |
| [20] | 刘峰, 王会利, 何茂华, 等. 利用正交试验设计优选氰 ·莠水悬浮剂配方[J]. 农药学学报, 20 03, 5(1): 88-92. LIU Feng, WANG Huili, HE Maohua, et al. Application of orthogonal design in suspension concentrate of cynanzine and atrazine mixture[J]. Chin J Pestic Sci, 2003, 5(1): 88-92. (in Chinese) |
| [21] | 魏方林, 朱国念. 均匀设计及偏最小二乘回归法在高渗乳油研制中的应用[J]. 农药, 2006, 45(6): 387-389. WEI Fanglin, ZHU Guonian. Using uniform design and partial least-squares regression to prepare hypertonic emulsifiable concentrates[J]. Agrochemicals, 2006, 45(6): 387-389. (in Chinese) |
| [22] | 陈立, 徐汉虹, 赵善欢. 应用均匀设计获取复配农药最佳增效配方[J]. 华南农业大学学报, 2000, 21(3): 33-35. CHEN Li, XU Hanhong, ZHAO Shanhuan. Application of the uniform experimental design to obtain the optimal synergistic mixture ratio of combined pesticides[J]. J South China Agric, 2000, 21(3): 33-35. (in Chinese) |
| [23] | 张星一, 陈大为, 卢 炜. 多种统计学优化方法在盐酸川芎嗪缓释制剂处方设计中的比较研究[J]. 中国新药杂志, 2010, 19(5): 365-370. ZHANG Xingyi, CHEN Dawei, LU Wei. Comparison of several statistic designs in the development of ligustrazine hydrochloride (TMPH) sustained release formulations[J]. Chin J New Drugs, 2010, 19(5): 365-370. (in Chinese) |
| [24] | KRAJNIK P, KOPAC J, SLUGA A. Design of grinding factors based on response surface methodology[J]. J Mater Process Technol, 2005, 162-163: 629-636. |
| [25] | 陆彬, 吴伟. 中心多点等距设计法优化醋酸地塞米松聚丙交酯微球的制备工艺[J]. 药学学报, 1999, 34(5): 387-391. LU Bin, WU Wei. Optimization of preparation of dexamethasone acetate-loaded poly(D,L-lactide)microspheres by central composite design[J]. Acta Pharmaceutica Sinica, 1999, 34(5): 387-391. (in Chinese) |
| [26] | MONTGOMERY D C. Response surface methodology[M]//MONTGOMERY D C. Design and Analysis of Experiments. 2nd ed. New York: John Wiley & Sons, 1984: 445-474. |
| [27] | ABU-LZZA K A, GARCIA L, LU D R. Preparation and evaluation of sustained release AZT-loaded microspheres: optimization of the release characteristics using response surface methodology[J]. J Pharm Sci, 1996, 85(2): 144-149. |
| [28] | MOLPECERES J, GUZMAN M, ABERTURAS R, et al. Application of central composite designs to the preparation of poly caprolactone nanoparticles by solvent displacement[J]. J Pharm Sci, 1996, 85(2): 206-213 |
| [29] | 何为, 薛卫东, 唐斌. 优化实验设计方法及数据分析[M]. 北京: 化学工业出版社, 2012: 237-242. HE Wei, XUE Weidong, TANG Bin. Design Method of Optimal Experiment and Data Analysis[M]. Beijing: Chemical Industry Press, 2012: 237-242. (in Chinese) |
| [30] | 陈效忠, 李守君, 李晓凤, 等. 中心组合设计优化复凝聚法制备甲维盐微囊工艺[J]. 农药, 2012, 51(10): 733-735. CHEN Xiaozhong, LI Shoujun, LI Xiaofeng, et al. Optimization of technology for complex coacervation on emamectin benzoate microcapsule preparation by center composite cesign[J]. Agrochemicals, 2012, 51(10): 733-735. (in Chinese) |
| [31] | 曲桂霞, 刘学, 李晓凤, 等. 星点试验设计优化甲维盐微囊悬浮剂制备工艺[J]. 吉林农业大学学报, 2012, 34(5): 540-544. QU Guixia, LIU Xue, LI Xiaofeng, et al. Optimized formulation of emamectin benzoate microcapsule using central composite design[J]. J Jilin Agric, 2012, 34(5): 540-544.(in Chinese) |
| [32] | 吴伟, 崔光华, 陆彬. 实验设计中多指标的优化: 星点设计和总评"归一值"的应用[J]. 中国药学杂志, 2000, 35(8): 531-533. WU Wei, CUI Guanghua, LU Bin. Optimization of multiple evariables: application of central composite design and overall desirability[J]. Chin Pharm J, 2000, 35(8): 531-533. (in Chinese) |
| [33] | KOSTANSKI J W, DELUCA P P. A novel in vitro release technique for peptide containing biodegradable microspheres[J]. AAPS Pharm Sci Tech, 2000, 1(1): E4. |
| [34] | SANADRAP P, MOS A J. Inuence of manufacturing parameters on the size characteristics and release properties of nifedipine from poly (DL-lactide-co-glycolide) microspheres[J]. Int J Pharm, 1993, 98: 157-164. |
| [35] | 陈庆华. 药物微囊化新技术及应用[M]. 北京: 人民卫生出版社, 2008: 96-97. CHEN Qinghua. Novel Technologies of Microencapsulation and the Application in Drug Delivery Systems[M]. Beijing: People's Medical Publishing House, 2008: 96-97 (in Chinese) |
| [36] | BODMEIER R, MCGINITY J W. Solvent selection in the preparation of poly (D, L-lactide) microspheres prepared by the solvent evaporation method[J]. Int J Pharm, 1988, 43(1-2): 179-186. |
| [37] | ZHANG S F, CHEN PH, ZHANG F, et al. Preparation and physicochemical characteristics of polylactide microspheres of emamectin benzoate by modified solvent evaporation/extraction method[J]. J Agric Food Chem, 2013, 61(50): 12219-12225. |
| [38] | HNAIEN M, RUFFIN E, BORDES C, et al. Integrity characterization of myoglobin released from poly ( ε -caprolactone) microspheres using two analytical methods: UV/Vis spectrometry and conductometric bi-enzymatic biosensor[J]. Eur J Pharmacol Biopharm, 2011, 78(2): 298-305. |
 2014, Vol. 16
2014, Vol. 16


