东莨菪内酯(scopoletin)是植物体内一种重要的酚类植物抗毒素,属于香豆素类化合物,其化学名称为6-甲氧基-7-羟基香豆素(化学结构式见Scheme 1),具有抗肿瘤、抗炎、抗氧化等多种药理活性[1, 2, 3, 4],同时还具有良好的杀虫、抗菌杀菌及化感等农用生物活性[5, 6, 7, 8, 9, 10]。张永强等[11, 12, 13]曾报道从黄花蒿Artemisia annua L.7月份叶中提取的东莨菪内酯对朱砂叶螨Tetranychus cinnabarinus和柑橘全爪螨Panonychus citri具有较强的触杀作用,表现出了一定的农用开发前景。由于东莨菪内酯良好的杀螨活性,全国农药标准化技术委员会已于2012年正式将其农药中文通用名称定为“甲氧香螨酯”,英文通用名称为scopoletin。
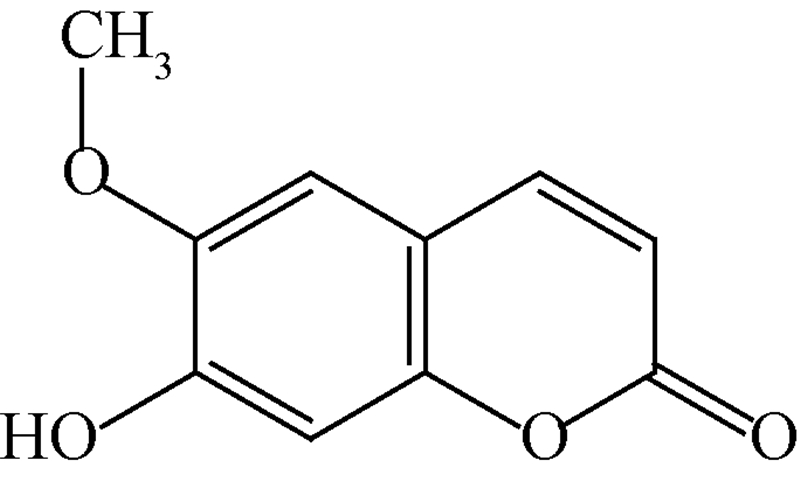 | Scheme 1 |
农药的光化学降解与其在环境中的持久性密切相关,是影响农药在环境中归趋的重要依据之一,也是评价农药在水体中残留性的重要指标[14]。目前尚未见有关东莨菪内酯光解的研究报道。笔者采用高效液相色谱仪,建立了水溶液中东莨菪内酯残留的分析方法,并在实验室条件下研究了其光解特性,以期为东莨菪内酯的环境风险评价提供科学依据。
1 材料与方法 1.1 仪器与试剂Agilent 1260高效液相色谱仪(带VWD检测器,美国Agilent公司);BSA124S-CW型电子天平(精确到0.1 mg,北京赛多利斯科学仪器有限公司);LDZX-50KB型立式压力蒸汽灭菌器(上海申安医疗器械厂);PB-10型pH计(德国赛多利斯公司);CCT-3320型超纯水系统(成都威思达智能科技有限公司);UV1000紫外分光光度计(上海天美科学仪器有限公司);TES-1332A照度计(东莞泰纳电子科技有限公司);BL-GHX-V型光化学反应仪(上海比朗仪器有限公司),其中液面距光源3.1 cm,配有500 W高压汞灯(照度为1.5×105~1.6×105 lx)、18 W紫外灯(254 nm,照度为1.25×103~1.32×103 lx,平均紫外强度为1 144 μW/cm2)以及500 W氙灯(照度为2.9×103~3.1×103 lx)。
东莨菪内酯(scopoletin)标准品(纯度≥99%,购于上海源叶生物科技有限公司),由于其微溶于水[15],故用甲醇将该标准品配制成1 000 mg/L的母液;甲醇、磷酸为色谱纯,其余试剂均为分析纯;试验用水为灭菌后的纯水。
不同pH值缓冲溶液配制:pH 5、7、9的缓冲液参考文献[16]方法配制,pH 6、8的缓冲液参考文献[17]方法配制,均现配现用,使用前灭菌并重新进行pH校准。
1.2 测定方法 1.2.1 光解试验分别取40 mL 反应液于6支具塞夹套石英管中(长60 mm,内径7.5 mm),磁力搅拌下使反应液均匀受光,利用冷凝水控制反应液和光源温度,待光化学反应仪稳定后进行光解试验。以氙灯为光源时分别于光照后第0、1、3、5、7、9、11和14 h取样,以汞灯为光源时分别于光照后第0、1、2、3、5、6、7和8 min取样,以紫外灯为光源时取样时间为第0、10、20、30、40、50、60和70 min。样品过0.22 μm微孔滤膜,避光保存。参考文献报道[18],采用优化后的HPLC法检测溶液中东莨菪内酯的质量浓度,根据不同时间段溶液中东莨菪内酯的质量浓度拟合得到光解动力学方程。每处理重复3次,同时设黑暗对照。黑暗对照除试管用铝箔包裹外,其他条件均与光照处理相同。
1.2.1.1 初始浓度对水中东莨菪内酯光解的影响用纯水将1 000 mg/L的东莨菪内酯母液分别稀释成40、20、10和5 mg/L的系列光反应液,于500 W 氙灯下进行光解,反应液温度控制在25 ℃±1 ℃。
1.2.1.2 不同光源对水中东莨菪内酯光解的影响用纯水将东莨菪内酯母液稀释成10 mg/L的反应液,分别于500 W高压汞灯、18 W紫外灯和500 W 氙灯下进行光解,反应液温度控制在25 ℃±1 ℃。
1.2.1.3 不同pH条件对水中东莨菪内酯光解的影响分别用pH为5、6、7、8、9的缓冲液将东莨菪内酯母液稀释成10 mg/L 的反应液,于500 W氙灯下进行光解,反应液温度控制在25 ℃±1 ℃。
1.2.1.4 不同温度对水中东莨菪内酯光解的影响用纯水将东莨菪内酯母液稀释成10 mg/L的反应液,于500 W氙灯下进行光解,温度分别控制为5、15、25、35、45、55和65 ℃,温差不超过±1 ℃。 1.2.2 HPLC 检测条件
采用Agilent 1260 高效液相色谱仪进行测定。通过对流动相比例、进样量、色谱柱温度等进行优化,确定其最佳检测条件为:Venusil XBP C18色谱柱(250 mm×4.6 mm,5 μm);VWD检测器;柱温30 ℃;流速为1 mL/min;进样量为10 μL;流动相:V(甲醇)∶V(0.05%磷酸)=40∶60;检测波长345 nm;运行时间18 min。在此条件下,东莨菪内酯的保留时间约为8.37 min。
1.2.3 添加回收率试验用纯水稀释东莨菪内酯标准品母液,使其质量浓度分别为40、20、10、5和0.5 mg/L,按1.2.2 节条件进行测定。每个添加水平重复5次,同时设不加药的空白对照。
1.3 结果计算与数据处理按(1)式计算不同光照时间下东莨菪内酯的光解率。
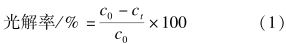
通过(2)式和(3)式分别计算东莨菪内酯在不同溶液中的光解动力学方程及半衰期[19]。


式中,ct为t时刻反应液中东莨菪内酯的质量浓度(mg/L),c0为东莨菪内酯的初始质量浓度(mg/L),k为光解速率常数(h-1),t1/2为光解半衰期(h)。
试验数据采用Excel 2003和SPSS statistic 17.0软件进行统计分析。
2 结果与讨论 2.1 检测方法的准确度和精密度
在添加水平为0.5、5、10、20和40 mg/L时,东莨菪内酯在纯水中的平均回收率在84%~96%之间,相对标准偏差(RSD)在1.9%~0.38%之间,表明所建立方法的准确度及精密度均较好,符合农药残留分析要求。东莨菪内酯标样及水中添加0.5 mg/L 东莨菪内酯样品的色谱图见图 1。
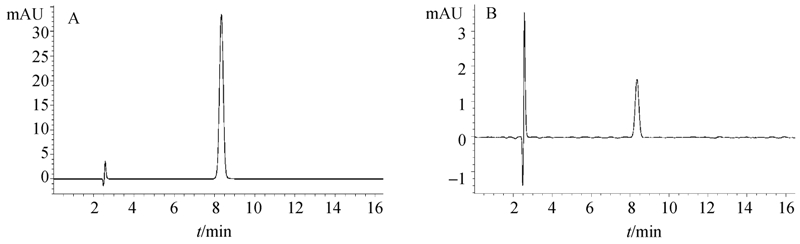 | 图 1 东莨菪内酯标样及水中的添加回收色谱图(345 nm) Fig. 1 HPLC chromatogram of scopoletin standard solution and water sample fortified with scopoletin at level of 0.5 mg/L at 345 nm |
研究发现:在试验设定的初始质量浓度范围内,东莨菪内酯的光解均符合一级动力学方程(表 1),其光解速率与初始质量浓度呈负相关;此外,随着光解时间的推移,单一浓度下的光解速率逐渐趋于平缓(图 2)。这与武霓等[20]的研究结果一致。分析其原因可能是由于反应初期水溶液中存在大量的东莨菪内酯分子,它们相互之间对光子存在竞争吸收,在光能一定的条件下,随东莨菪内酯初始质量浓度增加,单位分子接受到的光能减少,从而使其光解速率相应降低;而随着反应时间延长,光解产物增多,光解产物在光能的激发下继续发生降解并与农药分子竞争吸收光能量,从而使得光解速率趋于平缓[20, 21]。
| 表 1 不同初始质量浓度下东莨菪内酯的光解动力学参数 Table 1 Photolytic kinetics parameters of scopoletin at four different initial concentrations |
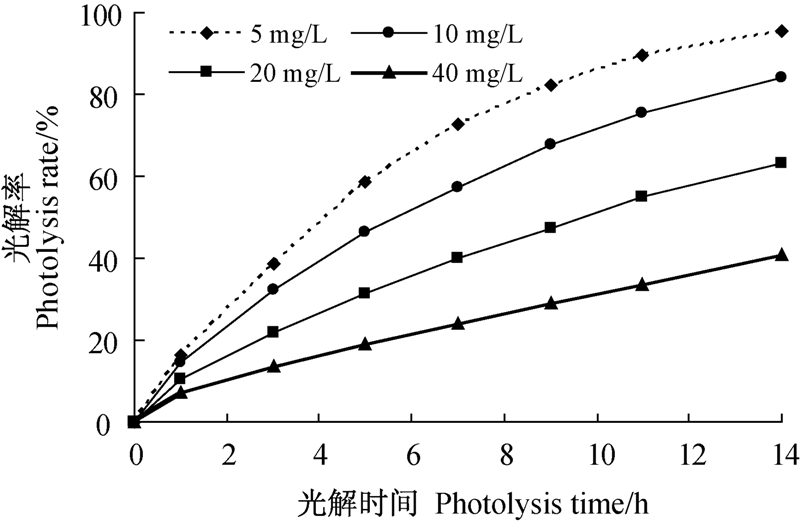 |
图 2 不同初始质量浓度东莨菪内酯在水中的光降解
Fig. 2. Photolysis of scopoletin with different
initial concentrations in water
注:光源为500 W氙灯;反应温度25 ℃±1 ℃。
Note: Light source was 500 W xenon lamp; reaction temperature was 25 ℃±1 ℃. |
东莨菪内酯在不同光源下的光解结果均符合一级动力学方程(表 2),但光解速率存在显著差异,其在500 W汞灯和18 W紫外灯下的光解速率明显高于在500 W 氙灯下的。东莨菪内酯在高压汞灯、紫外灯和氙灯下的光解半衰期分别为0.052 5、0.297和5.42 h,其中氙灯下的光解半衰期是高压汞灯下的103倍左右,而高压汞灯和紫外灯下的半衰期相对比较接近。这主要是由于3种光源所发射的光波在不同波段的能量分布差异显著,同时还与东莨菪内酯自身的吸收波长有关。通常高压汞灯的发射光谱主要集中在紫外光区,光的能量较高,而氙灯光谱集中在可见光区,光能较低[22]。
| 表 2 东莨菪内酯在不同光源下的光解动力学参数 Table 2 Photolytic kinetics parameters of scopoletin under different light sources |
图 3为东莨菪内酯在纯水中的吸收光谱。从中可看出,东莨菪内酯在紫外光区吸收较强,其最大吸收波长在345 nm处,而在长波长区基本不吸收,因此氙灯光波中能被东莨菪内酯吸收的部分所占比例很少。因此,东莨菪内酯在高压汞灯下光解非常迅速,在紫外光下次之,在氙灯下光解速率最慢。
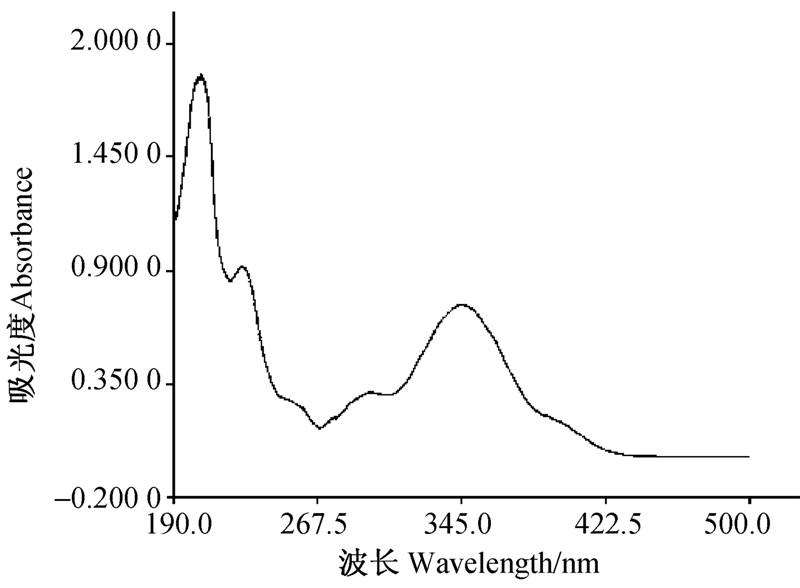 | 图 3 东莨菪内酯在纯水中的紫外-可见吸收光谱 Fig. 3 UV-Vis absorption spectra of scopoletin in pure water |
东莨菪内酯在不同pH值缓冲溶液中的光解规律均符合一级动力学方程(表 3),其光解速率随pH值的增大而加快。由黑暗对照可知,处理期间东莨菪内酯在不同pH值缓冲溶液中均未降解,排除了东莨菪内酯在处理期间水解的可能性,表明水中东莨菪内酯的降解途径为光降解。由表 3可看出,pH值对水溶液中东莨菪内酯的光解具有明显影响,在500 W氙灯照射下,东莨菪内酯在pH值为9的缓冲液中光解速率最快,其半衰期比在pH 5时缩短了8.09 h;pH 在6、7、8范围内时,pH值对东莨菪内酯光解速率的影响很小。其原因可能是由于东莨菪内酯属于酯类物质,除光解外,其在碱性溶液中吸收光能还同时发生了光水解的缘故[23]。
| 表 3 东莨菪内酯在不同pH值下的光解动力学参数 Table 3 Photolytic kinetics parameters of scopoletin in different pH value buffer solutions |
从表 4中可看出,在5~65 ℃下,东莨菪内酯的光解符合一级动力学方程,且光解速率随温度升高呈先升高后降低的趋势,其中在15 ℃时光解速率达到最大值0.135 h-1,即半衰期最短为5.13 h。光解速率仅在5~15 ℃范围内随温度的升高而加快,可能是由于光化学反应不是普通的热反应,因此温度对光解速率增加的作用有限;而在15~65 ℃范围内,光解速率随温度的升高而降低,其原因可能是由于东莨菪内酯本身的结构特性,其酚羟基的H易电离成为H+,从而表现出弱酸性[24],当温度升高时,电离平衡正向移动,H+增多,溶液的酸性增大,根据2.2.3节结果,酸性增大将不利于东莨菪内酯光水解反应的进行,因而使得其光解速率降低。
| 表 4 东莨菪内酯在不同温度下的光解动力学参数 Table 4 Photolytic kinetics parameters of scopoletin at different temperatures |
不同条件下,东莨菪内酯在水溶液中的光解均符合一级动力学方程。其光解速率与初始质量浓度、光源、pH值及温度相关:不同初始浓度下,东莨菪内酯的光解速率随初始质量浓度的增大而降低;不同光源下,其光解速率从大到小依次为500 W高压汞灯>18 W紫外灯>500 W氙灯,即东莨菪内酯在高压汞灯下光解最快;不同pH值下,其光解速率随pH值的增大而升高,即东莨菪内酯在碱性条件下光解最快;在5~ 65 ℃范围内,其光解速率随温度升高呈先升高后降低趋势。东莨菪内酯光解反应机理及光解产物的研究正在进行中。
| [1] | KIM H J, JANG S I, KIM Y J, et al. Scopoletin suppresses pro-inflammatory cytokines and PGE2 from LPS-stimulated cell line, RAW 264.7 cells[J]. Fitoterapia, 2004, 75(3-4): 261-266. |
| [2] | EFFERTH T, HERRMANN F, TAHRANI A, et al. Cytotoxic activity of secondary metabolites derived from Artemisia annua L. towards cancer cells in comparison to its designated active constituent artemisinin[J]. Phytomedicine, 2011, 18(11): 959-969. |
| [3] | NOH J R, GANG G T, KIM Y H, et al. Antioxidant effects of the chestnut (Castanea crenata) inner shell extract in t-BHP-treated HepG2 cells, and CCl4-and high-fat diet-treated mice[J]. Food Chem Toxicol, 2010, 48(11): 3177-3183. |
| [4] | GNONLONFIN G J B, SANNI A, BRIMER L. Review scopoletin:a coumarin phytoalexin with medicinal properties[J]. Critical Reviews in Plant Sciences, 2012, 31(1): 47-56. |
| [5] | PETERSON J K, HARRISON H F, JACKSON D M. Biological activities and contents of scopolin and scopoletin in sweetpotato clones[J]. HortScience, 2003, 38(6): 1129-1133. |
| [6] | VERA N, POPICH S, LUNA L, et al. Toxicity and synergism in the feeding deterrence of some coumarins on Spodoptera frugiperda Smith (Lepidoptera: Noctuidae)[J]. Chem Biodivers, 2006, 3(1): 21-26. |
| [7] | TAGUCHI G, FUJIKAKA S, YAZAWA T, et al. Scopoletin uptake from culture medium and accumulation in the vacuoles after conversion to scopolin in 2,4-D-treated tobacco cells[J]. Plant Sci, 2000, 151(2): 153-161. |
| [8] | DUTSADEE C, NUNTA C. Induction of peroxidase, scopoletin, phenolic compounds and resistance in Hevea brasiliensis by elicitin and a novel protein elicitor purified from Phytophthora palmivora[J]. Physiol Mol Plant P, 2008, 72(4-6): 179-187. |
| [9] | KIM Y O, LEE E J. Comparison of phenolic compounds and the effects of invasive and native species in East Asia: support for the novel weapons hypothesis[J]. Ecol Res, 2011, 26(1): 87-94. |
| [10] | BHOWMIK P C, INDERJIT. Challenges and opportunities in implementing allelopathy for natural weed management[J]. Crop Prot, 2003, 22(4): 661-671. |
| [11] | 张永强, 丁伟, 赵志模, 等. 黄花蒿提取物对朱砂叶螨生物活性的研究[J]. 中国农业科学, 2008, 41(3): 720-726. ZHANG Yongqiang, DING Wei, ZHAO Zhimo, et al. Studies on acarcidal bioactivities of the extracts from Artemisia annua L. against Tetranychus cinnabarinus Bois. (Acari: Tetranychidae)[J]. Scientia Agricultura Sinica, 2008, 41(3): 720-726. (in Chinese) |
| [12] | 张永强, 丁伟, 田丽, 等. 黄花蒿提取物对柑橘全爪螨的生物活性[J]. 中国农业科学, 2009, 42(6): 2217-2222. ZHANG Yongqiang, DING Wei, TIAN Li, et al. Acaricidal bioacitivity of Artemisia annua L. extracts against Panonychus citri (Acari: Tetranychidae)[J]. Scientia Agricultura Sinica, 2009, 42(6): 2217-2222. (in Chinese) |
| [13] | 张永强. 黄花蒿杀螨物质活性追踪及杀螨作用机理研究 [D]. 重庆: 西南大学, 2008. ZHANG Yongqiang. Studies on acaricidal action mechanism and bio-guided isolation of bioactive substance from Artemisia annua L. [D]. Chongqing: Southwest University, 2008. (in Chinese) |
| [14] | FILIPE O M S, SANTOS S A O, DOMINGUES M R M, et al. Photodegradation of the fungicide thiram in aqueous solutions. Kinetic studies and identification of the photodegradation products by HPLC-MS/MS[J]. Chemosphere, 2013, 91(7): 993-1001. |
| [15] | 魏丽娟, 周金培, 戴岳. 天然产物东莨菪素的研究进展[J]. 海峡药学, 2009, 21(4): 10-13. WEI Lijuan, ZHOU Jinpei, DAI Yue. Progress in the study of natural product scopoletin[J]. Strait Pharmaceutical Journal, 2009, 21(4): 10-13. (in Chinese) |
| [16] | 朴秀英, 王晓军, 陶传江, 等. 磺酰脲除草剂单嘧磺隆水解和水中光解研究[J]. 现代农药, 2012, 11(4): 42-45. PIAO Xiuying, WANG Xiaojun, TAO Chuanjiang, et al. Hydrolysis and photolysis of sulfonylurea herbicide monosulfuron in water[J]. Modern Agrochemicals, 2012, 11(4): 42-45. (in Chinese) |
| [17] | 楼书聪. 化学试剂配制手册[M]. 南京: 江苏科学技术出版社, 2002. LOU Shucong. Chemical Reagent Preparation Manual [M]. Nanjing: Jiangsu Science and Technology Press, 2002. (in Chinese) |
| [18] | 张紫佳, 张勉, 朱恩圆, 等. 丁公藤类药材及其混用品中总东莨菪内酯的含量测定[J].中国药学杂志, 2004, 39(12): 936-938. ZHANG Zijia, ZHANG Mian, ZHU Enyuan, et al. Determination of total scopoletin in Caulis erycibes and its adulterants[J]. Chin Pharm J, 2004,39(12): 936-938. (in Chinese) |
| [19] | 国家环境保护总局. 化学农药环境安全评价试验准则[S]. 2004. National Environmental Protection Agency. The experimental rule of security evaluation of chemical pesticide[S]. 2004. (in Chinese) |
| [20] | 武霓, 刘晓凤, 王鸣华. 甲萘威在液相中的光化学降解研究[J]. 吉林农业大学学报, 2013, 35(2): 206-210. WU Ni, LIU Xiaofeng, WANG Minghua. Photochemical degradation of carbaryl in virious solvents[J]. J Jilin Agric Univ, 2013, 35(2): 206-210. (in Chinese) |
| [21] | 孙晓燕, 赵百萍, 王鸣华. 溴虫腈在不同溶剂中的光化学降解[J]. 农药学学报, 2013, 15(4): 469-474. SUN Xiaoyan, ZHAO Baiping, WANG Minghua. Study on photochemical degradation of chlorfenapyr in different solvents[J]. Chin J Pestic Sci, 2013, 15(4): 469-474. (in Chinese) |
| [22] | 刘芃岩, 刘海娣, 李冰. 水相低浓度甲氰菊酯的光降解研究[J]. 环境科学与技术, 2013, 36(3): 136-140. LIU Pengyan, LIU Haidi, LI Bing. Study on the photochemical degradation of fenpropathrin of low concentration in water phase[J]. Environ Sci Tech, 2013, 36(3): 136-140. (in Chinese) |
| [23] | 邹雅竹, 龚道新, 汪传刚. 顺式氯氰菊酯在不同pH值下的光化学降解[J]. 湖南农业大学学报: 自然科学版, 2006, 32(3): 333-335. ZOU Yazhu, GONG Daoxin, WANG Chuangang. On photolysis ofα-cypermethrin in different buffer solutions[J]. J Hunan Agric Univ: Nat Sci, 2006, 32(3): 333-335. (in Chinese) |
| [24] | 颜朝国. 有机化学[M]. 郑州: 郑州大学出版社, 2007: 244. YAN Chaoguo. Organic Chemistry[M]. Zhengzhou: Zhengzhou University Press, 2007: 244.(in Chinese) |
 2014, Vol. 16
2014, Vol. 16


