文章信息
- 储小燕, 张娅菲, 朱雷, 李玉, 冯士彬, 吴金节, 王希春
- CHU Xiaoyan, ZHANG Yafei, ZHU Lei, LI Yu, FENG Shibin, WU Jinjie, WANG Xichun
- 自噬对DON诱导仔猪海马神经细胞损伤的影响
- Effect of autophagy on piglet hippocampal nerve cells damaged by deoxynivalenol
- 南京农业大学学报, 2019, 42(1): 160-167
- Journal of Nanjing Agricultural University, 2019, 42(1): 160-167.
- http://dx.doi.org/10.7685/jnau.201804028
-
文章历史
- 收稿日期: 2018-04-14
自噬作为一种进化上保守的分解代谢过程, 通过去除过量或不必要的蛋白质以及受损或老化的细胞器发挥稳态调节因子的作用[1]。此外, 自噬是通过回收大分子对营养和环境压力做出反应, 并提供能量和分子构建[2]。早在20世纪50年代末, Clark[3]通过电镜观察发现在新生代小鼠肾脏中含有非晶状物质的囊泡结构和细胞质细胞器并引入了自噬。自噬可在多种条件下被激活, 如缺氧、内质网压力和营养饥饿等, 自噬膜吞噬一部分含胞浆蛋白质和细胞器, 并与溶酶体融合以裂解内部成分[4]。自噬最初被描述为是对饥饿的细胞反应[5]。后来, 已知自噬诱导在各种细胞应答中起关键作用, 例如预防细菌和病毒的感染[6-7]、抗原呈递[8]、神经发育[9]和脂质代谢[10]等。谢俊泽等[11]研究发现镉可以引起BRL3A细胞自噬水平的上升, 激活的自噬又对镉导致的细胞损伤具有一定保护作用。
脱氧雪腐镰刀菌烯醇(deoxynivalenol, DON), 是由镰刀菌侵染小麦和玉米等谷类作物产生的一种B型单端孢霉烯族毒素, 由于其在食物链中具有高暴露水平和高污染频率的特性已成为全球农业领域的重要问题之一, 对人类和动物的健康构成了严重威胁[12-13]。欧洲经济共同体食品科学委员会(SCF)通过研究DON对动物流行病学的影响, 在2002年已经设定了每日可接受DON摄入量为1.0 μg·kg-1[14]。已有研究表明, DON主要是对动物的免疫系统、胃肠道和大脑产生毒性作用。Park等[15]研究发现, 猪摄入DON后, 采食量下降, 体质量增长缓慢, 摄入的DON中至少有67%被吸收, 表明猪对呕吐毒素具有高度敏感性。范梦雪等[16]研究发现, DON对仔猪海马神经细胞具有明显的毒性, 能够诱导细胞损伤并发生凋亡。耿芳芳等[17-18]研究报道, DON体内暴露可对雏鸡产生一定的神经毒性, 引起雏鸡生长缓慢、便血, 血清以及脑组织脂质过氧化反应, 对脑组织造成不同程度的损伤, 其中海马组织超微结构发生明显的变化, 降低了脑中[Ca2+]i与钙调蛋白(CAM)含量以及CAM mRNA相对表达量。
目前已有很多研究人员通过体外试验发现DON暴露能够引起细胞凋亡和坏死, 而关于DON致神经细胞损伤中是否有自噬的参与及其作用尚未见报道。由于海马神经细胞在中枢神经系统中比较集中, 且最容易被外界因素影响而受到损伤, 故本试验以仔猪海马神经细胞为模型, 用不同浓度的DON处理细胞, 通过添加自噬抑制剂氯喹(chloroquine, CQ)和自噬激活剂雷帕霉素(rapamycin, RAP), 采用CCK-8法检测细胞活性, 以探讨自噬对DON诱导仔猪海马神经细胞损伤的影响, 为进一步研究DON对神经细胞的毒性机制提供试验依据。
1 材料与方法 1.1 细胞以及主要试剂和设备仔猪海马神经细胞, 赛齐生物有限公司; DON标准品, 美国Sigma公司; DMEM高糖培养基, 美国HyClone公司; 胎牛血清、二甲基亚砜, 美国Clark公司; 胰酶细胞消化液、BCA蛋白浓度测定试剂盒、羊抗兔二抗, 碧云天生物技术公司; CCK-8细胞增殖-毒性检测试剂盒, 东仁化学研究所; LC3抗体, 美国SANTA公司; β-actin抗体, 北京锐抗生物科技有限公司; DH5α感受态细胞、EndoFree Midi Plasmid Kit无内毒素质粒中量提取试剂盒, 北京天根生化科技有限公司; GFP-LC3质粒, 武汉淼灵质粒平台; Lipofectamine® 2000转染试剂, 美国Thermo公司; 雷帕霉素(rapamycin, RAP)、氯喹(chloroquine, CQ), 美国Selleckchem公司。
CO2恒温培养箱, 美国Thermo公司; TEOL-2010电子透射显微镜, 日本电子株式会社; XDS-1倒置显微镜, 重庆光电仪器有限公司; Multiskan Mk3型酶标仪, 美国Thermo公司; 凝胶成像系统, 美国Bio-Rad公司; IX71倒置荧光显微镜, 日本Olympus公司;
1.2 细胞培养与试验分组将1 mg DON标准品粉末溶于5 mL超纯水中, 配成200 ng·mL-1的DON母液。将不同剂量的DON母液添加到DMEM细胞培养液中, 使其终质量浓度分别为0、125、250、500、1 000和2 000 ng·mL-1。
将复苏后的仔猪海马神经细胞悬液移至5 cm×5 cm正方细胞培养瓶内, 用适量的DMEM高糖培养基(添加体积分数为10%的胎牛血清和适量的抗生素)在培养条件为37 ℃、5% CO2、饱和湿度的细胞培养箱中进行培养。将处于对数生长期的仔猪海马神经细胞, 以1×105 mL-1的密度接种于6孔细胞培养板, 继续培养24 h, 再分别加入含有不同质量浓度(0、125、250、500、1 000和2 000 ng·mL-1)DON的细胞培养液攻毒24 h, CQ联合组和RAP联合组在添加上述浓度DON之前0.5 h分别添加5 μmol·L-1 CQ和50 nmol·L-1 RAP。每个浓度设置3个复孔。
1.3 DON对仔猪海马神经细胞形态和超微结构的影响取1.2节经不同质量浓度DON染毒后的仔猪海马神经细胞, 于倒置显微镜下观察细胞的生长状况及形态变化, 然后将胰酶消化后的细胞轻轻吹掉并收集, 再以1 000 r·min-1离心5 min, 用2.5%戊二醛固定细胞后制作电镜切片, 观察细胞超微结构的变化。
1.4 CCK-8法检测细胞存活率取1.2节经不同质量浓度DON染毒后的仔猪海马神经细胞置6孔细胞培养板, 再向每孔中加入10 μL CCK-8试剂, 放入细胞培养箱中继续培养1~4 h, 直至出现明显的颜色反应。用酶标仪读取D450值, 计算细胞存活率。
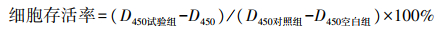
|
将处于对数生长期的仔猪海马神经细胞接种于6孔板, 每孔接种1×106个细胞, 当细胞密度达到60%~ 70%时, 将每200 μL培养液中含有2 μg质粒DNA和6 μL转染试剂的DMEM混合液室温静置15 min, 换液后将混合液以每孔200 μL加入到6孔板中液面以下, 培养6 h后换液, 加入不同质量浓度的(0、125、250、500、1 000和2 000 ng·mL-1)DON于37 ℃、5% CO2的恒温培养箱中继续培养24 h。取出6孔板, PBS洗2次后, 在荧光显微镜下观察细胞内是否有绿色荧光蛋白的表达以及细胞内荧光蛋白是否发生点状聚集的现象。
1.6 Western blot检测DON对仔猪海马神经细胞LC3蛋白的表达取1.2节经不同质量浓度DON处理后的仔猪海马神经细胞, 按照BCA蛋白浓度测定试剂盒说明书提取总蛋白用于LC3蛋白表达水平的评估。采用BCA工作液测定各试验组提取物的总蛋白含量, 调节总蛋白含量使其一致。将上述蛋白样品加入5×SDS上样缓冲液, 95 ℃水浴处理5~10 min后4 ℃保存备用。以40 μg的总蛋白上样量进行SDS-PAGE电泳, 80 V电泳30 min左右, 当样品到达分离胶边界后把电压调为120 V, 继续电泳60 min左右, 随后依照负极、海绵、靠胶滤纸、胶、PVDF膜、靠膜滤纸、海绵、正极的次序放入电泳槽, 120 V电压下转膜28 min, 转膜完成后将其置于5% BSA溶液中, 在摇床上室温封闭4 h。置LC3抗体中冷藏条件下过夜孵育, 置羊抗兔二抗中室温摇床孵育45 min。按照ECL发光液说明书配制发光液, 用凝胶成像系统成像, 再用软件将所取得的图片进行灰度扫描分析。
1.7 数据分析本试验数据均以平均值±标准差(x±SD)表示, 采用SPSS 17.0统计软件中ANOVA进行单因子方差分析; 运用GraphPad Prism 5.0数据软件绘制柱状图。
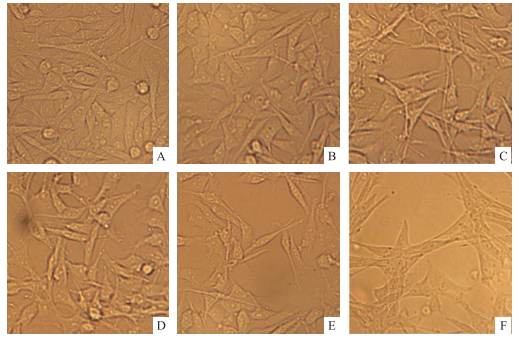
2 结果与分析 2.1 DON对仔猪海马神经细胞生长状况的影响在倒置显微镜下观察各组细胞的生长状况, 如图 1所示:对照组细胞(图 1-A)胞体饱满致密, 突起明显且交织成网络状, 呈不规则的放射型。而经不同质量浓度(125、250、500、1 000和2 000 ng·mL-1)DON染毒处理24 h后, 细胞密度逐渐降低, 排列稀疏, 细胞形态受损且发生皱缩, 当DON浓度达2 000 ng·mL-1时, 细胞开始出现凋亡的特征变化(图 1-B—图 1-F)。
|
图 1 脱氧雪腐镰刀菌烯醇(DON)对仔猪海马神经细胞生长状况的影响(×400) Fig. 1 Effect of deoxynivalenol(DON)on growth state in piglet hippocampal nerve cells(PHNC)(×400) A—F分别表示DON处理质量浓度为0、125、250、500、1 000、2 000 ng·mL-1。 A-F represent DON concentrations are 0, 125, 250, 500, 1 000, 2 000 ng·mL-1, respectively. |
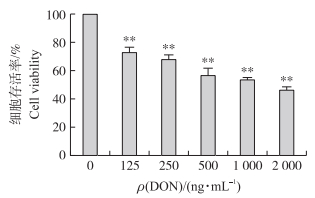
由图 2可见:仔猪海马神经细胞经DON作用24 h后的存活率随着DON浓度的增加而降低, 呈现出明显的量效关系, 并且与对照组相比均差异极显著(P < 0.01)。
|
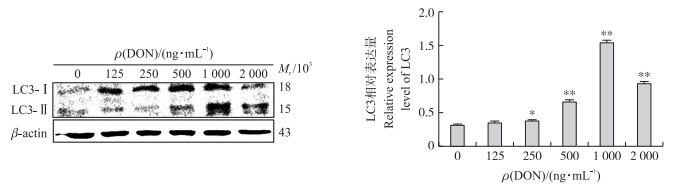
图 4 DON对仔猪海马神经细胞LC3表达的影响 Fig. 4 The Effect of DON on LC3 expression in PHNC |
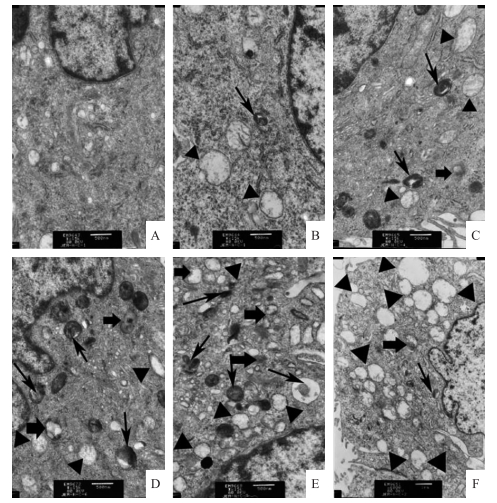
细胞经过DON处理, 制片后使用透射电镜观察仔猪海马神经细胞亚细胞结构的细微变化。由图 3可见:对照组细胞胞质均匀, 处理组细胞胞质中出现空泡, 且出现了双层或多层膜包裹的自噬小体和晚期自噬溶酶体结构, 高浓度组刺激所产生的空泡化更明显。在DON为1 000 ng·mL-1时, 细胞内出现的自噬小体和晚期自噬溶酶体最多; 在DON为2 000 ng·mL-1时细胞内部分视野可见自噬小体, 且出现的胞质空泡化最多。
|
图 3 DON对仔猪海马神经细胞超微结构的影响(×15 000)
Fig. 3 Effect of DON on ultrastructure in PHNC(×15 000)
A—F分别表示DON处理质量浓度分别为0、125、250、500、1 000、2 000 ng·mL-1。→, ▲, 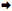 分别指胞质自噬小体、细胞空泡化及晚期自噬溶酶体。
A-F represent DON concentrations are 0, 125, 250, 500, 1 000, 2 000 ng·mL-1, respectively.
→, ▲, 分别指胞质自噬小体、细胞空泡化及晚期自噬溶酶体。
A-F represent DON concentrations are 0, 125, 250, 500, 1 000, 2 000 ng·mL-1, respectively.
→, ▲, 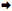 show cytoplasmic autophagosome, vacuolated and late autophagic lysosomes, respectively. show cytoplasmic autophagosome, vacuolated and late autophagic lysosomes, respectively.
|
以125、250、500、1 000和2 000 ng·mL-1的DON处理细胞24 h, Western blot检测LC3表达。如图 4所示:随着DON处理浓度的上升, LC3-Ⅱ的表达量先升高后降低, 当DON为1 000 ng·mL-1时, LC3-Ⅱ的表达量最高。与对照组相比, 250~2 000 ng·mL-1 DON处理组LC3表达量显著(P < 0.05)或极显著(P < 0.01)增加。
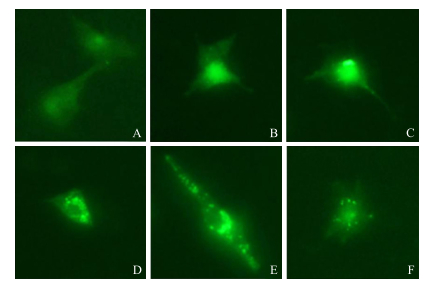
2.5 DON对仔猪海马神经细胞GFP-LC3蛋白表达的影响自噬被诱导时, GFP-LC3大部分呈点状分布, 自噬受抑制时, GFP-LC3弥散分布于细胞中, 且GFP-LC3带有绿色荧光。经不同浓度DON处理仔猪海马神经细胞后, 再用GFP-LC3转染细胞, 在荧光显微镜下观察绿色荧光蛋白的点状聚集情况。由图 5可见:对照组细胞内绿色荧光蛋白成弥散性分布, 随着DON浓度的增加, 细胞内绿色荧光蛋白开始出现点状分布, 且在DON为1 000 ng·mL-1时绿色荧光蛋白点状分布最明显。
|
图 5 荧光显微镜观察GFP-LC3蛋白的表达(×200) Fig. 5 Detection of the GFP-LC3 displayed in PHNC by fluorescence microscopy(×200) A—F分别表示DON处理质量浓度分别为0、125、250、500、1 000、2 000 ng·mL-1。 A-F represent DON concentrations are 0, 125, 250, 500, 1 000, 2 000 ng·mL-1, respectively. |
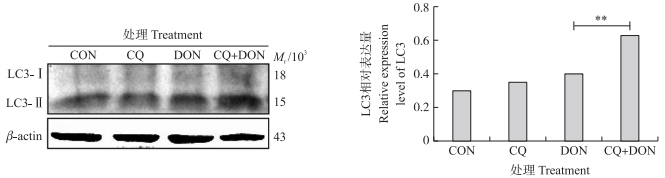
5 μmol·L-1 CQ和1 000 ng·mL-1 DON单独或联合处理细胞24 h, Western blot检测LC3表达结果如图 6所示:CQ和DON联合处理组与单独DON攻毒组相比, LC3-Ⅱ的表达量升高且差异极显著(P < 0.01)。
|
图 6 自噬抑制剂氯喹(CQ)对DON诱导仔猪海马神经细胞LC3蛋白表达的影响 Fig. 6 The effect of autophagy inhibitor chloroquine(CQ)on the expression of LC3 protein in PHNC induced by DON 1)CON:对照组Control group; CQ:5 μmol·L-1CQ; DON:1 000 ng·mL-1DON; CQ+DON:5 μmol·L-1CQ+1 000 ng·mL-1 DON。下同。The same as follows. 2)*, **分别表示与单独DON处理组相比差异显著(P < 0.05)和差异极显著(P < 0.01)。下同。 * and ** show significant difference(P < 0.05)and highly significant difference(P < 0.01)compared with separate DON treatment group, respectively. The same as follows. |
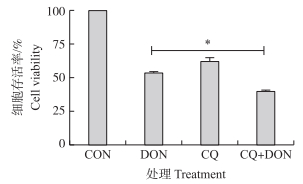
5 μmol·L-1 CQ和1 000 ng·mL-1 DON单独或联合处理细胞24 h, CCK-8法检测细胞存活率, 结果如图 7所示:CQ和DON联合处理组与单独DON攻毒组相比, 细胞存活率下降且差异显著(P < 0.05)。表明自噬水平的下降可显著降低细胞活性。
|
图 7 自噬抑制剂CQ对DON诱导仔猪海马神经细胞存活率的影响 Fig. 7 The effects of autophagy inhibitor CQ on cell viability in PHNC induced by DON |
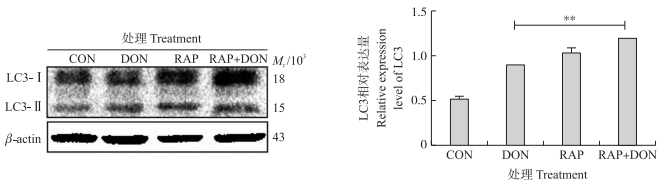
自噬激活剂雷帕霉素(RAP)50 nmol·L-1和1 000 ng·mL-1 DON单独或联合处理细胞24 h, Western blot检测LC3表达, 结果如图 8所示:RAP和DON联合处理组与单独DON攻毒组相比, LC3-Ⅱ的表达量升高且差异极显著(P < 0.01)。
|
图 8 自噬激活剂雷帕霉素(RAP)对DON诱导仔猪海马神经细胞LC3蛋白表达的影响 Fig. 8 The effect of autophagy inducer rapamycin(RAP)on the expression of LC3 protein in PHNC induced by DON CON:对照组Control group; DON:1 000 ng·mL-1 DON; RAP:50 nmol·L-1 RAP; RAP+DON:50 nmol·L-1 RAP+1 000 ng·mL-1 DON. |
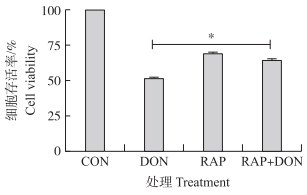
50 nmol·L-1 RAP和1 000 ng·mL-1 DON单独或联合处理细胞24 h, CCK-8法检测细胞存活率, 结果如图 9所示:RAP和DON联合处理组与单独DON攻毒组相比, 细胞活性显著上升(P < 0.05)。表明自噬水平的上升可显著提高细胞活性。
|
图 9 自噬激活剂RAP对DON诱导仔猪海马神经细胞存活率的影响 Fig. 9 The effects of autophagy inducer RAP on cell viability in PHNC induced by DON |
国内外有很多关于DON对动物脑、胃肠道、生殖以及免疫系统影响的报道, 已有研究证明, DON对原核细胞和真核细胞均具有显著的毒性作用[19]。Savard等[20]研究发现, DON能够通过血-脑屏障到达脑部, 通过刺激脑部不同区域导致脑组织异常, DON在较低的慢性剂量下会引起猪厌食, 在较高的急性剂量下会引起猪呕吐。陈晓芳等[21]研究报道, DON可通过引起线粒体功能障碍, 激活Caspases-3并调节Bcl-2家族基因, 从而诱导仔猪海马神经细胞凋亡。目前关于DON对猪的神经细胞毒性研究仍不深入, 故本试验选用DON最敏感实验动物仔猪的海马神经细胞作为研究对象, 探讨自噬在DON诱导神经细胞损伤中的作用。
自噬是所有真核生物正常发育所必需的一种降解过程, 可以消化有缺陷的细胞成分, 与细胞的生长、发育和死亡密切相关[22]。LC3有LC3-Ⅰ和LC3-Ⅱ两种存在形式, 在修饰过程中前体LC3先被ATG4切割, 形成可溶性的LC3-Ⅰ, 在酶的作用下与磷脂酰乙醇胺结合, 形成脂溶性的LC3-Ⅱ, 存在于自噬的各个阶段。当溶酶体与自噬小体发生融合, LC3-Ⅱ即被溶酶体中的水解酶降解, 因此, LC3-Ⅱ被认为是自噬体上的特异性标志分子[23]。Codogno等[24]研究指出, 自噬小体以及自噬溶酶体是评价自噬发生的重要指标。Han等[25]在研究DON致猪卵母细胞自噬和凋亡的试验中指出, 自噬泡和自噬小体越多, LC3表达越强。本试验结果发现, 高剂量的DON可引起细胞内自噬小体和自噬泡增加, 同时LC3-Ⅱ含量也明显增加, pEGFP-LC3质粒瞬时转染的结果进一步说明了高剂量的DON可引起细胞自噬水平上升, 多方面证明了DON可诱导仔猪海马神经细胞发生自噬, 这与上述的研究结果一致。
自噬可以清除受损的细胞器和代谢产物, 促进细胞生长繁殖, 维持细胞的稳态, 而过度的自噬会破坏细胞的稳态, 诱导细胞死亡[26]。Xia等[27]研究发现, 二氢青蒿素(DHM)诱导的自噬能抑制HepG2细胞的增殖, DHM呈剂量和时间依赖性的促进LC3-Ⅰ表达。司梦雪等[28]研究表明, 自噬能够延迟睾丸支持细胞(TM4)发生凋亡, 自噬在玉米赤霉烯酮(ZEA)对TM4细胞的毒性损伤中发挥保护作用。Zhang等[29]研究发现, 通过缺氧激活自噬诱导了肺动脉平滑肌细胞的增殖, 通过添加自噬抑制剂抑制自噬减少了细胞的增殖。而Yang等[30]的研究发现, 镉可引起肾小球系膜细胞内产生大量的ROS, 从而引起细胞自噬性死亡。为了研究自噬在DON诱导仔猪海马神经细胞损伤中的作用, 本试验通过加入自噬激活剂和自噬抑制剂来改变细胞自噬发生的水平, 从而探究自噬水平的高低对仔猪海马神经细胞存活率的影响。从本试验结果可以看出, CQ和DON联合处理组LC3-Ⅱ的表达量极显著高于单独DON攻毒组, 且联合处理组的细胞活性显著低于DON单独处理组细胞活性, 表明CQ成功阻断自噬体与溶酶体的结合, 致使LC3-Ⅱ大量堆积, 抑制DON诱导仔猪海马神经细胞发生自噬的过程, 即抑制自噬会降低细胞的存活率。RAP和DON联合处理组LC3-Ⅱ的表达量极显著高于单独DON攻毒组, 且细胞活性显著高于DON单独处理组细胞活性, 表明DON在诱导仔猪海马神经细胞产生自噬过程中, RAP可以使自噬表达水平上调, 即促进自噬可以提高细胞存活率。以上结果表明, 自噬可以降低DON对仔猪海马神经细胞的损伤作用, 对细胞起到一定的保护作用。
综上所述, DON可以引起仔猪海马神经细胞形态的改变, 诱导自噬小体和晚期自噬溶酶体增多, 高浓度的DON引起细胞明显的空泡化, 促进细胞自噬水平的上升; 同时研究证明激活自噬提高了细胞活性, 而抑制自噬降低了细胞活性, 表明自噬对DON诱导仔猪海马神经细胞损伤具有一定的保护作用。
| [1] |
Pantovic A, Krstic A, Janjetovic K, et al. Coordinated time-dependent modulation of AMPK/Akt/mTOR signaling and autophagy controls osteogenic differentiation of human mesenchymal stem cells[J]. Bone, 2013, 52(1): 524-531. DOI:10.1016/j.bone.2012.10.024 |
| [2] |
Kim Y C, Guan K L. mTOR:a pharmacologic target for autophagy regulation[J]. Journal of Clinical Investigation, 2015, 125(1): 25-32. |
| [3] |
Clark S L, Jr. Cellular differentiation in the kidneys of newborn mice studied with the electron microscope[J]. The Journal of Biophysical and Biochemical Cytology, 1957, 3(3): 349-362. DOI:10.1083/jcb.3.3.349 |
| [4] |
Yoshimori T. Autophagy:a regulated bulk degradation process inside cells[J]. Biochemical & Biophysical Research Communications, 2004, 313(2): 453-458. |
| [5] |
Nakatogawa H, Suzuki K, Kamada Y, et al. Dynamics and diversity in autophagy mechanisms:lessons from yeast[J]. Nature Reviews Molecular Cell Biology, 2009, 10(7): 458-467. |
| [6] |
Nakagawa I, Amano A, Mizushima N, et al. Autophagy defends cells against invading group A Streptococcus[J]. Science, 2004, 306(5698): 1037-1040. DOI:10.1126/science.1103966 |
| [7] |
Orvedahl A, Levine B. Autophagy in mammalian antiviral immunity[M]//Levine B, Yoshimori T, Deretic V. Current Topics in Microbiology and Immunology. Berlin: Springer, 2009: 267-285.
|
| [8] |
English L, Chemali M, Duron J, et al. Autophagy enhances the presentation of endogenous viral antigens on MHC class I molecules during HSV-1 infection[J]. Nature Immunology, 2009, 10(7): 480-487. |
| [9] |
Fimia G M, Stoykova A, Romagnoli A, et al. Ambra1 regulates autophagy and development of the nervous system[J]. Nature, 2007, 447(7148): 1121-1125. |
| [10] |
Singh R, Kaushik S, Wang Y, et al. Autophagy regulates lipid metabolism[J]. Nature, 2009, 458(7242): 1131-1135. DOI:10.1038/nature07976 |
| [11] |
谢俊泽, 杨小康, 严磊, 等. 自噬在镉致BRL3A细胞损伤中的保护作用[J]. 中国兽医学报, 2016, 36(11): 1899-1902. Xie J Z, Yang X K, Yan L, et al. Induction of cytoprotective autophagy in BRL3A cells by cadmium[J]. Journal of Chinese Veterinary Science, 2016, 36(11): 1899-1902 (in Chinese with English abstract). |
| [12] |
Ng S, Wu Y T, Chen B, et al. Impaired autophagy due to constitutive mTOR activation sensitizes TSC2-null cells to cell death under stress[J]. Autophagy, 2011, 7(10): 1173-1186. DOI:10.4161/auto.7.10.16681 |
| [13] |
Savard C, Nogues P, Boyer A, et al. Prevention of deoxynivalenol- and zearalenone-associated oxidative stress does not restore MA-10 Leydig cell functions[J]. Toxicology, 2016, 341/342/343: 17-27. |
| [14] |
Liu Y P, Lu Y, Wang L Y, et al. Occurrence of deoxynivalenol in wheat, Hebei Province, China[J]. Food Chemistry, 2016, 197: 1271-1274. DOI:10.1016/j.foodchem.2015.11.047 |
| [15] |
Park S H, Kim J, Kim D, et al. Mycotoxin detoxifiers attenuate deoxynivalenol-induced pro-inflammatory barrier insult in porcine enterocytes as an in vitro evaluation model of feed mycotoxin reduction[J]. Toxicology in Vitro, 2016, 38: 108-116. |
| [16] |
范梦雪, 陈晓芳, 姜云晶, 等. 脱氧雪腐镰刀菌烯醇对仔猪海马神经细胞的毒性作用[J]. 中国兽医科学, 2017, 47(1): 121-127. Fan M X, Chen X F, Jiang Y J, et al. Toxic effects of deoxynivalenol on hippocampal nerve cells of piglets[J]. Chinese Veterinary Science, 2017, 47(1): 121-127 (in Chinese with English abstract). |
| [17] |
耿芳芳, 许伟, 范梦雪, 等. 脱氧雪腐镰刀菌烯醇对雏鸡脂质过氧化反应及脑部形态结构的影响[J]. 南京农业大学学报, 2016, 39(3): 460-466. Geng F F, Xu W, Fan M X, et al. Effects of deoxynivalenol on lipid peroxidation reaction and brain morphology in chicken[J]. Journal of Nanjing Agricuitural University, 2016, 39(3): 460-466 (in Chinese with English abstract). DOI:10.7685/jnau.201510024 |
| [18] |
耿芳芳, 范梦雪, 姜云晶, 等. DON暴露对雏鸡神经递质及钙调蛋白含量的影响[J]. 西北农林科技大学学报(自然科学版), 2017, 45(2): 56-62. Geng F F, Fan M X, Jiang Y J, et al. Effects of deoxynivalenol exposure on neurotransmitter and calmodulin contents in chicken[J]. Journal of Northwest A & F University(Natural Science Edition), 2017, 45(2): 56-62 (in Chinese with English abstract). |
| [19] |
Bensassi F, Gallerne C, Dein O S E, et al. Involvement of mitochondria-mediated apoptosis in deoxynivalenol cytotoxicity[J]. Food and Chemical Toxicology, 2012, 50(5): 1680-1689. DOI:10.1016/j.fct.2012.01.015 |
| [20] |
Savard C, Pinilla V, Provost C, et al. In vitro, effect of deoxynivalenol(DON)mycotoxin on porcine reproductive and respiratory syndrome virus replication[J]. Food & Chemical Toxicology, 2014, 65(1): 219-226. |
| [21] |
陈晓芳, 张娅菲, 储小燕, 等. 脱氧雪腐镰刀菌烯醇对仔猪海马神经细胞凋亡及线粒体膜电位的影响[J]. 南京农业大学学报, 2018, 41(3): 526-533. Chen X F, Zhang Y F, Chu X Y, et al. Effects of deoxynivalenol on apoptosis and mitochondrial membrane potential in piglet hippocampal nerve cells[J]. Journal of Nanjing Agricuitural University, 2018, 41(3): 526-533 (in Chinese with English abstract). DOI:10.7685/jnau.201705035 |
| [22] |
Ganley I G, Lam D H, Wang J, et al. ULK1.ATG13.FIP200 complex mediates mTOR signaling and is essential for autophagy[J]. Journal of Biological Chemistry, 2009, 284(18): 12297-12305. DOI:10.1074/jbc.M900573200 |
| [23] |
Poornima P, Weng C F, Padma V V. Neferine from Nelumbo nucifera induces autophagy through the inhibition of PI3K/Akt/mTOR pathway and ROS hyper generation in A549 cells[J]. Food Chemistry, 2013, 141(4): 3598-3605. DOI:10.1016/j.foodchem.2013.05.138 |
| [24] |
Codogno P, Meijer A J. Autophagy and signaling:their role in cell survival and cell death[J]. Cell Death Differ, 2005, 12(2): 1509-1518. |
| [25] |
Han J, Wang Q C. Deoxynivalenol exposure induces autophagy/apoptosis and epigenetic modification changes during porcine oocyte maturation[J]. Toxicology and Applied Pharmacology, 2016, 300: 70-76. DOI:10.1016/j.taap.2016.03.006 |
| [26] |
Edinger A L, Thompson C B. Death by design:apoptosis, necrosis and autophagy[J]. Current Opinion in Cell Biology, 2004, 16(6): 663-669. DOI:10.1016/j.ceb.2004.09.011 |
| [27] |
Xia J, Guo S, Fang T, et al. Dihydromyricetin induces autophagy in HepG2 cells involved in inhibition of mTOR and regulating its upstream pathways[J]. Food & Chemical Toxicology, 2014, 66(4): 7-13. |
| [28] |
司梦雪, 王冰洁, 冯楠楠, 等. 自噬在玉米赤霉烯酮诱导TM4细胞凋亡中的作用[J]. 畜牧与兽医, 2018, 50(8): 104-109. Si M X, Wang B J, Feng N N, et al. Effect of autophagy on apoptosis induced by zearalenone in TM4 cells[J]. Animal Husbandry & Veterinary Medicine, 2018, 50(8): 104-109 (in Chinese with English abstract). |
| [29] |
Zhang H, Gong Y, Wang Z, et al. Apelin inhibits the proliferation and migration of rat PASMCs via the activation of PI3K/Akt/mTOR signal and the inhibition of autophagy under hypoxia[J]. Journal of Cellular & Molecular Medicine, 2014, 18(3): 542-553. |
| [30] |
Yang L Y, Wu K H, Chiu W T, et al. The cadmium-induced death of mesangial cells results in nephrotoxicity[J]. Autophagy, 2009, 5(4): 571-572. DOI:10.4161/auto.5.4.8311 |