文章信息
- 刘盼盼, 许苗苗, 祁文静, 陆兆新, 吕凤霞, 别小妹, 张充, 赵海珍
- LIU Panpan, XU Miaomiao, QI Wenjing, LU Zhaoxin, LÜ Fengxia, BIE Xiaomei, ZHANG Chong, ZHAO Haizhen
- 不同单硬脂酸甘油酯含量的大豆油油凝胶性能和微观结构分析
- Analysis of properties and micro-structure of soybean oil oleogels containing different 1-stearoyl-rac-glycerol contents
- 南京农业大学学报, 2018, 41(3): 547-554
- Journal of Nanjing Agricultural University, 2018, 41(3): 547-554.
- http://dx.doi.org/10.7685/jnau.201706046
-
文章历史
- 收稿日期: 2017-06-29
固体脂肪是涂抹脂、巧克力、生奶油、冰激凌及焙烤食品等的主要成分, 没有固体脂肪, 很多食品将不能成型。传统的固体脂肪为氢化植物油(例如植脂末、人造奶油和代可可脂)或者含高饱和脂肪酸的天然油脂。饱和脂肪、反式脂肪与动脉粥样硬化、胰岛素耐受性、炎症、氧化应激和肥胖等慢性疾病息息相关[1-2]。食品工业中需要一种能够取代饱和脂肪或反式脂肪的食品成分, 并要求这种成分不影响食品原有的风味、口感, 能够维持原有的被消费者所接受的感官特性。脂肪酸酯与脂肪酸、醇或其他脂肪酸酯通过酯交换过程形成另一种酯, 是形成类固态脂肪的有效方法, 但这其中涉及分子的化学修饰[3]。
油凝胶是由少量(一般≤10%)的单一凝胶因子或复合凝胶因子与液体植物油加热溶解后, 降低温度到凝胶点以下形成的具有三维网络结构的热可逆的类固体脂肪物质。这种软物质不仅具有固体脂肪的功能性质(提供食品独特的风味及口感, 尤其是塑性), 而且不改变液体植物油的健康及营养成分(如低饱和脂肪酸、高不饱和脂肪酸等特性)[4]。常见的凝胶因子有γ-谷维素、β-甾醇、多糖、乙基纤维素、蜡(如蜂蜡、米糠蜡和巴西棕榈蜡)等。
单硬脂酸甘油酯是食品中常用的乳化剂, 也可作为凝胶因子结构化液体植物油。Chen等[5]研究表明, 水能够通过水合甘油分子头部影响榛果油、己烷中单硬脂酸甘油酯的聚集和稳定性。Alfutimie等[6]研究了矿物油、棕榈油及橄榄油对甘油单硬脂酸酯、甘油单油酸酯混合物相态的影响, 在这3种溶剂中, 共有8种相态存在。Alfutimie等[7]研究水对甘油单硬脂酸酯、甘油单油酸酯混合物相态的影响, 结果表明在水中共有9种相态的存在。目前, 关于单硬脂酸甘油酯的含量对大豆油油凝胶的性能和微观结构的影响鲜有报道。本试验以大豆油为溶剂, 以6个不同含量的单硬脂酸甘油酯作为凝胶因子, 通过临界成胶含量、双折射现象、保油性、流变分析、热分析和傅里叶变换红外光谱分析对油凝胶的三维网络结构及凝胶机制进行探究, 为凝胶因子含量的选择及复配奠定基础。
1 材料与方法 1.1 试剂与仪器单硬脂酸甘油酯(> 90%)购自上海麦恪林生化科技有限公司; 大豆油(三级, 浸出, 非转基因)购自山东鲁花集团有限公司。
TMS PRO食品物性分析仪购自美国FTC公司; Physica MCR301流变仪购自奥地利Anton Paar公司; DSC8000差示扫描量热仪购自美国Perkin Elmer公司; Nicolet Is10傅里叶变换红外光谱仪购自美国Thermo Fisher公司; Nikon 80i正置显微镜购自日本Nikon公司。
1.2 试验方法根据所需单硬脂酸甘油酯的含量(单硬脂酸甘油酯与油凝胶的质量比), 分别准确称取一定质量的单硬脂酸甘油酯、大豆油(总质量为150 g)于250 mL的锥形瓶中, 于80 ℃的恒温水浴锅中搅拌均匀, 加热15 min, 即为油凝胶热溶液。其中, 单硬脂酸甘油酯含量分别为3%、5%、7%、9%、12%和15%(质量分数)。纯大豆油用0%表示, 纯单硬脂酸甘油酯用100%表示。
1.2.1 临界成胶含量分析将10 mL热溶液分装于玻璃试管中, 继续加热15 min。在室温20 ℃静置成胶12 h, 将试管倒置(倒置前不晃动或轻微晃动), 观察试管中单硬脂酸甘油酯、大豆油系统的流动性能, 系统不流动即视为凝胶[8]。
1.2.2 质构分析将50 mL热溶液分装于玻璃小烧杯中, 继续加热15 min。在室温20 ℃静置成胶12 h, 通过穿刺试验进行凝胶强度的测定。穿刺深度:15 mm; 穿刺速度:180 mm·min-1。以12.7 mm的圆柱形探头穿刺凝胶系统15 mm深度时的硬度为凝胶强度(N)[9]。
1.2.3 流变学分析将50 mL热溶液分装于玻璃小烧杯中, 继续加热15 min。在室温20 ℃静置成胶12 h后, 切取油凝胶并放置在流变仪的温控底盘上, 上盘与下盘的间隙为1 mm。
通过三剪切速率扫描对油凝胶系统进行流体类型的判定, 研究表观黏度及剪切应力随剪切速率的变化趋势。流体类型判定的程序为:第一剪切阶段0.01~150 s-1, 第二剪切阶段150~0.01 s-1, 第三剪切阶段0.01~150 s-1。
表观黏度随剪切速率的变化通过幂次定律[10]进行拟合:

|
(1) |
式中:η为表观黏度(Pa·s); κ为黏性常数或者稠度系数(Pa·sn); γ为剪切速率(s-1); n为流动特性指数或非牛顿指数。n-1=0时, 体系为牛顿流体; n-1 > 0时, 体系为剪切增稠流体; n-1 < 0时, 体系为剪切稀化流体。
通过应变扫描探究样本的线性黏弹性范围[11]。应变扫描程序:频率为1 Hz, 应变范围为0.01%~ 100%。
频率扫描程序:形变量为0.02%, 频率范围为1~100 Hz。
复合模量随频率的变化可通过幂次定律进行拟合[12]:

|
(2) |
式中:G*为复合模量(Pa); z为配位数(无量纲常数); A为凝胶强度或相互作用强度(Pa·s1/z), A值越大, 三维网络结构间的作用力越大; ω为频率(Hz)。
1.2.4 差示扫描量热分析将50 mL热溶液分装于玻璃小烧杯中, 继续加热15 min。在室温20 ℃静置成胶12 h, 分别称取5~7 mg油凝胶样本、大豆油和单硬脂酸甘油酯于铝制坩埚中。将锅底和锅盖压紧、严密密封后, 放样本槽中进行分析; 同时, 在基准室中放一个严密密封的铝制坩埚作为空白对照。对样本分析前, 用铟对差示扫描量热仪进行校正。温控程序为:从20 ℃升温至100 ℃, 降温至-20 ℃, 保持3 min, 再升温至100 ℃, 升温、降温速率皆为10 ℃·min-1。第一阶段升温为平衡样本[13]。
1.2.5 傅里叶变换红外光谱分析将50 mL热溶液分装于玻璃小烧杯中, 继续加热15 min。在室温20 ℃静置成胶12 h, 取适量大豆油、单硬脂酸甘油酯和油凝胶样本均匀平铺于衰减全反射附件表面(钻石窗口), 在20 ℃室温扫描获得红外光谱图。波数扫描范围为550~4 000 cm-1, 分辨率为4 cm-1, 扫描信号累加次数为32次。
1.2.6 偏振光显微镜分析将50 mL热溶液分装于玻璃小烧杯中, 继续加热15 min。取1滴油凝胶热溶液于载玻片中央, 用盖玻片轻轻压成均匀的薄片[14], 置于20 ℃的室温环境中静置成胶12 h, 进行观察。调节显微镜到暗场模式, 进行油凝胶的偏振光显微镜观察, 放大倍数为10。
1.2.7 持油性分析取8 mL热溶液于10 mL的离心管中, 继续加热15 min。将离心管在20 ℃的室温环境中静置成胶12 h, 进行离心, 离心后将离心管倒置约3 min, 沥干离心出来的油。离心参数:转速为9 000 r·min-1, 时间为15 min, 温度为20 ℃[15]。
不同单硬脂酸甘油酯含量的油凝胶持油性计算公式如下:

|
(3) |
式中:m1为离心管的质量(g); m2为离心管与油凝胶系统的质量(g); m3为离心后离心管与沉淀的质量(g); x为单硬脂酸甘油酯占油凝胶的质量分数。
1.3 数据分析使用Origin 8.0绘图及数据的拟合; SPSS 18.0进行单因素方差分析。数值以x±SD表示。
2 结果与分析 2.1 单硬脂酸甘油酯在大豆油中的临界成胶含量分析试验结果表明:倒置试管时, 单硬脂酸甘油酯含量为3%的凝胶系统具有一定的流动性; 单硬脂酸甘油酯含量为5%、7%、9%、12%和15%时, 凝胶系统不具有流动性, 凝胶性能良好。倒置时轻微晃动试管, 单硬脂酸甘油酯含量为3%和5%时, 系统具有一定流动性能; 单硬脂酸甘油酯含量为7%、9%、12%和15%时, 系统不具有流动性, 凝胶性能良好。因此, 单硬脂酸甘油酯在大豆油中的临界成胶含量为7%。
2.2 油凝胶的硬度分析单硬脂酸甘油酯含量为9%、12%和15%时, 油凝胶的凝胶强度分别为(0.13±0.01)N、(0.19±0.00)N和(1.03±0.09)N。单硬脂酸甘油酯含量为15%时, 凝胶硬度与9%和12%时的差异显著(P < 0.05)。单硬脂酸甘油酯含量为7%时, 探头所检测到的样本高度与样本的实际高度不一致, 测得的硬度值不作考虑。
2.3 油凝胶的流变学分析 2.3.1 流体类型由表 1可知:通过幂次定律拟合表观黏度随剪切速率的变化, 第一剪切阶段拟合系数为0.92~0.97, 第二、三剪切阶段拟合系数近似为1.00, 拟合效果较好; 由拟合公式得到n-1值, 单硬脂酸甘油酯含量为7%、9%、12%和15%时, 油凝胶体系均符合n-1 < 0, 为非牛顿流体中的剪切稀化流体。
| 单硬脂酸甘油酯含量/% 1-stearoyl-rac-glycerol content |
黏性常数/(Pa·sn) Consistency index | n-1 | 拟合系 Fitting coefficient | |||||
| 1 | 2, 3 | 1 | 2, 3 | 1 | 2, 3 | |||
| 7 | 198.92±12.65 | 18.11±0.73 | -0.55±0.01 | -0.96±0.01 | 0.92±0.01 | 1.00±0.00 | ||
| 9 | 254.84±9.19 | 26.64±0.76 | -0.61±0.02 | -0.99±0.01 | 0.94±0.00 | 1.00±0.00 | ||
| 12 | 405.89±45.94 | 56.65±5.60 | -0.68±0.02 | -0.99±0.01 | 0.96±0.00 | 1.00±0.00 | ||
| 15 | 580.99±140.23 | 69.73±7.12 | -0.63±0.08 | -0.83±0.02 | 0.97±0.01 | 1.00±0.00 | ||
| 注: 1:第一剪切阶段The first shear stage; 2, 3:第二、三剪切阶段The second and third shear stages; n:流动特性指数Flow behavior index. | ||||||||
由图 1可见:在第一剪切阶段, 油凝胶的应力值陡然增加, 油凝胶系统结构遭到破坏; 在第二、三剪切阶段, 油凝胶系统结构没有明显的破坏, 且剪切速率降低及增加过程中, 剪切应力出现滞回曲线, 表明油凝胶系统为触变性流体; 单硬脂酸甘油酯含量为15%时, 油凝胶的应力曲线与7%、9%和12%明显不同, 且其出现触变性的剪切速率在10 s-1之前, 这可能归因于油凝胶更具有刚性的三维网络结构。
随着单硬脂酸甘油酯含量增加, 油凝胶系统的复合模量增加, 凝胶强度增强[16]。由图 2可见:单硬脂酸甘油酯的含量为7%、9%、12%和15%时, 油凝胶的线性黏弹性范围分别为0.010%~0.048%、0.010%~0.082%、0.010%~0.028%及0.010%~0.027%;单硬脂酸甘油酯含量为7%、9%时, 线性黏弹性范围逐渐增大, 可能归因于三维网络结构柔性的增加; 单硬脂酸甘油酯含量为12%、15%时, 线性黏弹性范围逐渐降低, 可能归因于三维网络结构刚性的增强。

|
图 2 不同单硬脂酸甘油酯含量对油凝胶线性黏弹性范围的影响 Figure 2 Effects of different 1-stearoyl-rac-glycerol contents on linear viscoelastic range of oleogels |
由应变扫描可知, 形变量为0.02%, 单硬脂酸甘油酯含量为7%、9%、12%和15%时, 油凝胶系统处于线性黏弹性范围。因此选用0.02%的形变量进行频率扫描。
由表 2可见:通过幂次定律拟合复合模量随频率的变化, 拟合系数为0.92~0.98, 拟合效果良好; 凝胶因子含量增加, 凝胶强度增加, 配位数增大。
| 单硬脂酸甘油酯含量/% 1-stearoyl-rac-glycerol content |
凝胶强度/(Pa·s1/z) Gel strength |
配位数 Coordination number |
拟合系数 Fitting coefficient |
| 7 | 1 413.27±186.70 | 3.32±0.11 | 0.92±0.02 |
| 9 | 2 355.32±174.81 | 4.03±0.33 | 0.95±0.02 |
| 12 | 7 389.77±160.38 | 6.91±0.58 | 0.97±0.02 |
| 15 | 563 123.20±29 249.31 | 9.44±0.10 | 0.98±0.01 |
由表 3和图 3可见:纯单硬脂酸甘油酯有2个结晶峰和2个融解峰; 纯大豆油的相转变温度低于0 ℃; 油凝胶在0 ℃以上, 有与单硬脂酸甘油酯相对应的2个结晶峰和2个融解峰, 在0 ℃以下, 有与大豆油相对应的相转变温度; 单硬脂酸甘油酯含量为7%时, 较高融解峰相转变温度较低, 其他单硬脂酸甘油酯含量对油凝胶的相转变温度并没有显著影响。
| 单硬脂酸甘油酯含量/% 1-stearoyl-rac-glycerol content |
T1/℃ | T2/℃ | T3/℃ | T4/℃ |
| 7 | 49.54±0.34b | 9.52±0.01b | 12.30±0.18b | 52.80±0.71c |
| 9 | 51.11±1.21b | 9.28±0.11b | 11.96±0.10b | 54.63±0.69bc |
| 12 | 51.50±1.39b | 9.02±0.18b | 11.50±0.37b | 55.99±0.68b |
| 15 | 52.06±0.11b | 8.64±0.01b | 11.46±0.02b | 56.54±0.18b |
| 100 | 60.70±0.43a | 10.58±0.47a | 13.86±0.30a | 65.85±0.19a |
| 注: 1) T1:较高结晶峰温度Higher peak temperature of crystallization; T2:较低结晶峰温度Lower peak temperature of crystallization; T3:较低融解峰温度Lower peak temperature of melting; T4:较高融解峰温度Higher peak temperature of melting. 2)不同小写字母表示处理间差异显著(P < 0.05)。下同。Different lowercase letters indicate significant difference among treatments at 0.05 level. The same as follows. | ||||

|
图 3 大豆油、单硬脂酸甘油酯和油凝胶的相转变 Figure 3 Phase transition of soybean oil, 1-stearoyl-rac-glycerol and oleogels a, b:大豆油的相转变Phase transition of soybean oil. 0%表示大豆油0% represents soybean oil; 100%表示单硬脂酸甘油酯100% represents 1-stearoyl-rac-glycerol.下同。The same as follows. |
由图 4可以看出:波数为2 923~2 849 cm-1时为亚甲基的不对称、对称伸缩振动峰; 波数为1 743~1 736 cm-1时为酯键羰基基团的强吸收带; 波数为1 470~1 464 cm-1时为亚甲基的弯曲振动峰; 波数为1 177~1 160 cm-1时为酯基中碳氧单键的伸缩振动峰; 波数为722~719 cm-1时为长链烷基的面内摇摆振动峰, 这与前人[17-19]的研究结果一致。大豆油和油凝胶中波数为3 009~3 008 cm-1的峰为不饱和脂肪酸的顺式碳碳双键的弱强度伸缩振动峰。单硬脂酸甘油酯为3 296 cm-1的峰为单硬脂酸甘油酯甘油分子头部—OH伸缩振动吸收峰; 油凝胶为3 355~3 334 cm-1的峰为—OH伸缩振动吸收峰。

|
图 4 大豆油、单硬脂酸甘油酯和油凝胶的傅里叶变换红外谱图 Figure 4 Fourier transform infrared spectrum analysis of soybean oil, 1-stearoyl-rac-glycerol and oleogels |
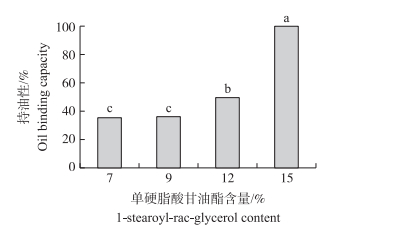
由图 5可见:凝胶因子含量增加, 双折射现象增强。随着单硬脂酸甘油酯含量增加, 离心时油凝胶三维网络结构的持油能力增强(图 6)。单硬脂酸甘油酯含量为15%时, 油凝胶三维网络结构的持油性高达99.84%, 持油性最好(P < 0.05)。这与前面的频率扫描、偏振光显微观察的结果相吻合。

|
图 5 不同单硬脂酸甘油酯含量(7%、9%、12%、15%)对油凝胶双折射现象的影响 Figure 5 Effects of different 1-stearoyl-rac-glycerol contents(7%, 9%, 12%, 15%)on the birefringence phenomenon of oleogels |
|
图 6 不同单硬脂酸甘油酯含量对油凝胶持油性的影响 Figure 6 Effects of different 1-stearoyl-rac-glycerol contents on oil binding capacity of oleogels |
本试验表明, 倒置试管, 单硬脂酸甘油酯含量为5%时成胶, 这与在榛果油[20]中的成胶含量一致; 倒置并晃动试管, 单硬脂酸甘油酯含量为7%时成胶, 单硬脂酸甘油酯在大豆油中的临界成胶含量为7%。单硬脂酸甘油酯含量增加, 油凝胶的硬度增大, 表观黏度增大, 凝胶强度增加, 配位数增大; 双折射现象更为明显; 持油性增强。这归因于凝胶因子含量足够大时, 凝胶因子间形成连续的网络结构, 凝胶因子含量继续增加, 连续网络结构的结合区数量增加[9]。纯单硬脂酸甘油酯的较低温度峰为固态的亚阿尔法相(sub-alpha phase)与反向层状相的转变, 较高温度峰为反向层状相与液态的各向同性相的转变[13, 21]; 大豆油的相转变温度与Calligaris等[22]研究的葵花籽油的相转变温度(-11.5 ℃、-6.8 ℃)较相似, 可能归因于大豆油和葵花籽油相似的脂肪酸组成, 尤其是都含有较高的亚油酸含量; 单硬脂酸甘油酯的含量不影响油凝胶的热可逆性, 对油凝胶的相转变温度也没有显著影响; 与纯单硬脂酸甘油酯的相转变温度相比, 油凝胶的相转变温度较低, 这可能归因于单硬脂酸甘油酯含量降低即大豆油含量增加、体积分数增加, 从而引起的稀释效应[23]; 过冷导致油凝胶的融解峰总是在结晶峰的右侧; 晶体中, 更为柔性的链构象向更为刚性的链构象转变导致熵值增大, 从而导致更低的融解峰温度[23], 这可能导致了单硬脂酸甘油酯存在2个融解峰和2个结晶峰。油凝胶在3 355~3 334 cm-1出现3—OH氢键的伸缩振动峰[21, 24-25], 大豆油在相应的波数范围内并没有出现吸收峰, 表明油凝胶主要是通过单硬脂酸甘油酯形成的分子间氢键物理性地缠绕大豆油于三维网络结构中, 形成半固态、固态脂肪替代物。因此, 可通过改变单硬脂酸甘油酯的含量调整油凝胶的理化性质和微观结构。另外, 添加助表面活性剂、复配凝胶因子、改变溶剂类型等也可以调整油凝胶的理化性质和微观结构, 目前本研究室正在开展相关的研究。
| [1] | Monguchi T, Hara T, Hasokawa M, et al. Excessive intake of trans fatty acid accelerates atherosclerosis through promoting inflammation and oxidative stress in a mouse model of hyperlipidemia[J]. Journal of Cardiology, 2017, 70(2): 121-127. DOI: 10.1016/j.jjcc.2016.12.012 |
| [2] | Zhao X N, Shen C, Zhu H, et al. Trans-fatty acids aggravate obesity, insulin resistance and hepatic steatosis in C57BL/6 mice, possibly by suppressing the IRS1 dependent pathway[J]. Molecules, 2016, 21(6): 705. DOI: 10.3390/molecules21060705 |
| [3] |
张超然, 王胜男, 齐宝坤, 等. 酶法酯交换与化学法酯交换技术制备塑性脂肪及其物理性质对比研究[J].
粮食与油脂, 2014, 27(11): 25-29.
Zhang C R, Wang S N, Qi B K, et al. Enzymatic and chemical interesterification to produce plastic fats and comparison of the physical properties[J]. Cereals and Oils, 2014, 27(11): 25-29. DOI: 10.3969/j.issn.1008-9578.2014.11.007 (in Chinese with English abstract) |
| [4] | Mert B, Demirkesen I. Reducing saturated fat with oleogel/shortening blends in a baked product[J]. Food Chemistry, 2016, 199: 809-816. DOI: 10.1016/j.foodchem.2015.12.087 |
| [5] | Chen C H, Terentjev E M. Effects of water on aggregation and stability of monoglycerides in hydrophobic solutions[J]. Langmuir, 2010, 26(5): 3095-3105. DOI: 10.1021/la904139b |
| [6] | Alfutimie A, Curtis R, Tiddy G J T. The phase behaviour of mixed saturated and unsaturated monoglycerides in hydrophobic system[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2015, 482: 329-337. |
| [7] | Alfutimie A, Curtis R, Tiddy G J T. The phase behaviour of mixed saturated and unsaturated monoglycerides in water system[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2015, 465: 99-105. |
| [8] |
曹礼华, 张东娟, 陈辉, 等. 乳酸环丙沙星温度敏感型原位凝胶的制备及其体外释药评价[J].
南京农业大学学报, 2013, 36(2): 125-131.
Cao L H, Zhang D J, Chen H, et al. Preparation of the ciprofloxacin lactate thermosensitive in situ gel and its drug releasing performance in vitro[J]. Journal of Nanjing Agricultural University, 2013, 36(2): 125-131. DOI: 10.7685/j.issn.1000-2030.2013.02.021 (in Chinese with English abstract) |
| [9] | Almeida I F, Bahia M F. Comparison of the mechanical properties of two oleogels[EB/OL]. [2017-06-25]. https://www.researchgate.net/publication/228838214. |
| [10] |
王晨, 李晓瑞, 沈一丁, 等. 离子型表面活性剂与疏水缔合聚丙烯酰胺的相互作用[J].
功能材料, 2012, 43(23): 3316-3321.
Wang C, Li X R, Shen Y D, et al. Interactions between ionic surfactants and hydrophobically associating polyacrylamide in aqueous solution[J]. Journal of Functional Materials, 2012, 43(23): 3316-3321. DOI: 10.3969/j.issn.1001-9731.2012.23.032 (in Chinese with English abstract) |
| [11] | Alfonso J E M, Valencia C. Linear and nonlinear viscoelasticity of oleogels based on vegetable oil and ethylene vinyl acetate copolymer/isotactic polypropylene blends[J]. Journal of Applied Polymer Science, 2015, 132(34): 42477. |
| [12] | Gabriele D, Cindio B D, Antona P D. A weak gel model for foods[J]. Rheologica Acta, 2001, 40(2): 120-127. DOI: 10.1007/s003970000139 |
| [13] | Chen C H, van Damme I, Terentjev E M. Phase behavior of C18 monoglyceride in hydrophobic solutions[J]. Soft Matter, 2009, 5: 432-439. DOI: 10.1039/B813216J |
| [14] | Uvanesh K, Sagiri S S, Senthilguru K, et al. Effect of span 60 on the microstructure, crystallization kinetics, and mechanical properties of stearic acid oleogels:an in-depth analysis[J]. Journal of Food Science, 2016, 81(2): E380-E387. DOI: 10.1111/jfds.2016.81.issue-2 |
| [15] | Öǧütcü M, Yılmaz E. Oleogels of virgin olive oil with carnauba wax and monoglyceride as spreadable products[J]. Grasas Aceites, 2014, 65(3): 1-11. |
| [16] |
吴菊清, 魏朝贵, 韩敏义, 等. NaCl对猪肉肌原纤维蛋白乳化体系加工特性的影响[J].
南京农业大学学报, 2014, 37(6): 83-88.
Wu J Q, Wei C G, Han M Y, et al. Effect of NaCl on processing properties of pork myofibrillar protein emulsion[J]. Journal of Nanjing Agricultural University, 2014, 37(6): 83-88. DOI: 10.7685/j.issn.1000-2030.2014.06.012 (in Chinese with English abstract) |
| [17] |
刘玲玲, 武彦文, 张旭, 等. 傅里叶变换红外光谱结合模式识别法快速鉴别食用油的真伪[J].
化学学报, 2012, 70(8): 995-1000.
Liu L L, Wu Y W, Zhang X, et al. Application of fourier transform infrared spectroscopy combined with pattern recognition method for rapid authentication of edible oil[J]. Acta Chimica Sinica, 2012, 70(8): 995-1000. (in Chinese with English abstract) |
| [18] |
周玲玲, 姚志湘, 粟晖, 等. ATR/FTIR法检测植物油的品质指标[J].
中国油脂, 2016, 41(4): 96-99.
Zhou L L, Yao Z X, Su H, et al. Determination of quality indicators of vegetable oil by ATR/FTIR[J]. China Oils and Fats, 2016, 41(4): 96-99. (in Chinese with English abstract) |
| [19] |
杨本志, 潘秋月, 潘丹杰, 等. 利用FTIR/ATR快速测定大豆油的过氧化值[J].
中国粮油学报, 2013, 28(4): 108-112.
Yang B Z, Pan Q Y, Pan D J, et al. Rapid determination of soybean oil peroxide value by FTIR/ATR[J]. Journal of the Chinese Cereals and Oils Association, 2013, 28(4): 108-112. (in Chinese with English abstract) |
| [20] | Yılmaz E, ÖAǧütcü M. Properties and stability of hazelnut oil organogels with beeswax and monoglyceride[J]. Journal of the American Oil Chemists Society, 2014, 91(6): 1007-1017. DOI: 10.1007/s11746-014-2434-1 |
| [21] | Chen C H, Terentjev E M. Aging and metastability of monoglycerides in hydrophobic solutions[J]. Langmuir, 2009, 25(12): 6717-6724. DOI: 10.1021/la9002065 |
| [22] | Calligaris S, Arrighetti G, Barba L, et al. Phase transition of sunflower oil as affected by the oxidation level[J]. Journal of the American Oil Chemists Society, 2008, 85(7): 591-598. DOI: 10.1007/s11746-008-1241-y |
| [23] | Muthukumar M. Nucleation in polymer crystallization[J]. Advances in Chemical Physics, 2004, 128: 1-63. |
| [24] |
严红梅, 蒋艳荣, 唐欢, 等. 复合辅料微晶纤维素-单硬脂酸甘油酯的研究[J].
中草药, 2014, 45(9): 1245-1251.
Yan H M, Jiang Y R, Tang H, et al. Study on co-processd excipient of microcrystalline cellulose and glycerol monostearate[J]. Chinese Traditional and Herbal Drugs, 2014, 45(9): 1245-1251. DOI: 10.7501/j.issn.0253-2670.2014.09.009 (in Chinese with English abstract) |
| [25] | Zhao W J, Li Y Y, Sun T, et al. Heat-set supramolecular organogels composed of β-cyclodextrin and substituted aniline in N, N-dimethylformamide[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2011, 374(1/2/3): 115-120. |





