文章信息
- 王华夏, 顾峰, 廖瑛, 茅翔, 丁铲, 范红结
- WANG Huaxia, GU Feng, LIAO Ying, MAO Xiang, DING Chan, FAN Hongjie
- 新城疫病毒感染通过蛋白激酶激活NF-κB信号通路诱导干扰素和炎症因子的表达
- NDV activates NF-κB pathway through PKR to induce the expression of IFN-β and inflammatory factor
- 南京农业大学学报, 2017, 40(3): 488-493
- Journal of Nanjing Agricultural University, 2017, 40(3): 488-493.
- http://dx.doi.org/10.7685/jnau.201611038
-
文章历史
- 收稿日期: 2016-11-30
2. 中国农业科学院上海兽医研究所, 上海 200241
2. Shanghai Veterinary Research Institute, Chinese Academy of Agricultural Sciences, Shanghai 200241, China
新城疫是由新城疫病毒(Newcastle disease virus, NDV)引起的急性、高度传染性的烈性动物传染病, 严重危害养禽业, 被世界卫生组织(OIE)规定为必须通报传染病。在病毒感染家禽过程中, 由于溶血、合胞体形成和细胞死亡, 引起严重的组织损伤, 发生全身出血性病变, 导致家禽死亡。通常在烈性病毒感染过程中, 体液中的多种细胞因子水平如TNFα、IL-1、IL-6、IL-8、IFN-α、IFN-β、IFN-γ等升高, 诱导抗病毒蛋白的表达, 及免疫细胞吞噬受感染细胞, 从而启动获得性免疫。当过量细胞因子产生形成细胞因子风暴时, 又可引起组织器官免疫性损伤和病毒血症。已有研究证明, NDV感染能诱导大量干扰素和细胞因子的表达[2-4]。
NDV属于单股负链RNA病毒[5], 复制过程中会产生双链RNA(dsRNA)。dsRNA激活的蛋白激酶(PKR)能够识别和结合病毒dsRNA, 自我磷酸化激活, 通过磷酸化真核翻译起始因子(eukaryotic initiation factor 2α, eIF2α)关闭蛋白翻译[6], 或者通过激活NF-κB信号通路, 诱导干扰素和细胞因子的表达, 发挥抗病毒效应[7-8]。在正常状态下, 抑制性κB(IκB)与NF-κB的结合, 使NF-κB以非活化的形式存在于胞浆中。当细胞受到感染或其他刺激时, IκB激酶(IKK)复合体被激活, 进而磷酸化IκB, 引起IκB多聚泛素化并被运输到蛋白酶体降解, NF-κB被释放并进入细胞核, 调控细胞因子的转录。PKR缺失时, dsRNA刺激不能够引起IKK激酶复合体的活化, 说明IKK激酶活性依赖于PKR的活化[9-12]。另外, 有文献报道, PKR通过磷酸化IκB, 激活NF-κB通路[13]。已有报道表明, NDV感染可激活PKR, 并诱导干扰素和细胞因子的大量表达[14]。本文旨在揭示NDV感染过程中诱导细胞因子表达的信号途径。
1 材料与方法 1.1 试验材料 1.1.1 毒株和细胞NDV参考强毒株Herts/33, 购自中国兽药监察所; 人宫颈癌细胞HeLa系购自于美国组织培养物细胞库(ATCC)。
1.1.2 抗体和主要试剂Phospho-PKR单克隆抗体(ab32036) 购自Abcam公司, Histone多克隆抗体(17168-1-AP)购自武汉三鹰生物技术有限公司。PKR单克隆抗体(12297s)、phospho-IκBα(2859s)、IκBα(4814P)单克隆抗体均购自Cell Signaling Technology公司。HRP标记的山羊抗鼠、山羊抗兔IgG购自Jackson公司; NDV NP抗体由上海兽医研究所丁铲实验室制备。DMEM培养基购自Hyclone公司; FBS购自Gibco公司; SYBR Green QPCR Mix购自东盛生物公司; ECL化学发光试剂盒购自Thermo公司。异硫氰酸荧光素(FITC)标记的山羊抗兔IgG、四乙基若丹明异硫氰酸盐标记的山羊抗鼠IgG购自Sigma公司。2-氨基嘌呤(2-aminopurine, 2-AP)(207-197-4) 购自Sigma-Aldrich公司, IKK16(S2882) 购自Selleck公司。细胞核蛋白与细胞浆蛋白抽提试剂盒(P0028) 购自碧云天生物技术有限公司。其他试剂均为分析纯级。
1.1.3 主要仪器高速台式冷冻离心机5804R(德国Eppendorf公司); 细胞培养箱(美国Thermo公司); BIO-RAD3000X1型电泳仪(美国BIO-RAD公司); 倒置荧光显微镜(日本尼康公司); 全自动化学发光图像分析系统(Tanon 5200, 上海天能科技有限公司)。
1.2 试验方法 1.2.1 引物设计参照GenBank中人的IFN-β、IL-6、IL-8基因序列设计3对引物并由上海生工生物工程有限公司合成。引物序列见表 1。
| 引物对名称Primer pairs names | 引物对序列Primer pairs sequences |
| IFN-β-F/R | 5′-GCTTGGATTCCTACAAAGAAGCA-3′/5′-ATAGATGGTCAATGCGGCGTC-3′ |
| IL-6-F/R | 5′-ACTCACCTCTTCAGAACGAATTG-3′/5′-CCATCTTTGGAAGGTTCAGGTTG-3′ |
| IL-8-F/R | 5′-TTTTGCCAAGAAGTGCTAAAGA-3/5′-AACCCTCTGCACCCAGTTTTC-3′ |
| β-actin-F/R | 5′-GATCTGGCACCACACCTTCT-3′/5′-GGGGTGTTGAAGGTCTCAAA-3′ |
5×105 mL-1 HeLa细胞培养于6孔板(Thermo公司), 用TCID50为109.85 mL-1和1 MOI(multiplicity of infection, 感染复数)的NDV感染细胞后, 分别取0、4、8、16和20 h的细胞, 提取RNA, 反转录为cDNA后置-80 ℃保存。qPCR检测采用SYBR GreenⅠ染料法进行测定, 配制PCR体系:1 μL cDNA, 上、下游引物各1 μL, 12.5 μL SYBR Green qPCR Master Mix, 9.5 μL双蒸水。PCR反应程序:94 ℃预变性2 min, 94 ℃变性15 s, 55 ℃退火30 s, 72 ℃延伸30 s, 40个循环。通过熔解曲线分析, 用2-ΔΔCT法计算相对表达量。
1.2.3 Western blot分析HeLa细胞培养于6孔板, 分别于NDV感染后0、4、8、12、16、20和24 h, 去除培养液, 以PBS洗细胞3次, 加入200 μL 1×蛋白上样缓冲液裂解细胞。吸取细胞裂解液到Eppendorf管, 煮沸10 min, 充分裂解细胞和变性蛋白, 以12 000 r · min-1离心5 min, 变性蛋白用于SDS-PAGE电泳。进行湿法转印 (250 mA 1.5 h)。完成后用含50 g · L-1脱脂乳的TBST室温封闭硝酸纤维素膜1 h, 4 ℃孵育一抗过夜, TBST漂洗3次。将HRP标记的二抗以1:3 000的比例稀释到含50 g · L-1脱脂乳的TBST, 与硝酸纤维素膜一起室温孵育1 h, TBST漂洗3次。使用Supersignal West Pico Chemiluminescent Substrates试剂盒, 在全自动化学发光图像分析系统上显色。
1.2.4 间接免疫荧光(IFA)检测p65入核情况载玻片内置于6孔板内, HeLa细胞培养于盖玻片上。NDV感染16 h后用体积分数为4%的多聚甲醛室温固定、0.5% Triton-100透化各10 min, 30 g · L-1 BSA封闭30 min, 然后进行一抗与荧光二抗的孵育, 细胞核染色, 最后载玻片上加抗荧光猝灭封片剂封片, 避光风干3 h。激光共聚焦显微镜(Nikon C1Si)观察, 拍照。
1.2.5 抑制剂处理5×105 mL-1 HeLa细胞培养于6孔板, 用TCID50为109.85 mL-1和1 MOI的NDV感染细胞, 1 h后换液, 分别加入终浓度为5 μmol · L-1的IKK16、10 mg · mL-1的2-AP, 16 h后处理细胞用于RT-PCR、Western blot检测和间接免疫荧光反应。
1.2.6 细胞核与细胞浆蛋白分离检测p65入核HeLa细胞培养于6孔板, NDV感染16 h后取细胞, PBS洗1次, 刮细胞, 吸弃上清液, 留下沉淀。加入添加苯甲基磺酰氟(PMSF)的细胞浆蛋白抽提试剂, 抽提得到细胞浆蛋白; 再对沉淀加入添加PMSF的细胞核蛋白抽提试剂, 抽提得到细胞核蛋白。可以立即使用, 也可以-70 ℃冻存。再将样品煮沸变性, 用Western blot检测p65在细胞核和细胞质的分配。
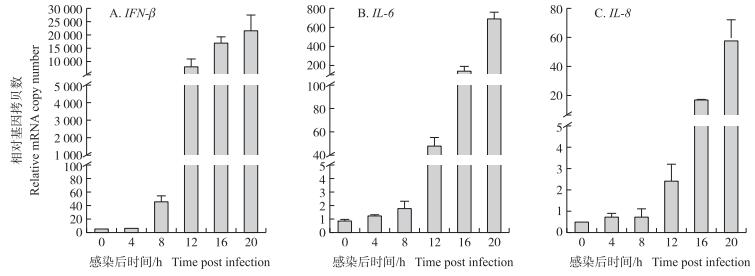
2 结果与分析 2.1 NDV感染对IFN-β、IL-6、IL-8表达的影响分别收集未被感染和1 MOI NDV Herts/33感染0、4、8、12、16、20 h的HeLa细胞, RT-PCR检测IFN-β、IL-6、IL-8 mRNA水平变化。由图 1可见:IFN-β在感染后8 h表达显著上调, 感染后16 h上调表达7 000倍, 感染后20 h上调表达接近20 000倍(图 1-A)。IL-6和IL-8 mRNA也随着感染时间的延长而上调表达, 在感染后20 h分别上调表达856倍和57倍(图 1-B, C)。说明NDV感染HeLa细胞后能够诱导干扰素和细胞因子的显著表达。
|
图 1 NDV感染诱导干扰素和细胞因子基因的表达 Figure 1 Up-regulation of IFN and cytokines expression at different time point during NDV infection |
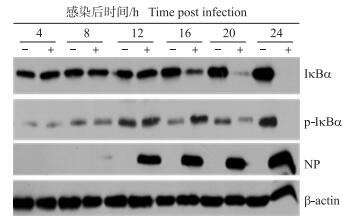
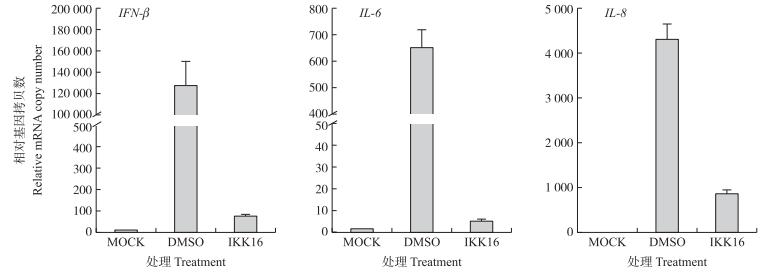
1 MOI Herts/33感染HeLa细胞, 分别于感染后0、4、8、12、16、20和24 h检测NF-κB的激活情况。图 2显示:NDV感染后16 h, IκB发生磷酸化降解; 感染后20和24 h, 几乎检测不到IκB, 说明NDV能通过IκB磷酸化激活NF-κB。RT-PCR结果显示:在NDV感染后16 h, 用5 μmol · L-1 IKK16抑制IKK激酶复合体的活性, 进而抑制NF-κB通路的激活, IFN-β、IL-6、IL-8 mRNA表达显著下降(图 3)。以上结果说明NDV感染通过激活NF-κB通路来诱导IFN-β、IL-6、IL-8的表达。
|
图 2 NDV感染后不同时间IκBα磷酸化和降解情况 Figure 2 Phosphorylation and degradation of IκBα at different time during NDV infection -, +:未感染组和感染组Uninfection and infection:IκBα:NF-κB抑制蛋白NF-κB inhibitory protein; p-IκBα:磷酸化IκBα Phosphorylation of IκBα; NP:NDV核衣壳蛋白Nucleocapsid protein of NDV |
|
图 3 IKK16阻断NFκB信号通路后对干扰素和细胞因子基因表达影响 Figure 3 Influence of IFN and cytokine expression by pharmacological inhibition of NFκB with IKK16 MOCK:未感染NDV Uninfection; DMSO:感染NDV并加DMSO Infection and DMSO; IKK16:感染NDV并加IKK16 Infection and IKK16 |
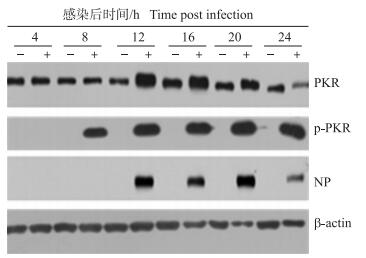
NDV增殖的过程中会产生dsRNA, 胞浆中的PKR能够识别并结合dsRNA, 进而被激活。以1 MOI Herts/33感染HeLa细胞, 分别于感染后4、8、12、16、20和24 h裂解细胞, Western blot检测PKR的表达水平和磷酸化水平。从图 4可看到:感染后12~20 h, PKR被诱导表达并被磷酸化激活。感染后24 h, 由于细胞开始死亡, 总PKR和磷酸化PKR略有减少。说明NDV感染HeLa细胞, PKR可被诱导表达并被磷酸化激活。
|
图 4 NDV感染后不同时间PKR的诱导表达和磷酸化激活 Figure 4 Up-regulation of PKR and phosphorylation of PKR at different time during NDV infection -, +:未接毒组和接毒组Uninfection and infection; PKR:蛋白激酶Protein kinase; p-PKR:磷酸化PKR Phosphorylation of PKR; NP:NDV核衣壳蛋白Nucleocapsid protein of NDV |
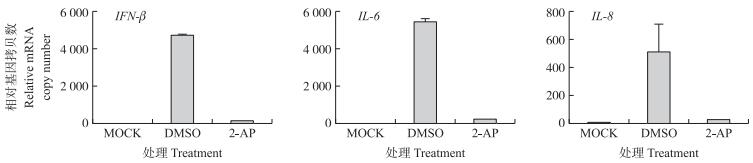
2-氨基嘌呤 (2-AP) 是PKR活性抑制剂。在NDV感染后使用10 mg · mL-1的2-AP抑制PKR的酶活性, 感染后16 h裂解细胞, 用RT-PCR检测IFN-β、IL-6、IL-8 mRNA的转录水平。图 5显示, 2-AP强烈抑制了IFN-β、IL-6、IL-8的转录。以上结果说明NDV可激活PKR并介导干扰素和细胞因子的表达。
|
图 5 用2-氨基嘌呤 (2-AP) 抑制PKR活性后对干扰素和细胞因子表达的影响 Figure 5 Influence of IFN and cytokine expression by pharmacological inhibition of PKR activity with 2-aminopurine (2-AP) MOCK:未感染NDV Uninfection; DMSO:感染NDV并加DMSO Infection and DMSO; 2-AP:感染NDV并加2-AP Infection and 2-AP |
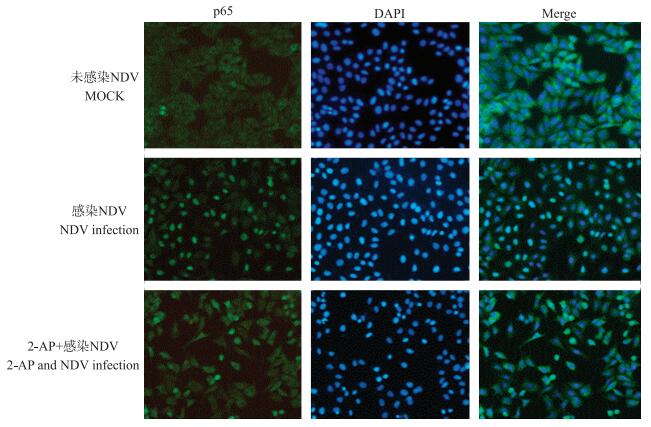
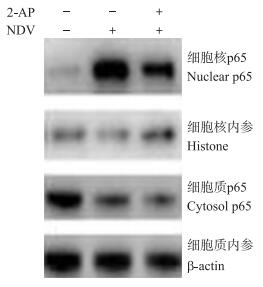
以上结果表明, 在NDV感染过程中, PKR和NF-кB先后被激活, 进而介导干扰素和细胞因子的表达。PKR是否传递信号进而激活NF-кB, 需要进一步证实。对NF-кB (p65) 的免疫荧光定位结果显示:在NDV感染过程中, p65进入细胞核; 使用10 mg · mL-1的2-AP抑制PKR活性后, 部分抑制了p65进入细胞核 (图 6), 说明PKR的活性正向调控NF-кB活性。进一步用核质分离试验验证试验结果。Western blot分析结果 (图 7)显示:在NDV感染16 h后, 大量p65进入细胞核, 而在2-AP抑制PKR活性后, 进入细胞核的p65减少。以上结果说明, PKR识别NDV后, 可通过IκB的磷酸化降解而促进p65入核, 正向调控NF-κB的活性, 进而调节干扰素和炎症细胞因子的表达。
|
图 6 2-AP抑制PKR活性对p65入核影响的细胞定位 Figure 6 The cell location of the effect of the PKR activity inhibition by 2-AP on nuclear translocation of p65 |
|
图 7 2-AP抑制PKR活性对p65入核影响的Western blot分析 Figure 7 Western blot analysis of the effect of the PKR activity inhibition by 2-AP on nuclear translocation of p65 |
PKR是由干扰素诱导产生的抗病毒蛋白[15]。一方面, PKR能被双链RNA激活, 进一步磷酸化真核翻译起始因子 (eIF2α), 导致蛋白翻译关闭, 通过抑制病毒蛋白合成来抑制病毒复制[16]; 另一方面, PKR还会通过调控干扰素和细胞因子的表达, 发挥抗病毒活性。已有报道称新城疫病毒可激活PKR, 并磷酸化eIF2α, 从而引起Ⅰ型干扰素释放, 最终产生抗病毒效应[13]。但新城疫病毒是如何通过PKR调控IFN-β的表达, 尚未明确。为了验证NDV是如何通过PKR诱导干扰素和炎症因子的表达, 本试验用NDV感染HeLa细胞从而激活PKR与NF-κB信号通路, 进而转录因子p65入核, 最终诱导IFN-β、IL-6、IL-8的高效表达。当用药物抑制PKR活性后, 发现p65入核减少, 进而干扰素和细胞因子的表达也随之减少。说明NDV感染能够通过PKR调控NF-κB信号通路, 引起细胞因子表达, 发挥抗病毒效应。
机体防御反应的建立为模式识别受体识别病原相关分子模式, 而后多种转录因子参与调控。本文仅从模式识别受体PKR激活NF-κB信号通路来阐述抗病毒的效应, 已有文献报道, 胞内模式识别受体TLR3、RIG-I/MDA5在NDV感染中也发挥重要的作用, TLR3活化后通过接头分子TRIF引起IKK-ε及TBK-1的活化, 最后磷酸化IRF3, 而RIG-I/MDA5活化后通过接头分子MAVS招募一些连接酶来磷酸化IRF3, 最终都引起IRF3入核从而介导干扰素和一些抗病毒因子的表达[17-18]。本课题组未发表研究资料结果表明, PKR、RIG-I可以与应激颗粒形成一个平台来发挥抗病毒效应, 但具体哪个模式识别受体占主导地位, 并没有一个定论。PKR有可能通过结合和磷酸化IKKβ来正向调控NF-кB (p65) 的活性[11-12], 也可通过直接磷酸化IκBα, 导致IκBα被泛素化降解来激活NF-κB (p65)[13]。
综上所述, 本试验发现新城疫病毒感染能够通过PKR调控NF-κB信号通路, 从而引起细胞因子表达, 这有助于理解PKR在NDV感染过程中发挥的抗病毒作用, 为新城疫的防治打下理论基础。但是, PKR调控NF-κB信号通路的具体机制尚不清楚。PKR识别病毒感染并把信号传递到NF-κB的过程还需要进一步研究。
| [1] |
丁壮, 尹仁福, 薛聪, 等. 新城疫流行病学新特点及鹅新城疫防控策略[J].
中国兽医学报, 2015, 35(1): 159–168.
Ding Z, Yi R F, Xue C, et al. New epidemiological characteristics of Newcastle disease and control strategy of Newcastle disease in goose[J]. Chinese Journal of Veterinary Science, 2015, 35(1): 159–168. (in Chinese) |
| [2] | Susta L, Cornax I, Diel D G, et al. Expression of interferon gamma by a highly virulent strain of Newcastle disease virus decreases its pathogenicity in chickens[J]. Microbial Pathogenesis, 2013, 61: 73–83. |
| [3] | Rue C A, Susta L, Cornax I, et al. Virulent Newcastle disease virus elicits a strong innate immune response in chickens[J]. Journal of General Virology, 2011, 92(4): 931–939. DOI: 10.1099/vir.0.025486-0 |
| [4] | Liu W Q, Tian M X, Wang Y P, et al. The different expression of immune-related cytokine genes in response to velogenic and lentogenic Newcastle disease viruses infection in chicken peripheral blood[J]. Molecular Biology Reports, 2012, 39(4): 3611–3618. DOI: 10.1007/s11033-011-1135-1 |
| [5] |
段云兵, 汪军卿, 仇旭升, 等. 新城疫病毒M蛋白通过自身核定位信号介导进入宿主细胞核[J].
南京农业大学学报, 2014, 37(2): 105–110.
Duan Y B, Wang J Q, Qiu X S, et al. Martrix protein of Newcastle disease virus localizes to the nuclei by its buclear localization signal[J]. Journal of Nanjing Agricultural University, 2014, 37(2): 105–110. DOI: 10.7685/j.issn.1000-2030.2014.02.017 (in Chinese) |
| [6] | Liao Y, Gu F, Mao X, et al. Regulation of de novo translation of host cells by manipulation of PERK/PKR and GADD34-PP1 activity during Newcastle disease virus infection[J]. Journal of General Virology, 2016, 97(4): 867–879. DOI: 10.1099/jgv.0.000426 |
| [7] | Rafique S, Idrees M, Ilyas M, et al. Positional effect of phosphorylation sites 266 and 267 in the cytoplasmic domain of the E2 protein of hepatitis C virus 3a genotype:interferon resistance analysis via sequence alignment[J]. Virology Journal, 2011, 8(1): 1–6. DOI: 10.1186/1743-422X-8-1 |
| [8] | Yang Y L, Reis L F, Pavlovic J, et al. Deficient signaling in mice devoid of double-stranded RNA-dependent protein kinase[J]. EMBO Journal, 1995, 14(24): 6095–6106. |
| [9] | Schmolke M, Viemann D, Roth J, et al. Essential impact of NF-κB signaling on the H5N1 influenza A virus-induced transcriptome[J]. The Journal of Immunology, 2009, 183(8): 5180–5189. DOI: 10.4049/jimmunol.0804198 |
| [10] | Kumar A, Yang Y L, Flati V, et al. Deficient cytokine signaling in mouse embryo fibroblasts with a targeted deletion in the PKR gene:role of IRF-1 and NF-κB[J]. EMBO J, 1997, 16(2): 406–416. DOI: 10.1093/emboj/16.2.406 |
| [11] | Zamanian-Daryoush M, Mogensen T H, Didonato J A, et al. NF-κB activation by double-stranded-RNA-activated protein kinase(PKR)is mediated through NF-κB-inducing kinase and IκB kinase[J]. Mol Cell Biol, 2000, 20(4): 1278–1290. DOI: 10.1128/MCB.20.4.1278-1290.2000 |
| [12] | Valovka T, Hottiger M O. p65 controls NF-κB activity by regulating cellular localization of IκBβ[J]. Biochem J, 2011, 434(2): 253–263. DOI: 10.1042/BJ20101220 |
| [13] | Kumar A, Haque J, Lacoste J, et al. Double-stranded RNA-dependent protein kinase activates transcription factor NF-κB by phosphorylating IκB[J]. Proc Natl Acad Sci USA, 1994, 91(14): 6288–6292. DOI: 10.1073/pnas.91.14.6288 |
| [14] | Zhang S, Sun Y, Chen H, et al. Activation of the PKR/eIF2α signaling cascade inhibits replication of Newcastle disease virus[J]. Virol J, 2014, 11: 62. DOI: 10.1186/1743-422X-11-62 |
| [15] | Der S D, Zhou A, Williams B R, et al. Identification of genes differentially regulated by interferon α, β, or γ using oligonucleotide arrays[J]. Proc Natl Acad Sci USA, 1998, 95(26): 15623–15628. DOI: 10.1073/pnas.95.26.15623 |
| [16] | Clemens M J, Elia A. The double-stranded RNA-dependent protein kinase PKR:structure and function[J]. Journal of Interferon and Cytokine Research, 1997, 17(9): 503–524. DOI: 10.1089/jir.1997.17.503 |
| [17] | Yoo J S, Takahasi K, Ng C S, et al. DHX36 enhances RIG-Ⅰ signaling by facilitating PKR-mediated antiviral stress granule formation[J]. PLoS Pathogens, 2014, 10(3): e1004012. DOI: 10.1371/journal.ppat.1004012 |
| [18] | Cheng J, Sun Y, Zhang X, et al. Toll-like receptor 3 inhibits Newcastle disease virus replication through activation of pro-inflammatory cytokines and the type-1 interferon pathway[J]. Archives Virology, 2014, 159(11): 2937–2948. DOI: 10.1007/s00705-014-2148-6 |




