文章信息
- 王雨, 马立敏, 周睿颖, 唐晓清, 白钰
- WANG Yu, MA Limin, ZHOU Ruiying, TANG Xiaoqing, BAI Yu
- 盐胁迫对5个产地菘蓝幼苗光合特性及抗逆指标的影响
- Effects of salt stress on photosynthetic characteristics and indexes of adverse circumstances-resistance of Isatis indigotica Fort. seedlings from five areas
- 南京农业大学学报, 2017, 40(3): 416-424
- Journal of Nanjing Agricultural University, 2017, 40(3): 416-424.
- http://dx.doi.org/10.7685/jnau.201608011
-
文章历史
- 收稿日期: 2016-08-08
土壤盐渍化已经成为影响现代农业发展的全球性问题[1]。我国盐渍化土壤占地面积达3 460万hm2, 约为全国耕地面积的10%, 而设施农业的迅速发展使得土壤的次生盐渍化问题日益突出[2], 盐碱地面积的不断扩大严重制约着农业生产及发展。土壤中的致害盐类主要是以NaCl为主的中性盐[3], 其对植物的伤害主要表现在渗透胁迫、离子毒害和营养失衡3个方面。渗透胁迫会抑制根系对水分吸收, 进而降低光合作用和蒸腾作用效率; 植物体内Na+和Cl-的大量积累打破了细胞内的离子平衡, 破坏细胞膜结构并致使代谢紊乱; 盐离子与营养元素相互竞争则导致植物体内营养亏缺, 从而影响植物的正常生长和发育[4]。
菘蓝(Isatis indigotica Fort.)为十字花科二年生的草本植物, 其干燥叶入药为中药大青叶, 具有凉血消斑、泻火定惊等功效; 其干燥根入药为板蓝根, 具有利咽凉血、清热解毒的功效[5], 在抗流感病毒方面具有显著功效[6]。作为常用大宗药材大青叶及板蓝根的基原植物, 菘蓝在全国种植范围广、面积大, 然而土壤盐渍化的日益加重威胁着菘蓝的种植和生产, 高盐胁迫会显著抑制菘蓝种子的萌发及幼苗的生长[7]。目前, 对于植物的耐盐性研究主要集中于水稻[8]、小麦[9]、玉米[10]等作物, 菘蓝耐盐性的研究则鲜见报道。因此, 本试验以河北保定(HB)、内蒙古包头(NB)、辽宁铁岭(LT)、安徽亳州(AH)、山东滨州(SB)5个产地的菘蓝栽培居群为研究对象, 探究盐胁迫下菘蓝幼苗生长、光合特性、保护酶系统及渗透调节物质的变化规律, 以期为菘蓝抗盐材料的筛选及耐盐生理研究提供理论依据。
1 材料与方法 1.1 试验材料以河北保定(HB)、内蒙古包头(NB)、辽宁铁岭(LT)、安徽亳州(AH)、山东滨州(SB)5个产地的菘蓝(Isatis indigotica Fort.)栽培居群为试验材料, 经南京农业大学中药研究所王康才教授鉴定为十字花科植物菘蓝。
1.2 试验方法采用避雨盆栽试验, 将5个产地的菘蓝种子经10% NaClO消毒后, 播种于塑料盆(盆高20 cm, 口径26 cm, 底径18 cm)中, 栽培基质为蛭石和有机质(质量比为1:1), 基质基本理化性质:碱解氮含量116.5 mg·kg-1, 有效磷含量330.1 mg·kg-1, 速效钾含量515.4 mg·kg-1, 有机质含量151.0 g·kg-1, pH6.46, EC 0.59 ms·cm-1, 总孔隙度65.66%, 通气孔隙为17.13%, 自然采光。出苗后用1/2氮浓度的Hoagland营养液浇灌培养, 待幼苗长至4叶期时每盆定苗10株并开始处理, 分别浇施0、50、100、150 mmol·L-1 NaCl处理液, 并以0 mmol·L-1 NaCl处理为对照(CK), 每个处理3次重复, 每个重复3盆苗, 处理液均用1/2 Hoagland营养液配制[11]。为避免盐的冲击效应, 盐浓度每天递增50 mmol·L-1, 直至到达预定浓度, 而后每天以预定盐浓度的处理液浇灌1次, 处理液的浇灌量为基质持水量的2倍, 以保证之前积余的盐能够被全部冲出, 从而维持各处理盐浓度的恒定。于处理30 d后幼苗7叶期测定各项相关指标。
1.3 测定指标及方法 1.3.1 生长指标的测定各处理随机选取10株菘蓝幼苗分别测定其叶片和根的鲜质量, 105 ℃杀青15 min后, 60 ℃烘干至恒质量, 称干质量, 并计算含水率。含水率=(单株鲜质量-单株干质量)/单株鲜质量×100%。
1.3.2 光合特性测定选取菘蓝幼苗由内至外第二轮功能叶片, 用Li-6400便携式光合仪测定其净光合速率(Pn)、气孔导度(Gs)、细胞间隙CO2浓度(Ci)和蒸腾速率(Tr)。测定光照强度为1 000 μmol·m-2·s-1, 选择天气晴朗的上午进行测定, 测定时间为08:00—10:30, 各处理选生长一致的菘蓝幼苗8株进行测定。
1.3.3 叶绿素含量的测定以95%(体积分数)乙醇于黑暗环境中提取叶绿素, 采用分光光度法[12]测定, 各处理每次随机取样3株, 试验重复3次。
1.3.4 保护酶活性的测定采用氮蓝四唑(NBT)法测定超氧化物歧化酶(SOD)活性, 采用愈创木酚法[12]测定过氧化物酶(POD)活性。各处理每次随机取样3株, 试验重复3次。
1.3.5 丙二醛(MDA)含量的测定采用硫代巴比妥酸(TBA)法[13]测定叶片中的MDA含量, 各处理3次重复。
1.3.6 可溶性蛋白含量的测定采用考马斯亮蓝G-250法测定可溶性蛋白含量。称取0.5 g新鲜菘蓝幼苗叶片, 加入8 mL蒸馏水研磨成匀浆, 于室温下放置1 h后于4 000 r·min-1离心20 min, 上清液转入10 mL容量瓶后定容; 吸取提取液0.1 mL于试管中, 加入5 mL考马斯亮蓝G-250试剂充分混匀, 室温放置2 min, 以空白为对照, 于595 nm下测定吸光度, 并计算菘蓝幼苗叶片中可溶性蛋白含量[12], 各处理3次重复。
1.3.7 脯氨酸含量的测定采用磺基水杨酸法[14]测定菘蓝叶片中的脯氨酸含量。
1.4 数据处理及分析用SPSS 19.0软件及Excel 2003对试验所得数据进行处理及分析, 采用LSD法进行处理间的差异显著性比较。
2 结果与分析 2.1 盐胁迫对菘蓝幼苗生物量及含水率的影响从表 1可以看出:盐胁迫下, 5个产地菘蓝幼苗含水率、叶片及根的鲜质量和干质量总体上均呈下降的趋势。其中HB(河北保定)和SB(山东滨州)菘蓝幼苗含水率、叶片鲜质量和干质量在50 mmol·L-1的NaCl处理时均高于对照(0 mmol·L-1 NaCl), 之后随着NaCl浓度的升高而下降。随着盐浓度的不断升高, 不同产地间菘蓝的生长状况表现出较大差异。HB、SB、NB(内蒙古包头)3个产地菘蓝幼苗生物量的降幅较为一致, 而盐胁迫后LT(辽宁铁岭)及AH(安徽亳州)菘蓝叶片及根的生长受到明显抑制, 其幼苗含水率、叶片和根的鲜质量及干质量均大幅度下降。150 mmol·L-1 NaCl胁迫后, LT菘蓝幼苗含水率、叶片和根的鲜、干质量均大幅度下降, 各指标与对照间差异达均到极显著水平(P < 0.01)。AH菘蓝幼苗含水率比对照显著降低了1.04%(P < 0.05), 叶片的鲜、干质量分别比对照下降了47.00%和45.20%, 根的鲜、干质量分别比对照下降了51.20%和52.30%, 且与对照间差异极显著。150 mmol·L-1 NaCl胁迫下, LT和AH的菘蓝幼苗均表现出萎蔫, 叶片卷曲发黄, 植株矮小, 甚至部分植株死亡。说明盐胁迫下, LT及AH菘蓝幼苗较其他产地对盐更为敏感, 同时盐胁迫对菘蓝幼苗根的生长抑制强于叶片。
| 产地 Area |
c(NaCl)/ (mmol·L-1) |
单株叶鲜质量/g Leaf fresh weight per plant |
单株叶干质量/g Leaf dry weight per plant |
单株根鲜质量/g Root fresh weight per plant |
单株根干质量/g Root dry weight per plant |
含水率/% Water content |
| HB | 0 | 2.21±0.14Aa | 0.26±0.09Bb | 0.98±0.08Bb | 0.12±0.04Aa | 88.09±1.60Aa |
| 50 | 2.47±0.03Aa | 0.29±0.08Aa | 1.12±0.05Aa | 0.13±0.01Aa | 88.30±1.06Aa | |
| 100 | 1.98±0.04Bb | 0.22±0.01Bb | 0.78±0.12Cc | 0.08±0.01Bb | 88.13±1.51Aa | |
| 150 | 1.59±0.04Cc | 0.18±0.11Cc | 0.62±0.04Dd | 0.07±0.01Bb | 87.69±1.37Ab | |
| SB | 0 | 1.98±0.06ABb | 0.23±0.03Aab | 1.11±0.05Aa | 0.14±0.08Aa | 88.03±1.55Aa |
| 50 | 2.12±0.85Aa | 0.25±0.01Aa | 1.02±0.07Aa | 0.13±0.02ABa | 87.90±0.90Aa | |
| 100 | 1.68±0.37BCb | 0.21±0.01Aab | 0.82±0.03Bb | 0.10±0.01ABb | 87.60±1.21Aab | |
| 150 | 1.43±0.21Cc | 0.19±0.03Ab | 0.76±0.17Bb | 0.09±0.01Bb | 87.22±1.41Ab | |
| NB | 0 | 2.42±0.06Aa | 0.37±0.03Aa | 1.37±0.06Aa | 0.19±0.05Aa | 85.52±1.38Aa |
| 50 | 2.51±0.22Aa | 0.37±0.06Aa | 1.29±0.05Aa | 0.18±0.02Aa | 85.53±0.82Aa | |
| 100 | 1.92±0.38Bb | 0.29±0.08Bb | 0.93±0.02Aab | 0.13±0.06Aa | 85.26±1.34Aa | |
| 150 | 1.84±0.13Bb | 0.26±0.12Bb | 0.84±0.11Aab | 0.12±0.04Ab | 85.22±1.10Aa | |
| LT | 0 | 1.73±0.27Aa | 0.21±0.07Aa | 0.87±0.04Aa | 0.13±0.03Aa | 87.82±1.38Aa |
| 50 | 1.68±0.06Aa | 0.18±0.03Ab | 0.72±0.02Bb | 0.10±0.01Ab | 87.91±0.55Aa | |
| 100 | 1.24±0.08Bb | 0.15±0.01Bc | 0.61±0.21Cc | 0.09±0.01Bb | 87.03±2.04Ab | |
| 150 | 1.13±0.02Cc | 0.13±0.01Bc | 0.41±0.02Cd | 0.07±0.01Bc | 86.34±0.36Bc | |
| AH | 0 | 3.27±0.39Aa | 0.42±0.06Aa | 1.41±0.04Aa | 0.16±0.10Aa | 87.82±1.96Aa |
| 50 | 3.17±0.52Aa | 0.41±0.06Aa | 1.22±0.23Bb | 0.15±0.01ABa | 87.54±2.02Aa | |
| 100 | 2.34±0.62Bb | 0.30±0.08ABb | 0.95±0.08Cc | 0.11±0.01Bb | 87.24±1.13Aa | |
| 150 | 1.68±0.09Cc | 0.23±0.11Bb | 0.59±0.03Dd | 0.07±0.05Cc | 86.78±1.46Ab | |
| 注: 1) HB:河北保定Baoding, Hebei; SB:山东滨州Binzhou, Shandong; NB:内蒙古包头Baotou, Inner Mongolia; LT:辽宁铁岭Tieling, Liaoning; AH:安徽亳州Bozhou, Anhui 2) 不同大、小写字母分别表示差异极显著(P < 0.01) 和显著(P < 0.05)。Different capital and small letters in the same column show significant difference at 0.01 and 0.05 levels, respectively. The same as follows. |
||||||
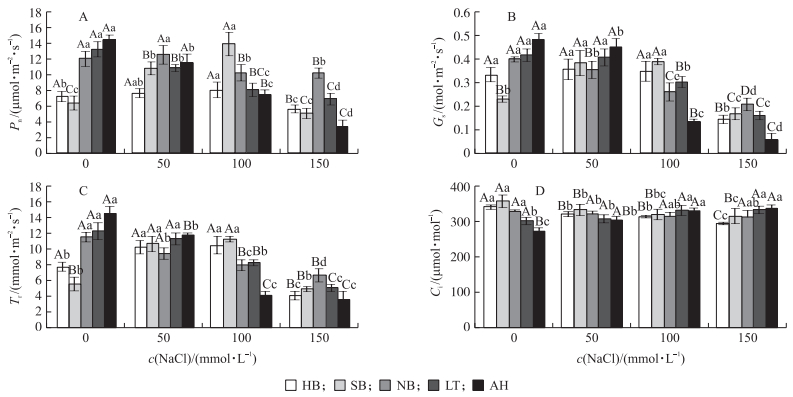
由图 1-A可见:盐胁迫后5个产地菘蓝幼苗的Pn出现不同程度的变化。HB和SB菘蓝幼苗的Pn随着盐浓度的增加呈先上升后下降的趋势, 在100 mmol·L-1 NaCl处理时最高, 而NB、LT及AH菘蓝幼苗的Pn则随着盐浓度的升高而降低。50 mmol·L-1 NaCl的轻度胁迫时, LT和AH菘蓝的Pn分别比对照降低了18.21%和20.18%, 而NB菘蓝的Pn则与对照无显著差异。150 mmol·L-1 NaCl胁迫下, NB、LT和AH菘蓝的Pn显著降低, 分别比对照下降了15.48%、47.93%和76.77%, 与对照间差异达到极显著水平。值的注意的是, 5个产地菘蓝幼苗各对照的Pn表现出较大的差异, 这可能与不同产地间菘蓝自身的遗传差异性有关。
|
图 1 盐胁迫对菘蓝叶片光合特性的影响 Figure 1 Effects of salt stress on photosynthetic characteristics of Isatis indigotica leaves |
盐胁迫下, 5个产地菘蓝幼苗Gs的变化规律与其Pn的变化规律基本一致(图 1-B)。随着盐胁迫程度的增加, HB及SB菘蓝幼苗的Gs先上升, 100 mmol·L-1 NaCl处理下最大, 而后急剧下降。NB、LT和AH菘蓝的Gs均随盐浓度的升高呈不同幅度的下降, 其中AH产地菘蓝的Gs在100 mmol·L-1 NaCl胁迫时急剧下降, 与对照间差异极显著, 降低了72.41%。当盐浓度升至150 mmol·L-1时, HB、SB、NB、LT和AH菘蓝幼苗的Gs均显著低于对照, 分别比对照降低了56.87%、27.33%、48.12%、61.78%和88.56%。
2.2.3 蒸腾速率(Tr)图 1-C显示:盐胁迫下各产地菘蓝幼苗Tr与Pn的变化规律相同。5个产地间菘蓝幼苗对照的Tr存在较大差异。与对照相比, 50 mmol·L-1 NaCl处理时, HB和SB菘蓝幼苗Tr均显著升高, 分别为对照的1.32和1.93倍, 在100 mmol·L-1 NaCl处理时略微上升后, 于150 mmol·L-1高浓度盐胁迫下急剧下降。NB、LT和AH菘蓝幼苗的Tr在50 mmol·L-1 NaCl处理时明显下降。当盐浓度升至100 mmol·L-1时, NB、LT和AH的Tr出现大幅度的下降, 分别比对照降低了31.21%、33.03%和71.87%, 与对照间呈极显著差异。在高盐浓度(150 mmol·L-1 NaCl)胁迫下, 除SB外, 其余各产地菘蓝幼苗的Tr均显著低于对照。
2.2.4 胞间CO2浓度(Ci)5个产地菘蓝幼苗的Ci在盐胁迫下的变化规律并不一致(图 1-D)。HB和SB菘蓝幼苗的Ci与其Pn的趋势一致, 均随盐浓度的逐渐升高而下降, 且2个产地菘蓝经盐胁迫后的各处理均显著低于对照, NB菘蓝幼苗Ci的变化规律则不明显。随着盐浓度的升高, LT和AH菘蓝的Ci却随其Pn下降而上升, 在100 mmol·L-1 NaCl处理下, LT和AH菘蓝的Ci分别比对照显著增加了9.85%和21.35%。在150 mmol·L-1 NaCl处理下, AH菘蓝的Ci继续升高并比对照增加了24.05%, 与对照间差异达到极显著水平。
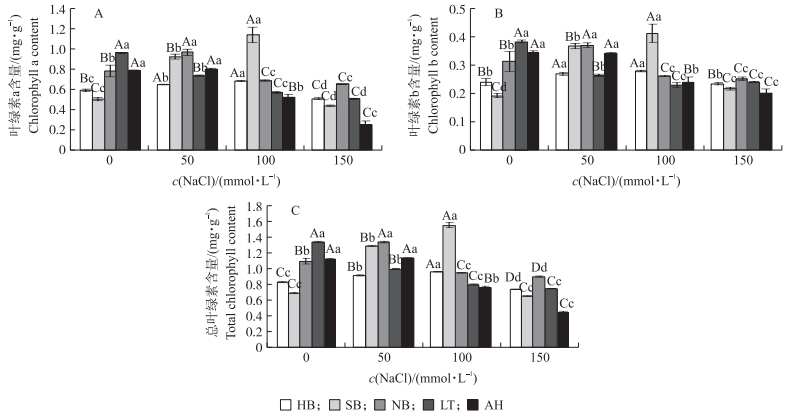
2.3 盐胁迫对菘蓝幼苗叶绿素含量的影响从图 2可见:HB和SB菘蓝幼苗叶片的叶绿素含量均随着盐浓度的升高呈先上升后下降趋势。HB菘蓝叶片的叶绿素含量随着盐浓度的增加而平缓上升, 并在100 mmol·L-1 NaCl胁迫下达到峰值, 其叶绿素a、叶绿素b和总叶绿素含量分别比对照增加了16.00%、16.67%和16.16%, 而在150 mmol·L-1 NaCl胁迫时显著降低。盐胁迫下, SB菘蓝的叶绿素含量变化幅度较大, 除150 mmol·L-1 NaCl处理外的各处理间差异达到极显著水平。NB、LT和AH菘蓝的叶绿素a、叶绿素b和总叶绿素含量随盐胁迫程度的增加整体呈递减的趋势。其中, NB菘蓝的叶绿素a、叶绿素b和总叶绿素含量在50 mmol·L-1 NaCl胁迫时显著升高, 之后开始逐步下降。LT菘蓝各盐浓度处理间叶绿素a含量的差异达到显著水平。150 mmol·L-1 NaCl处理下, AH菘蓝幼苗的叶绿素a、叶绿素b和总叶绿素含量分别比对照降低了68.80%、41.40%和73.27%。说明HB菘蓝对盐的耐受性较强, 盐胁迫对其叶绿素合成的影响不大, NB、LT及AH菘蓝对盐胁迫较为敏感, 适当的盐胁迫反而能够促进SB菘蓝叶绿素的合成。
|
图 2 盐胁迫对菘蓝幼苗叶绿素含量的影响 Figure 2 Effects of salt stress on chlorophyll content of Isatis indigotica seedlings |
盐胁迫下, 5个产地菘蓝幼苗SOD活性均随盐浓度的升高呈先上升后下降的趋势(表 2)。其中, HB、SB和NB菘蓝幼苗的SOD活性在盐胁迫下变化平缓。随着盐浓度的升高, LT和AH菘蓝幼苗的SOD活性均升高,并在100 mmol·L-1 NaCl胁迫下达到最大值,分别为对照的1.19和2.61倍,而后随着盐浓度的继续增加,2个产地菘蓝幼苗的SOD活性均开始下降。盐胁迫下,AH菘蓝幼苗SOD活性变化幅度最大,不同处理间的差异达到极显著水平。5个产地菘蓝幼苗的POD活性变化与SOD活性的变化规律一致,均随盐浓度的增加先升高,而后开始下降(表 2)。盐胁迫下各产地菘蓝幼苗POD活性变化明显,除AH外,其余产地菘蓝幼苗的POD活性均在100 mmol·L-1 NaCl处理时达到最大,而后开始下降。AH菘蓝幼苗的POD活性在50 mmol·L-1 NaCl处理时即达到最高,比对照增加了38.60%。5个产地菘蓝幼苗体内MDA的含量均随盐浓度的升高而增加。盐胁迫下,HB和SB菘蓝MDA含量平缓上升。除NB外其余各产地的不同盐浓度处理间,菘蓝幼苗的MDA含量差异均达到极显著水平。在150 mmol·L-1 NaCl胁迫下,5个产地菘蓝幼苗体内MDA含量均达到最大值。盐胁迫下,AH菘蓝体内MDA的含量变化幅度最大。综上说明,盐胁迫下AH菘蓝幼苗自身的调节能力弱,耐受性较差,而盐胁迫对HB、SB和NB菘蓝幼苗的影响较小。同时,100 mmol·L-1的NaCl胁迫对菘蓝幼苗是一个极限耐受盐度,即超过该浓度的盐胁迫已超出了菘蓝自身保护酶的防御能力,从而致使保护酶系统遭到破坏,2种保护酶的活性均显著下降,丙二醛大量积累。
| 产地 Area |
c(NaCl)/ (mmol·L-1) |
SOD活性/(U·g-1) SOD activity |
POD活性/(U·g-1·min-1) POD activity |
MDA含量/(μmol·g-1) MDA content |
| HB | 0 | 354.3±6.1Bb | 1 140.0±21.6Bc | 3.32±0.022Dd |
| 50 | 372.5±4.7Bb | 1 416.7±25.6Ab | 4.00±0.010Cc | |
| 100 | 417.1±8.2Aa | 1 603.3±27.2Aa | 6.76±0.006Bb | |
| 150 | 363.1±9.5Bb | 1 416.7±9.9Ab | 13.37±0.018Aa | |
| SB | 0 | 323.4±9.5Bc | 943.3±26.5Cc | 5.20±0.013Dd |
| 50 | 343.3±4.7ABb | 1 046.7±16.1Aa | 7.10±0.012Cc | |
| 100 | 363.1±6.7Aa | 1 643.3±24.4Aa | 9.93±0.004Bb | |
| 150 | 328.4±6.9Bbc | 1 630.0±28.7Aa | 11.63±0.015Aa | |
| NB | 0 | 359.7±13.5Ab | 1 236.7±29.9Cc | 9.76±0.047Bc |
| 50 | 397.5±12.5Aa | 1 470.0±23.5Bb | 10.56±0.041Bb | |
| 100 | 376.5±9.3Aab | 2 050.0±35.3Aa | 16.16±0.022Aa | |
| 150 | 360.6±17.5Ab | 1 173.3±24.0Dd | 16.60±0.012Aa | |
| LT | 0 | 530.8±12.8Bb | 896.7±37.7Cc | 8.04±0.025Dd |
| 50 | 556.8±24.0Bb | 946.7±25.1Bb | 14.49±0.031Cc | |
| 100 | 628.9±10.9Aa | 1 160.0±37.4Aa | 17.43±0.018Bb | |
| 150 | 514.0±9.7Bb | 486.0±23.0Bb | 21.37±0.090Aa | |
| AH | 0 | 114.9±4.3Dd | 1 400.0±36.4Cc | 13.91±0.048Dd |
| 50 | 239.0±10.9Cc | 1 940.0±17.1Aa | 18.50±0.045Bc | |
| 100 | 299.4±9.4Aa | 1 686.7±18.5Bb | 21.42±0.097Bb | |
| 150 | 258.3±6.3Bb | 1 533.3±19.9BCbc | 37.08±0.133Aa |
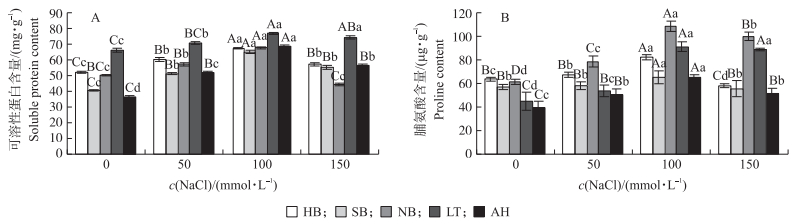
由图 3-A可以看出:随着盐胁迫程度的逐渐增加, 5个产地菘蓝体内可溶性蛋白含量均呈先升高后下降的趋势, 并均在100 mmol·L-1 NaCl处理时达到最大值; 之后随着盐浓度的继续升高, 各产地菘蓝体内可溶性蛋白含量又开始出现不同程度的下降。盐胁迫下, LT菘蓝幼苗的可溶性蛋白含量一直维持在较高水平且变化平缓, 其他产地菘蓝幼苗的可溶性蛋白含量均呈大幅度变化, 其中以AH菘蓝可溶性蛋白含量变化幅度最大, 在50和100 mmol·L-1 NaCl处理时, AH菘蓝幼苗体内可溶性蛋白含量分别比对照高出42.30%和88.90%, 且各处理间差异均达到显著水平。
|
图 3 盐胁迫对菘蓝渗透调节物质的影响 Figure 3 Effects of salt stress on osmoregulation substances of Isatis indigotica seedlings |
盐胁迫下, 除AH外, 其余4个产地菘蓝体内脯氨酸含量的变化与其可溶性蛋白含量的变化规律一致(图 3-B)。HB和SB菘蓝体内的脯氨酸含量受盐度影响较小, 变化较为平缓。在100 mmol·L-1 NaCl胁迫下, NB、LT和AH菘蓝脯氨酸的含量分别为各自对照的1.77、2.03和1.65倍, 且各处理间的差异均达到极显著水平。
HB和SB的菘蓝幼苗耐盐性较好, 盐胁迫对其体内可溶性蛋白和脯氨酸的积累影响不大, 对NB、LT、AH菘蓝幼苗的渗透胁迫作用则较为明显。
3 讨论盐渍环境往往会对植物生长产生抑制, 最终导致其生物量等生长指标的下降[15]。本试验中, 盐胁迫下5个产地菘蓝幼苗含水率、叶鲜质量及干质量、根鲜质量及干质量总体上均呈明显的下降趋势, 在150 mmol·L-1 NaCl胁迫下, 5个产地菘蓝幼苗的生物量均降至最低, 这说明高浓度的盐胁迫对菘蓝幼苗生长具有显著的抑制作用。根作为植物的吸收器官, 其对逆境胁迫的感受最为直接[16]。盐胁迫过程中, 菘蓝幼苗根鲜质量及干质量的下降幅度明显大于叶片, 说明盐胁迫对于菘蓝根的生长抑制作用更为明显, 这与陈宝悦等[17]的研究结果一致。
光合作用作为植物重要的生命过程, 对植物的正常生长代谢具有至关重要的作用, 而盐胁迫则会使植物的光合特性发生变化。本试验中, 盐胁迫对5个产地菘蓝幼苗光合特性的影响并不相同, 50 mmol·L-1 NaCl的轻度胁迫提高了HB和SB菘蓝幼苗的Pn、Gs及Tr, 说明轻度盐胁迫促进了HB和SB菘蓝的光合作用, 这与Kurban等[18]的研究结果相同。盐胁迫下AH菘蓝幼苗的Pn、Gs和Tr下降幅度显著高于LT和AH产地, 表明AH的菘蓝幼苗对盐胁迫更为敏感。不同产地菘蓝Ci与Pn的变化趋势并不完全一致, 这表明盐胁迫下引起不同产地菘蓝幼苗光合速率下降的原因并不相同。150 mmol·L-1 NaCl胁迫下, HB和SB菘蓝幼苗的Ci、Gs随Pn的下降而降低, 说明此时Pn的下降主要是由于叶片的气孔导度降低, 导致外界CO2无法正常向细胞中的扩散, 光合作用底物不足所致[19]。随着盐胁迫程度的增加, LT和AH菘蓝幼苗的Ci却随Pn的降低而升高, 说明非气孔限制因素是盐胁迫下LT和AH菘蓝Pn下降的原因。这可能是由于盐胁迫下LT和AH菘蓝的叶绿体结构受损、叶肉细胞的光化学活性降低, 最终导致其光合效率的下降[20]。NB菘蓝Ci的变化规律不明显, 其具体调控机制还需进一步研究。
叶绿素作为植物光合作用的重要色素, 其含量和结构决定着植物光合作用效率的高低, 同时也是衡量植物耐盐性的重要生理指标之一[21]。本试验中, 适度的盐胁迫(50和100 mmol·L-1 NaCl)提高了菘蓝幼苗的叶绿素含量, 这可能是由于在该盐浓度下, HB和SB菘蓝幼苗自身调节能力较强, 为了维持其光合作用的正常水平而加速了叶绿素的合成, 从而提高自身的耐盐能力[22]。LT、AH菘蓝幼苗的叶绿素含量均随盐浓度的升高而下降, 这可能由于这2个产地菘蓝幼苗的耐盐性较差, 盐胁迫造成的离子毒害引起叶绿素解体, 导致叶绿素含量降低[23]。
盐胁迫下植物体内会产生大量的活性氧, 从而造成植物细胞结构受损, 甚至导致死亡, SOD和POD能够清除植物体内多余的活性氧, 减轻盐胁迫对植物造成的损伤[24]。本试验结果表明, 50 mmol·L-1 NaCl处理的5个产地菘蓝幼苗SOD和POD活性均升高, 说明轻度的盐胁迫能够诱导菘蓝体内保护酶活性的增强, 从而提高盐渍环境下菘蓝幼苗的适应能力。而随着盐浓度的继续升高, 菘蓝幼苗体内的盐含量逐渐积累, 已经超出了其体内保护酶的清除能力极限, 导致其保护酶系统失衡, 膜质过氧化程度加剧, 最终致使菘蓝体内SOD和POD活性下降, MDA大量积累, 这与刘爱荣等[25]的研究结果一致。
在盐胁迫等逆境条件下, 植物体内脯氨酸的积累有利于细胞从外界的高渗环境中摄入水分, 从而提高耐盐能力[26]。此外植物细胞中的可溶性蛋白也是一种有机渗透物质[27]。本试验中, 盐胁迫下5个产地菘蓝幼苗的可溶性蛋白和脯氨酸含量均呈先升高后降低的趋势, 并在100 mmol·L-1 NaCl胁迫时达到峰值。这可能是由于盐胁迫下菘蓝通过刺激体内脯氨酸的积累, 并诱导产生大量蛋白质以提高自身的耐盐性, 而100 mmol·L-1 NaCl为菘蓝幼苗的极限耐受盐度, 更高浓度的盐胁迫则会超过菘蓝自身的耐受能力, 导致脯氨酸及蛋白质正常合成受阻, 含量下降, 这与刘凤歧等[28]和冯大伟等[29]的研究结果一致。
综上所述, 5个产地的菘蓝幼苗对盐胁迫均有一定的耐受能力, 100 mmol·L-1 NaCl为菘蓝幼苗的极限耐受盐度。不同产地菘蓝幼苗的耐盐性具有显著差异, 5个产地菘蓝幼苗的耐盐性从大到小依次排序为:HB、SB、NB、LT、AH。
| [1] | Kronzucker H J, Szczerba M W, Schulze L M, et al. Non-reciprocal interactions between K+ and Na+ ions in barley(Hordeum vulgare L.)[J]. Journal of Experimental Botany, 2007, 59(10): 2793–2801. |
| [2] |
彭英, 刘晓静, 汤兴利, 等. 盐胁迫对北沙参生长及生理特性的影响[J].
江苏农业学报, 2014, 30(6): 1273–1278.
Peng Y, Liu X J, Tang X L, et al. Growth and physiological characteristics of Glehnia littoralis inresponse to salt stress[J]. Jiangsu Agricultural Sciences, 2014, 30(6): 1273–1278. (in Chinese) |
| [3] |
曲元刚, 赵可夫. NaCl和Na2CO3对玉米生长和生理胁迫效应的比较研究[J].
作物学报, 2004, 30(4): 334–341.
Qu Y G, Zhao K F. Comparative studies on growth and physiological reaction of Zea mays under NaCl and Na2CO3 stresses[J]. Acta Agronomica Sinica, 2004, 30(4): 334–341. (in Chinese) |
| [4] | Munns R, Tester M. Mechanisms of salinity tolerance[J]. Annual Review of Plant Biology, 2008, 59(1): 651–681. DOI: 10.1146/annurev.arplant.59.032607.092911 |
| [5] |
国家药典委员会.
中华人民共和国药典(一部)[M]. 北京: 中国医药科技出版社, 2015: 21-206.
Chinese Pharmacopoeia Commission. Pharmacopoeia of People's Republic of China:Volume 1[M]. Beijing: China Medical Science Press, 2015: 21-206. (in Chinese) |
| [6] |
徐丽华, 黄芳, 陈婷, 等. 板蓝根中的抗病毒活性成分[J].
中国天然药物, 2005, 3(6): 350–360.
Xu L H, Huang F, Chen T, et al. Antivirus constituents of radix of Isatis indigotica[J]. Chinese Journal of Natural Medicines, 2005, 3(6): 350–360. (in Chinese) |
| [7] |
张海艳. NaCl胁迫对菘蓝种子萌发及幼苗生长的影响[J].
山东农业科学, 2015, 47(4): 56–58.
Zhang H Y. Effects of NaCl stress on seed germination and seedling growth of Isatis indigotica[J]. Shandong Agricultural Sciences, 2015, 47(4): 56–58. (in Chinese) |
| [8] |
徐晨, 凌风楼, 徐克章, 等. 盐胁迫对不同水稻品种光合特性和生理生化特性的影响[J].
中国水稻科学, 2013, 27(3): 280–286.
Xu C, Ling F L, Xu K Z, et al. Effect of salt stress on photosynthetic characteristics and physiological and biochemical traits of different rice varieties[J]. Chinese Journal of Rice Science, 2013, 27(3): 280–286. (in Chinese) |
| [9] |
张敏, 蔡瑞国, 李慧芝, 等. 盐胁迫环境下不同抗盐性小麦品种幼苗长势和内源激素的变化[J].
生态学报, 2008, 28(1): 310–320.
Zhang M, Cai R G, Li H Z, et al. Responses of seedling growth and endogenous hormone contents in different wheat cultivars to salt stress[J]. Acta Ecologica Sinica, 2008, 28(1): 310–320. (in Chinese) |
| [10] |
彭云玲, 李伟丽, 王坤泽, 等. NaCl胁迫对玉米耐盐系与盐敏感系萌发和幼苗生长的影响[J].
草业学报, 2012, 21(4): 62–71.
Peng Y L, Li W L, Wang K Z, et al. Effects of salt stress on seed germination and seedlings growth of salt-tolerant line and salt-sensitive line of maize[J]. Acta Prataculturae Sinica, 2012, 21(4): 62–71. DOI: 10.11686/cyxb20120408 (in Chinese) |
| [11] |
张志良, 翟伟菁.
植物生理学实验指导[M]. 3版. 北京: 高等教育出版社, 2003: 23-24.
Zhang Z L, Zhai W J. Plant Physiology Experiment Instruction[M]. 3rd ed. Beijing: Higher Education Press, 2003: 23-24. (in Chinese) |
| [12] |
王学奎.
植物生理生化实验原理和技术[M]. 2版. 北京: 科学出版社, 2006: 134-191.
Wang X K. Principles and Techniques of Plant Physiological Experiment[M]. 2nd ed. Beijing: Science Press, 2006: 134-191. (in Chinese) |
| [13] |
李合生, 孙群, 赵世杰, 等.
植物生理实验原理与技术[M]. 2版. 北京: 高等教育出版社, 2006: 169-170.
Li H S, Sun Q, Zhao S J, et al. Principles and Techniques of Plant Physiological Experiment[M]. 2nd ed. Beijing: Higher Education Press, 2006: 169-170. (in Chinese) |
| [14] |
张殿忠, 汪沛洪, 赵会贤. 测定小麦叶片游离脯氨酸的方法[J].
植物生理学通讯, 1990(4): 62–65.
Zhang D Z, Wang P H, Zhao H X. Determination of the content of free proline in wheat leaves[J]. Plant Physiology Communications, 1990(4): 62–65. (in Chinese) |
| [15] | Summart J, Thanonkeo P, Panichajakul S, et al. Effect of salt stress on growth, inorganic ion and proline accumulation in Thai aromatic rice, Khao Dawk Mali 105, callus culture[J]. African Journal of Biotechnology, 2010, 9(2): 145–152. |
| [16] |
陈丽芳, 陆巍, 孙锦, 等. 外源亚精胺对盐胁迫下黄瓜幼苗光合作用和根叶碳水化合物积累的影响[J].
南京农业大学学报, 2011, 34(3): 31–36.
Chen L F, Lu W, Sun J, et al. Effects of exogenous spermidine on photosynthesis and carbohydrate accumulation in roots and leaves of cucumber(Cucumis sativus L.)seedlings under salt stress[J]. Journal of Nanjing Agricutural University, 2011, 34(3): 31–36. DOI: 10.7685/j.issn.1000-2030.2011.03.006 (in Chinese) |
| [17] |
陈宝悦, 曹玲, 王艳芳, 等. NaCl胁迫对芹菜生长、生理生化特性及品质的影响[J].
华北农学报, 2014, 29(B12): 218–222.
Chen B Y, Cao L, Wang Y F, et al. Effects of NaCl stress on growth, physiological and biochemical characteristics and quality of celery[J]. Acta Agriculturae Boreali-Sinica, 2014, 29(B12): 218–222. (in Chinese) |
| [18] | Kurban H, Saneoka H, Nehira K, et al. Effect of salinity on growth, photosynthesis and mineral composition in leguminous plant Alhagi pseudoalhagi(Bieb.)[J]. Soil Science and Plant Nutrition, 1999, 45(4): 851–862. DOI: 10.1080/00380768.1999.10414334 |
| [19] |
孙璐, 周宇飞, 李丰先, 等. 盐胁迫对高粱幼苗光合作用和荧光特性的影响[J].
中国农业科学, 2012, 45(16): 3265–3272.
Sun L, Zhou Y F, Li F X, et al. Impacts of salt stress on characteristics of photosynthesis and chlorophyll fluorescence of sorghum seedlings[J]. Scientia Agricultura Sinica, 2012, 45(16): 3265–3272. DOI: 10.3864/j.issn.0578-1752.2012.16.005 (in Chinese) |
| [20] | Farquhar G D, Sharkey T D. Stomatal conductance and photosynthesis[J]. Annual Review of Plant Physiology, 1982, 33(1): 74–79. |
| [21] |
李学孚, 倪智敏, 吴月燕, 等. 盐胁迫对'鄞红'葡萄光合特性及叶片细胞结构的影响[J].
生态学报, 2015, 35(13): 4436–4444.
Li X F, Ni Z M, Wu Y Y, et al. Effects of salt on photosynthetic characteristics and leaf cell structure of 'Yinhong' grape seedlings[J]. Acta Ecologica Sinica, 2015, 35(13): 4436–4444. (in Chinese) |
| [22] |
周丹丹, 刘德玺, 李存华, 等. 盐胁迫对朴树和速生白榆幼苗光合特性及叶绿素荧光参数的影响[J].
西北植物学报, 2016, 36(5): 1004–1011.
Zhou D D, Liu D X, Li C H, et al. Photosynthetic characteristics and chlorophyll fluorescence parameters of Celtis sinensis and Ulmus pumila L. seedling under salt stress[J]. Acta Botanica Boreali-Occidentalia Sinica, 2016, 36(5): 1004–1011. (in Chinese) |
| [23] |
薛忠财, 高辉远, 柳洁. 野生大豆和栽培大豆光合机构对NaCl胁迫的不同响应[J].
生态学报, 2011, 31(11): 3101–3109.
Xue Z C, Gao H Y, Liu J. Different response of photosynthetic apparetus between wild soybean(Glycine soja)and cultivated soybean(Glycine max)to NaCl stress[J]. Acta Ecologica Sinica, 2011, 31(11): 3101–3109. (in Chinese) |
| [24] | Meloni D A, Oliva M A, Martinez C A, et al. Photosynthesis and activity of superoxide dismutase, peroxidase and glutathione reductase in cotton under salt stress[J]. Environmental and Experimental Botany, 2003, 49(1): 69–76. DOI: 10.1016/S0098-8472(02)00058-8 |
| [25] |
刘爱荣, 张远兵, 方园园, 等. 盐胁迫对金盏菊生长抗氧化能力和盐胁迫蛋白的影响[J].
草业学报, 2011, 20(6): 52–59.
Liu A R, Zhang Y B, Fang Y Y, et al. Effects of salt stress on the growth, antioxidant ability and stress protein of Calendula officinalis[J]. Acta Prataculturae Sinica, 2011, 20(6): 52–59. DOI: 10.11686/cyxb20110607 (in Chinese) |
| [26] |
李如升, 石德成. NaCl胁迫对甘草幼苗的生长及相关生理指标的影响[J].
江苏农业科学, 2010(2): 257–258.
Li R S, Shi D C. Effect of salt stress on growth and physiological index of Glycyrrhiza uralensis seedlings[J]. Jiangsu Agricultural Sciences, 2010(2): 257–258. (in Chinese) |
| [27] |
王鑫, 孔祥生. 盐胁迫对流苏树愈伤组织生理生化特性的影响[J].
江苏农业科学, 2014, 42(11): 54–57.
Wang X, Kong X S. Effect of salt stress on physio-biochemical indices of Chionanthus retusus callus[J]. Jiangsu Agricultural Sciences, 2014, 42(11): 54–57. (in Chinese) |
| [28] |
刘凤歧, 刘杰淋, 朱瑞芬, 等. 4种燕麦对NaCl胁迫的生理响应及耐盐性评价[J].
草业学报, 2015, 24(1): 183–189.
Liu F Q, Liu J L, Zhu R F, et al. Physiological responses and tolerance of four oatvarieties to salt stress[J]. Acta Prataculturae Sinica, 2015, 24(1): 183–189. DOI: 10.11686/cyxb20150122 (in Chinese) |
| [29] |
冯大伟, 张洪霞, 刘广洋, 等. 不同品种菊芋对黄河三角洲土壤盐胁迫的响应研究[J].
核农学报, 2013, 27(11): 1771–1776.
Feng D W, Zhang H X, Liu G Y, et al. Responses of different varieties of Helianthus tuberosus to salt stress in yellow river delta[J]. Journal of Nuclear Agricultural Sciences, 2013, 27(11): 1771–1776. DOI: 10.11869/hnxb.2013.11.1771 (in Chinese) |




