文章信息
- 何辉, 乔绪稳, 陈瑾, 于晓明, 张元鹏, 侯继波, 郑其升, 孙卫东
- HE Hui, QIAO Xuwen, CHEN Jin, YU Xiaoming, ZHANG Yuanpeng, HOU Jibo, ZHENG Qisheng, SUN Weidong
- 密码子优化的猪瘟病毒荧光抗体的表达及初步应用
- Expression and preliminary application of gene optimized fluorescent antibody against Classical swine fever virus
- 南京农业大学学报, 2017, 40(2): 295-301
- Journal of Nanjing Agricultural University, 2017, 40(2): 295-301.
- http://dx.doi.org/10.7685/jnau.201605030
-
文章历史
- 收稿日期: 2016-05-18
2. 国家兽用生物制品工程技术研究中心, 江苏 南京 210014
2. National Research Center of Veterinary Biological Engineering and Technology, Nanjing 210014, China
猪瘟是由猪瘟病毒 (Classical swine fever virus, CSFV) 引起的一种急性、热性、高度接触性的传染病, 对世界养猪业造成了极大的经济损失[1], 世界动物卫生组织 (OIE) 将其列为A类动物传染病[2], 我国也将此病列为一类动物疫病。近年来, 猪瘟的流行趋势发生了很大的变化, 呈现典型猪瘟和非典型猪瘟共存, 隐性感染和持续感染并现, 给猪瘟的防控带来很大的困难[3], 这使得CSFV病原检测在防控猪瘟流行中的作用变得越来越重要。病毒的分离鉴定是诊断猪瘟最准确的方法[4], 然而, 由于猪瘟病毒在感染的细胞中增殖滴度低且不能产生细胞病理变化, 我们不能通过细胞形态的改变判定是否感染猪瘟病毒。免疫荧光法因具有操作简单、敏感、特异、直观的特点, 既可用于检测不同部位病料组织切片中CSFV, 又可以检测体外培养细胞中的CSFV[5], 是检测猪瘟病毒比较理想的方法。目前, 实验室主要通过间接免疫荧光法 (indirect immunofluorescence assays, IFA) 对分离的猪瘟病毒进行鉴定, 该方法虽然在猪瘟的诊断和猪瘟病毒滴度测定的作用很大, 但是其所用的猪瘟病毒单克隆抗体制备周期长, 操作繁琐, 生产成本较高, 不利于免疫荧光法在猪瘟病毒分离鉴定上的推广。本试验利用大肠杆菌表达系统对猪瘟病毒纳米抗体和绿色荧光蛋白进行共表达, 表达得到的荧光抗体可用于直接免疫荧光 (direct immunofluorescence assays, DFA), 与间接免疫荧光相比, 该方法具有操作时间短、试验误差小、抗体容易得到、制备成本低等优点。
绿色荧光蛋白 (GFP) 是一种存在于水母、水媳和珊瑚等腔肠动物体内的生物发光蛋白。该蛋白由Shimomura等[6]于1962年从维多利亚多管水母中分离纯化出来, 并于1994年被Chalfie等[7]在大肠杆菌中成功表达。GFP蛋白因具有荧光性质稳定、生色团形成不需要辅助因子和底物、可用于标记活细胞蛋白质等优点, 已经逐渐取代了许多其他常规荧光标记物[8]。此外, GFP具有分子量小、与目的蛋白融合而不改变目的蛋白的性质和定位的特点, 研究人员可利用基因工程技术表达出含有绿色荧光的融合蛋白用于对肿瘤的监测和疾病的检测[9]。单结构域重链可变区抗体又称为纳米抗体, 该抗体来源于骆驼科动物的血清, 只具有单条重链的可变区[10]。虽然纳米抗体不具有天然的轻链, 但是它依靠3个更长、更灵活的互补决定区 (CDRs) 使得它比一般抗体更特异、高亲和地与抗原结合[11-12]。纳米抗体因其有单个结构域特性, 它的相对分子质量只有大约15×103, 因此其更容易在大肠杆菌中进行可溶性表达。此外, 纳米抗体在不同pH值下生物活性非常稳定[13-14]。这使得纳米抗体越来越被广泛地研究和运用。
本文主要通过大肠杆菌表达系统对猪瘟病毒的纳米抗体与EGFP进行融合表达, 以获得猪瘟荧光抗体 (VHH), 利用镍柱亲和层析的方法对可溶性荧光抗体纯化和浓缩, 通过特异性鉴定试验、重复性试验和直接免疫荧光试验来验证VHH是否具备运用于CSFV直接免疫荧光检测的潜在价值。
1 材料与方法 1.1 病毒、细胞和试剂猪瘟兔化弱毒 (attenuated lapinized Chinese strain of CSFV, C-strain)、伪狂犬病病毒 (Porcine pseudorabies virus, PRV)、猪细小病毒 (Porcine parvovirus virus, PPV)、猪圆环病毒2型 (Porcine circovirus type 2, PCV-2) 均由国家兽用生物制品工程技术研究中心鉴定、保存; 猪瘟病毒纳米抗体基因序列来源于文献[15], EGFP基因序列获取于NCBI (GenBank登录号:U55762.1), 融合基因VHH-EGFP的优化合成由南京金斯瑞生物科技有限公司完成, 原核表达载体pET32a (+)、宿主菌BL21、DH5α均为国家兽用生物制品工程技术研究中心保存; PK15细胞由国家兽用生物制品工程技术研究中心传代、保存。限制性内切酶、T4 DNA连接酶购自大连TaKaRa公司; 质粒提取试剂盒及胶回收试剂盒购自上海捷瑞生物工程有限公司; 异丙基硫代半乳糖苷 (IPTG) 购自Sigma公司; Ni-NTA His·Bind Resin纯化树脂购自GE公司; 抗His标签单抗、HRP标记羊抗鼠二抗、FITC标记羊抗鼠二抗以及BCA蛋白浓度测定试剂盒购自碧云天生物技术研究所; 猪瘟单克隆抗体BIO 275购自BioX Diagnostics; DAB显色试剂盒购自武汉博士德生物工程有限公司; 其他化学试剂均为国产或进口分析纯。
1.2 重组质粒的构建用限制性内切酶NdeⅠ和BamHⅠ对pUC57-VHH-EGFP和pET32a (+) 进行双酶切, 酶切后分别回收目的片段VHH-EGFP与pET32a (+) 载体片段, 回收得到的样品在T4 DNA连接酶作用下16 ℃过夜, 连接产物转化E.coli DH5α感受态细胞, 涂布含有氨苄青霉素的LB平板, 37 ℃倒置培养过夜。挑取单菌落接种含有氨苄青霉素的液体LB培养基扩大培养, 提取质粒, 用NdeⅠ和BamHⅠ酶切, 凝胶电泳鉴定, 阳性质粒命名为pET-VHH-EGFP。
1.3 荧光抗体的表达与鉴定 1.3.1 荧光抗体的表达将鉴定正确后的重组质粒pET-VHH-EGFP转化入表达菌BL21, 涂布氨苄青霉素LB平板筛选阳性菌株, 挑取阳性单克隆菌落接种于3 mL含氨苄青霉素的液体LB培养基, 于摇床37 ℃过夜培养。按照1:100的比例将过夜培养得到的新鲜种子液接入到含氨苄青霉素的液体LB培养基中, 于37 ℃、220 r·min-1条件下培养至菌体A600值为0.6, 加入终浓度为0.4 mmol·L-1的IPTG, 于15 ℃、190 r·min-1诱导24 h。按照相同的方法将pET32a (+) 空载体转入BL21中作为对照组进行诱导表达。诱导表达后的混合物12 000 r·min-1离心10 min得到表达菌体, 菌体沉淀用PBS洗涤2次, 最后用Binding Buffer对菌体沉淀进行等体积重悬。重悬后的菌体进行高压破碎, 随后对破碎菌体12 000 r·min-1离心15 min, 收集上清夜和沉淀。
1.3.2 荧光抗体蛋白可溶性鉴定取重悬后对照菌株、pET-VHH-EGFP/BL21全菌各100 μL, 加入25 μL 5×SDS Loading Buffer于金属浴100 ℃作用10 min, 并按照相同的方法处理pET-VHH-EGFP/BL21破碎后上清液和沉淀。煮沸后的样品经120 g·L-1 SDS-PAGE电泳以鉴定荧光蛋白的表达及可溶性。
1.3.3 Western-blot鉴定取1.3.2处理的样品进行120 g·L-1 SDS-PAGE电泳, 通过半干转转印仪将蛋白条带转印到PVDF膜上; 转印后的PVDF膜用5%脱脂乳于37 ℃封闭1 h, 后弃去脱脂乳并用TBST漂洗10 min。用含有2% BSA TBST溶液稀释His单抗 (1:5 000), 于37 ℃孵育PVDF膜1 h, 随后用TBST充分漂洗5次, 每次洗涤8 min, 再用含2% BSA的TBST缓冲液稀释HRP标记的羊抗鼠二抗 (1:10 000), 37 ℃孵育1 h, TBST缓冲液充分漂洗5次, 每次8 min; 按照DAB试剂盒说明书显色。
1.4 重组蛋白的纯化及定量用5倍体积的蒸馏水对镍柱进行冲洗, 用5倍体积的Binding Buffer对镍柱进行平衡。对pET-VHH-EGFP/BL21诱导菌破碎离心后取蛋白上清液过0.45 μm滤器, 滤后上清液缓慢过镍柱, 用5 mL分别含5、10、20、30 mmol·L-1咪唑的Washing Buffer对镍柱进行洗涤, 用5 mL含200 mmol·L-1咪唑的Elution Buffer洗脱目的蛋白。收集蛋白各浓度洗涤液以及洗脱液进行120 g·L-1的SDS-PAGE电泳, 对纯化后的蛋白样品采用BCA蛋白定量试剂盒进行定量。
1.5 重组蛋白直接免疫荧光检测 (DFA) 方法的建立 1.5.1 猪瘟病毒的培养将长成单层的PK15细胞, 用0.5 g·L-1胰酶, 于37 ℃作用2 min, 至细胞出现空隙后弃消化液并加入生长液, 反复吹打至细胞分散成单个。然后将细胞分装至96孔板, 于37 ℃细胞培养箱培养36 h, 弃细胞培养液, 接入CSFV吸附1 h后, 弃病毒液, 加入3%FBS DMEM细胞维持液培养72 h。
1.5.2 免疫荧光试验病毒培养72 h后弃细胞维持液, 用PBS洗涤3次; 参照文献[16-17]的方法, 每孔加入100 μL预冷的固定液 (60%丙酮、40%乙醇), 置于-20 ℃固定20 min; 弃去固定液, 用PBS洗涤3次, 每孔加入猪瘟荧光抗体0.1 mL, 置于37 ℃孵育60 min, 用PBS洗涤3次, 荧光显微镜观察结果。
1.5.3 CSFV接种浓度优化培养PK15细胞至细胞长至80%, 将1×106 TCID50·mL-1 CSFV兔化弱毒进行10-7~10-1梯度稀释后接种100 μL至PK15细胞, 每个浓度梯度3个重复。同时设立不接病毒组作为阴性对照。于37 ℃、5%二氧化碳条件下吸附1 h; 去除病毒液, 加入细胞维持液, 再次放入细胞培养箱37 ℃、5%二氧化碳条件下培养; 72 h后进行免疫荧光检测, 根据荧光细胞的数量及荧光强弱确定最适病毒接种浓度。
1.5.4 荧光抗体工作浓度优化以优化的最适病毒接种浓度 (10-3稀释病毒) 接种细胞, 同时设立不接种病毒组作为对照。将定量后的荧光抗体浓度调整为200 μg·mL-1, 将荧光抗体稀释到工作浓度梯度20、10、5和2.5 μg·mL-1。每个浓度梯度3个重复, 以不接种CSFV的对照组孵育20 μg·mL-1的荧光抗体, 选取荧光清晰明亮且稀释度数最大的为最佳工作浓度。
1.5.5 荧光抗体孵育时间的优化按照上述确定的最佳反应条件, 进行直接免疫荧光试验, 荧光抗体孵育的时间分别为30、45和60 min, 观察孵育时间对荧光抗体效力的影响, 确定最佳的孵育时间。
1.5.6 荧光抗体特异性鉴定制备长成单层的PK15细胞培养板分别接种伪狂犬病毒 (PRV)、猪细小毒病 (PPV)、圆环病毒2型 (PCV2)、猪瘟病毒, 并设立不接种病毒的空白对照组。按照最佳荧光抗体工作浓度进行直接免疫荧光试验, 在荧光显微镜下观察各组是否产生荧光及荧光的强弱, 并与接种CSFV病毒组进行荧光数量及强弱的比较。
1.5.7 重复性试验取相同批次的细胞培养板, 用同一批的荧光抗体, 相同条件下在不同时间进行荧光试验, 观察荧光强弱是否改变, 检测是否具有重复性。
1.5.8 与间接免疫荧光试验的比较按照1.5.1节的方法培养PK15细胞并接种10-7~10-1梯度稀释后的猪瘟兔化弱毒100 μL, 每个浓度设置9个重复并均分为A、B、C 3个组。A组按照优化的荧光抗体工作浓度和孵育时间进行直接免疫荧光试验; B组分别孵育猪瘟单抗 (1:100稀释) 和FITC标记的羊抗鼠二抗 (1:500稀释) 进行间接免疫荧光试验; C组作为空白对照组。
2 结果与分析 2.1 重组表达质粒的酶切鉴定将构建完成的质粒pET-VHH-EGFP用NdeⅠ和BamHⅠ进行双酶切, 酶切后产物在含有溴化乙锭的10 g·L-1琼脂糖凝胶上进行电泳, 在紫外线下观察 (图略)。结果显示:与pET32a质粒相比, pET-VHH-EGFP酶切后在1 100 bp位置有一条明显的特异性条带, 与目的条带大小相符, 证明pET-VHH-EGFP表达载体构建成功。
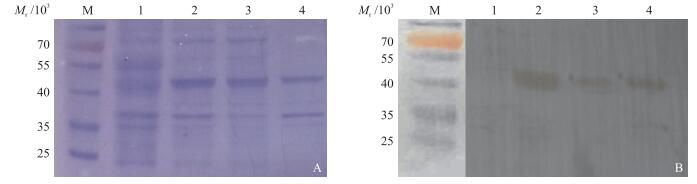
2.2 重组蛋白表达的鉴定对1.3.2节处理的样品进行120 g·L-1 SDS-PAGE电泳。结果 (图 1-A) 显示:pET-VHH-EGFP/BL21表达菌在相对分子质量40×103位置有1个明显特异性条带。用His抗体作为一抗、羊抗鼠抗体作为二抗进行Western blot分析表明, pET-VHH-EGFP/BL21诱导后全菌、破碎后上清液以及沉淀均在40×103位置出现特异性条带, 而诱导后的对照菌株不显现该条带, 证明该位置蛋白即为要表达的目的蛋白。通过对比pET-VHH-EGFP/BL21诱导菌和对照菌可知, 荧光抗体成功在大肠杆菌中表达, 并且表达含量较高, 但是分析pET-VHH-EGFP/BL21诱导菌破碎后上清液和沉淀, 发现表达的荧光抗体只有部分可溶, 其主要以包涵体形式表达 (图 1-B泳道3、4)。
|
图 1 SDS-PAGE (A) 和Western blot (B) 分析荧光抗体的可溶性 Figure 1 VHH solubility identification by SDS-PAGE (A) and Western blot (B) M.蛋白分子质量标准品; 1.空载体全菌; 2.诱导后全菌; 3.诱导菌破碎后上清液; 4.诱导菌破碎后沉淀 M.Molecular size markers; 1.Whole bacterium pET32a/BL21 after IPTG-induced; 2.Whole bacterium pET-VHH-EGFP/BL21 after IPTG-induced; 3-4.Supernatant, inclusion body of pET-VHH-EGFP/BL21 with IPTG induction after high pressure crushing |
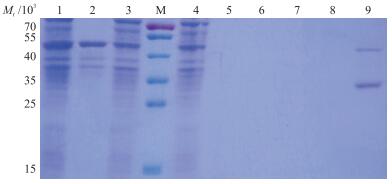
对重组蛋白纯化过程中各咪唑浓度的洗涤液、洗脱液样品处理并进行120 g·L-1 SDS-PAGE电泳分析, 结果如图 2所示:诱导菌pET-VHH-EGFP/BL21破碎后的上清液经过镍柱纯化和各浓度Washing Buffer的洗涤后仍含有2条明显的蛋白条带, 这2条条带分别位于相对分子质量40×103、35×103处, 与预期纯化后只有1条相对分子质量为40×103目的条带不一致。通过与对照菌株对比发现, 相对分子质量为35×103, 蛋白为BL21本体表达蛋白, 该蛋白能非特异性与镍柱结合且结合能力较强, 当使用200 mmol·L-1咪唑的洗脱液时才能与重组蛋白一起被洗脱, 这与该宿主菌表达的其他蛋白的镍柱纯化试验结果一致, 而相对分子质量40×103位置蛋白为纯化后的目的蛋白。对纯化后的蛋白用BCA试剂盒进行蛋白定量, 得出纯化蛋白的总浓度为0.97 mg·mL-1, 通过对洗脱样品电泳图进行薄层扫描分析表明, 重组蛋白占总蛋白比例约为23%, 即重组蛋白浓度为223.1 μg·mL-1。
|
图 2 荧光抗体的镍柱纯化 Figure 2 Purified the VHH with nickel column M.蛋白分子质量标准品; 1.诱导后全菌; 2.诱导菌破碎后沉淀; 3.诱导菌破碎后上清液; 4.破碎后上清过镍柱流穿液; 5-9.分别为含5、10、20、30和200 mmol·L-1咪唑的洗脱液。 M.Molecular size markers; 1.Whole bacterium pET-VE/BL21 after IPTG-induced; 2-3.Inclusion body, supernatant of pET-VE/BL21 with IPTG induction after high pressure crushing; 4.The outflow of Ni affinity column; 5-9.The elution of the Ni affinity column with 5, 10, 20, 30 and 200 mmol·L-1 imidazole, respectively. |
接种不同稀释度猪瘟兔化弱毒病毒的PK15细胞均生长良好, 但是与荧光孵育后荧光的强度和荧光点数量随着接种猪瘟病毒的含量增加而递增, 而不接种PK15的对照组细胞不出现荧光, 根据显微镜镜检结果, 当猪瘟病毒稀释度达在10-1~10-3时, 荧光数量清晰明亮, 因此判定10-3为接种猪瘟病毒最佳稀释度。
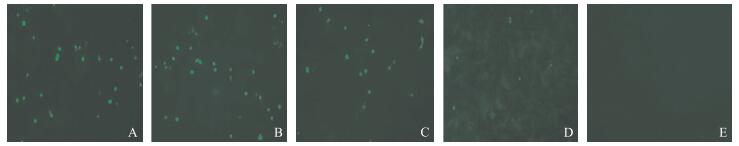
2.4.2 荧光抗体工作浓度的优化镜检结果表明:4个工作浓度的荧光抗体孵育猪瘟病毒感染的PK15细胞后均出现特异性绿色荧光, 当荧光抗体工作浓度为20和10 μg·mL-1时, 显微镜下出现的荧光点数量比其他稀释度更多、荧光点更清晰明亮 (图 3)。因此认为10 μg·mL-1是荧光抗体的最佳工作浓度。
|
图 3 荧光抗体工作浓度的优化 Figure 3 Optimized the working concentration of VHH by gradient dilution A~D.20、10、5和2.5 μg·mL-1荧光抗体分别孵育感染CSFV的PK15细胞; E.20 μg·mL-1荧光抗体孵育正常PK15细胞 A-D.Incubated PK15 cells which infected CSFV with 20, 10, 5 and 2.5 μg·mL-1VHH respectively; E.Incubated normal PK15 cells with 20 μg·mL-1 VHH |
试验结果表明 (图略):荧光抗体作用45和60 min都能达到很好效果, 接种CSFV病毒细胞孔有数量较多且清晰的特异性绿色荧光, 而孵育时间达到30 min时荧光点清晰, 但是荧光数量不如45和60 min时多, 因此选择45 min作为最佳作用时间。
2.4.4 荧光抗体特异性试验镜检结果表明:接种伪狂犬病毒 (PRV)、猪细小毒病 (PPV)、圆环病毒2型 (PCV2) 及不接种病毒的PK15细胞均不出现特异性绿色荧光或少量微弱荧光点, 而接种CSFV病毒的PK15细胞出现数量较多且亮度较强的绿色荧光 (图 4), 说明本文表达的猪瘟荧光抗体与其他病毒无交叉反应, 具有良好的特异性。
|
图 4 荧光抗体的特异性检验 Figure 4 Evaluated the specificity of VHH by crossing reaction with other virus A~E.荧光抗体分别接种孵育CSFV、PCV2、PRV、PPV的PK15细胞和正常PK15细胞。 A-E.VHH incubated with PK15 cell which infected CSFV, PCV2, PRV, PPV and normal PK15 cells. |
通过对相同批次抗原板在相同条件下不同时间的检测, 结果完全相同, 说明本试验建立的方法重复性良好。
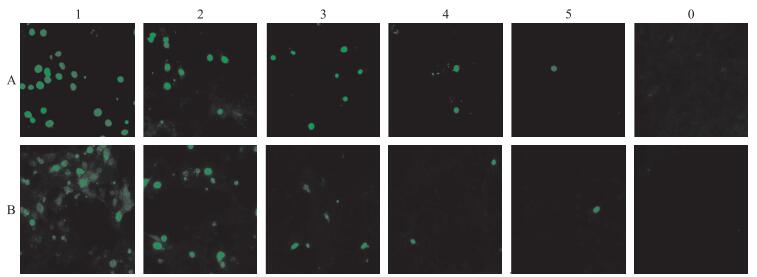
2.4.6 与间接免疫荧光试验的比较用表达的荧光抗体VHH和商品化的猪瘟单克隆抗体分别孵育相同稀释梯度的猪瘟病毒, 并设立不接种病毒的PK15细胞作为空白对照。荧光显微镜镜检结果 (图 5) 表明:随着CSFV病毒稀释梯度的升高, 荧光强度相应减弱, 空白对照组不出现荧光。相同病毒稀释浓度下, 用VHH进行直接免疫荧光检测与商品化的猪瘟单克隆抗体荧光强度相似, 但是直接免疫荧光清晰度要明显高于间接免疫荧光。
|
图 5 直接免疫荧光 (A) 与间接免疫荧光 (B) 试验效果比较 Figure 5 The effectiveness comparison between direct immunofluorescence assays (DFA)(A) and indirec immunofluorescence assay (IFA)(B) A1~A5.VHH分别孵育不同浓度梯度 (10-3~10-7) 的CSFV后进行直接免疫荧光; B1~B5.猪瘟单克隆抗体孵育不同浓度梯度 (10-1~10-7) 的CSFV进行间接免疫荧光; A0、B0.不含CSFV的空白对照组。 A1-A5.VHH was incubated with different concentrations (10-3-10-7) of CSFV to develop DFA; B1-B5.Monoclonal antibodies were incubated with different concentrations (10-1-10-7) of CSFV to develop IFA; A0, B0.PK15 cell without CSFV. |
猪瘟是由猪瘟病毒引起的一种在全世界分布的急性、热性和高度接触性传染病。目前猪瘟的确诊主要依靠实验室检测的方法[17], 其中荧光抗体法具有特异性强、操作简便、诊断快速、结果直观等优点, 非常适用于对猪瘟的诊断。由于猪瘟病毒在细胞上增殖不产生细胞病理变化, 而荧光抗体可在荧光显微镜下发光的特点, 使研究人员可直观对猪瘟病毒在细胞上的动态分布进行定位并可运用于新型疫苗的效力评估[18]。此外, 对发病猪不同组织制作冷冻切片可对猪瘟病毒在各组织中的分布进行定位, 从而对猪瘟病毒的感染特性和致病机制进行相关的研究[5, 19]。
本试验成功构建了猪瘟荧光抗体的原核表达重组质粒, 根据SDS-PAGE蛋白电泳和Western blot对诱导菌高压破碎后的上清液、沉淀分析可知, 荧光抗体在大肠杆菌中成功实现可溶性表达。运用镍柱纯化的方法对破碎后菌体上清液进行纯化可得到浓度约为223.1 μg·mL-1的荧光抗体, 通过将该荧光抗体设置不同的浓度梯度孵育感染CSFV的PK15细胞, 结果表明当荧光抗体工作浓度为20和10 μg·mL-1时, 出现的荧光点数量比其他稀释度更多, 荧光点更清晰明亮, 因此判定10 μg·mL-1的荧光抗体的浓度为最佳工作浓度。以最佳工作浓度荧光抗体孵育接种了CSFV、PRV、PPV、PCV2及不接种病毒的PK15细胞对荧光抗体的特异性进行鉴定, 镜检结果表明, 只有接种CSFV病毒的PK15细胞出现明显且亮度较强的绿色荧光, 而其他组不出现或出现少数微弱的荧光点, 说明本试验表达的猪瘟荧光抗体与其他病毒无交叉反应, 纯化后得到的荧光抗体具有良好的特异性。重复性试验和对疑似CSFV病料检测结果证明, 本试验建立的方法重复性良好且准确、可靠。通过对荧光抗体、商品化猪瘟单克隆抗体进行免疫荧光试验发现, 相同病毒稀释浓度下, 用VHH进行直接免疫荧光检测与商品化的猪瘟单克隆抗体荧光强度相差不大, 但是直接免疫荧光清晰度要明显高于间接免疫荧光。与商品化的猪瘟单克隆抗体相比, VHH具有生产操作简单、制备周期短和成本低等优点, 具备运用于CSFV的直接免疫荧光检测的潜在价值。
本试验通过大肠杆菌表达系统, 成功得到特异性良好的荧光抗体, 但是通过大肠杆菌表达的荧光抗体仍然存在很多不足:虽然该荧光抗体在本试验中得到可溶性表达, 但是主要以包涵体表达。破碎上清液经镍柱纯化后得到2条明显的蛋白条带, 通过与对照菌株进行对比, 发现相对分子质量为35×103的蛋白为BL21本体表达的蛋白。为了使纯化的荧光抗体纯度更高, 我们将在后续的试验中更换表达菌株, 去除杂蛋白的干扰。此外, 与诱导菌破碎后上清液相比, 镍柱纯化后的荧光抗体浓度还不够理想, 并且在前期的镍柱纯化过程中, 100 mmol·L-1浓度的咪唑缓冲液就能将一部分目的蛋白洗脱下来, 至200 mmol·L-1浓度时目的蛋白已经完全被洗脱下来, 但同时杂蛋白也被洗脱, 这可能是因为荧光抗体中的His标签吸附能力较弱, 有研究表明通过改变标签的位置或者增加标签的数量可提高荧光蛋白的挂柱能力[20-21], 在后续的试验中我们也将通过这些方法进行标签挂柱能力的优化以获得浓度和纯度更高的荧光抗体。总之, 本试验成功实现荧光抗体重组蛋白在大肠杆菌中的可溶性表达, 纯化后得到的荧光抗体具有良好的特异性, 可用于建立CSFV抗原直接免疫荧光的检测方法。
| [1] | Lin G J, Deng M C, Chen Z W, et al. Yeast expressed classical swine fever E2 subunit vaccine candidate provides complete protection against lethal challenge infection and prevents horizontal virus transmission[J]. Vaccine, 2012, 30: 2336–2341. DOI: 10.1016/j.vaccine.2012.01.051 |
| [2] | Luo Y Z, Li S, Sun Y, et al. Classical swine fever in China:a minireview[J]. Veterinary Microbiology, 2014, 172(1-2): 1–6. DOI: 10.1016/j.vetmic.2014.04.004 |
| [3] |
陈溥言.
兽医传染病学[M]. 北京: 中国农业出版社, 2012: 210.
Chen P Y. Veterinary Lemology[M]. Beijing: China Agriculture Press, 2012: 210. (in Chinese) |
| [4] | Greiser-Wilke I, Blome S, Moennig V. Diagnostic methods for detection of Classical swine fever virus:status quo and new developments[J]. Vaccine, 2007, 25(30): 5524–5530. DOI: 10.1016/j.vaccine.2006.11.043 |
| [5] |
许保疆, 游一, 郭成留, 等. 单克隆抗体间接免疫荧光检测猪瘟病毒方法的建立[J].
中国兽医学报, 2010, 30(12): 1566–1570.
Xu B J, You Y, Guo C L, et al. Establishment of indirect immunofluorescence assy for detecting Classical swine fever virus[J]. Chinese Journal of Veterinary Science, 2010, 30(12): 1566–1570. (in Chinese) |
| [6] | Shimomura O, Johnson F H, Saiga Y. Extraction, purification and properties of aequorin, a bioluminescent protein from the luminous hydromedusan, Aequorea[J]. Journal of Cellular and Comparative Physiology, 1962, 59: 223–239. DOI: 10.1002/(ISSN)1553-0809 |
| [7] | Chalfie M, Tu Y, Euskirchen G, et al. Green fluorescent protein as a marker for gene expression[J]. Science, 1994, 263: 802–805. DOI: 10.1126/science.8303295 |
| [8] |
陈航, 缪生俊, 王蒴, 等. 抗人大肠癌单链抗体与绿色荧光蛋白融合基因的构建和表达[J].
解剖科学进展, 2012, 18(3): 208–211.
Chen H, Miao S J, Wang S, et al. Construction and expression of recombinant fusion protein of single chain Fv antibody fragment against human colorectal carcinoma and green fluorescent protein[J]. Progress of Anatomical Sciences, 2012, 18(3): 208–211. (in Chinese) |
| [9] |
高国辉, 黄奇迪, 王金丹, 等. Anti-HER2-ScFv-GFP融合蛋白靶向结合体外乳腺癌细胞表面受体的研究[J].
中国细胞生物学报, 2011, 33(5): 485–491.
Gao G H, Huang Q D, Wang J D, et al. The study of targeting selectivity and binding the surface of breast cancer cells with the fusion protein anti-HER2-ScFv-GFP in vitro experiments[J]. Chinese Journal of Cell Biology, 2011, 33(5): 485–491. (in Chinese) |
| [10] | Hamers-Casterman C, Atarhouch T, Muyldermans S, et al. Naturally occurring antibodies devoid of light chains[J]. Nature, 1993, 363: 446–448. DOI: 10.1038/363446a0 |
| [11] | de Genst E, Silence K, Decanniere K, et al. Molecular basis for the preferential cleft recognition by dromedary heavy-chain antibodies[J]. Proc Nalt Acad Sci USA, 2006, 103: 4586–4591. DOI: 10.1073/pnas.0505379103 |
| [12] | Desmyter A, Transue T R, Ghahroudi M A, et al. Crystal structure of a camel single-domain VH antibody fragment in complex with lysozyme[J]. Nat Struct Biol, 1996, 3: 803–811. DOI: 10.1038/nsb0996-803 |
| [13] | Dumoulin M, Conrath K, van Meirhaeghe A, et al. Single-domain antibody fragments with high conformational stability[J]. Protein Science, 2002, 11: 500–515. |
| [14] | Harmsen M M, van Solt C B, van Zijderveld-van Bemmel A M, et al. Selection and optimization of proteolytically stable llama single-domain antibody fragments for oral immunotherapy[J]. Applied Genetics and Molecular Biotechnology, 2006, 72: 544–551. |
| [15] |
中国农业科学院兰州兽医研究所. 双峰驼源抗猪瘟兔化弱毒疫苗株E2抗原重链抗体VHH和用途: 中国, 103467599[P]. 2013-12-25.
Lanzhou Veterinary Research Institute, Chinese Academy of Agricultural Sciences. The research and application of bactrian camel source anti-C-strain E2 antigen heavy chain antibody VHH:China, 103467599[P]. 2013-12-25(in Chinese). |
| [16] |
张韧. 猪瘟病毒荧光抗体的制备及应用[D]. 武汉: 华中农业大学, 2013.
Zhang R. Preparation and preliminary application of fluorescent antibody to classical swine fever virus[D]. Wuhan:Huazhong Agricultural University, 2013(in Chinese with English abstract). |
| [17] |
张艳英, 高桂生, 高光平, 等. 猪瘟病毒3种检测方法的比较[J].
中国畜牧兽医, 2013, 40(3): 205–208.
Zhang Y Y, Gao G S, Gao G P, et al. Comparison of three detection methods for Classical swine fever virus[J]. Chinese Animal Husbandry and Veterinary Medicine, 2013, 40(3): 205–208. (in Chinese) |
| [18] |
戴志红, 蒋卉, 李翠, 等. 用间接免疫荧光检测方法评价猪瘟活疫苗效力的研究[J].
中国兽药杂志, 2014, 48(1): 34–37.
Dai Z H, Jiang H, Li C, et al. Using an indirect immunofluorescence assay for evaluating the efficacy of live Classical swine fever virus vaccine (C strain)[J]. Chinese Journal of Veterinary Medicine, 2014, 48(1): 34–37. (in Chinese) |
| [19] |
景娇, 张小敏, 何丹妮, 等. 猪瘟病毒Core蛋白的原核表达和抗体制备及应用[J].
畜牧与兽医, 2015, 47(6): 7–11.
Jing J, Zhang X M, He D N, et al. Prokaryotic expression of Classical swine fever virus Core protein and application of its polyclonal antibody[J]. Animal Husbandry and Veterinary Medicine, 2015, 47(6): 7–11. (in Chinese) |
| [20] |
许艳, 万敏, 张培英, 等. 六聚组氨酸在重组蛋白中的位置对镍柱亲和层析的影响[J].
医学分子生物学杂志, 2004, 1(2): 90–93.
Xu Y, Wan M, Zhang P Y, et al. Effects of position of hexahistine in recombinant protein on nickel chelating affinity chromatography[J]. Journal of Medical Molecular Biology, 2004, 1(2): 90–93. (in Chinese) |
| [21] | Xu C G, Fan X J, Fu Y J, et al. Effect of location of the His-tag on the production of soluble and function Buthus martensii Karsch insect toxin[J]. Protein Expression and Purification, 2008, 59(1): 103–109. DOI: 10.1016/j.pep.2008.01.009 |




