文章信息
- 李晓亮, 李翔, 张征, 雷治海
- LI Xiaoliang, LI Xiang, ZHANG Zheng, LEI Zhihai
- 神经介素U在体外对猪淋巴细胞活性及自然杀伤细胞活性的影响
- Effects of neuromedin U on lymphocytes and nature killer cell activities of pigs in vitro
- 南京农业大学学报, 2017, 40(1): 157-162
- Journal of Nanjing Agricultural University(Social Science), 2017, 40(1): 157-162.
- http://dx.doi.org/10.7685/jnau.201512017
-
文章历史
- 收稿日期: 2015-12-22
神经介素U(neuromedin U,NMU),又称神经调节肽U,1985年首次从猪脊髓中分离提纯[1],与神经介素B、C,K、L、N、S一起组成神经介素家族。NMU主要有25肽和8肽两种形式,即NMU-25和NMU-8[2]。NMU在动物机体内分布广泛,主要有2种受体,分别为NMUR1和NMUR2。NMUR1主要分布于泌尿、生殖系统等外周组织,NMUR2主要分布于中枢神经系统[3]。研究发现NMU参与调控摄食与肥胖[4-6]、热应激[7]、昼夜节律[8] 、抗抑郁与抗焦虑[9-10]、抗肿瘤[11]等方面,显示了NMU具有重要的生理作用。研究表明,NMU mRNA在抗原递呈细胞中表达,如单核细胞、树突细胞,其受体NMUR 1 mRNA在T细胞和自然杀伤(NK)细胞中表达,在其他免疫细胞中也有低表达,提示NMU及其受体系统在免疫方面也具有重要作用[12]。在体外,NMU可促进多种细胞因子的分泌与释放[13],并对巨噬细胞分泌IL-6起重要作用[14]。目前,关于NMU及其受体的基因克隆、分布定位和生理功能等方面的研究已有大量报道,但研究涉及物种相对较少,特别是有关NMU对猪免疫调控的研究鲜有报道。因此,本试验研究了NMU及其受体NMUR1和NMUR2在猪外周血淋巴细胞(peripheral blood lymphocytes,PBL)的表达及其蛋白的分布,并研究了NMU在体外对猪PBL的活性及NK细胞活性的影响,为了解NMU的生理功能提供理论和试验依据。
1 材料与方法 1.1 试验动物90日龄健康小梅山公猪,购自江苏省句容市农博园种猪场。
1.2 主要药物与试剂神经介素U(GL Biochem公司,纯度大于98%);RPMI-1640培养液(Hyclone公司);胎牛血清(FBS,Natocor公司);CCK-8试剂盒(Biosharp公司);二甲基亚砜(DMSO,Amresco公司);Trizol试剂、反转录酶(M-MLV)、RNA酶抑制剂、dNTPs、寡聚脱氧胸腺嘧啶核苷酸(Oligo dT18) 、rTaq DNA 聚合酶(TaKaRa公司);焦碳酸二乙酯(DEPC)和琼脂糖(南京生兴生物技术有限公司);DNA marker(DL2000) 、DNA 胶回收试剂盒(Axygen公司);NMU抗体为兔抗猪多克隆抗体(LSBio,LS-C9260) ;NMUR1抗体为兔抗人多克隆抗体(Bioss,bs-11420R);NMUR2抗体为兔抗人多克隆抗体(Bioss,bs-11421R);即用型 SABC 免疫组化染色试剂盒(山羊抗兔)(武汉博士德生物技术有限公司);其他试剂均为国产分析纯。NMU、NMUR 1、NMUR2 和GAPDH引物由上海英骏生物技术有限公司合成。猪外周血淋巴细胞分离液(TBD,LTS1110) 、K562细胞为本实验室长期保存细胞。
1.3 猪外周血淋巴细胞的分离从猪前腔静脉无菌采集血液,肝素抗凝后与等体积的RPMI-1640培养液混匀,缓慢加至等体积的淋巴细胞分离液,恢复至室温。2 000 r·min-1 离心20 min,收集白膜层细胞置于新离心管中,加入5倍体积的RPMI-1640后混匀,1 500 r·min-1 离心10 min,弃上清液后洗涤2~3次,最后用适量的10% FBS RPMI-1640重悬细胞,调整细胞密度为5×106 mL-1,置于塑料培养瓶中培养2 h,弃去贴壁细胞,即为外周血淋巴细胞。调整细胞密度为5×106 mL-1后用台盼蓝染色,检测细胞活率大于95%后待用。
1.4 K562细胞的培养人慢性髓系白血病细胞株K562细胞,加入含有10%胎牛血清的RPMI-1640培养液中,37 ℃、5% CO2条件下培养,常规换液、传代,培养至对数生长期后,作为靶细胞用于CCK-8试剂盒检测NK细胞活性。
1.5 RT-PCR反应 1.5.1 细胞总RNA的提取取上述分离得到的外周血淋巴细胞悬液2 mL,2 000 r·min-1离心 5 min后弃上清液,0.01 mol·L-1PBS洗涤2次后按照Trizol说明书提取细胞总RNA。用12 g ·L-1变性琼脂糖凝胶电泳检测RNA条带的完整性。核酸定量仪检测RNA的纯度及浓度后-70 ℃分装冻存。
1.5.2 RNA的反转录按照M-MLV反转录试剂盒的说明书,RNA反转录(RT)在无RNA酶的环境下按两步法进行。RT反应体系为10 μL,包括1 μg总RNA、0.4 μmol·L-1 Oligod T引物1 μL,加入ddH2O至7 μL,70 ℃变性5 min,立即放冰上冷却,再加5×M-MLV Buffer 2 μL、dNTP 0.5 μL 、RNA酶抑制剂0.25 μL、RTase M-MLV 0.25 μL,混匀后于42 ℃水浴60 min,72 ℃水浴10 min。反转录产物cDNA分装后于-20 ℃保存备用。
1.5.3 猪外周血淋巴细胞NMU、NMUR 1、NMUR2 cDNA部分序列片段的克隆根据本实验室杨桂红[15]克隆测得的猪NMU、NMUR 1、NMUR2 及GenBank数据库中GAPDH[16]的序列分别设计特异性引物,并交由上海英骏生物技术有限公司合成。PCR反应体系为25 μL,包含模板cDNA 1 μL,10×PCR Buffer 2.5 μL,2.5 mmol·L-1 dNTs 2 μL,Mg2+ 1.5 μL,20 pmol·L-1的上、下游引物各1 μL,1.0 U Taq DNA聚合酶0.25 μL,ddH2O补至25 μL。用DEPC水取代模板cDNA作对照,以检测是否有外源性DNA污染。使用混合组织样本进行引物验证及PCR反应条件和循环数的优化,摸索出最优PCR反应条件。反应所用的引物序列及条件见表 1。
| 基因Gene | 引物对序列(5′→3′)Primer pairs sequence | 退火温度/℃Annealing temperature | 产物片段长度/bpProduct size |
| NMU NMUR1 NMUR2 GAPDH | ATGCAGGGAGTCGCGAAC/CATTTTAAATGTAACCTTCTGATC TTTGATCTTGAGGACTTGAACTTGACCCAT/CGAACACCACGACCAGCACAAACA GTGGGAGTC GCTGGCAATA/CTGTGGGTTGTTCTGGGAGTGAGGTCGGAGTGAACGGATTTG/CAGTCTTCTGGGTGGCAGTGAT | 58 58 60 57 | 526 811 897 549 |
将PBL于1 000 r·min-1离心 10 min后,弃上清液;用0.01 mol·L-1 PBS洗涤2次后,用4%多聚甲醛室温固定15 min;用0.01 mol·L-1 PBS洗涤2次,得到细胞密度为2×106 mL-1的悬液;取30~50 μL细胞悬液滴加到多聚赖氨酸处理的载玻片上,室温风干后-20 ℃保存备用。
免疫组织化学染色(IHC)程序:干净的载玻片用新鲜配制的0.5% H2O2/甲醇溶液室温处理30 min;蒸馏水洗涤3次,滴加5% BSA封闭液,37 ℃作用30 min,倾去多余液体后滴加一抗(兔抗NMU多克隆抗体1:800稀释;兔抗NMUR1多克隆抗体1:500稀释;兔抗NMUR2多克隆抗体1:500稀释)。阴性对照组使用0.1 mol·L-1 PBS代替一抗。湿盒内4 ℃孵育过夜,37 ℃复温1 h,0.1 mol·L-1 PBS洗涤5次;滴加二抗(羊抗兔,SABC试剂盒),37 ℃孵育30 min,PBS洗涤5次;滴加SABC,37 ℃孵育30 min,PBS洗涤 5次;滴加DAB显色液(现用现配),室温显色5 min,显微镜下观察控制显色程度,并用蒸馏水终止显色反应;苏木精复染后梯度乙醇脱水,透明,中性树胶封片。
1.7 NMU对猪外周血淋巴细胞活性的影响调整1.3节中PBL细胞密度为2×106 mL-1,加入96孔细胞培养板中,每孔200 μL,分别加入终浓度为0.01、0.1、1、10、100和1 000 nmol·L-1 NMU(用RPMI-1640培养液稀释),对照组加入RPMI-1640培养液,每组5个重复,置于37 ℃、5% CO2培养箱内孵育44 h,加入20 μL CCK-8,继续孵育4 h后,用酶标仪检测各孔A450值。按下述公式计算淋巴细胞活性[17]。
| $细胞活性 = \left[ {1 - \left( {{A_{450\left( 加药 \right)}} - {A_{450\left( 空白 \right)}}} \right)} \right]/\left[ {{A_{450\left( 未加药对照 \right)}} - {A_{450\left( 空白 \right)}}} \right] \times 100\% $ |
|
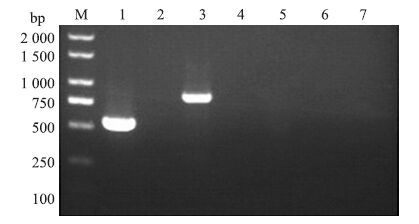
图 1 猪外周血淋巴细胞(PBL)中NMU、NMUR 1 和NMUR2 mRNA RT-PCR产物电泳图 Figure 1 Electrophoresis of the RT-PCR products of NMU, NMUR 1 and NMUR2 mRNA in the peripheral blood lymphocytes(PBL)of pigs 1.GAPDH;2.NMU;3.NMUR 1 ;4.NMUR 2 ;5~7.分别为NMU、NMUR 1和NMUR2 的阴性对照Negative control of NMU,NMUR 1 and NMUR2 ;M.DNA marker(DL2000) |
调整PBL细胞密度为2×106 mL-1,以每孔3 mL接种于6孔细胞培养板中,加入终浓度为0.01、0.1、1、10、100和1 000 nmol·L-1 NMU,对照组加入RPMI-1640培养液,置于37 ℃、5% CO2培养箱中培养48 h。收集NMU诱导后的PBL细胞和K562(靶细胞)细胞,按照效应细胞与靶细胞比例(效靶比)15:1、30:1、60:1分别接入96孔细胞培养板,设为效靶细胞孔(均设5个复孔),并设靶细胞孔及效应细胞孔,每孔均为200 μL,充分振荡混匀后于37 ℃、5% CO2条件下培养4~6 h,用酶标仪检测各孔吸光度值(A450)。按下述公式计算NK细胞活性。
| $细胞活性 = \left[ {1 - \left( {{A_{450\left( 效靶细胞孔 \right)}} - {A_{450\left( 效应细胞孔 \right)}}} \right)/{A_{450\left( 靶细胞孔 \right)}}} \right] \times 100\% $ |
数据用SPSS 19.0软件统计,数据结果均以平均数±标准误(x±SE)表示,差异显著性用独立样本t检验和单因子方差分析(One-way ANOVA),用LSD法确定差异显著性。
2 结果与分析 2.1 NMU、NMUR 1和NMUR2 mRNA在PBL中的表达用特异性引物对提取的细胞总RNA进行RT-PCR,然后用琼脂糖凝胶电泳分析。结果显示:在猪的PBL中有NMUR 1 mRNA表达,检测到NMUR 1 的单一条带,片段大小为811 bp(图 1),经测序确定为目的片段,但未扩增出NMU及NMUR 2 基因片段。扩增猪的GAPDH用于验证cDNA的质量,片段大小为549 bp。
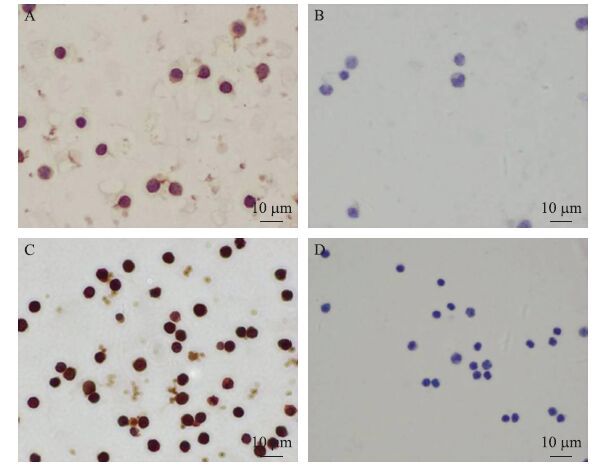
2.2 NMU、NMUR1和NMUR2在PBL中的分布免疫组织化学染色结果(图 2)显示:PBL呈现NMU和NMUR1的免疫阳性反应(棕褐色着色)。经苏木精复染(显示胞核),可见NMU、NMUR1均主要分布于PBL的胞浆和胞膜中(图 2-A、C),阴性对照未见免疫阳性染色(图 2-B、D)。在PBL上未见NMUR2的阳性反应。
|
图 2 猪PBL中NMU和NMUR1的免疫组织化学染色 Figure 2 NMU and NMUR1 immunoreactivity in PBL of pigs A和C分别为猪外周血淋巴细胞中NMU和NMUR1的免疫阳性;B和 D分别为NMU和NMUR1的阴性对照(苏木精复染细胞核) A,C is NMU and NMUR1 immunoreactivity in peripheral blood lymphocytes of pigs;B,D is negative controls of NMU and NMUR1(Cells were counterstained with hematoxylin) |
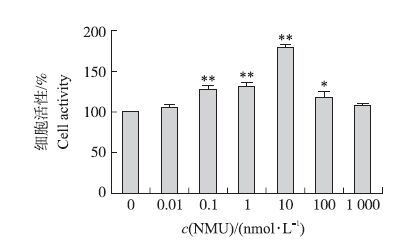
不同浓度的NMU(0.01、0.1、1、10、100和1 000 nmol·L-1) 在体外对猪PBL活性的影响见图 3。其中,NMU为0.1、1 和10 nmol·L-1时极显著提高猪PBL细胞活性(P<0.01) ,且当NMU浓度为10 nmol·L-1时,PBL活性水平达到峰值(179.4±3.0) %。NMU为100 nmol·L-1时可以显著提高猪PBL的细胞活性(P<0.05) 。
|
图 3 NMU对猪PBL细胞活性的影响(n=5) Figure 3 Effect of NMU treatment on cell viability of pig PBL *P<0.05;* *P<0.01. The same as follows. |
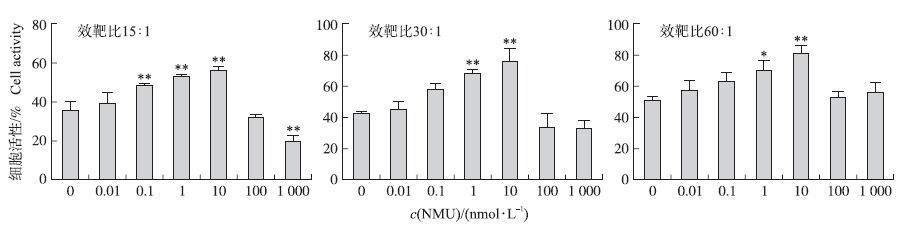
不同浓度的NMU在体外对猪NK细胞活性的影响检测结果(图 4)显示:NMU作用PBL细胞48 h后,在效靶比为15:1时,与对照组比较,0.1、1 和10 nmol·L-1 NMU均能极显著提高NK细胞的细胞活性(P<0.01) ,而1 000 nmol·L-1的NMU却极显著抑制NK细胞的细胞活性(P<0.01) ;在效靶比为30:1时,与对照组比较,1和10 nmol·L-1的NMU均能极显著提高NK细胞的细胞活性(P<0.01) ;在效靶比为60:1时,与对照组相比,10 nmol·L-1 NMU能极显著地提高NK细胞的细胞活性(P<0.01) ,1 nmol·L-1 NMU也能显著提高NK细胞的细胞活性(P<0.05) 。综合各个效靶比,NMU为10 nmol·L-1时NK细胞的活性最强。
|
图 4 不同浓度NMU对不同效靶比下猪外周血NK细胞活性的影响(n=5) Figure 4 Effects of different concentrations of NMU on the activity of NK cells in peripheral blood of pigs under different effect of targets ratio |
越来越多的研究表明,NMU及其受体系统在调控机体免疫方面起重要作用。Moriyama等[18]发现NMU可以通过NMUR1介导肥大细胞脱颗粒,导致血管舒张,水肿和中性粒细胞浸润。Abbondanzo等[19]研究表明,敲除小鼠的NMUR1可以阻断完全弗氏佐剂介导的炎症反应。NMU还可以通过自分泌或旁分泌途径作用于巨噬细胞,从而对巨噬细胞分泌IL-6产生重要作用[14]。最新研究发现,在抗原介导的小鼠哮喘模型中,NMU敲除小鼠的气管嗜酸粒细胞减少,并且NMU可促进嗜酸粒细胞的浸润[20]。Rao等[21]研究表明,NMU促进内源性抗原介导的关节炎。
有关NMU对猪免疫调节作用的研究未见文献报道。本试验研究了猪PBL中NMU及其受体的基因表达和蛋白分布,以及NMU在体外对PBL细胞和NK细胞活性的影响。RT-PCR结果显示,在猪PBL中有NMUR 1 基因的表达,而免疫细胞化学染色结果显示,PBL内有NMUR1和NMU蛋白分布。该结果从形态学上提供了NMU可能通过其受体调控猪PBL免疫功能的证据,但其作用机制仍需进一步研究。
淋巴细胞在机体免疫应答中发挥重要的作用,它的功能状态可直接反映机体的免疫状态,而其增殖活性是机体细胞免疫水平的一个重要指标。本试验结果表明,0.1~100 nmol·L-1的NMU均能显著提高猪PBL的细胞活性。NK细胞激活后可释放穿孔素、颗粒酶B,分泌IFN-γ等细胞因子,从而杀伤肿瘤细胞[22]。本试验结果显示,在各效靶比水平上,10 nmol·L-1的NMU均能极显著提升NK细胞杀伤K562细胞的能力。综合PBL细胞活性试验的结果,推测NMU提高NK细胞活性可能与其提高PBL细胞活性有关,也可能与NMU增强NK细胞自身杀伤能力有关。
综上所述,NMU及其受体能在PBL表达或分布,NMU在体外可通过提高猪PBL的细胞活性,增强NK细胞对K562细胞的杀伤能力等,实现对猪免疫的调节作用。本试验结果为NMU参与猪的免疫调节提供了新的思路和试验依据。
| [1] | Minamino N, Kangawa K, Matsuo H. Neuromedin U-8 and U-25:novel uterus stimulating and hypertensive peptides identified in porcine spinal cord[J]. Biochem Biophys Res Commun, 1985,130(3): 1078–1085. DOI: 10.1016/0006-291X(85)91726-7 |
| [2] | Lee W H, Liu S B, Shen J H, et al. Identification and molecular cloning of a novel neuromedin U analog from the skin secretions of toad Bombina maxima[J]. Regulatory Peptides, 2005,129(1/2/3): 43–47. |
| [3] | Martinez V G, O'Driscoll L. Neuromedin U:a multifunctional neuropeptide with pleiotropic roles[J]. Clinical Chemistry, 2015,61(3): 471–482. DOI: 10.1373/clinchem.2014.231753 |
| [4] | Micewicz E D, Bahattab O S, Willars G B, et al. Small lipidated anti-obesity compounds derived from neuromedin U[J]. European Journal of Medicinal Chemistry, 2015,101: 616–626. DOI: 10.1016/j.ejmech.2015.07.020 |
| [5] | Dalbøge L S, Pedersen S L, Witteloostuijn S B, et al. Synthesis and evaluation of novel lapidated neuromedin U analogs with increased stability and effects on food intake[J]. Journal of Peptide Science, 2015,21(2): 85–94. DOI: 10.1002/psc.2727 |
| [6] | Dalbøge L S, Pedersen S L, Secher T, et al. Neuromedin U inhibits food intake partly by inhibiting gastric emptying[J]. Peptides, 2015,69: 56–65. DOI: 10.1016/j.peptides.2015.04.010 |
| [7] | Telegdy G, Adamik A. Mediators involved in the hyperthermic action of neuromedin U in rats[J]. Regulatory Peptides, 2014,192/193: 24–29. DOI: 10.1016/j.regpep.2014.07.004 |
| [8] | Aizawa S, Sakata I, Nagasaka M, et al. Negative regulation of neuromedin U mRNA expression in the rat pars tuberalis by melatonin[J]. PLoS ONE, 2013,8(7): e67118. DOI: 10.1371/journal.pone.0067118 |
| [9] | Tanaka M, Csabafi K, Telegdy G. Neurotransmissions of antidepressant-like effects of neuromedin U-23 in mice[J]. Behavioural Brain Research, 2013,259(2): 196–199. |
| [10] | Telegdy G, Adamik A. Anxiolytic action of neuromedin-U and neurotransmitters involved in mice[J]. Regulatory Peptides, 2013,186(3): 137–140. |
| [11] | Lin T Y, Huang W L, Lee W Y, et al. Identifying a neuromedin U receptor 2 splice variant and determining its roles in the regulation of signaling and tumorigenesis in vitro[J]. PLoS ONE, 2015,10(8). DOI: 10.1371/journal.pone.0136836 |
| [12] | Hedrick J A, Morse K, Shan L, et al. Identification of a human gastrointestinal tract and immune system receptor for the peptide neuromedin U[J]. Mol Pharmacol, 2000,58: 870–875. |
| [13] | Johnson E N, Appelbaum E R, Carpenter D C, et al. Neuromedin U elicits cytokinerelease in murine Th2-type t cell clone D10.G4.1[J]. Immunol, 2004,173: 7230–7238. DOI: 10.4049/jimmunol.173.12.7230 |
| [14] | Moriyama M, Matsukawa A, Kudoh S, et al. The neuropeptide neuromedin U promotes IL-6 production from macrophages and endotoxin shock[J]. Biochem Biophys Res Commun, 2006,341: 1149–1154. DOI: 10.1016/j.bbrc.2006.01.075 |
| [15] | 杨桂红. 神经介素S及其受体在母猪体内的分布和对母猪生殖调节的研究[D]. 南京:南京农业大学,2011. Yang G H. Study on the distribution of neuromedin s and its receptor and the regulation to reproduction in female pigs[D]. Nanjing:Nanjing Agricultural University,2011(in Chinese with English abstract). http://cdmd.cnki.com.cn/Article/CDMD-10307-1012271588.htm |
| [16] | 郑路程, 苏娟, 房蕊, 等. 促性腺激素抑制激素在公猪下丘脑-垂体-睾丸轴的分布定位研究[J]. 南京农业大学学报, 2014, 37(5): 101–105. Zheng L C, Su J, Fang R, et al. Distribution and localization of gonadotropin-inhibitory hormone(GnIH)in the hypothalamus-pituitary-testis axis of boars[J]. Journal of Nanjing Agricultural University, 2014,37(5): 101–105. DOI: 10.7685/j.issn.1000-2030.2014.05.016 (in Chinese) |
| [17] | 姚义荣, 王营, 刘军权, 等. 白桦脂酸对人NK细胞杀伤SW1990胰腺癌细胞影响及机制探讨[J]. 中华肿瘤防治杂志, 2015, 22(1): 34–38. Yao Y R, Wang Y, Liu J Q, et al. Explore the effect and mechanism of betulinic acid on NK cells killing pancreatic cancer SW1990 cells[J]. Chin J Cancer Prev Treat, 2015,22(1): 34–38. (in Chinese) |
| [18] | Moriyama M, Sato T, Inoue H, et al. The neuropeptide neuromedin U promotes inflammation by direct activation of mast cells[J]. Exp Med, 2005,202: 217–224. DOI: 10.1084/jem.20050248 |
| [19] | Abbondanzo S J, Manfra D J, Chen S C, et al. Nmur1-/-mice are not protected from cutaneous inflammation[J]. Biochem Biophys Res Commun, 2009,378: 777–782. DOI: 10.1016/j.bbrc.2008.11.148 |
| [20] | Moriyama M, Fukuyama S, Inoue H, et al. The neuropeptide neuromedin U activates eosinophils and is involved in allergen-induced eosinophilia[J]. Am J Physiol Lung Cell Mol Physiol, 2006,290: 971–977. DOI: 10.1152/ajplung.00345.2005 |
| [21] | Rao S M, Auger J L, Gaillard P, et al. The neuropeptide neuromedin U promotes autoantibody-mediated arthritis[J]. Arthritis Res Ther, 2012,14: R29. DOI: 10.1186/ar3732 |
| [22] | Stewart S E, Kondos S C, Matthews A Y, et al. The perforin pore facilitates the delivery of cationic cargos[J]. Journal of Biological Chemistry, 2014,289(13): 9172–9181. DOI: 10.1074/jbc.M113.544890 |




