文章信息
- 李传海, 尚健, 聂文芳, 李立峰, 曹慧
- LI Chuanhai, SHANG Jian, NIE Wenfang, LI Lifeng, CAO Hui
- 家鸽粪便细菌多样性的高通量测序分析及其环境意义
- Illumina sequencing of 16S rDNA tag revealed bacterial communities in pigeon feces and its environmental implication
- 南京农业大学学报, 2017, 40(1): 116-122
- Journal of Nanjing Agricultural University(Social Science), 2017, 40(1): 116-122.
- http://dx.doi.org/10.7685/jnau.201604014
-
文章历史
- 收稿日期: 2016-04-05
2. 宣城市种植业局, 安徽 宣城 242000
2. Xuancheng Planting Industry Bureau, Xuancheng 242000, China
家鸽具有多种观赏和经济价值,它不仅提供鲜美的肉蛋食品,还是人们喜爱的蓝天信使,家鸽中的白鸽在多种庆典活动中也经常被放飞使用。家鸽养殖分为圈养和散养两种形式,圈养家鸽养殖技术规范、数量大、生长快、效益高,但家鸽的直肠较短,食物的快速消化产生大量禽粪;散养家鸽活动空间极大,其体表和粪便携带的大量微生物随家鸽飞行而传播,有一定的致病风险[1-2]。研究家鸽粪便微生物群落组成和多样性,对于理解禽类疾病传播与预防,以及微生物扩散和地理分布具有重要的理论和实践意义。
对于家鸽与微生物之间关系的研究,主要集中在病原微生物的分离、鉴定和致病性方面。目前,已经从鸽粪中分离到的病原微生物包括新型隐球菌[3]、沙门氏菌[4]、肠道杆菌[5]、衣原体[6]、病毒[7-8]等,其中新型隐球菌能够引起中枢神经系统感染和肺部感染,沙门氏菌可引起人和动物肠道感染和伤寒,大肠杆菌O157:H7可引起人出血性腹泻和肠炎,沙眼衣原体、鹦鹉热衣原体和肺炎衣原体可引起肺部感染,家鸽还能引发人类感染禽流感[9-10]。在鸽粪微生物多样性方面,现有的文献报道十分有限,且研究对象主要是病原微生物类群。例如,沙特112个干燥鸽粪中含有16个属20个种的真菌[11];伊朗鸽粪中微孢子虫的检出率为21%,它们分属于4个种[12];香港和匈牙利鸽粪中含有7个病毒科[7]。事实上,各类禽类肠道中存在高度多样性的微生物菌群,它们在生理、免疫、营养及其与宿主代谢过程中起着重要作用[13-17];禽粪排出动物体外进入土壤、水体环境中,由于有别于动物肠道环境,相应的微生物群落结构也会发生变化,某些微生物甚至可以作为表征水体污染的微生物学指标[2];此外,这些来自于禽粪中的“外来微生物”与环境中的“土著微生物”将产生各种竞争和适应作用,引发一系列生物学效应。
笔者采集了3个规模化养殖场鸽粪样品,提取鸽粪微生物总DNA并扩增细菌16S rDNA V3V4区,采用Illumina MiSeq高通量测序方法研究鸽粪中细菌群落组成与结构特征,明确鸽粪中病原微生物主要类群,为全面、准确地认识鸽粪微生物多样性与环境风险提供科学依据。
1 材料与方法 1.1 鸽粪样品的采集鸽粪样品于2015年3月23日采集于安徽省宣城市宣州区和平养鸽专业合作社(30°48′45″N,118°49′6″E)、乌边村和平组养鸽场(30°48′53″N,118°49′5″E)和辉煌养鸽场(31°3′24″N,118°41′13″E)3个规模化养鸽场,分别命名为HP、WB和HH。每个样品5点随机取样,采集的新鲜鸽粪混匀、装袋置于冰盒中,带回实验室分别于-20 ℃和-80 ℃保存备用。HP和WB为美国落地王鸽粪,HH为白羽王鸽粪,鸽龄20 d左右,体质量约700 g,以玉米、小麦、豌豆和高粱等粮食为主要饲料,均无发病情况。
1.2 鸽粪总DNA的提取纯化所有粪便样品均采用Omega 公司的 DNA 提取试剂盒提取微生物总DNA,具体的操作步骤按照试剂盒说明书进行,每个样品3个重复,提取完毕用10 g·L-1的琼脂糖凝胶电泳检测DNA浓度,并将3管重复混为一管,于-20 ℃保存备用。
1.3 细菌Illumina MiSeq测序将提取的总DNA样品送上海天昊遗传分析中心测序分析。测序使用Illumina MiSeq 2×300测序平台对细菌16S rDNA(V3V4) (515f-907r)进行测序。测序数据经拼接、过滤、剔除嵌合体,舍弃低质量序列,优质序列用于可操作分类单元(operational taxonomic unit,OTU)分类与多样性指数计算及物种丰度分析。
1.4 数据分析使用QⅡme软件对原始序列进行处理,并且在Cutoff值为 0.03水平上划分OTU。利用Muthur软件计算多样性指数(Ace、Chao、Shannon、Simpson)、稀释性曲线及聚类分析。用R语言软件绘制群落组成柱状图和Venn图。运用Excel 2010和SPSS 19.0软件进行相关数据处理和统计分析。
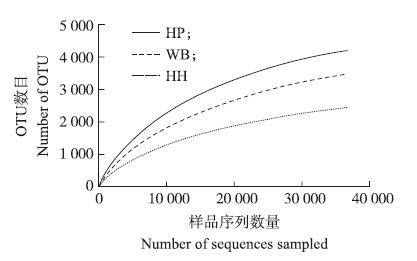
2 结果与分析 2.1 鸽粪细菌群落多样性分析对3个家鸽粪便样品细菌16S rDNA(V3V4) Illumina MiSeq进行了高通量测序,总共获得12万条优质序列,平均长度为466 bp。在Cutoff值为0.03水平上划分OTU,HP、WB、HH分别有4 215、3 672和2 446个OTU类型,覆盖率分别为96.76%、97.43%和97.59%。从表 1可以看出:3个样品的Chao和Ace指数分别为3 075~4 789和3 355~5 197,而Simpson和Shannon指数分别为0.011 9~0.025 9和5.00~6.17,且Chao、Ace和Shannon指数从大到小的样品分别为HP、WB、HH。说明鸽粪细菌群落结构复杂、种群丰富,不同养殖场和家鸽品种之间粪便细菌群落多样性均有差异。由物种稀释性曲线(图 1)可知,随着测序数量的增加,OTU数量逐渐趋于平缓,测序深度完全满足后续分析要求,覆盖值均大于96%,库容值较高,表明测序深度能够反映鸽粪中细菌群落组成状况。
| 样品编号Sample code | 序列数Reads | OTU种类Type of OTU | 覆盖值/%Coverage | 细菌多样性指数Bacterial diversity indices | |||
| Ace | Chao | Shannon | Simpson | ||||
| HP | 37 389 | 4 215 | 96.76 | 5 197 | 4 789 | 6.17 | 0.011 9 |
| WB | 45 320 | 3 762 | 97.43 | 4 779 | 4 424 | 5.61 | 0.018 9 |
| HH | 36 662 | 2 446 | 97.59 | 3 355 | 3 075 | 5.00 | 0.025 9 |
|
图 1 各样品高通量测序结果的稀释性曲线 Figure 1 The rarefaction curve of high-through sequencing result |
对3个鸽粪样品中的12万条16S rDNA序列进行了系统发育分析,3个样品共有13个门、31个纲、55个目、101个科、164个属。在门的水平上有98.27%物种可以注解,在属的水平上有79.4%的物种可以注解,但在种的水平上仅有20.81%物种能明确归类,可见由于高通量测序深度大,获得了更多的物种遗传信息。其中,HP样品中有9个门、18个纲、34个目、74个科、 117个属;WB样品中有9个门、17个纲、37个目、78个科、116个属;HH样品中有12个门、25个纲、41个目、65个科、97个属。其中HP样品和WB样品在不同分类水平数量的差异并不明显,然而与HH样品差异较大,这可能与采样地点和家鸽品系有关。
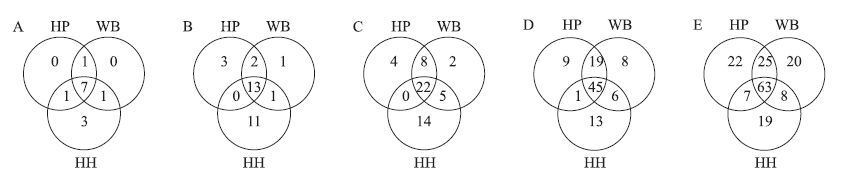
采用Venn图直观表示3种鸽粪样品细菌群落结构在门、纲、目、科、属水平上的异同(图 2),7个门类群出现在所有样品中,约占总类群的99.95%,因此在门的分类水平上3个鸽粪样品中微生物组成几乎完全一致;在纲的分类水平上,3种样品有13个纲是共同拥有的,约占总类群的99.89%;3个样品22个目是共有的,约占总类群的99.24%;45个科普遍存在于3个样品中,约占总类群的98.68%;在属的水平上,有63个属是3个样品共有的,约占总类群的97.48%。由此可见,随着分类地位的降低,鸽粪中的微生物组成差别在不断增加,但总体而言微生物种类在数量上差异并不明显,同时也表明3种鸽粪样品中微生物种群稳定,完全可以反映鸽粪细菌群落结构和多样性。
|
图 2 3种样品在不同分类水平上的Venn图 Figure 2 The Venn diagram of different level of taxonomy in three samples A、B、C、D、E分别为3种样品在门、纲、目、科、属水平上的Venn图。 A,B,C,D,E are represented the Venn diagram at phylum,class,order,family,genus in three samples. |
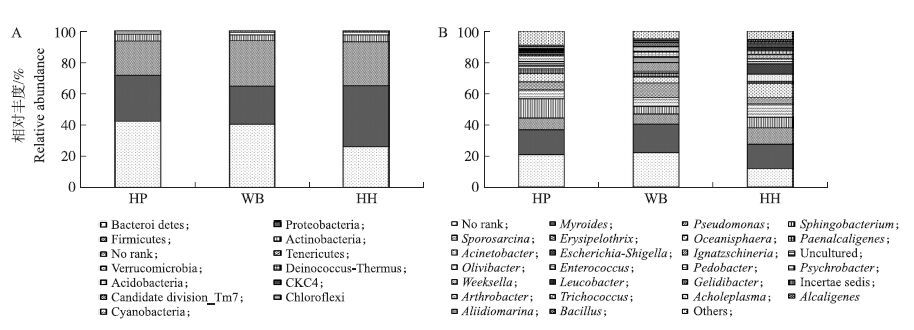
鸽粪中细菌群落组成丰富,但优势微生物比例也很高。图 3-A显示:拟杆菌门(Bacteroidetes)、变形菌门(Proteobacteria)、厚壁菌门(Firmicutes)是鸽粪共有的优势微生物门,覆盖了92%以上的物种数,且HP和WB样品中Bacteroidetes的相对丰度高于HH样品,而Proteobacteria则呈现相反的趋势,这可能与家鸽品系有关。WB样品中Firmicutes的相对丰度最高,其次是HH样品,HP样品最少,因此,家鸽粪便中Firmicutes的相对丰度与其品系关系不大,可能与养殖环境等其他环境因素有关,有待于进一步研究。在属的水平上,香味菌属(Myroides)、假单胞菌属(Pseudomonas)、鞘氨醇杆菌属(Sphingobacterium)、芽孢八叠球菌属(Sporosarcina)、丹毒丝菌属(Erysipelothrix)、Oceanisphaera、类产碱杆菌属(Paenalcaligenes)、不动杆菌属(Acinetobacter)、大肠杆菌-志贺菌属(Escherichia-Shigella)、依格纳季氏菌属(Ignatzschineria)、Olivibacter为鸽粪优势菌属(图 3-B),其相对丰度在3%以上,有16个属的相对丰度大于1%,21个属相对丰度大于0.5%(表 2)。其中Myroides、Pseudomonas、Sphingobacterium、Sporosarcina、Erysipelothrix、Oceanisphaera为3个样品的共有优势菌属,HP样品中其相对丰度分别为16.05%、7.49%、12.47%、5.77%、5.1%、5.5%;WB样品中其相对丰度分别为18.2%、6.6%、4.87%、5.48%、9.74%、3.58%;HH中其相对丰度分别为15.64%、10.5%、6.86%、8.63%、3.91%、9.09%。Olivibacter、Paenalcaligenes为HP样品中独有的优势菌属,其相对丰度分别为3.57%和3.08%;Ignatzschineria为WB样品中特有的优势菌属,其相对丰度为5.44%;Escherichia-Shigella和Acinetobacter为HH样品中特有的优势菌属,其相对丰度分别为6.49%和4.63%。其中,在HH样品中Pseudomonas、Oceanisphaera、Sporosarcina、Escherichia-Shigella和Acinetobacter相对丰度高于HP和WB样品,且HP和WB样品差异不大,这可能与家鸽品系有关。而样品中Sphingobacterium、Paenalcaligenes、Ignatzschineria、Erysipelothrix、Olivibacter的相对丰度则并没有呈现出一定的规律,这可能与采样地点以及不同养殖场的管理方式有关,需进行更深入的研究。
|
图 3 鸽粪菌群在门(A)和属(B)水平上相对丰度 Figure 3 Relative abundance of the bacterial phyla(A)and genera(B)in pigeons feces communities |
| 门Phylum | 属Genus | 相对丰度/%Relative abundance | ||
| HP | WB | HH | ||
| Bacteroidetes | Myroides | 16.05 | 18.2 | 15.64 |
| Sphingobacterium | 12.47 | 4.87 | 6.86 | |
| Olivibacter | 3.57 | 0.08 | 1.84 | |
| Pedobacter | 1.07 | 2.86 | 0.12 | |
| Weeksella | 0.33 | 2.89 | 0.01 | |
| Gelidibacter | 0.22 | 2.48 | 0.01 | |
| Proteobacteria | Pseudomonas | 7.49 | 6.6 | 10.5 |
| Oceanisphaera | 5.5 | 3.58 | 9.09 | |
| Paenalcaligenes | 3.08 | 2.59 | 1.6 | |
| Acinetobacter | 1.47 | 1.16 | 4.63 | |
| Escherichia-Shigella | 0.28 | 0.12 | 6.49 | |
| Ignatzschineria | 1.37 | 5.44 | 0.06 | |
| Psychrobacter | 0.37 | 0.36 | 2.49 | |
| Firmicutes | Sporosarcina | 5.77 | 5.48 | 8.63 |
| Enterococcus | 0.75 | 0.83 | 2.94 | |
| Trichococcus | 0.48 | 0.14 | 0.98 | |
| Actinobacteria | Leucobacter | 0.56 | 0.25 | 2.04 |
| Arthrobacter | 0.32 | 0.89 | 0.71 | |
| Tenericutes | Erysipelothrix | 5.1 | 9.74 | 3.91 |
| 未培养Uncultured | 未培养Uncultured | 1.53 | 3.2 | 1.29 |
| 未分类No rank | 未分类No rank | 20.59 | 22.02 | 11.64 |
分析了3个鸽粪中病原微生物的菌属组成发现:Myroides、Pseudomonas、Sphingobacterium、Erysipelothrix和Acinetobacter菌属均有较高丰度(表 3),其中HP样品中相对丰度分别为16.05%、7.49%、12.47%、5.10%和1.47%,WB样品中的相对丰度分别为18.2%、6.6%、4.87%、9.74%和1.16%,HH样品中相对丰度分别为15.64%、10.5%、6.86%、3.91%和4.63%。基于《动物病原微生物分类名录》可知:鸽粪中均含有大量的潜在致病菌属,对人和动物及环境会造成一定的潜在风险。
| 属Genus | 相对丰度/%Relative abundance | 易感者Susceptible | 疾病Pathema |
| Myroides | 16.73 | 人Human | 尿路感染、免疫功能低下感染Urinary tract infections,immune function low |
| Pseudomonas | 8.03 | 人、动物和植物Human,animal and plant | 皮肤和皮下组织感染、呼吸道感染、尿道感染Skin and subcutaneous tissue infections,respiratory tract infections,urethral tract infections |
| Sphingobacterium | 7.96 | 人Human | 后呼吸道感染Post respiratory infections |
| Erysipelothrix | 6.49 | 人、动物、鸟类、鱼类Human,animal,bird and fish | 皮肤感染、败血病、脑膜炎、丹毒Skin infections,septicemia,meningitis,erysipelas |
| Acinetobacter | 2.28 | 人Human | 皮肤和伤口感染Skin and wound infections |
禽粪菌群组成极其复杂,其种类多,数量大,分布广。目前,有关禽类粪便微生物的研究较多,但是针对鸽粪中微生物多样性的研究却鲜有报道。本文通过高通量测序方法分析了鸽粪中细菌多样性,平均测序深度为39 790 Reads,去除单一OTU,共获得6 270个OTU,多样性指数和丰度指数从大到小的样品分别为HP、WB、HH。鸽粪细菌分布在13个门、31个纲、55个目、101个科和164个属,且鸽粪中存在18.1%细菌16S rDNA序列未能归类。鸽粪中细菌多样性高度丰富,有大量未命名细菌和不可培养微生物,且不同样品之间存在一定的差异,与其物种品系和取样地点有关[18]。与传统分子生物学方法相比,新一代测序技术提供了更多的微生物基因信息,能更加全面、准确地阐明微生物群落结构特征[19-20]。
通过分析发现Bacteroidetes、Proteobacteria和Firmicutes为鸽粪微生物的3个优势门,占微生物总数的93%左右。Lan等[21]通过构建16S rDNA克隆文库研究了鸡盲肠内微生物多样性,发现可培养细菌也是上述3个优势微生物门,只是组成比例有较大差别。其中Bacteroidetes、Proteobacteria受家鸽物种品系的影响较大,而Firmicutes则受取样地点的影响较大。Pajarillo等[22]对3种不同品系的纯种猪粪便微生物多样性研究中同样发现Bacteroidetes、Proteobacteria的相对丰度受猪品系的影响较大,本文的研究结果与之相一致。由于家鸽与猪的进化关系相对较远,本研究还发现Firmicutes在家鸽粪便微生物群落间的差异:Pseudomonas、Oceanisphaera、Sporosarcina、Escherichia-Shigella和Acinetobacter受家鸽品系的影响较大,而Sphingobacterium、Paenalcaligenes、Ignatzschineria、Erysipelothrix、Olivibacter则受不同养殖场的管理方式和各种环境变化的影响。大量的研究结果表明,动物粪便微生物区系受宿主基因型和取样环境的影响[23-24]。对优势菌属的深入分析发现,鸽粪中好氧微生物菌属较多,包括Myroides、Pseudomonas、Sphingobacterium、Sporosarcina、Oceanisphaera、Acinetobacter、Ignatzschineria和Olivibacter菌属,好氧菌属的16S rDNA序列比例占有效序列的52.1%,厌氧微生物Erysipelothrix、Paenalcaligenes、Escherichia-Shigella仅有11.0%,这与肠道微生物区系中含有大量的厌氧微生物明显不同[21]。可见,鸽粪排出体外后,细菌暴露空气中,好氧条件对肠道微生物进行了“环境选择”,因而厌氧菌的种类和数量急剧减少。鸽粪中某些菌属同样出现在人类和其他禽类粪便中,甚至土壤、水环境和空气中也广泛存在[25],但粪便中微生物组成与土壤、水、空气微生物群落结构有明显差别,因此,可以推断排放到环境中的鸽粪微生物将与土壤、水等环境中的土著微生物产生各种互作关系,影响土壤和水体微生物群落组成及其地理分布,甚至造成一系列环境微生物学效应。
本研究检测到家鸽粪便中存在某些致病菌,Myroides包括M.odoratus、M.odoratimimus、M.pelagicus、M.profundi和M.marinus 5个种,其中M.odoratimimus可引起有严重基础疾病和免疫功能低下患者的多种机会感染,如尿路感染、心内膜炎、脑膜炎和皮肤感染等疾病的发生[26-27]。Sphingobacterium包括S.spiritovorum、S.multivorum、S.mizutaⅡ、S.antarcticum、S.faecium和S.thalpophilum 6个种。Lambiase等[28]曾报道,囊性纤维化患者后呼吸道感染中几乎Sphingobacterium属的所有种都可能存在致病作用。Pseudomona对人和动物都有机会致病,尤其是Pseudomonas aeruginosa在患有囊性纤维小孩肺部感染中致病性极强[29]。Erysipelothrix rhusiopathiae可引起人、动物、鸟类和鱼类皮肤感染、败血症、丹毒和脑膜炎等疾病,通过与携带病原菌的动物或污水以及土壤接触传播,严重威胁到人类及动物健康和环境安全[30]。Acinetobacter广泛分布于水体和土壤等潮湿环境中,可引起肺部感染、伤口及皮肤感染、泌尿生殖系统感染、菌血症和脑膜炎等临床疾病[31]。因此,畜禽粪便如不经妥善处理直接排入环境,会对水体、土壤和空气造成严重的污染,并危及畜禽和人体的健康。
高通量测序技术能够更加全面、准确地分析粪便菌群多样性,提供粪便微生物组成的基本信息。本研究发现鸽粪中细菌多样性丰富,以厚壁菌门、拟杆菌门和变形菌门为主,且含有大量的未命名菌属和不可培养微生物;鸽粪中的优势菌属以好氧细菌为主,厌氧细菌比例较小。鸽粪中广泛分布病原微生物菌属,有诱发人和其他动物产生各种疾病的风险。这些菌属很多并存于水体、土壤、畜禽粪便中,这为分析粪便微生物与人体健康、动物健康和环境之间的关系及栖息地土壤、水体中微生物遗传进化和生物地理分布提供了一个窗口,且有待于进行更深入的研究和分析。
| [1] | Tanka C, Miyazawa T, Watarai M, et al. Bacteriological survey of feces from feral pigenons in Japan[J]. Journal of Veterinary Medical Science, 2005,67(9): 951–953. DOI: 10.1292/jvms.67.951 |
| [2] | Lu J, Santo Domingo J W, Lamendella R, et al. Phylogenetic diversity and molecular detection of bacteria in gull feces[J]. Applied and Environmental Microbiology, 2008,74(13): 3969–3976. DOI: 10.1128/AEM.00019-08 |
| [3] | Liu Z,Ma L,Zhong Y,et al. Isolation,identification and significance of cryptococcus neoformans and candida albicans from faecal specimen of pigeon[M]//Egui Z,Sabo S. Information Technology and Agricultural Engineering. Berlin:Springer,2012:507-512. |
| [4] | Pasmans F, van Immerseel F, Heyndrickx M, et al. Host adaptation of pigeon isolates of Salmonella enterica subsp.enterica serovar Typhimurium variant Copenhagen phage type 99 is associated with enhanced macrophage cytotoxicity[J]. Infection and Immunity, 2003,71(10): 6068–6074. DOI: 10.1128/IAI.71.10.6068-6074.2003 |
| [5] | Schmidt H, Scheef J, Morabito S, et al. A new Shiga toxin 2 variant(Stx2f)from Escherichia coli isolated from pigeons[J]. Applied and Environmental Microbiology, 2000,66(3): 1205–1208. DOI: 10.1128/AEM.66.3.1205-1208.2000 |
| [6] | Vanrompay D, Andersen A A, Ducatelle R, et al. Serotyping of European isolates of Chlamydia psittaci from poultry and other birds[J]. Journal of Clinical Microbiology, 1993,31(1): 134–137. |
| [7] | Phan T G, Vo N P, Boros Á, et al. The viruses of wild pigeon droppings[J]. PloS ONE, 2013,8(9): e72787. DOI: 10.1371/journal.pone.0072787 |
| [8] | Catroxo M H B, Martins A, Petrella S, et al. Research of viral agent in free-living pigeon feces(Columba livia)in the City of Sao Paulo,SP,Brazil,for transmission electron microscopy[J]. Int J Morphol, 2011,29(2): 628–635. DOI: 10.4067/S0717-95022011000200055 |
| [9] | Abolnik C. A current review of avian influenza in pigeons and doves(Columbidae)[J]. Veterinary Microbiology, 2014,170(3): 181–196. |
| [10] | Jia B B, Shi J Z, Li Y B, et al. Pathogenicity of Chinese H5N1 highly pathogenic avian influenza viruses in pigeons[J]. Archives of Virology, 2008,153(10): 1821–1826. DOI: 10.1007/s00705-008-0193-8 |
| [11] | Abulreesh H H, Organji S R, Elbanna K, et al. First report of environmental isolation of Cryptococcus neoformans and other fungi from pigeon droppings in Makkah,Saudi Arabia and in vitro susceptibility testing[J]. Asian Pacific Journal of Tropical Disease, 2015,5(8): 622–626. DOI: 10.1016/S2222-1808(15)60901-X |
| [12] | Pirestani M, Sadraei J, Forouzandeh M. Molecular characterization and genotyping of human related microsporidia in free-ranging and captive pigeons of Tehran,Iran[J]. Infection,Genetics and Evolution, 2013,20: 495–499. DOI: 10.1016/j.meegid.2013.10.007 |
| [13] | Benson A K, Kelly S A, Legge R, et al. Individuality in gut microbiota composition is a complex polygenic trait shaped by multiple environmental and host genetic factors[J]. Proc Natl Acad Sci USA, 2010,107(44): 18933–18938. DOI: 10.1073/pnas.1007028107 |
| [14] | Hintz H, Cymbaluk N. Nutrition of the horse[J]. Annual Review of Nutrition, 1994,14(1): 243–267. DOI: 10.1146/annurev.nu.14.070194.001331 |
| [15] | Neish A S. Microbes in gastrointestinal health and disease[J]. Gastroenterology, 2009,136(1): 65–80. DOI: 10.1053/j.gastro.2008.10.080 |
| [16] | Wardwell L H, Huttenhower C, Garrett W S. Current concepts of the intestinal microbiota and the pathogenesis of infection[J]. Current Infectious Disease Reports, 2011,13(1): 28–34. DOI: 10.1007/s11908-010-0147-7 |
| [17] | 张志成, 白小磊, 张旭鸽, 等. 鸽源大肠杆菌超广谱β-内酰胺酶与头孢菌素酶基因型分析[J]. 金陵科技学院学报, 2015, 31(2): 85–89. Zhang Z C, Bai X L, Zhang X G, et al. The analysis of genotype of Escherchia coil-producing ESBLs and ampC β-lactamases isolated from farm pigeons[J]. Journal of Jinling Institute of Technology, 2015,31(2): 85–89. (in Chinese) |
| [18] | Ley R E, Peterson D A, Gordon J I. Ecological and evolutionary forces shaping microbial diversity in the human intestine[J]. Cell, 2006,124(4): 837–848. DOI: 10.1016/j.cell.2006.02.017 |
| [19] | 夏围围, 贾仲君. 高通量测序和DGGE分析土壤微生物群落的技术评价[J]. 微生物学报, 2014, 54(12): 1489–1499. Xia W W, Jia Z J. Comparative analysis of soil microbial communities by pyrosequencing and DGGE[J]. Acta Microbiologica Sinica, 2014,54(12): 1489–1499. (in Chinese) |
| [20] | 赵爽, 张宁, 刘东阳, 等. 氯苯嘧啶醇施用对草坪斑枯病致病菌及根际土壤真菌的影响[J]. 南京农业大学学报, 2015, 38(4): 590–595. Zhao S, Zhang N, Liu D Y, et al. The impact of fenarimol application on the Magnaporthe poae and fungi in the rhizosphere soil of Kentucky bluegrass(Poa pratensis L.)[J]. Journal of Nanjing Agricultural University, 2015,38(4): 590–595. DOI: 10.7685/j.issn.1000-2030.2015.04.010 (in Chinese) |
| [21] | Lan P T N, Hayashi H, Sakamoto M, et al. Phylogenetic analysis of cecal microbiota in chicken by the use of 16S rDNA clone libraries[J]. Microbiology and Immunology, 2002,46(6): 371–382. DOI: 10.1111/mim.2002.46.issue-6 |
| [22] | Pajarillo E A B, Chae J P, Balolong M P, et al. Pyrosequencing-based analysis of fecal microbial communities in three purebred pig lines[J]. Journal of Microbiology, 2014,52(8): 646–651. DOI: 10.1007/s12275-014-4270-2 |
| [23] | Hildebrand F, Nguyen T L, Brinkman B, et al. Inflammation-associated enterotypes,host genotype,cage and inter-individual effects drive gut microbiota variation in common laboratory mice[J]. Genome Biol, 2013,14(1): R4. DOI: 10.1186/gb-2013-14-1-r4 |
| [24] | Pajarillo E A B, Chae J P, Kim H B, et al. Barcoded pyrosequencing-based metagenomic analysis of the faecal microbiome of three purebred pig lines after cohabitation[J]. Applied Microbiology and Biotechnology, 2015,99(13): 5647–5656. DOI: 10.1007/s00253-015-6408-5 |
| [25] | Santos S S, Pardal S, Proença D N, et al. Diversity of cloacal microbial community in migratory shorebirds that use the Tagus estuary as stopover habitat and their potential to harbor and disperse pathogenic microorganisms[J]. FEMS Microbiology Ecology, 2012,82(1): 63–74. DOI: 10.1111/fem.2012.82.issue-1 |
| [26] | Benedetti P, Rassu M, Pavan G, et al. Septic shock,pneumonia,and soft tissue infection due to Myroides odoratimimus:report of a case and review of Myroides infections[J]. Infection, 2011,39(2): 161–165. DOI: 10.1007/s15010-010-0077-1 |
| [27] | Ktari S, Mnif B, Koubaa M, et al. Nosocomial outbreak of Myroides odoratimimus urinary tract infection in a Tunisian hospital[J]. Journal of Hospital Infection, 2012,80(1): 77–81. DOI: 10.1016/j.jhin.2011.09.010 |
| [28] | Lambiase A, Rossano F, Pezzo M D, et al. Sphingobacterium respiratory tract infection in patients with cystic fibrosis[J]. BMC Research Notes, 2009,2(1): 262. DOI: 10.1186/1756-0500-2-262 |
| [29] | Proesmans M, Vermeulen F, Boulanger L, et al. Comparison of two treatment regimens for eradication of Pseudomonas aeruginosa infection in children with cystic fibrosis[J]. Journal of Cystic Fibrosis, 2013,12(1): 29–34. DOI: 10.1016/j.jcf.2012.06.001 |
| [30] | Wang Q, Chang B J, Riley T V. Erysipelothrix rhusiopathiae[J]. Veterinary Microbiology, 2010,140(3): 405–417. |
| [31] | Hanski I, von Hertzen L, Fyhrquist N, et al. Environmental biodiversity,human microbiota,and allergy are interrelated[J]. Proc Natl Acad Sci USA, 2012,109(21): 8334–8339. DOI: 10.1073/pnas.1205624109 |




