文章信息
- 钟飞燕, 张曼, 戴蓉, 江海东, 周琴
- ZHONG Feiyan, ZHANG Man, DAI Rong, JIANG Haidong, ZHOU Qin
- 蕾薹期干旱对油菜生长和抗氧化特性的影响及三唑酮的缓解效应
- Alleviative effects of triadimefon(TDM) on the growth and antioxidant in oilrape under drought at the bolting-stage
- 南京农业大学学报, 2016, 39(5): 730-738
- Journal of Nanjing Agricultural University, 2016, 39(5): 730-738.
- http://dx.doi.org/10.7685/jnau.201603006
-
文章历史
- 收稿日期: 2016-03-03
长江流域是我国冬油菜主要分布区, 虽然降雨充沛, 但全年降水分配不均, 季节性干旱时常发生, 给油菜生产造成巨大损失[1]。据国家粮油信息中心统计, 2010年云南、贵州发生的干旱造成油菜籽减产50万t, 较2009年减产50%。油菜蕾薹期是营养生长旺盛、生殖生长由弱转强的时期, 此期油菜花芽不断分化, 花蕾快速生长, 是决定有效花芽数的关键时期, 直接影响成熟期的角果数[2]。同时, 蕾薹期也是油菜对水分相对敏感的时期, 蕾薹期缺水导致花芽分化数减少, 有效分枝少, 花序短, 花器脱落严重, 单株角果数减少, 产量明显降低[3]。因此深入研究蕾薹期干旱对油菜生长及产量影响及如何有效提高油菜的抗旱性具有重要意义。
三唑酮(TDM)是一种外源植物生长调节剂, 化学名1-(4-氯苯氧基)-3, 3-二甲基-1-(1, 2, 4-三唑-1-基)-2-丁酮, 它能提高植物抗逆性[4]。有报道指出, 三唑酮处理离体黄瓜子叶[5]后, 能够提高叶绿素、可溶性蛋白和游离脯氨酸含量, 同时不同程度地抑制ROS的累积, 降低植株体内MDA含量。三唑酮处理的玫瑰切花POD活性维持在较高水平[6]; 三唑酮在处理逆境下的长春花[7]和黄瓜幼苗[8]时, 显著提高了植株叶片中SOD、CAT等抗氧化酶活性以及非酶抗氧化剂GSH和AsA的含量。但是否对油菜干旱也起到明显缓解效果有待研究。因此, 笔者以‘南农油4号’为材料, 研究TDM处理对蕾薹期遭受干旱胁迫的油菜生长、渗透调节及抗氧化系统与产量的影响, 为油菜抗旱栽培提供理论依据和技术支持。
1 材料与方法 1.1 试验材料供试材料为南京农业大学农学院种业系培育的油菜品种‘南农油4号’, 喷施药剂为99.6%的三唑酮原药(山西上格之路生物科学有限公司提供)。
1.2 试验设计试验于2013年10月17日至2014年6月4日在南京农业大学牌楼试验站进行。试验用盆高20 cm、内径25.5 cm, 每盆装土8 kg, 基肥为尿素、磷酸二氢钾, 施用量分别为8 g和4.6 g, 有机肥0.4 kg(有机质≥45%, 氮磷钾≥5%)。每盆播种20粒, 3叶期定苗, 每盆留长势一致的苗3株。试验共设3个处理:正常对照(CK)、干旱处理(D)和干旱+TDM处理(DT), 每个处理设3个重复。在油菜蕾薹期进行干旱处理, 通过称重法控制土壤相对含水量, 正常对照处理土壤相对含水量保持在75%, 干旱处理土壤相对含水量为45%。在干旱5 d时, 干旱+TDM处理喷施质量浓度为240 mg · L-1的TDM(TDM质量浓度根据预试验结果确定), 干旱处理与正常对照喷施等量蒸馏水, 喷施至叶片正反面均有药剂滴下为止(喷施量大约400 mL)。2个干旱处理持续干旱14 d后复水, 此后各处理进行同样水分管理。分别在干旱开始后5、8 d(TDM处理3 d)、11 d(TDM处理6 d)、14 d(TDM处理9 d)及复水后6 d(干旱开始后20 d)取样。取样时间为09:00—11:00, 所取植株按照根、茎、叶分样, 称取鲜质量后, 烘干至恒质量并称取干物质质量。同时取最上面3片完全展开叶, 经液氮处理后-40 ℃冷冻存放, 用于生理指标的测定。
1.3 测定指标与方法叶片相对含水量=(鲜质量-干质量)/(饱和质量-干质量)[9]。叶绿素含量测定采用丙酮提取比色法[9]。
气孔保卫细胞大小测定:在干旱处理11 d的上午10:00进行气孔样品的采集。在叶片上表皮均匀涂一层无色指甲油, 晾干后用透明胶带撕下, 放到载玻片上。在显微镜下观察表皮气孔保卫细胞为肾形, 两边对称, 气孔外缘清晰, 呈椭圆形, 通过目镜测微尺测出该椭圆的长短轴长[10]。在40×目镜下观察张开的气孔数量, 在100×目镜下测量气孔细胞长短轴(即气孔长度与宽度)。每片叶随机观察6个视野, 每处理3个重复。
可溶性糖含量测定采用蒽酮比色法[11]; 蔗糖采用间苯二酚比色法[11]; 可溶性蛋白含量采用考马斯亮蓝G-250法[9]; 游离脯氨酸含量测定参照Saladin等[12]的方法。
超氧化物歧化酶(SOD)活性测定采用NBT法, 过氧化物酶(POD)活性测定采用愈创木酚法, 过氧化氢酶活性(CAT)采用高锰酸钾滴定法[11]; 丙二醛(MDA)含量测定采用许长成等[13]的方法; 超氧阴离子(O2·)的产生速率测定采用羟胺法[11]; H2O2含量用南京建成生物公司提供的试剂盒测定; 抗坏血酸(AsA)含量测定参照汤章城[14]的方法; 还原型谷胱甘肽(GSH)含量测定参照Guri[15]的方法; 抗坏血酸过氧化物酶(APX)、谷胱甘肽过氧化物酶(GPX)活性测定参照Nakano等[16]的方法; 谷胱甘肽还原酶(GR)活性测定参照Sgherri等[17]的方法; 单脱氢抗坏血酸还原酶(MDHAR)活性测定参照Krivosheeva等[18]的方法。
考种与产量:在油菜成熟期, 每处理取10株进行考种; 每角粒数测定:每株随机取50角果进行粒数统计取平均值; 千粒质量测定:每株随机称1 000粒质量取平均值。
1.4 数据统计与分析采用Excel 2013处理试验数据, 采用SPSS 16.0软件对试验数据进行差异显著性分析, 利用Sigma Plot 12.5软件绘图。
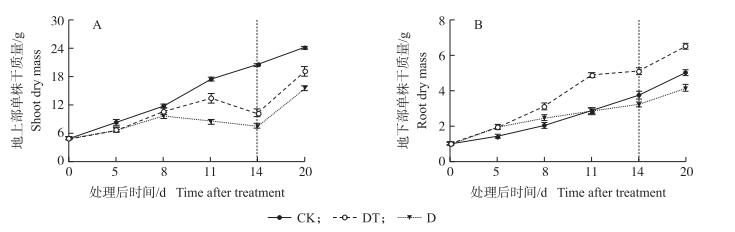
2 结果与分析 2.1 TDM和干旱胁迫对蕾薹期油菜生物量的影响如图 1所示, 随干旱胁迫时间的延长油菜地上部增长缓慢。在干旱11 d时, 干旱处理的地上部干质量仅是对照的60.74%;而干旱处理后喷施TDM能缓解干旱胁迫, DT处理地上部干质量较干旱处理增加57.42%。同时, 干旱胁迫也延缓了后期油菜地下部生长。干旱14 d时, 干旱处理的地下部干质量较对照下降13.83%;干旱处理后喷施TDM显著提高地下部干质量, DT处理的地下部干质量较干旱处理增加36.72%。
|
图 1 干旱胁迫下三唑酮(TDM)对蕾薹期油菜地上部干质量(A)和地下部干质量(B)的影响
Figure 1 The effect of triadimefon(TDM)application on shoot(A)and root(B)dry mass of oilrape at bolting-stage under drought-stress
1)图中竖线为干旱和复水的分界线。Vertical line is the dividing line of the drought and re-watering. 2)CK:正常对照Control; DT:干旱+TDM处理Drought+TDM; D:干旱处理Drought. The same as follows. |
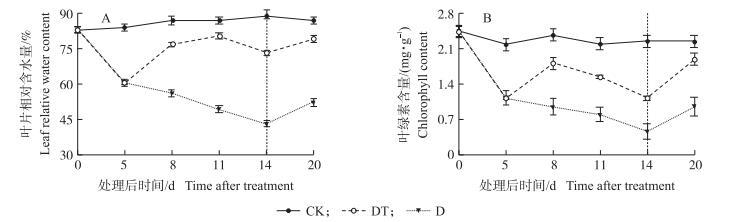
如图 2所示, 干旱胁迫导致油菜叶片相对含水量显著降低, 在干旱14 d时, 干旱处理较对照降低51.55%;干旱处理后喷施TDM能减缓相对含水量的下降, 在喷施6 d(干旱后11 d)与9 d(干旱后14 d)时, DT处理较干旱处理分别提高38.59%与41.17%。干旱导致叶绿素降解, 在干旱14 d时, 干旱处理叶片中叶绿素含量仅是对照的20%;干旱处理后喷施TDM能明显减缓叶绿素的降解速率, 尤其在TDM处理3 d时(干旱后8 d), DT处理的叶绿素含量较干旱处理提高45.15%。
|
图 2 干旱胁迫下喷施TDM对蕾薹期油菜叶片相对含水量(A)与叶绿素含量(B)的影响 Figure 2 The effect of TDM application on relative water content(A)and chlorophyll content(B)of oilrape at bolting-stage under drought-stress |
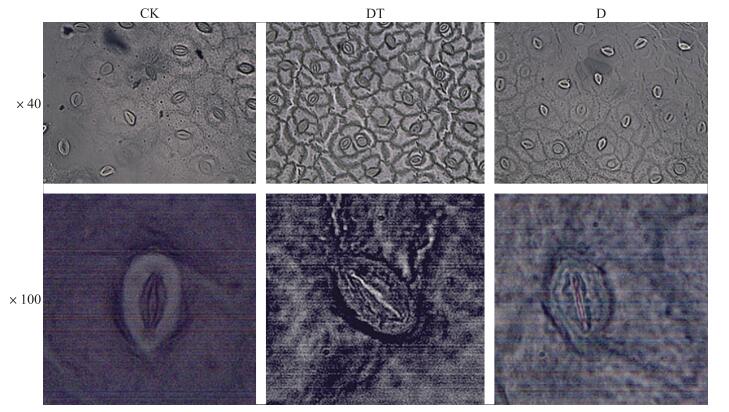
从图 3和表 1可见, 干旱胁迫导致单个气孔减小, 张开的气孔数量显著下降, 气孔关闭比例明显增加, 干旱处理气孔关闭比例是对照的2.8倍; 干旱处理后喷施TDM促进了气孔的开放, 使得单个气孔长度略有增加, 而气孔宽度显著增加, 同等视野下张开的气孔数量显著增加, DT处理张开的气孔数量较干旱处理增加51.85%。
|
图 3 干旱胁迫下喷施TDM对蕾薹期油菜叶片上表皮气孔形态的影响 Figure 3 The effect of TDM application on stomata morphology of oilrape leaves at bolting-stage under drought-stress |
| 处理 Treatment |
张开的气孔数量/mm-2 Number of opening stoma |
气孔关闭比例 Stomata closure proportion |
气孔长度/μm Stomata length |
气孔宽度/μm Stomata width |
| CK | 125±14a | 26.0%c | 18.73a | 9.25a |
| DT | 123±17a | 57.1%b | 17.62b | 8.81b |
| D | 81±10b | 73.5%a | 17.44b | 8.24c |
| 注:同列不同小写字母表示不同处理间在0.05水平差异显著。 Note:The different small letters in the same column indicate significant difference among treatment at 0.05 level. The same as below. |
||||
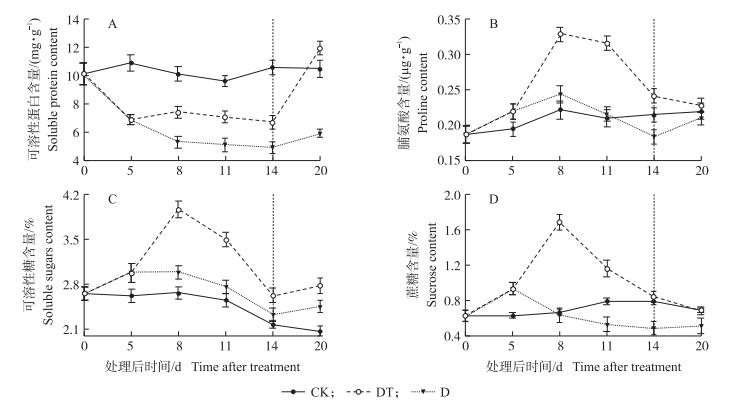
干旱胁迫导致油菜叶片可溶性蛋白含量逐渐降低(图 4-A)。干旱处理后喷施TDM能减缓可溶性蛋白含量的降低, 喷施TDM后的3、6、9 d, DT处理叶片可溶性蛋白含量分别较干旱处理提高28.14%、27.63%和26.33%。
|
图 4 干旱胁迫下喷施TDM对蕾薹期油菜叶片渗透性物质可溶性蛋白(A)、脯氨酸(B)、可溶性糖(C)与蔗糖(D)含量的影响 Figure 4 The effect of TDM application on the content of soluble protein(A), proline(B), soluble sugars(C)and sucrose(D)of oilrape at bolting-stage under drought-stress |
干旱初期, 脯氨酸含量增加, 随着干旱时间的延长其含量逐渐降低(图 4-B)。干旱处理后喷施TDM能显著增加脯氨酸的含量, 尤其在TDM处理3 d时增加幅度最大, 较干旱处理提高25.91%。
干旱导致油菜叶片可溶性糖含量增加(图 4-C)。干旱处理后喷施TDM, 可溶性糖含量首先大幅增加, 8 d后迅速下降, 但一直高于干旱与对照处理;在喷施TDM后3、6、9 d, DT处理可溶性糖含量较干旱处理分别提高24.49%、20.92%和11.41%。
干旱胁迫对蔗糖含量的影响也呈现先上升后下降的趋势(图 4-D)。在干旱8 d时, 蔗糖含量明显低于正常对照, 在干旱14 d时, 干旱处理蔗糖含量较对照下降38.62%。干旱处理后喷施TDM处理显著提高蔗糖含量, 并在喷施TDM 3 d时达到峰值, DT处理蔗糖含量较干旱处理提高62.18%。
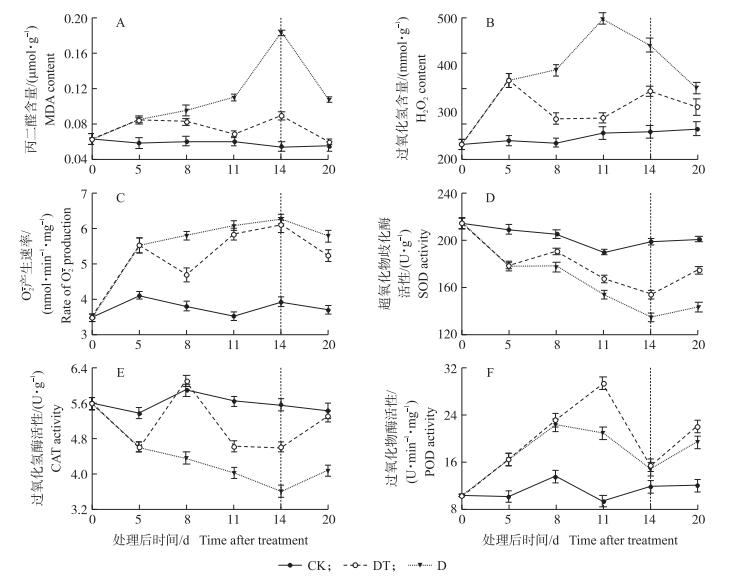
2.5 TDM和干旱胁迫对蕾薹期油菜叶片抗氧化系统的影响 2.5.1 对叶片MDA含量的影响如图 5-A所示, 随着干旱胁迫时间的延长, MDA含量呈上升趋势, 在干旱14 d时, D处理的MDA含量是对照的4.3倍。干旱处理后喷施TDM能有效减缓MDA含量的增加, 在喷施6和9 d时, DT处理MDA含量较干旱处理分别降低37.27%和51.09%。
|
图 5 干旱胁迫下喷施TDM对蕾薹期油菜叶片MDA含量(A)、H2O2含量(B)、O2·产生速率(C)及SOD(D)、CAT(E)和POD(F)活性的影响 Figure 5 The effect of TDM application on MDA content(A), H2O2 content(B), rate of O2· production(C)and the activities of SOD(D), CAT(E), POD(F)of oilrape leaves at bolting-stage under drought-stress |
如图 5-B、C所示, 干旱胁迫导致H2O2含量与O2·产生速率迅速提高。干旱处理后喷施TDM能降低H2O2含量与O2·产生速率并延缓他们后期的增加速率, 在喷施TDM 3 d时, DT处理H2O2含量与O2·产生速率较干旱处理下降26.43%与19.23%。
2.5.3 对叶片SOD、POD、CAT活性的影响如图 5-D所示, 随干旱时间的延长, 油菜叶片SOD活性不断降低, 在干旱14 d时, 干旱处理SOD活性较对照降低32.33%。而干旱处理后喷施TDM延缓了叶片中SOD活性降低的速率, 其活性显著高于干旱处理。
干旱胁迫导致CAT活性降低(图 5-E)。干旱处理后喷施TDM, CAT活性有一个明显增加的趋势, 随后逐渐降低, 其活性始终显著高于干旱处理的酶活性, 在TDM处理3 d时, DT处理的CAT活性较干旱处理提高28.36%。
POD活性变化趋势与SOD、CAT活性变化不同(图 5-F)。随干旱胁迫时间的延长, POD活性呈先升高后降低的趋势, 但其活性始终高于对照。干旱处理后喷施TDM, POD活性进一步提高, 尽管后期酶活性大幅下降, 但依然高于干旱处理。在TDM处理6 d时, POD活性达到峰值, 较干旱处理提高28.69%。
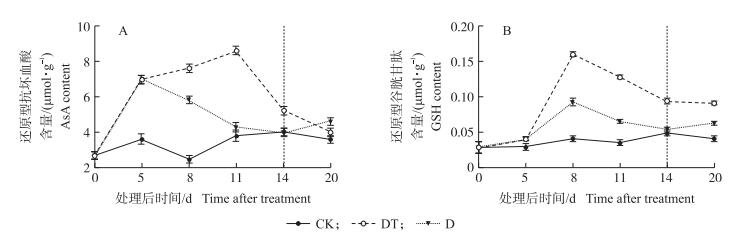
2.5.4 对叶片抗坏血酸及谷胱甘肽含量的影响如图 6所示, 干旱胁迫期间AsA含量呈单峰曲线, 峰值出现在干旱胁迫5 d, 较对照增加48.29%。干旱处理后喷施TDM显著减缓干旱后期AsA含量的降低, 使DT处理的AsA含量处于较高水平。GSH含量随干旱时间延长呈先升后降的趋势, 峰值出现在干旱处理8 d, 与对照相比增加55.71%。干旱处理后喷施TDM, GSH含量迅速提高, 其含量在TDM处理3 d时较干旱处理提高42.45%。
|
图 6 干旱胁迫下喷施TMD对蕾薹期油菜叶片AsA(A)和GSH(B)含量的影响 Figure 6 The effect of TDM application on AsA(A)and GSH(B)content of oilrape leaves at bolting-stage under drought-stress |
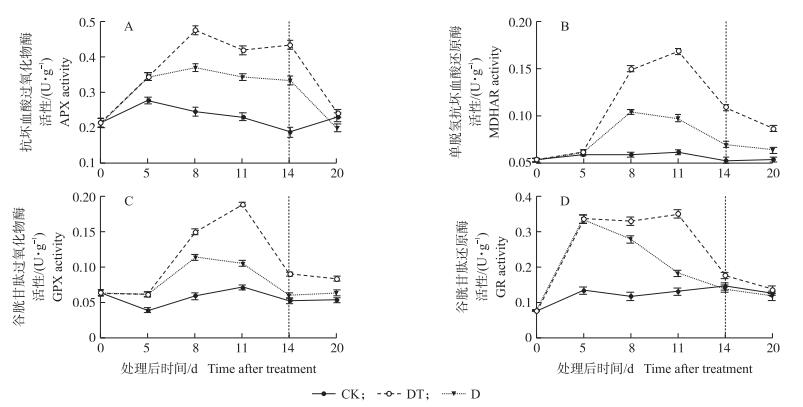
如图 7所示, 长期干旱胁迫下, APX、MDHAR、GPX、GR活性出现先升高后降低的趋势。在干旱8 d时, APX、MDHAR、GPX活性达到峰值, 比对照分别高出33.51%、42.87%、47.79%, 而GR活性在干旱5 d时达到峰值, 较对照酶活性提高59.92%。干旱处理后喷施TDM明显提高APX、MDHAR、GPX、GR活性, 且延缓后期其活性的降低:DT处理的APX活性在喷施TDM 3 d时较干旱处理提高22.35%(图 7-A); MDHAR活性在喷施TDM 6 d时较干旱处理提高41.89%(图 7-B); GPX活性在喷施TDM 6 d时较干旱处理提高62.13%(图 7-C); 在喷施TDM 3、6、9 d时, DT处理的GR活性较干旱处理分别提高15.67%、47.92%、21.56%(图 7-D)。
|
图 7 干旱胁迫下喷施TDM对蕾薹期油菜叶片APX(A)、MDHAR(B)、GPX(C)和GR(D)活性的影响 Figure 7 The effect of TDM application on the activities of APX(A), MDHAR(B), GPX(C)and GR(D)of oilrape leaves at bolting-stage under drought-stress |
如表 2结果所示, 干旱胁迫显著降低了油菜的主花序角果数、单角果粒数、千粒质量和单株产量, 其中单株产量较对照降低57.76%。干旱处理后喷施TDM显著提高了油菜主花序角果数、千粒质量及单株产量, DT处理的千粒质量和单株产量分别较干旱处理提高10.32%和21.72%。
| 处理 Treatment |
主花序角果数 PMIN |
分枝总角果数 PNB |
单株总角果数 PN |
单角果粒数 SN |
千粒质量/g WTS |
单株产量/g YP |
| CK | 34.00a | 137.33a | 179.67a | 27.88a | 4.34b | 21.07a |
| DT | 21.00b | 145.67a | 163.00a | 14.69b | 4.75a | 11.37b |
| D | 10.00c | 159.67a | 169.67a | 12.31b | 4.26b | 8.90c |
| Note: PMIN:Pod number on main inflorescence; PNB:Pod number on branch; PN:Pod per plant; SN:Seed per pod; WTS:Thousand-seed weight; YP:Yield per plant | ||||||
在遭受干旱胁迫时, 油菜植株形态会发生一系列变化, 叶片可溶性糖、脯氨酸等渗透调节物质含量随干旱胁迫时间的延长逐渐降低[19], 产量及其构成因素显著降低[20]。本研究表明:长期干旱胁迫导致蕾薹期油菜地上部与地下部干质量增长停滞, 叶绿素含量降低, 叶片气孔关闭; 可溶性糖、蔗糖、可溶性蛋白与脯氨酸的含量先升后降, 叶片相对含水量降低; 显著降低油菜的主花序角果数、单角果粒数、千粒质量和单株产量。
三唑类生长调节剂能延缓植物地上部的伸长, 促进根的生长[21]。本试验在干旱处理后喷施TDM, 一定程度上减轻干旱对油菜生物量的影响, 减少对叶绿素的降解, 增加气孔的宽度与张开的个数, 提高叶片相对含水量; 明显提高可溶性糖、蔗糖、可溶性蛋白与脯氨酸的含量并减缓后期降低的趋势; 明显提高了千粒质量, 主花序角果数, 最终提高单株产量。出现此结果可能是由于三唑酮主要通过抑制异戊稀途径来改变植物激素的水平, 进而调节植物的生长和发育[7]。TDM能通过减少酚类物质的降解减缓IAA的分解, 维持地下部与地上部的生长; 抑制ABA的合成, 控制气孔关闭程度[22], 降低水分蒸腾和维持光合作用的进行, 从而维持植株干物质积累, 提高水分利用率, 缓解干旱胁迫的伤害。通过降低脯氨酸氧化酶(PROX)活性增强谷氨酸激酶(γ-GK)活性来增加脯氨酸含量, 通过增加叶片中SS、SPS活性来增加可溶性糖及蔗糖的积累[23], 提高叶片渗透能力进一步减少水分蒸腾, 提高油菜抗旱性。TDM处理后千粒质量的提高是保产的主要原因。
3.2 蕾薹期干旱对油菜抗氧化系统的影响及TDM的缓解效应植物受到逆境胁迫, 体内活性氧水平升高, 膜脂过氧化程度加剧, 叶绿素等生物大分子被破坏[24], 短期胁迫可以提高叶片中SOD、POD、CAT、APX和GR活性[25], AsA、GSH含量显著升高, 通过清除大量的活性氧维持细胞正常代谢[26]。
本试验结果显示, 随着干旱胁迫时间的延长, 油菜叶片中叶绿素含量降低, H2O2含量与O2·产生速率增加, MDA含量增加, 膜脂过氧化程度加深; 油菜叶片SOD、CAT活性下降, POD、APX、GPX、MDHAR和GR活性与AsA、GSH含量先增后降。这可能是由于干旱程度较严重, 而大棚内气温太高, 双重胁迫可能使得活性氧对酶的氧化攻击促使SOD、CAT酶蛋白降解失活[27]。油菜叶片中的ROS主要依靠POD与A-G循环系统清除, 随干旱时间延长, POD酶活性降低, MDHAR和GR活性均逐渐降低, AsA和GSH的再生能力降低, 同时APX、GPX活性也降低, A-G循环平衡系统受到破坏, 叶绿体与细胞膜遭到严重破坏, 植株抗逆性降低。
喷施TDM后显著降低O2·产生速率、H2O2含量和MDA含量, 使SOD、CAT、POD活性显著提高, 同时有效减缓干旱后期APX与GPX活性的降低, 显著提高油菜叶片中MDHAR和GR的活性, AsA和GSH含量始终显著高于干旱处理。说明TDM能通过提高抗氧化酶活性与非酶抗氧化物质含量, 快速清除H2O2, 降低活性氧水平, 减少ROS的积累, 抑制MDA含量增加, 从而能够更好地保护叶绿体与细胞膜结构, 缓解干旱对油菜叶片的氧化损伤。
| [1] | 李慧琳, 陶霞, 万林, 等. 氯化胆碱对干旱胁迫下油菜幼苗生理特性的影响[J]. 水土保持学报, 2013, 27(5): 228–233, 243. Li H L, Tao X, Wan L, et al. Effects of choline chloride on physiological characteristics of rapeseed seedlings under drought stress[J]. Journal of Soil and Water Conservation, 2013,27(5): 228–233, 243. (in Chinese) |
| [2] | 胡立勇, 丁艳锋. 作物栽培学[M]. 北京: 高等教育出版社, 2008 : 381 -385. Hu L Y, Ding Y F. Crop Cultivation Science[M]. Beijing: Higher Education Press, 2008 : 381 -385. (in Chinese) |
| [3] | 白鹏, 冉春艳, 谢小玉. 干旱胁迫对油菜蕾薹期生理特性及农艺性状的影响[J]. 中国农业科学, 2014, 47(18): 3566–3576. Bai P, Ran C Y, Xie X Y. Influence of drought stress on physiological characteristics and agronomic traits for bud stage of rapeseed[J]. Agricultural Sciences China, 2014,47(18): 3566–3576. (in Chinese) |
| [4] | Jaleel C A, Gopi R, Manivannan P, et al. Endogenous hormonal and enzymatic responses of Catharanthus roseus with triadimefon application under water deficits[J]. Comptes Rendus Biologies, 2008,331(11): 844–852. DOI: 10.1016/j.crvi.2008.07.025 |
| [5] | 冯兆忠, 王静, 冯宗炜. 三唑酮对离体黄瓜子叶过氧化物酶活性及蛋白质含量的影响[J]. 环境科学, 2002, 23(5): 126–128. Feng Z Z, Wang J, Feng Z W. Effect of triadimefon on activity of peroxidase and soluble protein content in detached cucumber cotyledons[J]. Chinese Journal of Environmental Science, 2002,23(5): 126–128. (in Chinese) |
| [6] | 周晓馥, 徐洪伟. 三唑酮对玫瑰切花衰老指标的影响[J]. 植物生理学通讯, 2000, 36(5): 409–411. Zhou X F, Xu H W. Effects of triadimefon on indexes of senescence in cut rose[J]. Plant Physiology Communications, 2000,36(5): 409–411. (in Chinese) |
| [7] | Jaleel C A, Gopi R, Kishorekumar A, et al. Interactive effects of triadimefon and salt stress on antioxidative status and ajmalicine accumulation in Catharanthus roseus[J]. Acta Physiologiae Plantarum, 2008,30(3): 287–292. DOI: 10.1007/s11738-007-0119-1 |
| [8] | Feng Z, Guo A, Feng Z. Amelioration of chilling stress by triadimefon in cucumber seedlings[J]. Plant Growth Regulation, 2003,39(3): 277–283. DOI: 10.1023/A:1022881628305 |
| [9] | 王学奎. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2006 . Wang X K. Principle and Technology of Plant Physiology and Biochemistry Experiment[M]. Beijing: Higher Education Press, 2006 . (in Chinese) |
| [10] | 刘成洪, 王亦菲, 陆瑞菊, 等. 用气孔保卫细胞周长鉴定甘蓝型油菜植株倍性水平[J]. 上海农业学报, 2002, 18(3): 35–38. Liu C H, Wang Y F, Lu R J, et al. Etimation of plantlet ploidy level of Brassica napus by observing stoma guard cell circumferences[J]. Shanghai Journal of Agricultural Sciences, 2002,18(3): 35–38. (in Chinese) |
| [11] | 张志良, 瞿伟菁. 植物生理学实验指导[M]. 北京: 高等教育出版社, 2003 . Zhang Z L, Qu W J. Experiment Guide of Plant Physiology[M]. Beijing: Higher Education Press, 2003 . (in Chinese) |
| [12] | Saladin G, Magné C, Clément C. Stress reactions in Vitis vinifera L. following soil application of the herbicide flumioxazin[J]. Chemosphere, 2003,53(3): 199–206. DOI: 10.1016/S0045-6535(03)00515-0 |
| [13] | 许长成, 赵世杰, 邹琦. 植物组织内丙二醛的分离与鉴定[J]. 植物生理学通讯, 1992, 28(4): 288–290. Xu C C, Zhao S J, Zou Q. The communication and identification of malonaldehyde in plant tissue isolation[J]. Plant Physiology Communications, 1992,28(4): 288–290. (in Chinese) |
| [14] | 汤章城. 现代植物生理学实验指南[M]. 北京: 科学出版社, 1999 . Tang Z C. Experimental Guide of Modern Plant Physiology[M]. Beijing: Science Press, 1999 . (in Chinese) |
| [15] | Guri A. Variation in glutathione and ascorbic acid content among selected cultivars of Phaseolus vulgaris prior to and after exposure to ozone[J]. Canadian Journal of Plant Science, 1983,63(3): 733–737. DOI: 10.4141/cjps83-090 |
| [16] | Nakano Y, Asada K. Hydrogen peroxide is scavenged by ascorbate-specific peroxidase in spinach chloroplasts[J]. Plant and Cell Physiology, 1981,22(5): 867–880. |
| [17] | Sgherri C L M, Loggini B, Puliga S. Antioxidant system in Sporobolus stapfianus:changes in response to desiccation and rehydration[J]. Phytochemistry, 1994,35(3): 561–565. DOI: 10.1016/S0031-9422(00)90561-2 |
| [18] | Krivosheeva A, Tao D L, Ottander C, et al. Cold acclimation and photoinhibition of photosynthesis in Scots pine[J]. Planta, 1996,200(3): 296–305. |
| [19] | 郭雪松, 唐章林. PEG胁迫下42个油菜品种(系)耐旱性的评价[J]. 西南大学学报(自然科学版), 2009, 31(10): 1–7. Guo X S, Tang Z L. Evaluation of drought tolerance of 42 rapeseed genotypes in different PEG concentration treatments[J]. Journal of Southwestern University(Natural Science Edition), 2009,31(10): 1–7. (in Chinese) |
| [20] | Moosavi A A, Mansouri S, Zahedifar M, et al. Effect of water stress and nickel application on yield components and agronomic characteristics of canola grown on two calcareous soils[J]. Archives of Agronomy and Soil Science, 2014,60(20): 7090–7094. |
| [21] | Muthukumarasamy M, Gupta S D, Panneerselvam R. Enhancement of peroxidase, polyphenol oxidase and superoxide dismutase activities by triadimefon in NaCl stressed Raphanus sativus L[J]. Biologia Plantarum, 2000,43(2): 317–320. DOI: 10.1023/A:1002741302485 |
| [22] | 郑青松, 刘金隆, 石峰, 等. 渗透胁迫下植物细胞脱落酸的信号转导途径研究进展[J]. 南京农业大学学报, 2014, 37(5): 1–6. Zheng Q S, Liu J L, Shi F, et al. Research advance on signal transduction pathway indu ABA in plants under osmotic stress[J]. Journal of Nanjing Agricultural University, 2014,37(5): 1–6. DOI: 10.7685/j.issn.1000-2030.2014.05.001 (in Chinese) |
| [23] | 吴园园, 田一丹, 刘丽欣, 等. 三唑酮预处理对花期大豆干旱胁迫及复水后生理特性及产量的影响[J]. 核农学报, 2013, 27(11): 1749–1755. Wu Y Y, Tian Y D, Liu L X, et al. Effects of Triadimefon on morphological characteristics and yield traits of soybean under drought and re-watering at flowering stage[J]. Journal of Nuclear Agricultural Sciences, 2013,27(11): 1749–1755. (in Chinese) |
| [24] | 王俊力, 王岩, 赵天宏, 等. 臭氧胁迫对大豆叶片抗坏血酸-谷胱甘肽循环的影响[J]. 生态学报, 2011, 31(8): 2068–2075. Wang J L, Wang Y, Zhao T H, et al. Effects of ozone on ascorbate acid-glutathione cycle in soybean(Glycine max)leave[J]. Acta Ecologica Sinica, 2011,31(8): 2068–2075. (in Chinese) |
| [25] | Tian Z, Wang F, Zhang W, et al. Antioxidant mechanism and lipid peroxidation patterns in leaves and petals of marigold in response to drought stress[J]. Horticulture Environment and Biotechnology, 2012,53(3): 183–192. DOI: 10.1007/s13580-012-0069-4 |
| [26] | 尹永强, 胡建斌, 邓明军. 植物叶片抗氧化系统及其对逆境胁迫的响应研究进展[J]. 中国农学通报, 2007, 23(1): 105–110. Yin Y Q, Hu J B, Deng M J. Latest development of antioxidant system and responses to stress in plant leaves[J]. Chinese Agricultural Science Bulletin, 2007,23(1): 105–110. (in Chinese) |
| [27] | 江洪强, 邢兴华, 周琴, 等. 外源α-萘乙酸对花期长期干旱大豆叶片抗氧化系统的影响[J]. 应用生态学报, 2015, 26(6): 1718–1726. Jiang H Q, Xing X H, Zhou Q, et al. Effects of exogenous-naphthaleneacetic acid on the antioxidation system in soybean leaves subjected to long-term drought stress during flowering[J]. Journal of Applied Ecology, 2015,26(6): 1718–1726. (in Chinese) |




