文章信息
- 孙嘉瑞, 曹轶男, 张新晨, 赵其岭, 鲍恩东, 吕英军
- SUN Jiarui, CAO Yinan, ZHANG Xinchen, ZHAO Qiling, BAO Endong, LÜ Yingjun
- 三聚氰胺与三聚氰酸混合物对小鼠睾酮生成和调控的影响
- Effect of mixture of melamine and cyanuric acid on production and synthesis regulation of testosterone in mice
- 南京农业大学学报, 2016, 39(4): 650-655
- Journal of Nanjing Agricultural University, 2016, 39(4): 650-655.
- http://dx.doi.org/10.7685/jnau.201510037
-
文章历史
- 收稿日期:2015-10-26
2007年美国发生4 000多起家养猫、狗中毒死亡事件,经临床检验发现其死亡原因为肾脏损伤,损伤原因主要与饲料中含有三聚氰胺(MA)及其同系物三聚氰酸(CA)有关[1, 2, 3]。此事件之后中国又发生婴儿奶粉中非法添加大量三聚氰胺,导致婴儿肾衰竭甚至死亡的恶性事件[4]。经过此类恶性事件,人们又重新关注三聚氰胺的毒副作用。三聚氰胺作为生产食品、饲料包装或餐具的原料,在较高的温度或酸度环境下可分解或溶出,从而进入人或动物体内[5]。三聚氰酸是三聚氰胺生产过程中的副产物,两者往往混合在一起。日常生活中,三聚氰酸可用作水的稳定剂,被广泛用于消毒杀菌剂及新型漂白剂等诸多领域[6, 7]。因此在人们的日常生活中,通过皮肤、呼吸道途径接触三聚氰胺、三聚氰酸以及其同系物几乎是不可避免的。
以往对三聚氰胺与三聚氰酸混合物(MC)的毒性研究主要集中于肾脏[3, 8, 9]。但随着研究深入,发现二者的混合物能够直接破坏小鼠睾丸血睾屏障,导致雄性小鼠睾丸精原细胞坏死、精子减少并且畸形率增加[10, 11, 12]。此外二者的混合物还可降低机体抗氧化水平,导致氧化损伤以及能量代谢障碍[13]。睾酮在雄性动物生殖系器官发育和精子形成过程中起着重要作用,到目前为止,未见MC对雄性激素睾酮合成影响的报道。因此,本试验目的是研究三聚氰胺与三聚氰酸混合物对小鼠睾酮合成和调控的影响,从而对三聚氰胺与三聚氰酸混合物的毒性研究提供进一步的理论支持。
1 材料与方法 1.1 主要仪器与试剂主要仪器:Sorvall Legend Micro 17R微量离心机(美国Thermo Scientific公司);Zeiss荧光显微镜(德国 Carl Zeiss公司);SN-695型智能放免γ测量仪(上海核所日环光电有限公司);Infinite 200多功能酶标仪(瑞士TECAN公司);荧光定量PCR仪(美国Bio-Rad公司)。
主要试剂:三聚氰胺(MA)、三聚氰酸(CA)(上海安普化学仪器有限公司);碘[I125]睾酮放射免疫分析药盒(北京北方生物技术研究所有限公司);反转录试剂盒和荧光染料(南京诺维赞生物科技有限公司);多克隆抗体:StAR(类固醇激素合成急性调节蛋白)、P450scc(胆固醇侧链裂解酶)、P450 17α(细胞色素17α-羟化酶)、17β-HSD(17β-羟类固醇脱氢酶)、3β-HSD(3β-羟基类固醇脱氢酶)(Santa Cruz);GAPDH抗体和抗β-tubulin抗体(Cell Signaling);马抗山羊IgG二抗(碧云天生物技术有限公司);ECL化学发光试剂盒(美国Thermo公司)。
1.2 试验动物及处理40只4周龄雄性成年ICR小鼠购自南京医科大学动物实验中心,人工控制保持室温20~25 ℃条件下进行饲养,辅助人工照明,光/暗周期为12 h/12 h,自由摄食、饮水。适应性饲养1周后,将小鼠随机分成4组,每组10只,即对照组(玉米油灌胃)、三聚氰胺与三聚氰酸混合物低剂量组(MA、CA各1 mg·kg-1,MC2组)、中剂量组(MA、CA各5 mg·kg-1,MC10组)、高剂量组(MA、CA各25 mg·kg-1,MC50组)。试验小鼠每天灌胃1次,持续28 d。试验结束后称小鼠质量;眼球框内取血,3 000 r·min-1 离心10 min制备血清;分离睾丸和附睾,剥离表面结缔组织和脂肪并且称量;左侧睾丸固定于体积分数为10%福尔马林溶液中,右侧睾丸经液氮快速冷冻后,转移至-80 ℃冰箱保存备用。
1.3 血清中睾酮水平测定血清中睾酮含量通过放射免疫测定试剂盒测定,于SN-695型智能放免γ测量仪上测定各管沉淀中的放射性计数。
1.4 荧光定量PCR检测小鼠睾酮合成相关蛋白基因表达从睾丸组织中提取出总mRNA,酶标仪测定RNA浓度。调整所有样品总mRNA至相同浓度,及时反转录成cDNA并于-20 ℃保存。PCR引物用Primer Premier 5.0软件设计,由上海英骏生物技术有限公司合成,引物序列见表 1。荧光定量PCR反应体系(20 μL)包括:2 μL cDNA,10 μL Master Mix,上、下游引物各0.4 μL,7.2 μL三蒸水。荧光定量PCR仪检测4个基因的mRNA表达量,利用2-ΔΔCT法计算各基因的相对表达量。
| 基因Gene | GenBank 登录号 GenBank accession No. | 引物对序列(5′→3′)Primer pairs sequence | 产物长度/bpProduct length |
| StAR | NM_011485.4 | AAGGAAAGCCAGCAGGAGAAC/TCCATGCGGTCCACAAGT | 135 |
| P450scc | NM_019779.3 | CCATCAGATGCAGAGTTTCCAA/TGAGAAGAGTATCGACGCATCCT | 110 |
| P450 17α | NM_007809.3 | CCATCCCGAAGGACACACAT/CTGGCTGGTCCCATTCATTT | 100 |
| 17β-HSD | NM_010475.1 | ATGCCCTCCTGGCTCCTT/CACCCACAGCGTTCAATT | 167 |
| β-actin | NM_007393.3 | GAGACCTTCAACACCCCAGC/ATGTCACGCACGATTTCCC | 236 |
每只小鼠的左侧睾丸放于RIPA蛋白裂解液中匀浆,14 000 g 4 ℃离心5 min,吸取上清液,并用BCA试剂盒测定蛋白浓度。均一化蛋白浓度后,变性,点样,将蛋白转到PVDF膜后,先用50 g·L-1脱脂奶粉37 ℃恒温培养箱封闭2 h,然后加目的抗StAR、P450scc、P450 17α、17β-HSD抗体和抗GAPDH或β-tubulin抗体,4 ℃孵育过夜,再用TBST洗膜3次,加入马抗山羊IgG二抗,室温孵育1 h,TBST洗3次。用ECL化学发光试剂盒在WB检测系统中进行显影。用Quantity one 4.6.2软件(Bio-Rad,USA)分析Western blot的条带。
1.6 免疫组化检测小鼠睾丸间质细胞数量将固定于10%福尔马林溶液中的睾丸组织样品经梯度乙醇脱水,二甲苯透明后,常规法石蜡包埋,连续切成4 μm厚的切片,将切片先后脱蜡和梯度水化后,PBS浸洗以终止反应,使用微波加热法修复抗原,然后将切片置于含体积分数为3%过氧化氢的甲醇溶液中避光静置10 min以灭活内源性过氧化物酶及生物素,PBS清洗3次后,用5%胎牛血清37 ℃温箱中封闭30 min,然后用抗3β-HSD抗体4 ℃孵育过夜。过夜切片37 ℃复温30 min后用PBS清洗3次,用马抗山羊IgG 37 ℃温箱孵育1 h,PBST清洗3次,DAB显色后苏木精复染;梯度乙醇脱水后二甲苯透明,树胶封片。每组选出5张睾丸切片,每张切片选出10个放大200倍的视野,用软件Image Pro-plus 6.0测量睾丸间质细胞的面积(μm2)来反映间质细胞数量。
1.7 统计分析用SPSS 21.0的单因素分析法对试验各组进行方差分析和多重比较,结果以平均值±标准差(x±SD)表示。
2 结果与分析 2.1 小鼠临床症状变化高剂量(MC50)组的小鼠表现为厌食、行动缓慢、弓背和被毛凌乱失去光泽,低剂量(MC2)和中剂量(MC10)组的小鼠仅表现为轻微的饮食量减少。MC50组小鼠质量明显低于对照组,其他各组质量与对照组无明显差异;MC50组小鼠睾丸质量低于对照组,但无显著差异;剖检肾脏发现MC50和MC10组小鼠的肾脏肿胀,呈棕黄色;睾丸表观无明显变化,但体积与对照组相比较小,表明该混合物对小鼠肾脏和睾丸产生毒副作用。
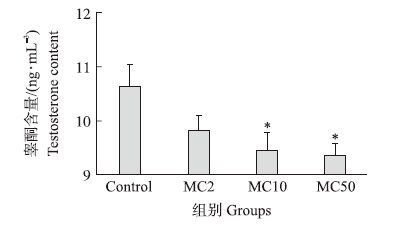
2.2 三聚氰胺与三聚氰酸混合物对小鼠血清睾酮含量的影响由图 1可见:小鼠经混合物处理后血清睾酮含量均低于对照组小鼠,且血清睾酮含量与MC剂量呈负相关,其中MC10和MC50组小鼠血清睾酮含量明显低于对照组(P<0.05)。
|
图 1 三聚氰胺(MA)与三聚氰酸(CA)混合物对小鼠血清睾酮含量的影响
Fig. 1 Effects of different doses of mixture of melamine (MA)and cyanuric acid(CA)on serum levels of testosterone in mice
在Control、MC2、MC10、MC50中MA和CA含量均分别为0、1、5和25 mg·kg-1. The content of MA and CA in Control,MC2,MC10 and MC50 is 0,1,5,25 mg·kg-1,respectively. *P<0.05,**P<0.01. The same as follows. |
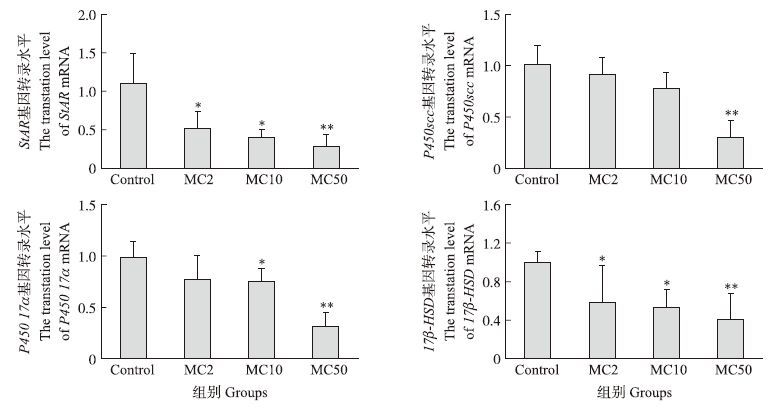
由图 2可知:MC处理组StAR mRNA表达量均低于对照组,其中MC2、MC10组StAR mRNA表达量与对照组差异显著(P<0.05),MC50组差异极显著(P<0.01);MC50组P450scc mRNA表达量极显著低于对照组(P<0.01);MC处理组P450 17α mRNA表达量均低于对照组,且MC10组与对照组差异显著(P<0.05),MC50组与对照组差异极显著(P<0.01);MC组17β-HSD mRNA表达量均降低,其中 MC2组、MC10组与对照组差异显著(P<0.05),MC50组与对照组差异极显著(P<0.01)。
|
图 2 三聚氰胺与三聚氰酸混合物对小鼠睾酮合成相关蛋白基因的影响 Fig. 2 Effects of mixture of melamine and cyanuric acid on mRNA expression of genes associated with testosterone synthesis |
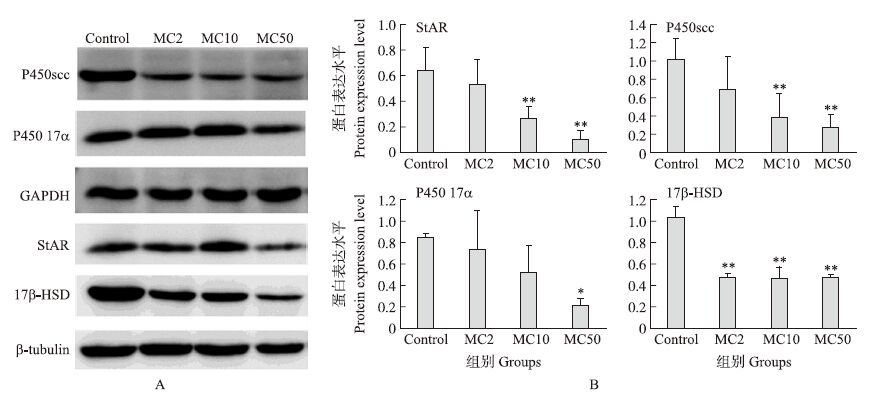
小鼠经三聚氰胺与三聚氰酸混合物处理后,StAR、P450scc、P450 17α和17β-HSD蛋白表达均低于对照组(图 3)。其中MC10和MC50组小鼠的StAR和P450scc蛋白表达与对照组相比差异极显著(P<0.01);MC50组小鼠的P450 17α蛋白表达极显著下降(P<0.01);此外,MC处理组的小鼠17β-HSD蛋白表达均极显著低于对照组(P<0.01)。
|
图 3 三聚氰胺与三聚氰酸混合物对小鼠睾酮合成相关蛋白表达的影响 Fig. 3 Effect of mixture of melamine and cyanuric acid on the expression level of testosterone synthesis proteins |
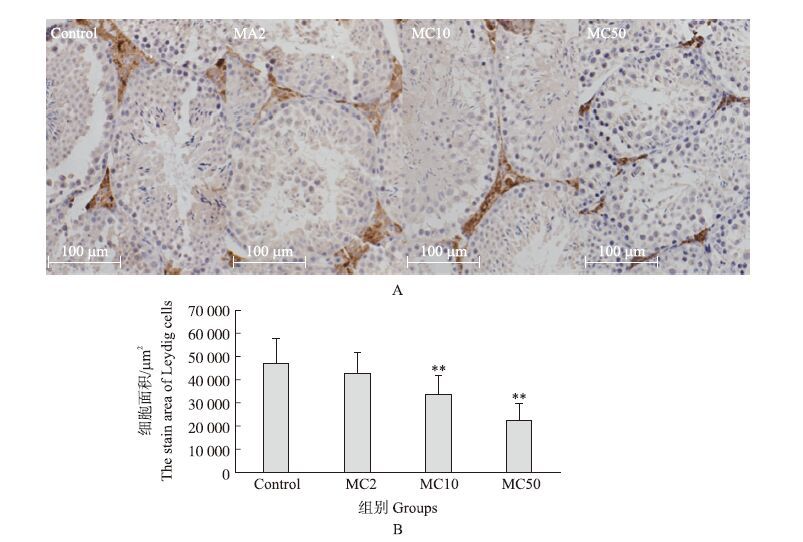
如图 4所示:MC处理组小鼠睾丸间质细胞数量均低于对照组,MC10和MC50组与对照组差异极显著(P<0.01),且小鼠睾丸间质细胞数量与混合物的浓度呈负相关。
|
图 4 三聚氰胺与三聚氰酸混合物对小鼠睾丸间质细胞(A)及细胞面积(B)的影响 Fig. 4 Effects of mixture of melamine and cyanuric acid on the stain area of Leydig cells 图中棕色的细胞为睾丸间质细胞。The Leydig cells were marked by brown signal. |
本试验结果表明对小鼠灌胃三聚氰胺与三聚氰酸混合物期间,小鼠出现了精神沉郁、采食量下降、弓背和被毛凌乱无光泽及体质量明显下降等临床症状,表明三聚氰胺与三聚氰酸混合物抑制了小鼠生长;此外小鼠肾脏肿大成棕黄色,睾丸质量减轻,表明该混合物对小鼠肾脏和睾丸产生毒副作用,这和以前的文章报道一致:Roy等[14]发现三聚氰胺与三聚氰酸混合物可导致小鼠肾小管中积聚大量结晶;Chang等[11]报道高剂量的三聚氰胺混合物可以破坏血睾屏障,促使精原细胞凋亡,减少了精子数量并诱导精子发生畸形。
睾酮作为一种重要的雄性激素,参与精原细胞的减数分裂及精子细胞向管腔的释放[15],同时可以促进睾丸发育,维持附睾结构及其功能,对第二性征的维持也有重要的作用。在本试验中,小鼠灌胃三聚氰胺与三聚氰酸混合物后,血清中睾酮含量明显下降,表明该混合物引起了睾酮生成障碍,从而可能引起睾丸发育缓慢以及精子数量减少和畸形发生。尽管睾酮的合成过程受到下丘脑-垂体-性腺轴以及反馈作用等多种因素调节,但睾丸间质细胞中类固醇合成酶介导和参与的生化反应,仍然是睾酮合成的基本途径[16]。类固醇合成急性调节蛋白(StAR)将游离的胆固醇从线粒体外膜转运到线粒体内膜,线粒体内膜上的细胞色素P450家族可将胆固醇进一步加工,其中胆固醇侧链裂解酶(P450scc)将胆固醇转化为孕烯醇酮,随后3β-羟基类固醇脱氢酶(3β-HSD)和17β-羟基类固醇脱氢酶(17β-HSD)将孕烯醇酮转化为雄烯二酮,最后在17β-HSD的催化作用下形成睾酮。本试验中睾酮合成相关蛋白基因和蛋白水平结果显示,各处理组的与睾酮合成相关蛋白StAR、P450scc、P450 17α和17β-HSD的mRNA水平和蛋白水平均低于对照组,表明三聚氰胺与三聚氰酸混合物可抑制StAR的合成从而造成向线粒体内膜转运的游离胆固醇减少,导致睾酮合成原料不足,而在睾酮合成后期,又可以通过抑制P450scc、P450 17α和17β-HSD干扰睾酮最终合成,因而造成血清中睾酮含量出现明显的下降。睾酮是在睾丸间质细胞中产生的,间质细胞的数量亦可影响机体血液中的睾酮含量。3β-HSD是睾丸间质细胞合成的主要酶类,因而可作为检测间质细胞数量的标志物[17],故在本试验中通过免疫组化试验方法观察睾丸中间质细胞的数量,结果显示三聚氰胺与三聚氰酸混合物可造成睾丸间质细胞数量下降,从而导致睾酮水平降低;但对于导致间质细胞数量减少的机制仍需要进一步研究。以往的报道表明,外源性物质例如化学物质二甲磺酸乙烷(ethane dimethanesulfonate)可诱导间质细胞凋亡,进而造成其数量大量减少[18, 19];此外,过高剂量的糖皮质激素也可诱导大鼠间质细胞凋亡,导致睾酮水平下降[20]。
综上所述,三聚氰胺与三聚氰酸混合物减少了间质细胞的数量并下调了睾酮合成相关蛋白的表达,从而导致睾酮合成障碍,直接或间接地影响了小鼠睾丸的发育和精子的生成。
| [1] | Hau A K,Kwan T H,Li P K. Melamine toxicity and the kidney[J]. Journal of the American Society of Nephrology,2009,20(2):245-250. |
| [2] | Reimschuessel R,Puschner B. Melamine toxicity-stones vs. crystals[J]. Journal of Medicinal Food,2010,6(4):468-469. |
| [3] | Reimschuessel R,Evans E R,Stine C B,et al. Renal crystal formation after combined or sequential oral administration of melamine and cyanuric acid[J]. Food and Chemical Toxicology,2010,48(10):2898-2906. |
| [4] | Langman C B,Alon U,Ingelfinger J,et al. A position statement on kidney disease from powdered infant formula-based melamine exposure in Chinese infants[J]. Pediatric Nephrology,2009,24(7):1263-1266. |
| [5] | 林志丹,徐保峰,李全忠,等. 美耐皿餐具中三聚氰胺残余单体的迁移行为研究[J]. 塑料工业,2012,40(8):73-76. Lin Z D,Xu B F,Li Q Z,et al. Migration behavior research of residual melamine monomer in melamine resin tableware[J]. China Plastics Industry,2012,40(8):73-76(in Chinese). |
| [6] | Canelli E. Chemical,bacteriological,and toxicological properties of cyanuric acid and chlorinated isocyanurates as applied to swimming pool disinfection:a review[J]. American Journal of Public Health,1974,64(2):155-162. |
| [7] | Dufour A P,Evans O,Behymer T D,et al. Water ingestion during swimming activities in a pool:a pilot study[J]. Journal of Water Health,2006,4(4):425-430. |
| [8] | Dorne J L,Doerge D R,Vandenbroeck M,et al. Recent advances in the risk assessment of melamine and cyanuric acid in animal feed[J]. Journal of Toxicology Applied Pharmacology,2013,270(3):218-229. |
| [9] | Park D,Kim T K,Choi Y J,et al. Increased nephrotoxicity after combined administration of melamine and cyanuric acid in rats[J]. Laboratory Animal Research,2011,27(1):25-28. |
| [10] | You H,Zhu J F,She R P,et al. Induction of apoptosis in the immature mouse testes by a mixture of melamine and cyanuricacid[J]. Journal of Integrative Agriculture,2012,11(12):2058-2066. |
| [11] | Chang L,She R,Ma L,et al. Acute testicular toxicity induced by melamine alone or a mixture of melamine and cyanuric acid in mice[J]. Reproductive Toxicology,2014,46(7):1-11. |
| [12] | Yin R H,Wang X Z,Bai W L,et al. The reproductive toxicity of melamine in the absence and presence of cyanuric acid in male mice[J]. Research in Veterinary Science,2013,94(3):618-627. |
| [13] | Lü Y,Liu Z,Tian Y,et al. Effect on morphology,oxidative stress and energy metabolism enzymes in the testes of mice after a 13-week oral administration of melamine and cyanuricv acid combination[J]. Regulatory Toxicology Pharmacology,2013,65(2):183-188. |
| [14] | Roy L M,Safa M,Mike Q,et al. Identification and characterization of toxicity of contaminants in pet food leading to an outbreak of renal toxicity in cats and dogs[J]. Toxicological Sciences,2008,106(1):251-262. |
| [15] | Walker W H. Testosterone signaling and the regulation of spermatogenesis[J]. Spermatogenesis,2011,1(2):116-120. |
| [16] | Lin H,Ge R S,Chen G R,et al. Involvement of testicular growth factors in fetal Leydig cell aggregation after exposure to phthalate in utero[J]. Proceeding of the National Academy of Science of the United States of America,2008,105(20):7218-7222. |
| [17] | Dupont E,Labrie F,Luu-The V,et al. Ontogeny of 3β-hydroxysteroid dehydrogenase/Δ5-Δ4 isomerase(3β-HSD)in rat testis as studied by immunocytochemistry[J]. Anatomy and Embryology,1993,187(6),583-589. |
| [18] | Taylor M F,de Boer-Brouwer M,Woolveridge I,et al. Leydig cell apoptosis after the administration of ethane dimethanesulfonate to the adult male rat is a Fas-mediated process[J]. Endocrinology,1999,140(8):3797-3804. |
| [19] | Taylor M F,Woolveridge I,Metcalfe A D,et al. Leydig cell apoptosis in the rat testes after administration of the cytotoxin ethane dimethanesulphonate:role of the Bcl-2 family members[J]. International Journal of Endocrinology,1998,157(2):317-326. |
| [20] | Gao H B,Tong M H,Hu Y Q,et al. Glucocorticoid induces apoptosisin rat Leydig cells[J]. Endocrinology,2002,143(1):130-138. |




