文章信息
- 田擎, 曾丹丹, 李彬, 张海峰, 王源超, 郑小波
- TIAN Qing, ZENG Dandan, LI Bin, ZHANG Haifeng, WANG Yuanchao, ZHENG Xiaobo
- 利用环介导等温扩增技术检测黑白轮枝菌
- Rapid detection of Verticillium albo-atrum using a loop-mediated isothermal amplification assay
- 南京农业大学学报, 2016, 39(4): 582-588
- Journal of Nanjing Agricultural University, 2016, 39(4): 582-588.
- http://dx.doi.org/10.7685/jnau.201510022
-
文章历史
- 收稿日期:2015-10-17
2. 江苏省出入境检验检疫局, 江苏 南京 210001
2. Jiangsu Entry-Exit Inspection and Quarantine Bureau, Nanjing 210001, China
黑白轮枝菌(Verticillium albo-atrum)最早于1918年发现于瑞典Hedlund,后随带菌种子传入西欧,进而向东欧和南欧扩展,1923至1950年基本遍布整个北欧,1976年以后便相继传入美国和加拿大,1980年传入日本[1-3],并快速扩展,成为许多地方苜蓿种植的一个重要限制因素[4-6]。我国新疆和台湾曾有苜蓿黄萎病发生的报道[7-8]。1996年,在新疆阿克苏地区温宿县托乎拉乡首次发现疫情[9]。2003至2005年,相继在巴州、伊犁州、阿勒泰地区发现39个疫情发生点。据调查,阿克苏地区温宿县托乎拉乡苜蓿被侵染后植株死亡率为35%~70%[10]。目前,该病发生范围仅限于南北疆的4地(州)9个县(市)、35个乡镇的37个村的苜蓿作物上,共有疫情发生点39个[10-12]。
黑白轮枝菌的寄主植物多达660余种,除侵染蛇麻草、车轴草、蚕豆、三叶草、美洲茶、天兰葵等多种植物外,还会对苜蓿、啤酒花、花生、茄子、棉花、番茄、黄瓜、罗马甜瓜和马铃薯等多种作物造成严重危害[13-15]。黑白轮枝菌主要危害苜蓿,引起苜蓿黄萎病。发病早期,病株上部叶片在温度较高时表现暂时萎蔫,继而中下部叶片失绿变黄,严重时变枯白色,表现整株萎蔫症状,后期植株因生育停滞而严重矮化;发病第2年产量减低15%~50%,从该年晚期至第3年病株大批枯死[14]。黑白轮枝菌主要由种子传播,也可经土壤、风、灌溉水、昆虫、收割机械、花粉等近距离传播[14-20],通过干草、块茎及病残体等进行远距离传播[6-7]。
苜蓿黄萎病是我国禁止进境的一种检疫性真菌病害[21-22]。新疆苜蓿栽培面积已达25万hm2,居全国第二。苜蓿是全区农牧业生产的支柱,一旦苜蓿黄萎病发生,将直接威胁畜牧业发展和其他作物生产。据估算,疫情一旦扩展蔓延,新疆每年至少造成上亿元(人民币)的经济损失,且无法消除后患[11]。为了阻止黑白轮枝菌传播范围的不断扩大,使苜蓿黄萎病得到控制,需要对其进行快速、准确的检测。而传统的检测方法主要有发病组织中病原菌的分离、以ITS为靶标的普通PCR分子检测[23]以及实时荧光PCR检测等[8],但这些检测需要的时间较长,准确性和灵敏度偏低,或需要昂贵的仪器。
环介导等温扩增技术(loop-mediated isothermal amplification,LAMP)是由日本荣研株式会社的Notomi等[24]于2000年开发的一种新型的核酸扩增方法,其特点是针对靶基因的6个区域设计4条特异性引物,在链置换DNA酶(Bst DNA polymerase)的作用下,于60~65 ℃恒温扩增,30~80 min后即可观察结果,具有操作简单、特异性强、灵敏度高、产物易检测等优点。LAMP反应不需要PCR仪和昂贵的试剂,反应结果可通过是否形成白色沉淀(浑浊)或染料染色后的颜色变化来判断,因而在食品检测与病害诊断等领域有着广泛的应用前景[25-26]。我们基于环介导等温扩增技术建立黑白轮枝菌检测的LAMP体系[24, 27-29],并对该方法的特异性、灵敏度及其在实际检测中的应用进行了研究。
1 材料与方法 1.1 材料1 0×ThermoPol Buffer和Bst DNA polymerase购自New England Biolabs公司;甜菜碱、MgSO4和羟基萘酚蓝(HNB)购自Sigma公司;dNTP等购自宝生物工程(大连)有限公司;移液管购自Eppendorf公司和AXYGEN公司;DNAsecure Plant Kit购自QIAGEN公司;PowerSoil DNA Isolation Kit购自MO BIO公司。引物由上海Invitrogen公司合成。
供试菌株包括黑白轮枝菌(Verticillium albo-atrum)和其近似种大丽轮枝菌(Verticillium dahliae)以及其他属的真菌和疫霉菌,名称和来源详见表 1。将供试黑白轮枝菌和其他真菌菌株转至PDA(马铃薯葡萄糖琼脂培养基)平板上,疫霉菌转至V8平板上,于25 ℃黑暗培养。黑白轮枝菌培养7 d后刮取菌丝,经冷冻抽干研磨成菌丝粉,-20 ℃保存备用。疫霉菌培养3 d后从菌落边缘切取10块(2 mm×2 mm)菌丝块转移至V8液体培养基中,其他菌株菌丝块转移至PDB(马铃薯葡萄糖液体培养基)中,于25 ℃黑暗培养3~5 d,过滤收集菌丝,经冷冻抽干研磨成菌丝粉,-20 ℃保存备用。
| 种名Species | 寄主Host | 来源Source | 菌株数量No.of isolate |
| 黑白轮枝菌Verticillium albo-atrum | 苜蓿Alfalfa | 新疆Xinjiang | 1 |
| 美国America | 1 | ||
| 大丽轮枝菌V.dahliae | 棉花Cotton | 江苏Jiangsu | 9 |
| 山东Shandong | 1 | ||
| 茄子Eggplant | 江苏Jiangsu | 1 | |
| 胶孢炭疽菌Colletotrichum gloeosporioides | 大豆Soybean | 江苏Jiangsu | 1 |
| 平头炭疽菌C. truncatum | 大豆Soybean | 江苏Jiangsu | 1 |
| 尖孢炭疽菌C. acutatum 大豆Soybean | 海南Hainan | 1 | |
| 大豆紫斑病菌Cercospora kikuchii | 大豆Soybean | 湖北Hubei | 1 |
| 米曲霉菌 Aspergillus oryzae | 大豆Soybean | 未知Unknown | 1 |
| 大豆炭腐病菌 Macrophomina phaseolina | 大豆Soybean | 江苏Jiangsu | 1 |
| 大豆南方茎溃疡病菌 Diaporthe phaseolorum var. meridionalis | 大豆Soybean | 未知Unknown | 1 |
| 大豆北方茎溃疡病菌 D. phaseolorum var. caulivora | 大豆Soybean | 未知Unknown | 1 |
| 大豆拟茎点种腐病菌 Phomopsis longicolla | 大豆Soybean | 湖北Hubei | 1 |
| 大豆疫霉病菌 Phytophthora sojae | 大豆Soybean | 未知Unknown | 1 |
| 尖镰孢菌 Fusarium oxysporum | 大豆Soybean | 湖北Hubei | 1 |
| 禾谷镰孢菌F.graminearum | 大豆Soybean | 江苏Jiangsu | 1 |
| 木贼镰孢菌F.equiseti | 大豆Soybean | 安徽Anhui | 1 |
| 层出镰孢菌F.proliferatum | 大豆Soybean | 安徽Anhui | 1 |
| 茄腐镰孢菌F.solani | 大豆Soybean | 江苏Jiangsu | 1 |
| 冬青丽赤壳菌 Calonectria ilicicola | 大豆Soybean | 江苏Jiangsu | 1 |
| 球黑孢菌 Nigrospora sphaerica | 大豆Soybean | 湖北Hubei | 1 |
| 立枯丝核菌 Rhizoctonia solani | 大豆Soybean | 江苏Jiangsu | 1 |
| 多主棒孢菌 Corynespora cassiicola | 大豆Soybean | 湖北Hubei | 1 |
| 玉蜀黍平脐蠕孢菌 Bipolaris maydis | 大豆Soybean | 江苏Jiangsu | 1 |
采用CTAB方法[30]提取DNA:取200 mg菌丝粉,研磨后移至预先加入900 μL 2% CTAB提取液和90 μL 10% SDS的2 mL Eppendorf管中,漩涡混匀,于65 ℃水浴1 h,中间每10 min上下颠倒几次。12 000 r·min-1离心10 min,取上清液加等体积酚、氯仿和异戊醇(体积比为25∶24∶1)混合液颠倒混匀,12 000 r·min-1离心10 min。将上清液转移至新管,加等体积氯仿,轻轻颠倒混匀后12 000 r·min-1离心5 min。取上清液转移至新的1.5 mL Eppendorf管中,加入2倍体积的无水乙醇,-20 ℃沉淀1 h以上。12 000 r·min-1离心10 min,倾去上清液,沉淀用70%乙醇洗涤2次,室温晾干。加入适量灭菌超纯水或TE(pH8.0)溶解沉淀(含20 μg·mL-1 RNase),于37 ℃处理1 h后,-20 ℃保存备用。
1.3 引物设计与筛选靶标基因的选取和引物的筛选是LAMP检测的关键因素。首先选取CHS、GS、HIS3、Tef-1α、Tub、Gpd和Rpb1等备选靶标,应用Bioedit软件将黑白轮枝菌及其相近种的靶标序列进行比对分析,选取在种内不同菌株间高度保守、种间有明显差异的靶标基因,使用PrimerExplore V4软件设计LAMP引物,将设计好的多套引物比对后进行特异性和灵敏度试验。特异性试验:该引物必须对不同地区、不同寄主来源的黑白轮枝菌具有广泛通用性;在与属内相近种及其他属重要病原菌进行扩增的试验中,所选引物必须只能特异识别黑白轮枝菌,而不能对非目标菌进行扩增。灵敏度试验:将目标菌株DNA测定浓度后梯度稀释,以此为模板进行LAMP反应,所选引物灵敏度必须达到pg水平。通过以上试验,最终选出1套以Tub DNA序列(GenBank accession No.DQ166896.1)为靶标,特异性强、灵敏度高,能快速、准确地检测出黑白轮枝菌的LAMP引物(表 2)。引物由英潍捷基贸易有限公司合成,用ddH2O溶解后分装,-20 ℃冰箱保存备用。
| 引物名称 Primer name | 序列(5′→3′) Sequence |
| V.a-FIP | CTTACGCACTGGCCGGTCTGAAGTCCATGAGCTGACCTTG |
| V.a-BIP | GCCTATTTTCGATTTGCGGGGCAGAAAGCAGCACCGATCTG |
| V.a-F3 | CGACGTCAAACCTGACCATA |
| V.a-B3 | TGCTCGCCAGAGATGTTCT |
| V.a-LF | GAGGTGAACCTAAGAGTGAGGAAA |
本研究采用的LAMP反应体系为:10×ThermoPol Buffer 2.5 μL,MgSO4 8 mmol·L-1,dNTPs 1.2 mmol·L-1,内引物FIP和BIP各1.6 μmol·L-1,外引物F3和B3各0.4 μmol·L-1,环引物LF 0.8 μmol·L-1,甜菜碱0.8 μmol·L-1,HNB 180 mmol·L-1,Bst DNA聚合酶8 U·μL-1,模板DNA(800 ng·μL-1)2 μL,灭菌水补至26 μL。62 ℃恒温反应70 min。试验至少重复3次。
1.5 扩增结果判断方法以HNB(羟基萘酚蓝)为显色指示剂,在反应前加入,每个反应体系中加入HNB(2.4 mmol·L-1)2 μL,LAMP反应结束后,通过肉眼观察指示剂颜色变化判定扩增结果,阳性为天蓝色,阴性为紫色。
1.6 LAMP体系的特异性验证分别提取黑白轮枝菌、大丽轮枝菌和其他病原菌(表 1)的基因组DNA,取2 μL作为模板进行LAMP扩增。试验至少重复3次。
1.7 LAMP体系灵敏度检测黑白轮枝菌的基因组DNA模板测定浓度后10倍稀释,使其质量浓度梯度依次为100 ng·μL-1、10 ng·μL-1、1 ng·μL-1、100 pg·μL-1、10 pg·μL-1、1 pg·μL-1、100 fg·μL-1、10 fg·μL-1。分别取不同浓度的DNA 2 μL作为模板进行LAMP反应。试验至少重复3次。
1.8 田间发病组织中黑白轮枝菌的检测从采自新疆地区的苜蓿样本中选取疑似样本7份,每份样本取200 mg发病植物组织,按照DNAsecure Plant Kit(Tiangen)说明书提取DNA。将其作为模板进行LAMP扩增,将黑白轮枝菌纯DNA作为阳性对照,以灭菌水作为阴性对照。
1.9 土样中人工添加黑白轮枝菌分生孢子的检测为了确定该技术体系对土壤中黑白轮枝菌的检测灵敏度,进行以下试验:加5 mL无菌水于黑白轮枝菌平板中,轻轻刮下分生孢子,制备孢子悬浮液备用。取不含黑白轮枝菌的土样(该土样经黑白轮枝菌LAMP引物检测呈阴性)6份,每份0.25 g(干质量),放入2 mL的EP管中,分别添加不同孢子数量(10 000、1 000、100、50、10、0)的孢子悬浮液。按照美国MOBIO公司的土壤微生物DNA强力提取试剂盒(Power Soil DNA Isolation Kit)说明书提取样品总DNA,将其作为模板进行LAMP扩增,并以黑白轮枝菌纯DNA作为阳性对照,灭菌水作为阴性对照。
1.10 苜蓿种子中人工添加黑白轮枝菌分生孢子的检测为了确定该技术体系对苜蓿种子中黑白轮枝菌的检测灵敏度,进行以下试验:按1.9节中的方法制备孢子悬浮液。选取同一品种、同一地区苜蓿种子样本(前期检测均不含黑白轮枝菌)6份,每份称取10 g,倒入250 mL干净三角瓶中,加入无菌水至100 mL,滴入20%吐温3~5滴。分别加入不同孢子数量(10 000、1 000、100、50、10、0)的孢子悬浮液,每个梯度设置3个重复。封住瓶口,置于摇床上220 r·min-1 30 min,振荡洗涤;振荡洗涤后的混合液用200目钢筛过滤,并用少量无菌水冲洗钢筛上的苜蓿种子及残体,滤液收集到原三角瓶中;将收集到的滤液装到50 mL离心管中,分次离心,6 500 r·min-1离心10 min,弃上清液,收集沉淀;将沉淀物置于37 ℃恒温箱中晾干。由于沉淀物中含有大量土壤成分,所以试验采用美国MOBIO公司的土壤微生物DNA强力提取试剂盒Power Soil DNA Isolation Kit 进行总DNA的提取,并以此作为模板用于LAMP扩增,以黑白轮枝菌菌株纯DNA作为阳性对照,以不加入黑白轮枝菌分生孢子的苜蓿种子样本DNA和水为阴性对照。试验至少重复3次。
2 结果与分析 2.1 LAMP引物的特异性以黑白轮枝菌作为阳性对照,水作为阴性对照,用其相似种大丽轮枝菌及其他属真菌和大豆疫霉菌(表 1)作为对照验证引物的特异性。62 ℃ 70 min条件下扩增,反应结束后只有含黑白轮枝菌基因组的反应管产生天蓝色的阳性反应,其他参试菌均呈紫色的阴性反应(图 1)。结果表明:本研究设计并筛选的针对黑白轮枝菌的LAMP引物(表 2)可以特异地检测出该病菌。

|
图 1 LAMP反应的特异性试验
Fig. 1 Specificity of LAMP detection method for Verticillium albo-atrum
A:种间特异性Specificity of LAMP detection among different strains of Verticillium spp.: 1 .阳性对照 Positive control;2~3.黑白轮枝菌不同菌株 Different strains of V.albo-atrum;4~8.大丽轮枝菌不同菌株Different strains of V.dahliae;9.阴性对照Negative control B:属间特异性Specificity of LAMP detection among different genus strains of fungi and oomycetes: 1.阳性对照Positive control;2.胶孢炭疽菌Colletotrichum gloeosporioides;3.平头炭疽菌C. truncatum;4.大豆炭腐病菌Macrophomina phaseolina;5.冬青丽赤壳菌Calonectria ilicicola;6.米曲霉菌Aspergillus oryzae;7.大豆紫斑病菌Cercospora kikuchii;8.球黑孢菌 Nigrospora sphaerica;9.多主棒孢菌Corynespora cassiicola;10.立枯丝核菌Rhizoctonia solani;11.大豆疫霉菌Phytophthora sojae;12.尖孢炭疽菌Colletotrichum acutatum;13.玉蜀黍平脐蠕孢菌Bipolaris maydis;14.大豆南方茎溃疡病菌Diaporthe phaseolorum var.meridionalis;15.大豆北方茎溃疡病菌D.phaseolorum var.caulivora;16.尖镰孢菌Fusarium oxysporum;17.禾谷镰孢菌F.graminearum;18.木贼镰孢菌F.equiseti;19.层出镰孢菌F.proliferatum;20.茄腐镰孢菌F.solani;21.阴性对照Negative control |
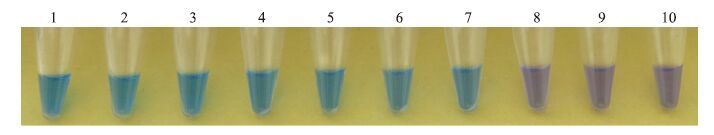
以1.7节中稀释的黑白轮枝菌基因组DNA作为模板进行LAMP反应,结果显示:该反应体系检测灵敏度为1 pg·μL-1(图 2)。
|
图 2 LAMP反应的灵敏度 Fig. 2 Sensitivity of the LAMP assay using serially diluted genomic DNA of V.albo-atrum 1.阳性对照Positive control;2~9.分别代表不同稀释倍数的基因组DNA Representing different dilution times of DNA:100 ng·μL-1,10 ng·μL-1,1 ng·μL-1,100 pg·μL-1,10 pg·μL-1,1 pg·μL-1,100 fg·μL-1,10 fg·μL-1;10.阴性对照Negative control |
对采自新疆地区的7份苜蓿黄萎病疑似病害样本中提取的DNA进行检测,有3份为阳性。结果表明,该方法能够排除寄主植物及其他非目标菌的干扰,准确检测出目标菌。并且其检测灵敏度较高,与传统方法相比,能更快速准确地检测到黑白轮枝菌,大大提高了检测效率。
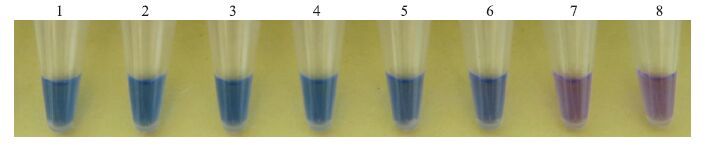
2.4 土样中人工添加黑白轮枝菌分生孢子的检测采用1.9节中提取的样品总DNA进行LAMP扩增,结果(图 3)显示,该检测技术在0.25 g土样含有10个黑白轮枝菌孢子的条件下可检测到目标病原菌。表明:本方法可以进行土样是否携带黑白轮枝菌的高灵敏度检测。
|
图 3 LAMP检测人工添加黑白轮枝菌孢子的土样 Fig. 3 LAMP detection of V.albo-atrum in soils containing different numbers of conidia 1.阳性对照Positive control;2~7.添加不同孢子数量(10 000,1 000,100,50,10,0)的土壤样品Soils with different number of conidia;8.阴性对照Negative control |
我们对采自新疆的7份土样进行检测,均未见阳性结果。
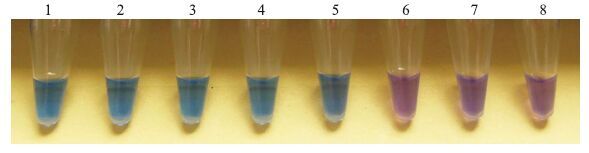
2.5 苜蓿种子中人工添加黑白轮枝菌分生孢子的检测为了确定该技术体系对苜蓿种子中黑白轮枝菌检测的灵敏度,以1.10节中提取样品总DNA为模板进行扩增,结果(图 4)显示:含10 000、1 000、100、50个孢子的苜蓿种子提取的总DNA反应均呈天蓝色的阳性反应,说明该技术对苜蓿种子中黑白轮枝菌的最低检测限为每10 g苜蓿种子50个孢子。因此,本方法可以用于种子中携带黑白轮枝菌的高灵敏度检测。
|
图 4 LAMP检测人工添加黑白轮枝菌孢子的苜蓿种子 Fig. 4 LAMP detection of V.albo-atrum in seeds of alfalfa containing different numbers of conidia 1.阳性对照Positive control;2~7.添加不同孢子数量(10 000,1 000,100,50,10,0)的苜蓿种子Seeds with different number of conidia;8.阴性对照Negative control |
苜蓿黄萎病是苜蓿的毁灭性病害,也是世界性检疫病害[31]。近年来,我国从美国、加拿大等国引进苜蓿的种子量呈逐年增加的趋势。由于苜蓿种子及混杂于其中的植物残体是黑白轮枝菌传播的重要载体,来自加拿大、美国等黄萎病发生区的苜蓿种子传带黑白轮枝菌的风险很大。而且我国当前苜蓿生产的主栽品种多为感病品种,许多苜蓿种植区的气候条件与欧洲、北美洲种植区极其相似[32],一旦苜蓿黄萎病蔓延开来,对苜蓿生产将造成毁灭性破坏[21]。因此,需要对其进行快速、准确的检测,以控制黑白轮枝菌的传入与传播。近年来,黑白轮枝菌的检测方法也在不断发展。2004年,Radisek等[33]利用AFLP和SCAR标记技术建立了区别鉴定啤酒花黄萎病菌PG1专化型和PG2专化型的分子标记技术。2005年,Zhang等[23]利用普通PCR方法在V.albo-atrum的ITS区域设计1对引物对黑白轮枝菌进行特异性检测。2007年Larsen等[13]根据分离自苜蓿的黄萎病菌的特异性SCAR片段,设计实时荧光PCR引物和探针,建立了黑白轮枝菌的实时荧光PCR检测方法。2011年,杜洪忠等[8]根据黑白轮枝菌的ITS基因序列,结合Zhang等[23]设计的引物Vaa-1和Vaa-2,设计了一条TaqMan探针Vaa-probe,建立了黑白轮枝菌的实时荧光PCR特异性检测方法。
本文首次报道应用环介导等温扩增技术(LAMP)建立黑白轮枝菌的LAMP检测体系。LAMP技术特异性强、灵敏度高,用时仅需70 min,能够从携带有黑白轮枝菌的发病寄主植物组织中检测出目标菌,表明该技术可以应用于口岸对黑白轮枝菌的检验检疫,同时亦可应用于田间苜蓿黄萎病的快速诊断。
南京农业大学植物病理学系胡白石教授为本研究采集并提供苜蓿黄萎病样本,谨致谢意。
| [1] | 冶海林,瞿付娟. 苜蓿黄萎病的发生和防治[J]. 植物医生,2007,20(6):25-26. Ye H L,Qu F J. The occurrence and control of Verticillium wilt of alfalfa[J]. Plant Doctor,2007,20(6):25-26(in Chinese). |
| [2] | 杨家荣,商鸿生,李仁. 苜蓿黄萎病病原菌研究[J]. 草业学报,1997,6(3):43-46. Yang J R,Shang H S,Li R. Study on the pathogen of Verticillium wilt of alfalfa[J]. Acta Prataculturae Sinica,1997,6(3):43-46.(in Chinese with English abstract). |
| [3] | 吴亚楠,李志强. 苜蓿黄萎病菌的检疫与防控[J]. 中国奶牛,2015(5):51-53. Wu Y N,Li Z Q. Research on Verticillium alboatrum Reinke & Berthold[J]. China Dairy Cattle,2015(5):51-53(in Chinese with English abstract). |
| [4] | Arny D C,Grau C R. Importance of Verticillium wilt of alfalfa in North America[J]. Canadian Journal of Plant Pathology,1985,7:187-190. |
| [5] | Heale J B. Verticillium wilt of alfalfa,back ground and current reseach[J]. Canadian Journal of Plant Pathology,1985,7:191-198. |
| [6] | 黄胜光,卢兆山,邱世明,等. 广西防城港首次截获苜蓿黄萎病菌[J]. 植物保护,2012,38(1):180-183. Huang S G,Lu Z S,Qiu S M,et al. First interception of Verticillium albo-atrum in Fangchenggang of Guangxi[J]. Plant Protection,2012,38(1):180-183(in Chinese with English abstract). |
| [7] | 张莉,王俊. 苜蓿黄萎病的综合防治措施[J]. 新疆农业科技,2012(2):30-31. Zhang L,Wang J. Comprehensive prevention and control measures of Verticillium wilt of alfalfa[J]. Xinjiang Agricultural Science and Technology,2012(2):30-31(in Chinese). |
| [8] | 杜洪忠,吴品珊,严进. 苜蓿黄萎病菌实时荧光PCR检测方法[J]. 植物检疫,2011,25(2):45-47. Du H Z,Wu P S,Yan J. Detection of Verticillium albo-atrum by Real-Time fluorescence PCR[J]. Plant Quarantine,2011,25(2):45-47(in Chinese with English abstract). |
| [9] | 王雪薇,马德成,喻宁莉,等. 新疆苜蓿黄萎病病原学研究[C]//中国植物病理学会第六届代表大会暨学术年会. 北京,1998:79-82. Wang X W,Ma D C,Yu N L,et al. Study on pathogen of Verticillium wilt of alfalfa in Xinjiang[C]//China Phytopathological Society Congress and Academic Annual Conference.Beijing,1998:79-82(in Chinese). |
| [10] | 马德成,秦晓辉,王培,等. 新疆局部地区苜蓿黄萎病防控与扑灭[J]. 植物检疫,2006,20(6):388,394. Ma D C,Qin X H,Wang P,et al. Prevention and extermination of Verticillium wilt of alfalfa in Xinjiang[J]. Plant Quarantine,2006,20(6):388,394(in Chinese). |
| [11] | 马宇含,叶梅,余虹丽,等. 新疆局部地区苜蓿黄萎病防控[J]. 新疆农业科技,2007(4):28. Ma Y H,Ye M,Yu H L,et al. Prevention and control of Verticillium wilt of alfalfa in Xinjiang[J]. Xinjiang Agricultural Science and Technology,2007(4):28(in Chinese). |
| [12] | 阿丽亚·阿不拉. 新疆苜蓿黄萎病疫情的传入及防治措施[J]. 新疆农业科技,2013(4):54. Aelia A. Spread and prevention measures of Verticillium wilt of alfalfa in Xinjiang[J]. Xinjiang Agricultural Science and Technology,2013(4):54(in Chinese). |
| [13] | Larsen R C,Vandemark G J,Hughes T J,et al. Development of Real-Time polymerase chain reaction assay for quantifying Verticillium albo-atrum DNA in resistant and susceptible alfalfa[J]. Phytopathology,2007,97(11):1519-1525. |
| [14] | 丁国云. 大豆黑痣病菌和苜蓿黄萎病菌随车轴草种子传入中国的风险[J]. 植物检疫,2007,21(S1):45-46. Ding G Y. Introduction risk of soybean Rhizoctonia leguminicola and Verticillium albo-atrum with clover seeds[J]. Plant Quarantine,2007,21(S1):45-46(in Chinese). |
| [15] | 姜莉. 苜蓿黄萎病的防治[J]. 新疆畜牧业,2011(8):58-59. Jiang L. The prevention and control of Verticillium wilt of alfalfa[J]. Xinjiang Animal Husbandry,2011(8):58-59(in Chinese). |
| [16] | Huang H C,Harper A M,Kokko E G,et al. Aphid transmission of Verticillium albo-atrum to alfalfa[J]. Canadian Journal of Plant Pathology,1983,5:141-147. |
| [17] | Huang H C,Richards K W,Kokko E G,et al. Role of the leafcutter bee in dissemination of Verticillium albo-atrum in alfalfa[J]. Phytopathology,1986,76:75-80. |
| [18] | Howard R J. Local and long distance spread of Verticillium species causing wilt of alfalfa[J]. Canadian Journal of Plant Pathology,1985,7:199-202. |
| [19] | Huang H C,Hanna M R,Kokko E G. Mechanisms of seed contamination by Verticillium albo-atrum in alfalfa[J]. Phytopathology,1985,75:482-488. |
| [20] | Isaac I. Wilt of lucerne caused by species of Verticillium[J]. Annals of Applied Biology,1957,45:550-558. |
| [21] | 王春林,吴立峰,王雪薇,等. 加拿大、美国苜蓿黄萎病发生控制情况及我国对策[J]. 植物检疫,2003,17(1):57-59. Wang C L,Wu L F,Wang X W,et al. Control the situation of Verticillium wilt of alfalfa in Canada and American,and the countermeasures of China[J]. Plant Quarantine,2003,17(1):57-59(in Chinese). |
| [22] | 吴翠萍,李彬,粟寒,等. 进境美国苜蓿草中苜蓿黄萎病菌的检疫鉴定[J]. 植物检疫,2011,25(1):42-46. Wu C P,Li B,Su H,et al. Detection of Verticillium albo-atrum in alfalfa samples imported from the United State[J]. Plant Quarantine,2011,25(1):42-46(in Chinese with English abstract). |
| [23] | Zhang Z G,Chen R H,Wang Y C,et al. Molecular detection of Verticillium albo-atrum by PCR based on ITS sequences[J]. Agricultural Sciences in China,2005,4(10):760-766. |
| [24] | Notomi T,Okayama H,Masubuchi H,et al. Loop-mediated isothermal amplification of DNA[J]. Nucleic Acids Research,2000,28(12):63. |
| [25] | Mori Y,Nagamine K,Tomita N,et al. Detection of loop-mediated isothermal amplification reaction by turbidity derived from magnesium pyrophosphate formation[J]. Biochemical and Biophysical Research Communications,2001,289(1):150-154. |
| [26] | 肖斌,朱永红,邹全明. 简便敏感的环介导等温扩增基因诊断新技术[J]. 中华检验医学杂志,2005,28(7):761-763. Xiao B,Zhu Y H,Zou Q M. Simple,sensitive and new technique for the diagnosis-loop mediated isothermal amplification technique[J]. Chinese Journal of Laboratory Medicine,2005,28(7):761-763(in Chinese). |
| [27] | Yasuyoshi M,Masataka K,Norihiro T,et al. Real-Time turbidimetry of LAMP reaction for quantifying template DNA[J]. Journal of Biochemical and Biophysical Methods,2004,59(2):145-157. |
| [28] | Nagamine K,Hase T,Notomi T. Accelerated reaction by loop-mediated isothermal amplification using loop primers[J]. Molecular and Cellular Probes,2002,16(3):223-229. |
| [29] | 沈浩,戴婷婷,吴翠萍,等. 基于环介导等温扩增技术检测大豆北方茎溃疡病菌[J]. 南京农业大学学报,2015,38(2):255-260. DOI:10.7685/j.issn.1000-2030.2015.02.012. Shen H,Dai T T,Wu C P,et al. The tef1α-LAMP method for rapid detection of Diaporthe phaseolorum var. caulivora[J]. Journal of Nanjing Agricultural University,2015,38(2):255-260(in Chinese with English abstract). |
| [30] | Murray M G,Thompson W F. Rapid isolation of high molecular weight plant DNA[J]. Nucleic Acids Research,1980,8(19):4321-4326. |
| [31] | 商鸿生. 苜蓿黄萎病传入北美[J]. 植物检疫,1984(3):15-16. Shang H S. The introduction of Verticillium wilt of alfalfa to North America[J]. Plant Quarantine,1984(3):15-16(in Chinese). |
| [32] | 陈婧,白应文,杨继娟,等. 苜蓿黄萎病菌中国菌株生物学特性研究[J]. 草地学报,2010,18(2):274-279. Chen J,Bai Y W,Yang J J,et al. Biologocal characteristics of Chinese strain of Verticillium albo-atrum from alfalfa[J]. Acta Agrestia Sinica,2010,18(2):274-279(in Chinese with English abstract). |
| [33] | Radisek S,Jakse J,Javornik B. Development of pathotype-specific SCAR makes for detection of Verticillium albo-atrum isolates from hop[J]. Plant Disease,2004,88:1115-1122. |




