文章信息
- 王秋举, 鞠雪, 罗莎, 陈玉柯, 董晓庆, 刘洪键, 张东鸣. 2016.
- WANG Qiuju, JU Xue, LUO Sha, CHEN Yuke, DONG Xiaoqing, LIU Hongjian, ZHANG Dongming. 2016.
- L-肉碱对H2O2诱导氧化应激FHM细胞的影响
- Effects of L-carnitine on H2O2-induced oxidative stress in FHM cells
- 南京农业大学学报, 39(3): 467-472
- Journal of Nanjing Agricultural University, 39(3): 467-472.
- http://dx.doi.org/10.7685/jnau.201507010
-
文章历史
- 收稿日期:2015-07-04
2. 吉林省水产技术推广站, 吉林 长春 130012
2. Fishery Technical Extension Station of Jilin Province, Changchun 130012, China
随着我国现代水产养殖业的迅速发展,水产养殖集约化程度越来越高,而鱼类在养殖过程中极易受到环境、日粮组成、饲养管理等方面影响而导致应激的产生。任何一种较为强烈的应激均会伴随着氧化应激的发生[1]。长期或过强的氧化应激会造成鱼体生长发育缓慢、免疫机能下降、发病率升高等危害,并降低水产品质量和饲料转化率,给水产养殖业造成严重经济损失[2, 3, 4]。L-肉碱(LC)是一种具有生物活性的类氨基酸,对人体和动物的健康具有重要作用。体内和体外的研究证明,LC最主要的生理功能是将不能直接穿入线粒体的长链脂肪酸运输进入线粒体并促进其β-氧化作用,为细胞提供更多三磷酸腺苷(ATP)[5],保障机体能量的供给[6]。近年来的研究表明[7, 8],LC还具有明显的抗氧化作用,它能降低脂质过氧化水平,增强机体抵抗力,对动物健康和疾病预防发挥重要作用。但目前这方面的研究多集中在哺乳动物上,对水产动物抗氧化功能的研究国内未见报道,LC对鱼类细胞的影响至今还是空白。因此,本研究以胖头鱥肌肉细胞系(fathead minnow muscle cell line,FHM)为研究对象,用H2O2诱导细胞氧化应激,旨在探讨LC对处于氧化损伤状态下的FHM细胞活力及抗氧化功能的影响,为鱼类抵抗氧化应激方面的研究提供新的解决途径。
1 材料与方法 1.1 材料胖头鱥肌肉细胞系(fathead minnow muscle cell line,FHM)购置于天津市水产研究所;LC和MTT试剂购自Sigma公司;M199培养基和胎牛血清(FBS)购自美国Gibco公司;二甲基亚砜购自Amresco公司;30% H2O2试剂和NaHCO3等其他药品均购自北京化工厂;总超氧化物歧化酶(T-SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GPX)及谷胱甘肽合成连接酶(γ-GCS)的活性,总谷胱甘肽(T-GSH)和丙二醛(MDA)含量检测试剂盒均购自南京建成生物工程研究所。
1.2 方法 1.2.1 FHM细胞培养经复苏后的FHM细胞在含有10% FBS的M199完全培养基(含1×106 IU · mL-1青霉素和链霉素)中,置25 ℃、5% CO2的恒温培养箱中培养,每隔1 d换液1次,瓶中细胞覆盖率为90%左右时进行传代。细胞按此方法培养3~4代后进行试验。
1.2.2 细胞活力的测定取生长对数期FHM细胞,用1 g · L-1胰蛋白酶消化制备细胞悬液,接种于96孔细胞培养板,接种数量为每孔2.5×104个,置25 ℃、5% CO2恒温培养箱中培养24 h。将细胞分为对照组、氧化应激组(用0.2和0.6 mmol · L-1的H2O2刺激细胞1 h)、LC添加组(不同浓度LC作用6 h后,H2O2刺激细胞1 h)。弃旧培养基,PBS清洗后,对照组和氧化应激组更换为无血清M199,LC组添加含有不同浓度LC(0.001、0.01、0.1、0.5、1.0和5.0 mmol · L-1)的无血清M199进行预处理,分别于6 h后取出培养板,对照组更换为无血清M199,氧化应激组与各LC添加组均用含0.2和0.6 mmol · L-1 H2O2的无血清M199刺激细胞,每处理6复孔,每孔100 μL,置25 ℃、5% CO2恒温培养箱中孵育,用MTT法测定细胞活力,具体步骤参考王秋举等[8]方法。
1.2.3 细胞抗氧化功能的测定取对数期的FHM细胞,用1 mg · mL-1胰蛋白酶消化制备细胞悬液,以每孔0.6×106个细胞接入6孔细胞培养板,置25 ℃、5% CO2恒温培养箱中培养24 h。细胞分组方法同1.2.2节,每孔2 mL,每组3个重复。试验结束后,弃上清液并收集细胞,细胞经胰酶消化、漂洗后,用超声波破碎仪进行破碎,制备细胞裂解液,置-20 ℃保存。
细胞及上清液中T-SOD、CAT、GPx活性和T-GSH、MDA含量等均按照试剂盒的使用说明书分别进行测定。
1.3 统计分析所有数据均以平均数±标准误(x±SE)表示(n=3),采用SPSS 17.0统计软件的ANOVA程序分析不同浓度LC对细胞抗氧化指标的影响,并用Duncan′s多重比较法检验各处理组之间的差异。
2 结果与分析 2.1 LC对H2O2诱导氧化应激FHM细胞活力的影响由图 1可知,H2O2和不同浓度的LC对FHM细胞活力具有明显的影响。与对照组相比,0.2和0.6 mmol · L-1 H2O2作用1 h,FHM细胞活力分别降低至72%和58%(图 1)。不同浓度LC(0.001、0.01、0.1、0.5、1.0和5.0 mmol · L-1)预处理细胞6 h,H2O2作用1 h,细胞活力的降低在一定程度上受到了抑制。其中,在0.2 mmol · L-1 H2O2作用下,0.001~0.5 mmol · L-1 LC组细胞活力显著高于H2O2氧化应激组(P<0.05),而采用0.6 mmol · L-1 H2O2作用细胞时,只有0.001 mmol · L-1 LC组细胞活力显著提高(P<0.05)。
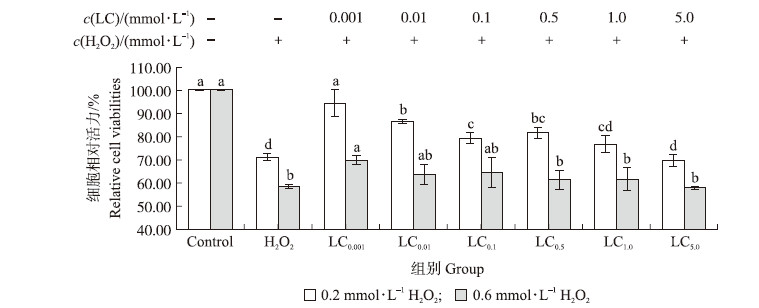 |
图 1 L-肉碱(LC)对H2O2诱导氧化应激胖头鱥肌肉细胞系(FHM)细胞活力的影响 Fig. 1 Effects of L-carnitine(LC)on viabilities in fathead minnow muscle cell line(FHM)cell exposed to H2O2-induced oxidative stress
不同小写字母表示相同浓度H2O2处理下组间差异显著(P<0.05)。 The different small letters mean significant differences among all groups at the same concentrantion of H2O2 at 0.05 level. |
由表 1和表 2可知,0.2和0.6 mmol · L-1 H2O2致使细胞中MDA含量分别升高121.37%和125.09%,而T-GSH含量分别降低88.12%和78.48%。与H2O2组相比,LC预处理能降低细胞MDA含量,且不同氧化程度细胞MDA含量的变化趋势一致,0.001、0.5和1.0 mmol · L-1 LC组MDA含量显著降低(P<0.05),0.01、0.1和5.0 mmol · L-1 LC组MDA含量无显著变化(P>0.05)。与0.2 mmol · L-1 H2O2组相比,0.001~1.0 mmol · L-1 LC预处理显著提升了细胞中T-GSH含量;与0.6 mmol · L-1 H2O2组相比,0.001~1.0 mmol · L-1 LC预处理,细胞中T-GSH含量均显著提高,5.0 mmol · L-1 LC组T-GSH含量无显著差异。
| 组别 Group | MDA含量/ (nmol·mg-1) MDA content | T-GSH含量/ (U·mg-1) T-GSH content | T-SOD活性/ (U·mg-1) T-SOD activity | CAT活性/ (U·mg-1) CAT activity | GPx活性/ (U·mg-1) GPx activity | γ-GCS活性/ (U·mg-1) γ-GCS activity |
| Control | 100 | 100 | 100 | 100 | 100 | 100 |
| H2O2 | 121.37±2.48a | 88.12±0.94d | 92.76±2.63c | 155.92±5.87c | 79.14±27.56b | 91.4±1.44b |
| LC0.001 | 90.79±13.21bc | 155.77±2.54a | 124.19±7.15a | 183.04±5.18abc | 99.05±5.76a | 94.06±2.80ab |
| LC0.01 | 114.29±11.90ab | 120.65±6.75b | 119.79±13.52ab | 176.26±15.66bc | 96.84±3.59a | 104.17±5.76ab |
| LC0.1 | 105.83±9.16ab | 104.48±3.73c | 99.15±3.58bc | 185.62±4.39abc | 95.25±5.49a | 109.26±3.42ab |
| LC0.5 | 72.96±1.64c | 96.57±3.18cd | 95.78±4.72c | 215.81±9.85a | 89.24±2.19ab | 113.38±7.05a |
| LC1.0 | 76.63±4.36c | 119.96±2.92ab | 119.00±4.91ab | 215.81±13.88a | 97.15±3.34a | 97.04±9.09ab |
| LC5.0 | 105.14±10.87ab | 89.86±4.50d | 89.25±4.53c | 205.64±9.04ab | 88.92±0.32ab | 91.82±8.99b |
| 注: 同列数据标有不同小写字母表示差异显著(P<0.05)。In the same column,values with the different letters mean significant difference at 0.05 level. The same as follows. | ||||||
| 组别 Group | MDA含量/ (nmol·mg-1) MDA content | T-GSH含量/ (U·mg-1) T-GSH content | T-SOD活性/ (U·mg-1) T-SOD activity | CAT活性/ (U·mg-1) CAT activity | GPx活性/ (U·mg-1) GPx activity | γ-GCS活性/ (U·mg-1) γ-GCS activity |
| Control | 100 | 100 | 100 | 100 | 100 | 100 |
| H2O2 | 125.09±8.87a | 78.48±2.10b | 90.61±1.94c | 170.87±5.51d | 54.78±0.50b | 83.12±0.34b |
| LC0.001 | 84.18±3.75c | 100.97±4.76a | 108.53±3.71a | 197.96±5.51cd | 105.39±5.14a | 82.91±3.41b |
| LC0.01 | 117.51±2.00ab | 94.33±1.43a | 97.15±1.20abc | 241.72±25.35c | 103.94±7.87a | 102.12±3.40a |
| LC0.1 | 113.30±6.25ab | 94.61±2.90a | 93.37±1.04bc | 320.91±15.03b | 92.69±4.15a | 88.79±1.32ab |
| LC0.5 | 98.05±2.88bc | 93.90±3.93a | 104.03±3.00bc | 364.67±4.17a | 94.07±11.13a | 88.73±1.42ab |
| LC1.0 | 83.19±10.82c | 91.93±1.56a | 98.89±7.67abc | 222.97±11.03c | 111.88±3.80a | 81.17±9.68b |
| LC5.0 | 115.35±7.63ab | 78.33±4.33b | 86.68±3.40c | 281.31±14.44bc | 97.65±5.45a | 94.22±4.78ab |
从表 1和表 2可知,LC对H2O2诱导氧化应激FHM细胞抗氧化酶T-SOD、CAT、GPx和γ-GCS活性具有明显的影响。0.2和0.6 mmol · L-1 H2O2刺激细胞1 h均降低了T-SOD、GPx和γ-GCS活性,并且H2O2刺激浓度越高,酶活性降低越多;而CAT活性呈相反变化趋势,0.2和0.6 mmol · L-1 H2O2的刺激致使细胞CAT活性分别提高至155.92和170.87 U · mg-1。与0.2 mmol · L-1 H2O2组相比,0.001、0.01和1.0 mmol · L-1 LC提高了细胞中T-SOD活性(P<0.05);除5.0 mmol · L-1 LC组,其他浓度LC预处理均显著提高了细胞中GPx活性;0.5 mmol · L-1 LC组细胞中γ-GCS活性以及0.5~5.0 mmol · L-1 LC组CAT活性均显著提升。与0.6 mmol · L-1 H2O2组相比,0.001~1.0 mmol · L-1 LC提高了细胞中T-SOD活性,但只有0.001 mmol · L-1 LC组达到显著水平;所有浓度LC预处理均显著提高了细胞中GPx活性,其中0.001、0.01和1.0 mmol · L-1 LC组GPx活性已恢复或高于对照组水平;除0.01 mmol · L-1 LC组,其他LC组细胞中γ-GCS活性均无显著性差异(P>0.05);所有LC组CAT活性均被提高,其中,0.01~5.0 mmol · L-1 LC均显著提高了细胞中CAT酶活性。
3 讨论对于有氧生物来说,氧在生命代谢过程中会产生一类具有强氧化性含氧代谢产物,称为活性氧(ROS)。ROS是一类具有强氧化能力的分子、离子和自由基,广泛存在于机体内并参与调节机体重要的生理及病理过程。ROS过多并超过抗氧化系统的清除能力,即氧化物和抗氧化物之间的动态平衡被打破,此时动物处于氧化应激状态[9]。高水平的ROS因其强氧化性会对核酸、蛋白质、脂质等重要生物大分子造成损伤,阻止其生理功能的发挥,严重时则会出现细胞凋亡,组织坏死或引发疾病,甚至危及生命。H2O2是生命有机体中重要的活性氧,也是实验室常用的氧化应激诱导剂[10, 11]。Boglarka等[12]报道1 mmol · L-1 H2O2刺激鸡耳蜗细胞后,细胞活力、活细胞数、细胞凋亡和坏死数均显著降低,明显诱导了细胞氧化应激。Jin等[13]研究表明,H2O2刺激人脐静脉内皮细胞2 h,细胞活力降低至70%左右,明显诱导了细胞死亡。从本试验研究结果可知,0.2和0.6 mmol · L-1 H2O2导致细胞活力降低为72%和58%左右,说明H2O2同样能导致鱼类细胞氧化损伤,诱导细胞产生氧化应激。
在本试验条件下,0.001~1.0 mmol · L-1 LC预处理明显抑制了0.2和0.6 mmol · L-1 H2O2导致的细胞活力降低。已有研究表明,0.001~1 mmol · L-1 LC能抵抗0.4 mmol · L-1 H2O2对HK细胞造成的氧化损伤,有效保护了HK细胞活力[14]。镍能诱导小鼠神经瘤细胞氧化应激,镍对小鼠神经瘤细胞活力的抑制作用呈现剂量依赖效应[5],1 mmol · L-1 LC预处理小鼠神经瘤细胞2 h,显著阻断了镍诱导细胞活力的降低,对氧化损伤的小鼠神经瘤细胞具有明显的保护作用。
抗氧化防御系统对于动物机体来说具有重要意义,细胞中ROS的清除是由抗氧化防御系统来完成的,该系统抗氧化能力的强弱直接关系到动物体的健康与疾病。水产动物的抗氧化系统主要包括非酶抗氧化剂系统和抗氧化酶系统两部分[15]。非酶系统主要包括:谷胱甘肽(GSH)、维生素C、β-胡萝卜素、维生素A、维生素E,金属硫蛋白和铁蛋白;而抗氧化酶系统主要是SOD、CAT和GPx等。SOD是动物体内普遍存在的一种金属抗氧化酶,它可以催化超氧阴离子发生歧化反应生成H2O2和水,以此消除细胞代谢中产生的超氧阴离子,保护细胞免受超氧阴离子的损伤[16]。CAT则是以H2O2为底物,将其分解为水和氧气,从而彻底消除自由基[17]。GPx酶能与GSH相互协作,清除有机氢过氧化物,阻断脂质过氧化的自由基链式反应[18]。谷胱甘肽连接酶(γ-GCS)是GSH合成途径的限速酶,因此,γ-GCS活性的高低对细胞中GSH稳态至关重要[19]。MDA是脂质过氧化的终产物,是检测细胞过氧化程度的敏感指标。
LC对水产动物抗氧化功能的研究起步较晚,多数均集中在哺乳动物方面。从本研究结果可知,添加适宜浓度LC能明显提高不同氧化应激程度FHM细胞的T-GSH水平及SOD、CAT、GPx和γ-GCS活性,并显著降低细胞脂质过氧化水平。He等[5]研究报道了LC明显降低了氧化应激状态小鼠神经细胞MDA水平,以及LDH的活性,证明LC能抑制细胞脂质过氧化程度,维持细胞的稳定性和完整性。Ye等[14]报道,LC能提高经过氧化氢诱导的HK细胞内GPx、SOD和CAT活性。日粮中添加葵花油增加了27周龄的海兰褐蛋鸡血清中MDA含量,降低抗氧化能力和抗氧化酶活性,而LC处理能有效保护SOD和GPx抗氧化酶活性,显著降低MDA含量[20]。Miguel-Carrasco等[21]报道,每天补充300 mg · kg-1 LC显著提高了血浆和心脏的CuZn-SOD和GPx等主要抗氧化酶活性及mRNA的表达水平。柱孢藻毒素能诱导鱼类产生氧化应激,而饲料中添加400和880 mg · kg-1 LC对柱孢藻毒素诱导氧化损伤的罗非鱼肝脏和肾脏抗氧化酶SOD、CAT、NADPH和γ-GCS活性有显著影响,并明显降低罗非鱼脂质过氧化程度、蛋白氧化和DNA氧化[22]。
| [1] | Lushchak V. Environmentally induced oxidative stress in aquatic animals[J]. Aquatic Toxicology,2011,101:13-30. |
| [2] | Dong G F,Huang F,Zhu X M,et al. Nutriphysiological and cytological responses of juvenile channel catfish(Ictalurus punctatus)to dietary oxidized fish oil[J]. Aquac Nutr,2012,18:673-684. |
| [3] | 王妤,庄平,章龙珍,等. 盐度对点篮子鱼的存活、生长及抗氧化防御系统的影响[J]. 水产学报,2011,35(1):66-73. Wang S,Zhuang P,Zhang L Z,et al. Effects of salinity on survival,growth and antioxidant defense system of Siganus guttatus[J]. Journal of Fisheries of China,2011,35(1):66-73(in Chinese with English abstract). |
| [4] | 鞠雪,王秋举,罗莎,等. 氧化鱼油对草鱼幼鱼脂质过氧化及抗氧化酶活性的影响[J]. 南京农业大学学报,2015,38(3):491-496. DOI:10.7685/j.issn.1000-2030.2015.03.021. Ju X,Wang Q J,Luo S,et al. Effects of oxidized fish oil on lipid peroxidation and antioxidant enzyme activities in juvenile grass carp(Ctenopharyngodon idellus)[J]. Journal of Nanjing Agricultural University,2015,38(3):491-496(in Chinese with English abstract). |
| [5] | He M D,Xu S C,Lu Y H,et al. L-carnitine protects against nickel-induced neurotoxicity by maintaining mitochondrial function in Neuro-2a cells[J]. Toxicology and Applied Pharmacology,2011,253:38-44. |
| [6] | Harpaz S. L-carnitine and its attributed functions in fish culture and nutrition:a review[J]. Aquaculture,2005,249:3-21. |
| [7] | Cao Y,Li X,Wang C J,et al. Role of NF-E2-related factor 2 in neuroprotective effect of L-carnitine against high glucose-induced oxidative stress in the retinal ganglion cells[J]. Biomedicine and Pharmacotherapy,2015,69:345-348. |
| [8] | 王秋举,鞠雪,王清滨,等. L-肉碱对vero细胞抗H2O2氧化应激的影响[J]. 中国畜牧杂志,2014(13):42-47. Wang Q J,Ju X,Wang Q B,et al. Effects of L-carnitine on vero cells against H2O2-induced oxidative stress[J]. Chinese Journal of Animal Science,2014(13):42-47(in Chinese). |
| [9] | 孙存普,张建中,段绍瑾. 自由基生物学导论[M]. 合肥:中国科技大学出版社,1999:1-57. Sun C P,Zhang J Z,Duan S J. An Biology Introduction to Free Radical[M]. Hefei:Press of University of Science and Technology of China,1999:1-57(in Chinese with English abstract). |
| [10] | Davies K J. An overview of oxidative stress[J]. IUBMB Life,2000,50:241-244. |
| [11] | Pacifici R E,Kono Y,Davies K J. Hydrophobicity as the signal for selective degradation of hydroxyl radical-modified hemoglobin by the multicatalytic proteinase complex,proteasome[J]. J Biol Chem,1993,268:15405-15411. |
| [12] | Boglarka R,Gabriella H,Dora R,et al. PACAP ameliorates oxidative stress in the chicken inner ear:an in vitro study[J]. Regulatory Peptides,2010,160:91-98. |
| [13] | Jin Y,Liu K,Peng J,et al. Rhizoma dioscoreae nipponicae polysaccharides protect HUVECs from H2O2-induced injury by regulating PPAR factor and the NADPH oxidase/ROS-NF-kB signal pathway[J]. Toxicology Letters,2015,232:149-158. |
| [14] | Ye J S,Li J,Yu Y M,et al. L-carnitine attenuates oxidant injury in HK-2 cells via ROS-mitochondria pathway[J]. Regulatory Peptides,2010,161:58-66. |
| [15] | Livingstone D R. Contaminant-stimulated reactive oxygen species production and oxidative damage in aquatic organisms[J]. Mar Pollut Bull,2001,42:656-666. |
| [16] | Yasmineh W G,Theologides A. Catalase,as a roving scavenger of hydrogen peroxide:a hypothesis[J]. J Lab Clin Med,1993,122(1):110-114. |
| [17] | 孙学亮,郭永军,季延滨,等. 三种复方中草药对中华绒鳌蟹生长和部分抗氧化指标的影响[J]. 经济动物学报,2014. DOI:10.13326/j.jea.2014.1038. Sun X L,Guo Y J,Ji Y B,et al. Effects of three kinds of compound chinese herbal on growth and antioxidative indicators in Eriocheir sinensis[J]. Journal of Economic Animal,2014. DOI:10.13326/j.jea.2014.1038(in Chinese with English abstract). |
| [18] | Li Z H,Velisek J,Zlabek V,et al. Hepatic antioxidant status and hematological parameters in rainbow trout(Oncorhynchus mykiss)after chronic exposure to carbamazepine[J]. Chem Biol Interact,2010,183:98-104. |
| [19] | Shelly C L. Glutathione synthesis[J]. Biochimica et Biophysica Acta,2013,1830(5):3143-3153. |
| [20] | 徐少辉,张亚男,武书庚,等. L-肉碱对饲粮中添加葵花油的产蛋鸡抗氧化功能及鸡蛋品质的影响[J]. 动物营养学报,2011,23(7):1201-1208. Xu S H,Zhang Y N,Wu S G,et al. Effects of L-carnitine on egg quality and antioxidative ability of laying hens fed diets supplemented with sunflower oil[J]. Chinese Journal of Animal Nutrition,2011,23(7):1201-1208(in Chinese with English abstract). |
| [21] | Miguel-Carrasco J L,Monserrat M T,Mate A,et al. Comparative effects of captopril and L-carnitine on blood pressure and antioxidant enzyme gene expression in the heart of spontaneously hypertensive rats[J]. Eur J Pharmacol,2010,632(1/2/3):65-72. |
| [22] | Guzmán G R,Prieto A I,Vázquez C M,et al. The protective role of L-carnitine against cylindrospermopsin-induced oxidative stress in tilapia(Oreochromis niloticus)[J]. Aquatic Toxicology,2013,132/133:141-150. |




