文章信息
- 耿芳芳, 许伟, 范梦雪, 宫佳杰, 胡文娟, 孟婷婷, 李玉, 冯士彬, 吴金节, 王希春. 2016.
- GENG Fangfang, XU Wei, FAN Mengxue, GONG Jiajie, HU Wenjuan, MENG Tingting, LI Yu, FENG Shibin, WU Jinjie, WANG Xichun. 2016.
- 脱氧雪腐镰刀菌烯醇对雏鸡脂质过氧化反应及脑部形态结构的影响
- Effects of deoxynivalenol on lipid peroxidation reaction and brain morphology in chicken
- 南京农业大学学报, 39(3): 460-466
- Journal of Nanjing Agricultural University, 39(3): 460-466.
- http://dx.doi.org/10.7685/jnau.201510024
-
文章历史
- 收稿日期:2015-10-18
真菌毒素是由真菌在其生长过程中产生的一系列具有毒性的次级代谢产物,可通过被污染的谷物饲料和/或由这些饲料喂养动物产生的动物性食品(如肉类,蛋等)进入食物链,从而危害人畜健康[1]。真菌毒素种类繁多,对畜禽生产造成严重经济损失的有黄曲霉毒素B1(AFB1)、脱氧雪腐镰刀菌烯醇(DON)、伏马菌素B1(FB1)、玉米赤霉烯酮(ZEN)和赭曲霉毒素A(OTA)等[2]。DON又称为呕吐毒素,是对农产品、畜牧业和人类健康危害最为严重的真菌毒素之一,在中国乃至世界范围内有着较高的污染率,具有神经毒性、细胞毒性、免疫毒性、致癌、致畸、致突变等多种毒性作用[3]。DON的神经毒性作用机制一直都是国内外学者研究的热点之一。研究报告指出,猫食用被DON污染的玉米之后,脑内有出血点[4]。Prelusky等[5]研究表明,DON能通过猪的血脑屏障,迅速达到浓度高峰,并影响神经递质的分泌。研究还发现,成年家禽对DON有一定的耐受能力[6],但是DON对雏鸡的毒害作用却不容忽视,DON能导致雏鸡食欲减退、生长迟滞以及其他相关疾病[7, 8, 9]。研究者认为,DON的毒性作用与脂质过氧化有着密切的关系,DON能够引起动物机体和体外培养的细胞发生明显的脂质过氧化反应,表现为抑制体内主要的抗氧化酶的活性,进而引起氧化应激[10, 11]。由于脑组织具有高浓度的不饱和脂肪酸、儿茶酚胺和高水平的氧化代谢能力,所以易受自由基的侵袭,发生脂质过氧化反应。但是DON对禽类神经组织脂质过氧化的影响研究较少,该效应在DON神经毒性中的作用还不清楚。基于以上研究现状,本试验通过DON对雏鸡的攻毒试验,根据血清和脑组织中脂质过氧化反应及对脑组织的损伤情况,研究DON对雏鸡的神经毒理作用,以完善DON毒性作用理论,为DON神经毒性的有效防治提供试验依据。
1 材料与方法 1.1 试验材料1日龄海兰蛋雏公鸡,购于安徽省安禽禽业有限公司;鸡用过氧化氢酶(CAT)、超氧化物歧化酶(SOD)、总抗氧化能力(T-AOC)、谷胱甘肽过氧化物酶(GSH-Px)活性和丙二醛(MDA)、一氧化氮(NO)含量的ELISA检测试剂盒,购于南京森贝伽生物科技有限公司;DON(含量不小于99%)、多聚甲醛,购自Sigma公司;环氧丙烷,购于国药集团化学试剂公司;戊二醛、环氧树脂,购自美国SPI公司;醋酸双氧铀、柠檬酸铅,购于北京达昱科仪公司。
1.2 动物的选择与分组120只健康海兰蛋雏公鸡,观察1周后,按单因素的试验设计,将雏鸡随机分成4组,每组30只,对照组和试验组饲喂相同全价饲料,低剂量组、中剂量组和高剂量组按采食量添加0.27、1.68和12.21 mg · kg-1剂量的DON进行灌胃,对照组灌服与试验组同等量的生理盐水。DON灌服剂量参照Yunus等[12]的试验报道。
1.3 饲养管理从第8天开始对试验组鸡进行灌胃染毒,每隔7 d染毒1次,共染毒5次。试验鸡自由采食和饮水,采用阶梯式笼养方式,严格按照雏鸡的饲养标准和免疫程序进行饲养管理,观察记录染毒期间雏鸡的临床表现和生长发育情况。第5次染毒后,所有鸡均继续正常饲喂1 d,即第36天进行样品采集并观察病理变化。
1.4 日粮组成雏鸡日粮由安徽某饲料公司提供,饲料配方及营养水平见表 1。
1.5 样品的采集与处理试验结束时,所有鸡只自由饮水,禁食12 h后,翅静脉采血,4 ℃、3 500 r · min-1离心15 min,分离血清,置于-20 ℃冰箱内保存,用于氧化及抗氧化指标的测定。同时,每组随机屠宰20只鸡,迅速取脑组织,观察病变。一部分用体积分数为10%的磷酸缓冲福尔马林溶液固定,用以进行病理组织学检查;一部分样品用体积分数4%的多聚甲醛进行固定,用于透射电镜观察;一部分脑组织加入一定量的PBS后进行快速匀浆,将匀浆液以10 000 r · min-1离心30 min,取其上清液保存于-20 ℃冰箱内,用于氧化及抗氧化指标的测定。
| % | |||
| 原料组成Ingredient compositions | 水平Levels | 营养组成Nutrition composition | 水平Levels |
| 玉米Corn | 58.00 | 消化能① Digestible energy | 13.27 |
| 豆粕Soybean meal | 24.00 | 粗蛋白Crud protein | 22.95 |
| 鱼粉Fish meal | 12.00 | 钙Calcium | 1.00 |
| 植物油Vegetable oil | 3.00 | 磷Phosphone | 0.50 |
| L-赖氨酸L-lysine | 0.15 | 赖氨酸Lysine | 1.52 |
| DL-蛋氨酸DL-methionine | 0.20 | 蛋氨酸Methionine | 0.6 |
| 石粉Limestone | 0.85 | 胱氨酸Cystine | 0.25 |
| 磷酸氢钙CaHPO4 | 0.35 | ||
| 添加剂Additives | 1.45 | ||
| 注:① 消化能单位为MJ · kg-1。The unit of the digestible energy is MJ · kg-1. | |||
将保存于-20 ℃冰箱内的血清和脑组织匀浆液的上清液恢复至常温,用于测定CAT、SOD、T-AOC、GSH-Px活性和MDA、NO含量,检测按照ELISA检测试剂盒说明书,采用Multiskan MK3酶标仪进行测定。
1.7 脑组织显微形态结构的观察 1.7.1 石蜡切片的制备从福尔马林溶液中取出脑组织,切取适当大小的组织块,用解剖刀修至平整,单层纱布包裹,细绳结扎并标记相应组织和组别,然后置于烧杯中,用流水冲洗过夜。经石蜡包埋后,采用YD-1508R轮转式切片机切片(厚度4 μm)。
1.7.2 HE染色将制备好的切片进行常规HE染色。染色后细胞核应为紫色,细胞浆则为红色,光镜下观察组织的病理变化。
1.8 脑组织超微形态结构的观察 1.8.1 脑组织超薄切片的制备取出固定于4%多聚甲醛中的脑组织,用刀片取1 mm×1 mm×1 mm大小的大脑皮质块5块,放入含有2.5%磷酸缓冲戊二醛固定液的1 mL离心管中,离心10 min(2 000 r · min-1,4 ℃)后,固定4~6 h,再将组织固定于1%锇酸中1 h;经体积分数分别为30%、50%乙醇脱水各15 min,在体积分数为70%的乙醇醋酸铀饱和液中浸泡6~12 h;再经80%、95%乙醇脱水各15 min,无水乙醇脱水40 min,2次,再分别经环氧丙烷过渡30 min、环氧丙烷-环氧树脂(体积比1 : 1)2 h、环氧丙烷-环氧树脂(体积比1 : 2)1 h、环氧树脂2 h包埋后,放入45 ℃烤箱中烘烤12 h,65 ℃烤箱中烘烤48 h。取出包埋好的组织进行超薄切片,切片厚度70 nm。
1.8.2 铅铀双重染色将切好的切片水洗后放入醋酸铀饱和水溶液中避光染色30 min,双蒸水洗3次,每次15 min;放入枸橼酸铅染液中染色15 min后双蒸水洗3次,每次15 min,捞片于200目铜网上,自然干燥后,采用TEOL-2010高分辨率透射电子显微镜观察并摄片。
1.9 数据处理试验数据均以平均数±标准差(x±SD)表示,采用SPSS 17.0统计软件中的ANOVA进行方差分析,多重比较采用Duncan′s法。
2 结果与分析 2.1 雏鸡生长状态饲养期间对照组雏鸡生长良好,饮食正常,精神状态良好,个体差异小。与对照组相比,从第2次灌胃开始,试验组雏鸡出现精神沉郁,食欲减退,个体差异大,有少量呈淡绿色稀粪,偶有血便,且症状随着染毒剂量的增加而加重。
2.2 脑组织剖检病理变化由图 1可见:雏鸡屠宰剖检后,迅速取出完整的脑部组织,可见对照组雏鸡脑组织无明显病理变化,颜色正常;而试验组鸡脑组织出现不同程度的肿胀和出血点,且随着染毒剂量的增加,呈现脑组织颜色逐渐变暗的现象。
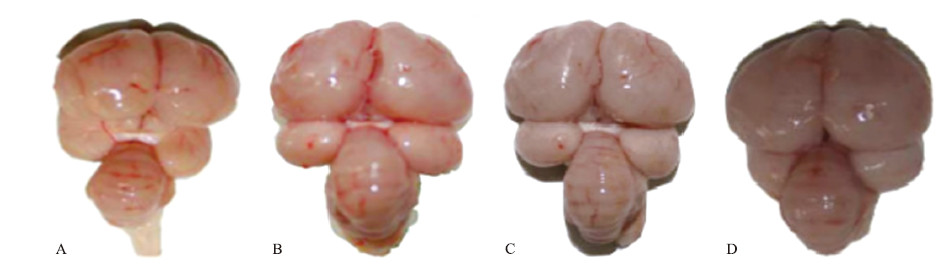 | 图 1 雏鸡脑组织病理变化 Fig. 1 Pathological changes of brain tissue in chicken A.对照组 Control group;B.低剂量组(DON 0.27 mg · kg-1)Low dose group;C.中剂量组(DON 1.68 mg · kg-1)Medium dose group;D.高剂量组(DON 12.21 mg · kg-1)High dose group |
由图 2可见:对照组(图 2-A)雏鸡脑组织形态结构正常,无明显病理变化;低剂量组(图 2-B)雏鸡脑细胞间隙增大,出现轻微的脑水肿现象,部分神经细胞周围的小胶质细胞增多;中剂量组(图 2-C)雏鸡脑细胞间隙增大,出现明显的脑水肿和非化脓性脑炎现象,神经细胞周围的小胶质细胞开始吞噬神经细胞;高剂量组(图 2-D)雏鸡脑细胞变得稀疏,出现明显的脑水肿和典型的非化脓性脑炎现象,并开始出现明显的噬神经现象,伴随有部分神经纤维断裂。
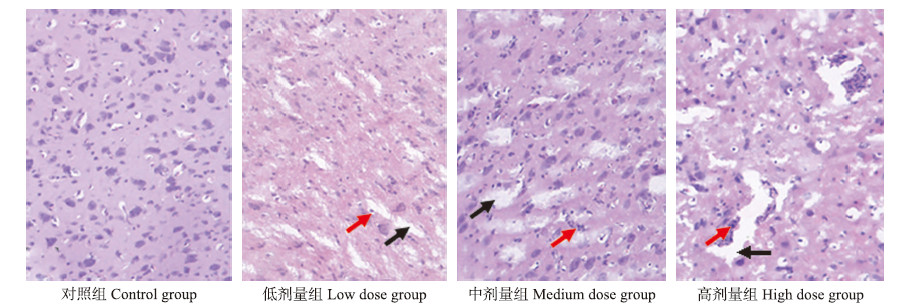 |
图 2 雏鸡脑组织切片(HE染色,40×) Fig. 2 Brain tissue slices of chicken(HE stain,40×)
图中红色箭头所指为神经细胞周围的小胶质细胞,黑色剪头所指为细胞间隙。 The red arrows indicate the microglia rounding of nerve cells and the black arrows indicate the intercellular space. |
由图 3可见:对照组雏鸡大脑皮质神经元呈现正常超微结构影像,神经元细胞膜、核膜完整,染色质分布均匀,线粒体和内质网形态、结构及周围突起正常。低剂量组脑神经元胞体出现轻度变性,主要表现为神经元细胞膜、核膜完整,染色质分布均匀,部分线粒体出现空泡变性,粗面内质网轻度扩展、断裂,核糖体减少,溶酶体体积增大、数量增多。中剂量组脑神经元胞体出现严重变性,主要表现为神经元细胞膜、核膜完整,胞体肿胀,细胞核正常,胞浆肿胀,粗面内质网扩展、断裂、减少,核糖体减少,线粒体空泡变性、减少,溶酶体体积增大、数量增多。高剂量组脑神经元胞体出现水样变性甚至坏死,主要表现为胞体肿胀,部分神经元细胞膜、核膜被破坏,胞浆肿胀严重,溶酶体体积增大、数量增多,线粒体肿胀、嵴间隙增宽,部分细胞器几乎消失。
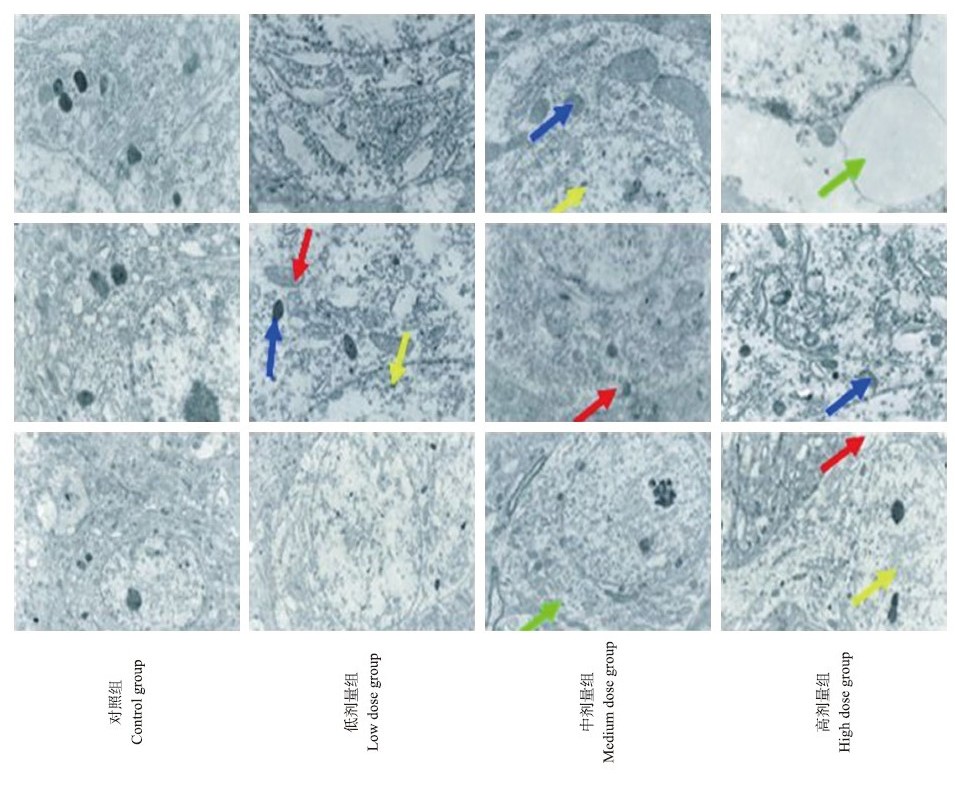 |
图 3 雏鸡脑组织的超微结构 Fig. 3 Ultrastructure of brain tissue in chicken
从左到右放大倍数依次为5 000、12 000、12 000。图中红色箭头所指为线粒体空泡变性;蓝色箭头所指为溶酶体;黄色箭头所指为核糖体;绿色箭头所指为胞浆肿胀现象。 From left to right,the image magnification times as 5 000,12 000,12 000,respectively. The red arrows indicate the mitochondrial vacuole degeneration,the blue arrows indicate the lysosome,the yellow arrows indicate the ribosome,and the green arrows indicate the cytoplasmic swelling. |
由表 2可见:与对照组相比,低、中和高剂量组血清CAT活性和NO含量显著降低(P<0.05),但各试验组之间差异不显著(P>0.05);低、中和高剂量组血清SOD活性显著降低(P<0.05),但中剂量组SOD活性与低剂量组和高剂量组之间差异均不显著(P>0.05);低、中和高剂量组血清MDA含量显著升高(P<0.05),各试验组之间MDA含量差异显著(P<0.05);中和高剂量组血清T-AOC和GSH-PX活性显著降低(P<0.05),低剂量组差异不显著(P>0.05)。
| 项目Items | 对照组Control group | 低剂量组Low dose group | 中剂量组Medium dose group | 高剂量组High dose group |
| CAT/(U·L-1) | 4.43±0.68a | 3.83±0.96b | 3.77±0.41b | 3.50±1.01b |
| SOD/(U·L-1) | 109.80±11.70a | 91.25±6.90ab | 85.90±8.90bc | 79.70±7.85c |
| T-AOC/(U·mL-1) | 58.44±6.94a | 51.47±2.98ab | 47.36±6.04b | 45.05±4.16b |
| GSH-Px/(μg·L-1) | 2.201±0.210a | 2.166±0.074a | 2.082±0.144b | 1.970±0.164b |
| MDA/(nmol·L-1) | 40.41±3.69a | 46.60±4.69b | 51.57±2.80c | 57.08±1.96d |
| NO/(μmol·L-1) | 63.65±8.25a | 51.71±9.88b | 49.91±4.22b | 47.25±8.81b |
| 注:同行上标字母不同者表示差异显著(P<0.05)。表 3同此。 Note:The data with different superscripts small letters in the same line indicate significant difference at 0.05 level. The same as in the Table 3. | ||||
由表 3可见:与对照组相比,低、中和高剂量组雏鸡脑组织SOD和GSH-Px活性显著降低(P<0.05),但各试验组之间差异不显著(P>0.05);高剂量组脑组织MDA含量显著升高(P<0.05),T-AOC活性显著降低(P<0.05),低和中剂量组之间差异不显著(P>0.05);中、高剂量组脑组织CAT活性和NO含量显著降低(P<0.05),低剂量组差异不显著(P>0.05),中剂量组与高剂量组之间差异不显著(P>0.05)。
项目Items | 对照组Control group | 低剂量组Low dose group | 中剂量组Medium dose group | 高剂量组High dose group |
| CAT/(U·L-1) | 6.14±1.05a | 5.28±0.58ab | 4.55±1.08bc | 3.78±1.10c |
| SOD/(U·L-1) | 214.75±41.06a | 159.02±42.13b | 145.34±30.24b | 160.02±20.71b |
| T-AOC/(U·mL-1) | 47.47±11.15a | 41.20±8.07a | 38.69±7.30a | 28.60±6.95b |
| GSH-Px/(μg·L-1) | 11.22±0.64a | 7.54±1.59b | 7.20±1.50b | 5.41±0.80b |
| MDA/(nmol·L-1) | 93.62±39.50b | 99.12±15.51b | 119.18±16.20b | 153.32±35.65a |
| NO/(μmol·L-1) | 166.58±17.00a | 157.16±34.82ab | 133.92±19.00b | 133.92±19.00b |
与其他真菌毒素相比,DON的毒性相对较弱,但由于其广泛存在于谷物与饲料中,且检出率很高,因此DON的毒性作用一直受到高度重视。据报道,成年鸡对DON的敏感性较低,饲料中含10 mg · kg-1 DON时可引起拒食和日增重降低[6]。在本试验中,虽然灌服剂量相对较低,但从第2周开始,试验组雏鸡精神沉郁,食欲减退,个体差异大,有少量呈淡绿色稀粪,偶有血便,且临床症状随着染毒剂量的增加而加重,究其原因可能是鸡的日龄较低,一次性灌服该剂量的DON造成雏鸡急性中毒。剖检试验组雏鸡,观察到脑部肿大,脑组织颜色暗淡,有出血点,这些现象与之前报道结果[4]一致,说明DON对雏鸡存在一定的神经毒性作用。
3.2 DON对雏鸡血清和脑组织氧化及抗氧化指标的影响自由基是生物体在代谢过程中不断产生的中间产物,在正常情况下,体内自由基处于不断产生与清除的动态平衡中。自由基具有强氧化性,可损害机体的组织和细胞,进而引起慢性疾病及衰老效应。GSH-Px和SOD是机体内常见的2种抗氧化酶,能有效清除体内多余的自由基,蒋竹英等[13]研究表明,DON可显著降低仔猪血清GSH-Px和SOD的活性,显著升高MDA含量。据报道,镰刀菌毒素可以通过损害细胞的抗氧化系统,加速自由基的产生,增加细胞的过氧化反应,而CAT可防止过氧化反应[14]。Kouadio等[15]报道DON能阻断鞘磷脂代谢,导致脂质过氧化,改变细胞膜结构,使细胞MDA产生增加。李洋[16]发现DON可降低SOD活性,显著升高MDA和NO含量,并且存在明显的剂量-效应关系。NO代谢失衡时,NO能以较高的浓度与机体内蛋白质、核酸、脂肪等相互作用损伤细胞或信息传递,对机体造成多种病理变化[17]。本试验取得了与上述报道相同的试验结果,雏鸡灌服DON后,可显著降低血清及脑组织中T-AOC、SOD、GSH-Px、CAT活性和NO含量,提高MDA含量。上述结果表明,DON可显著改变雏鸡氧化与抗氧化酶活性,导致机体产生脂质过氧化反应。
3.3 DON对雏鸡脑组织形态结构的影响大脑是控制运动、产生感觉及实现高级脑功能的高级神经中枢,损伤大脑也会对身体产生严重伤害。有研究表明,DON对鸡脑组织有一定的损伤作用[18]。研究发现,溶酶体也可参与神经细胞的凋亡[19, 20]。本试验通过普通病理切片发现各试验组大脑出现不同程度的脑水肿、典型的非化脓性脑炎、噬神经现象以及部分神经纤维断裂现象,通过超薄切片发现神经元胞体出现不同程度的损伤,特别是高剂量组神经元胞体水样变性甚至坏死,主要表现为胞体肿胀,部分神经元细胞膜、核膜被破坏,胞浆严重肿胀,线粒体肿胀、嵴间隙增宽,溶酶体体积增大、数量增多,部分细胞器几乎消失殆尽。2种切片观察结果均表明DON对脑组织造成了一定的损伤,并与DON剂量呈正相关。
综上所述,DON可影响雏鸡的正常生长状态,显著改变血清与脑组织中氧化与抗氧化酶活性,导致机体产生脂质过氧化反应,从而引起神经毒性作用,造成脑组织不同程度的损伤。
| [1] | Hussein S H,Jeffrey M B. Toxicity,metabolism,and impact of mycotoxins on humans and animals[J]. Toxicology,2001,167(2):101-134. |
| [2] | Ren Z H,Wang Y C,Deng H D,et al. Deoxynivalenol induces apoptosis in chicken splenic lymphocytes via the reactive oxygen species-mediated mitochondrial pathway[J]. Environmental Toxicology and Pharmacology,2015,39(1):339-346. |
| [3] | Ebrahem M,Kersten S,Valenta H,et al. Effects of feeding deoxynivalenol(DON)-contaminated wheat to laying hens and roosters of different genetic background on the reproductive performance and health of the newly hatched chicks[J]. Mycotoxin Research,2014,30(3):131-140. |
| [4] | Faixova Z,Faix S,Borutova R,et al. Efficacy of dietary selenium to counteract toxicity of deoxynivalenol in growing broiler chickens[J]. Acta Veterinaria Brno,2007,76(3):349-356. |
| [5] | Prelusky D B,Yeung J M,Thompson B K,et al. Effeck of deoxynivalenol on neurotransmitters in discrete regions of swine brain[J]. Archives of Environmental Contamination and Toxicology,1992,22(3):36-40. |
| [6] | Ghareeb K,Awad W A,Sid-Ahmed O E. Insights on the host stress,fear and growth responses to the deoxynivalenol feed contaminant in broiler chickens[J]. PLoS ONE,2014,9(1):1-7. |
| [7] | Swamy H V L N,Smith T K,MacDonald E J. Effects of feeding blends of grains naturally contaminated with Fusarium mycotoxins on brain regional neurochemistry of starter pigs and broiler chickens[J]. Journal of Animal Science,2004,82(7):2131-2139. |
| [8] | Girish C K,MacDonald E J,Scheinin M,et al. Effects of feedborne Fusarium mycotoxins on brain regional neurochemistry of turkeys[J]. Poultry Science,2008,87(7):1295-1302. |
| [9] | 李荣佳,李治忠,周闯,等. 新型复合吸附剂HG对黄曲霉毒素B1和呕吐毒素的吸附脱毒研究[J]. 南京农业大学学报,2015,38(1):113-119. DOI:10.7685/j.issn.1000-2030.2015.01.017. Li R J,Li Z Z,Zhou C,et al. Detoxification of aflatoxin B1 and deoxynivalenol by new compound adsorbent HG[J]. Journal of Nanjing Agricultural University,2015,38(1):113-119(in Chinese with English abstract). |
| [10] | Borutova R,Faix S,Placha I,et al. Effects of deoxynivalenol and zearalenone on oxidative stress and blood phagocytic activity in broilers[J]. Archives of Animal Nutrition,2008,62(4):303-312. |
| [11] | Krishnaswamy R,Devaraj S N,Padma V V. Lutein protects HT-29 cells against deoxynivalenol-induced oxidative stress and apoptosis:prevention of NF-κB nuclear localization and down regulation of NF-κB and cyclo-oxygenase-2 expression[J]. Free Radical Biology and Medicine,2010,49(1):50-60. |
| [12] | Yunus A W,Ghareeb K,Twaruzek M,et al. Deoxynivalenol as a contaminant of broiler feed:effects on bird performance and response to common vaccines[J]. Poultry Science,2012,91(4):844-851. |
| [13] | 蒋竹英,李丽立,唐利华,等. DON污染饲粮添加竹炭和竹醋液对断奶仔猪抗氧化性能及小肠黏膜形态的影响[J]. 西北农林科技大学学报(自然科学版),2013,41(12):37-42. Jiang Z Y,Li L L,Tang L H,et al. Effects of adding bamboo charcoal and bamboo vinegar to DON contaminated diets on oxidation resistance and small intestinal morphology of weaned piglets[J]. Journal of Northwest A&F University(Natural Science Edition),2013,41(12):37-42(in Chinese with English abstract). |
| [14] | Pestka J J,Zhou H R,Moon Y,et al. Cellular and molecular mechanisms for immune modulation by deoxynivalenol and other trichothecenes:unraveling a paradox[J]. Toxicology Letters,2004,153(1):61-73. |
| [15] | Kouadio J H,Mobio T A,Baudrimont I,et al. Comparative study of cytotoxicity and oxidative stress induced by deoxynivalenol,zearalenone or fumonisin B1 in human intestinal cell line Caco-2[J]. Toxicology,2005,213(1/2):56-65. |
| [16] | 李洋. 镰刀菌毒素ZEA、DON及其联合染毒对小鼠脑损伤机制的研究[D]. 雅安:四川农业大学,2013. Li Y. The research on injury mechanism of deoxynivalenol,zearalenone and co-infection on brain of mice[D]. Ya'an:Sichun Agricultural University,2013(in Chinese with English abstract). |
| [17] | Ledo A,Frade J,Barbosa R M,et al. Nitric oxide in brain:diffusion,targets and concentration dynamics in hippocampal subregions[J]. Molecular Aspects of Medicine,2004,25(1/2):75-89. |
| [18] | Awad W A,Hess M,Twaruzek M,et al. The impact of the Fusarium mycotoxin deoxynivalenol on the health and performance of broiler chickens[J]. International Journal of Molecular Sciences,2011,12(11):7996-8012. |
| [19] | Anagli J,Abounit K,Stemmer P,et al. Effects of cathepsins B and L inhibition on postischemic protein alterations in the brain[J]. Biochemical and Biophysical Research Communications,2008,366(1):86-91. |
| [20] | Yamashima T,Oikawa S. The role of lysosomal rupture in neuronal death[J]. Progress in Neurobiology,2009,89(4):343-358. |




