文章信息
- 危蓉萍, 杨东航, 卜莹莹, 纪燕玲, 于汉寿. 2016.
- WEI Rongping, YANG Donghang, BU Yingying, JI Yanling, YU Hanshou. 2016.
- 蜜蜂螺原体几丁质脱乙酰酶基因的克隆、表达及酶学性质
- Cloning, expression and enzymatic characterization of a chitin deacetylase gene from Spiroplasma melliferum
- 南京农业大学学报, 39(3): 417-424
- Journal of Nanjing Agricultural University, 39(3): 417-424.
- http://dx.doi.org/10.7685/jnau.201511001
-
文章历史
- 收稿日期:2015-11-02
螺原体属(Spiroplasma)细菌包含一组与节肢动物和植物相互作用的内共生体[1, 2],在系统发育上,螺原体属于柔膜菌纲,与芽孢杆菌纲及其他营自由生活的厚壁菌门亲缘关系较近[3, 4]。虽然大多数螺原体种与宿主营互生或共生关系,但某些种对植物或节肢动物具致病性。大部分致病性螺原体属Citri-Chrysopicola-Mirum枝[2],典型代表如导致柑橘僵化病的S.citri和玉米矮化病的S.kunkelli,以及导致中华绒螯蟹颤抖病的S.eriocheiris[5]和蜜蜂“爬蜂病”的S.melliferum[6]。Chen等[7]首次在中国从患“爬蜂病”的蜜蜂体内分离到螺原体菌株,将其命名为S.melliferum CH-1,并详细研究了其基本生物学特性。
应用比较基因组学和蛋白质组学研究发现,蜜蜂螺原体S.melliferum存在2种特有的基因——几丁质酶和几丁质脱乙酰酶基因,而在其他几种借助昆虫传播但对昆虫无致病性的螺原体(如S.citri和S.kunkelli)中没有发现这2种基因,因此推测其是致病相关基因,在蜜蜂螺原体侵入蜜蜂肠道过程中起关键作用[8, 9, 10]。GenBank数据比对显示S.melliferum几丁质酶基因在柔膜菌纲中没有同源序列,只与乳球菌属(Lactococcus)和肠球菌属(Enterococcus)中的几丁质酶基因有较高的同源性[8]。
几丁质作为结构内容物是昆虫表皮、中肠上皮细胞和围食膜的重要组成成分[11]。几丁质脱乙酰酶(chitin deacetylase,CDA)是几丁质降解酶系成员之一,能够催化几丁质中β-1,4-糖苷键连接的N-乙酰基葡糖胺中乙酰氨基的水解[10]。围食膜(peritrophic membrane)是大多数昆虫中肠细胞分泌的一层厚薄均匀的长管状薄膜,主要由蛋白质和几丁质微纤丝网格构成,几丁质酶和几丁质脱乙酰酶对昆虫肠道内的围食膜可能起到了破坏作用。例如蓓带夜蛾(Mamestra configurata)几丁质脱乙酰酶参与改变围食膜中几丁质的物理和化学性质,这一生化过程不仅改变几丁质的纤维结构,而且对围食膜蛋白的结合程度、围食膜的完整性和孔隙率产生影响[12]。由于密码子TGA在柔膜菌纲的多数种类中编码色氨酸而非终止密码子,因此柔膜菌含有这一密码子的基因在大肠杆菌中的表达受到限制[13]。为实现几丁质脱乙酰酶蛋白在大肠杆菌中的完整外源表达,需将密码子TGA定点突变为TGG。本研究中,我们成功克隆与定点突变并在大肠杆菌中完全表达了chid基因,获得具有活性的外源目的蛋白,为后续研究螺原体与宿主蜜蜂的相互作用提供了重要信息。
1 材料与方法 1.1 材料 1.1.1 菌株、载体及培养基菌株S.melliferum CH-1由本实验室分离、纯化并保存;表达载体pET-28a(+)由南京农业大学生命科学院郑会明老师馈赠;大肠杆菌(Escherichia coli)DH5α和BL21(DE3)购于百泰克公司。R2培养基[14];LB液体/固体培养基。
1.1.2 主要试剂0.2 mol · L-1 PB(1 L,58 g Na2HPO4,6 g NaH2PO4);0.02 mol · L-1 PB(pH7.9);Binding Buffer(0.05 mol · L-1 PB,0.5 mol · L-1 NaCl,0.02 mol · L-1 Imidazole);Elution Buffer(0.05 mol · L-1 PB,0.5 mol · L-1 NaCl,不同浓度Imidazole);Trans Buffer(1 L,Tris Base 11.26 g,Glycine 2.42 g,H2O 800 mL,Methanol 200 mL);TBST缓冲液(1 L,Tris Base 3 g,NaCl 8 g,KCl 0.2 g,吐温-20 2.35 mL,pH7.4);200 mg · L-1对硝基乙酰苯胺;10 mg · L-1对硝基苯胺(国产分析纯);终质量浓度为50 mg · L-1的卡那霉素;终浓度为1 mmol · L-1的IPTG;0.1 mol · L-1 PMSF;其他试剂均为进口或国产分析纯。
快速限制性内切酶BamHⅠ和XhoⅠ、T4 DNA连接酶购于TaKaRa公司;用于PCR反应的试剂、抗His标签鼠单克隆抗体、羊抗鼠IgG单克隆抗体购于上海浦迪生物科技有限公司;PCR引物由南京金斯瑞生物科技有限公司合成;质粒DNA小量制备试剂盒、柱式琼脂糖凝胶DNA回收试剂盒购于上海捷瑞生物工程有限公司;显影定影试剂盒、脱脂奶粉和PVDF膜购于罗氏生物科技;NTA-Ni2+柱由南京基蛋生物技术有限公司馈赠。
1.2 S.melliferum CH-1菌株基因组DNA的提取采用CTAB/NaCl法提取螺原体基因组。
1.3 几丁质脱乙酰酶相关基因chid的定点突变及扩增 1.3.1 PCR引物设计搜索S.melliferum CH-1全基因组序列精细图,发现1个由672个碱基序列编码的CDA蛋白基因chid,其5′端586~588位含有1个TGA密码子。利用Primer Premier 5.0软件设计了2对含保护碱基和酶切位点的引物(表 1):Chid-1和Chid-4为两侧引物,用于扩增片段全长,其5′端分别带有BamHⅠ和XhoⅠ酶切位点;Chid-2和Chid-3为含有突变位点以及27个互补碱基的中间引物,分别与两侧引物扩增产物Chid-U和Chid-D,将其作为OE-PCR的模板利用中间互补碱基扩增出突变后的chid基因全长。
| 引物Primers | 引物序列(5′→3′)Sequence of primers | 内切酶Restriction enzyme | 产物Products | 产物大小/bp Products size |
| Chid-1 | CGCGGATCCATGACAACAAGCAACTATGAAG | BamHⅠ | ||
| Chid-2 | TGATATCCCTGTTGTTTTAA CCAAACAAT | Chid-U | 617 | |
| Chid-3 | TGTT TGGTTAAAACAACAGGGATATCAAT | |||
| Chid-4 | CCGCTCGAGTTAATTCACCAAATTTCCATAATTTC | XhoⅠ | Chid-D | 100 |
| T7 | TAATACGACTCACTATAGGG | |||
| T7-t | TGCTAGTTATTGCTCAGCGG | Chid | 690 | |
| 注:阴影为突变碱基,下划线为限制性酶切位点。 Note:The bases for substitutions are shadowed,and the restriction sites are underlined. |
||||
首先以S.melliferum CH-1菌株基因组DNA为模板,分别用正向引物chid-1和突变引物chid-2以及突变引物chid-3和反向引物chid-4进行PCR1和PCR2扩增,产物为含突变位点的上游片段chid-U和下游片段chid-D,PCR产物用凝胶回收试剂盒纯化后作为模板用于重叠延伸PCR3(采用Taq酶和Pfu酶),此外分别用正向引物chid-1和反向引物chid-4不经OE-PCR定点突变进行chid基因全长扩增,纯化回收后构建重组质粒作为阳性对照。
1.4 重组质粒pETchid的构建PCR产物回收后,用QuickCut BamHⅠ和QuickCut XhoⅠ双酶切1 h后纯化酶切产物,连接到用同样两种酶酶切的pET-28a(+)载体上并转化到E.coli DH5α。以通用引物T7、T7-t进行PCR验证,筛选阳性克隆送华大基因公司测序鉴定。此外用质粒DNA小量制备试剂盒提取阳性克隆菌株的重组质粒,用QuickCut BamHⅠ和QuickCut XhoⅠ双酶切验证。最后将重组质粒转化到E.coli BL21(DE3),获得的菌株称为BLchid菌株,并用30%的甘油以体积比为1 : 1的比例混匀,-20 ℃保存备用。
1.5 几丁质脱乙酰酶的原核表达与纯化将BLchid菌株接种于1 mL含50 mg · L-1卡那霉素的LB液体培养基,各接2管,37 ℃培养至对数期(D600=0.5~0.6),一管不加诱导剂作为阴性对照,另一管加入终浓度为1 mmol · L-1的异丙基-β-D-硫代半乳糖苷(IPTG)后于28 ℃诱导4 h,8 000 r · min-1离心5 min,收集菌体,加入70 μL双蒸水混匀后沸水浴5 min,SDS-PAGE电泳检测蛋白表达情况。
将BLchid菌株接种于1 L含50 mg · L-1卡那霉素的LB液体培养基中,37 ℃培养至对数期,加入终浓度为1 mmol · L-1的IPTG,28 ℃诱导4 h,4 ℃、8 000 r · min-1离心10 min,去除上清液,细菌沉淀悬浮于20 mL Binding Buffer(含20 μL 0.1 mol · L-1 PMSF),分成2管经细胞超声破碎仪破碎后,4 ℃、10 000 r · min-1离心10 min,收集上清液,用0.22 μm的滤器过滤后通过预先用Binding Buffer平衡处理的NTA-Ni2+柱,加样结束后分别用含20、50、100、250、500 mmol · L-1咪唑的Elution Buffer洗涤NTA-Ni2+柱,每个浓度洗涤6个柱体积,含目的蛋白的过柱洗脱液用0.02 mol · L-1 PB 4 ℃透析过夜,SDS-PAGE电泳检测。
1.6 Western blotting验证将S.melliferum CH-1中克隆表达出的几丁质脱乙酰酶蛋白超声破碎的粗酶液及纯化后的滤过液用于SDS-PAGE和Western blotting验证,以抗His标签鼠单克隆抗体为一抗,以羊抗鼠IgG单克隆抗体为二抗,进一步确认经NTA-Ni2+柱洗脱下的蛋白为目的蛋白。
1.7 几丁质脱乙酰酶活力测定 1.7.1 蛋白质含量的测定采用Bradford方法[15]测定蛋白质含量,以牛血清蛋白(BSA)作为标准蛋白。
1.7.2 对硝基苯胺标准曲线的绘制及酶活力的测定参考刘丽萍等[16]的检测方法测定CDA蛋白样品的酶活力,酶活力单位定义为每小时产生1 μg对硝基苯胺所需要的酶量。酶活力计算公式为:酶活力(U · mL-1)=[(A400-A0)×酶液稀释倍数]/kT 。其中:A400为S.melliferumCH-1 CDA蛋白样品的吸光值;A0为对照样品(高温灭活)的吸光值;T为酶促反应时间(min);k为线性系数0.078 1。
1.7.3 酶的最适反应温度及温度稳定性测定分别设置6个温度梯度:30、35、40、45、50、55和60 ℃,按酶促反应体系加样测定其活力,每个温度3个平行,以酶活力最高为100%,绘制温度与酶活力的曲线。稳定性测定为取1 mL适当浓度酶液于各个梯度温度下预先温浴30 min,然后按酶促反应体系加样测定其活力,以不预温酶活力为100%,绘制不同温度对酶活力的曲线。
1.7.4 酶的最适pH值与pH值稳定性测定配置pH值分别为5、5.5、6、6.5、7、7.5的50 mmol · L-1的磷酸盐缓冲液和pH值为8、8.5的50 mmol · L-1的Tris-HCl缓冲液。按酶促反应体系加样测定其活力,每个pH值3个平行,以酶活力最高为100%,绘制pH值与酶活力的曲线。pH值稳定性测定时取适当浓度酶液0.5 mL,再加入各种pH值的Tris-HCl缓冲液3.5 mL,最适温度下保持30 min,之后分别用NaOH或HCl调节pH值到7.5,其余同上。以不调pH处理的酶活力为100%,绘制不同pH值对酶活力的曲线。
2 结果与分析 2.1 几丁质脱乙酰酶基因编码序列比对分析从S.melliferum CH-1全基因组序列精细图中扩增出672 bp的chid基因(GenBank登录号:KT891987)片段,完成定点突变后将chid基因翻译成一个完整的蛋白质氨基酸序列,利用tBLASTx工具(http://www.ncbi.nlm.gov/BLAST)进行比对。结果表明:S.melliferum CH-1中的几丁质脱乙酰酶与其他细菌几丁质脱乙酰酶具有较高相似性,同S.melliferum KC3/BC3/IPMB4A中的同源性最高达97%,尤其位于20~95氨基酸之间趋于保守。这可能是重要的功能域,分别包括3个保守的Motif:TFDDGP、KATFF、IGNH(图 1)。
 | 图 1 24种细菌几丁质脱乙酰酶氨基酸序列多重比对 Fig. 1 Multiple sequence aligment of chitin deacetylase from 24 bacteria |
琼脂糖凝胶电泳显示,成功克隆到617 bp的片段chid-U和100 bp的片段chid-D以及含酶切位点BamHⅠ和XhoⅠ的690 bp的chid片段全长(图 2)。将chid基因PCR产物通过琼脂糖凝胶回收试剂盒纯化后送华大基因测序验证,获得了正确定点突变的基因。后将该基因经限制性内切酶BamHⅠ和XhoⅠ双酶切克隆到pET-28a载体上,挑选转化子以T7、T7 terminator为引物进行菌液PCR验证,阳性克隆能扩增出690 bp左右大小的目的条带。
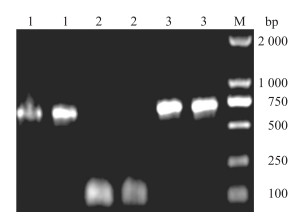 |
图 2 重叠延伸PCR扩增chid基因
Fig. 2 Overlap extension PCR of chid gene
M.DNA marker;1.含突变位点的上游片段chid-U;2.含突变位点的下游片段chid-D;3.重叠延伸PCR定点突变后的chid基因。 M.DNA marker;1.Upstream segment chid-U with mutation site;2.Downstream segment chid-D with mutation site;3.Overlap extension PCR of chid gene after site-directed mutagenesis. |
SDS-PAGE电泳检测表明:BLchid菌株经IPTG诱导后能体外完全表达CDA蛋白,相对分子质量约为28×103,且表达目的条带清晰,作为阳性对照的不完全表达CDA蛋白相对分子质量约为26×103,均与预期理论值一致(图 3-A)。将经细胞超声破碎离心收集的上清液和标记为包涵体的沉淀分别进行SDS-PAGE检测,结果显示目的蛋白在上清液和沉淀中都有分布,但大部分在上清液中,为有酶活性的可溶性蛋白(图 3-B)。上清液用0.22 μm的滤器过滤后通过NTA-Ni2+柱纯化,用不同浓度咪唑洗脱NTA-Ni2+柱,收集柱后液进行SDS-PAGE检测,发现大部分目的蛋白能被250 mmol · L-1的咪唑洗脱(图 3-C)。
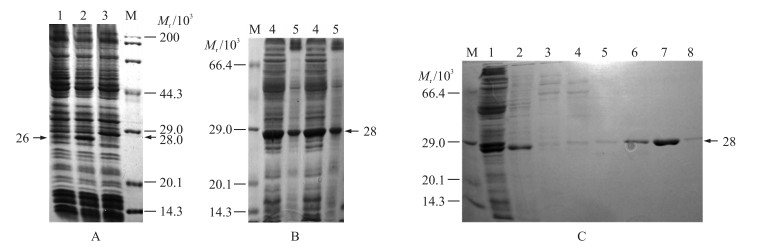 |
图 3 几丁质脱乙酰酶重组蛋白的SDS-PAGE分析
Fig. 3 Analysis of purification recombination CDA proteins by SDS-PAGE
A:1.不加IPTG诱导的CDA总蛋白;2.IPTG诱导后的不完全表达的CDA总蛋白;3.IPTG诱导后的完全表达的CDA总蛋白。B:4.CDA蛋白上清液;5.CDA蛋白沉淀。C:1.CDA蛋白上清液;2.20 mmol · L-1咪唑洗脱纯化后的CDA蛋白;3.50 mmol · L-1咪唑洗脱纯化后的CDA蛋白;4、5.100 mmol · L-1咪唑洗脱纯化后的CDA蛋白;6、7.250 mmol · L-1咪唑洗脱纯化后的CDA蛋白;8.500 mmol · L-1咪唑洗脱纯化后的CDA蛋白。M.蛋白marker A:1.Total CDA protein not induced by IPTG;2.Incomplete expression CDA protein induced by IPTG;3.Complete expression CDA protein induced by IPTG. B:4.Supernatant of CDA protein;5.Precipitation of CDA protein. C:1.Supernatant of CDA protein;2.Purified CDA protein eluted with 20 mmol · L-1 iminazole;3.Purified CDA protein eluted with 50 mmol · L-1 iminazole;4,5.Purified CDA protein eluted with 100 mmol · L-1 iminazole;6,7.Purified CDA protein eluted with 250 mmol · L-1 iminazole;8.Purified CDA protein eluted with 500 mmol · L-1 iminazole. |
利用Western blotting技术对BLchid菌株中克隆表达出的S.melliferum CH-1几丁质脱乙酰酶蛋白进一步进行特异性检测,将超声破碎的粗酶液及纯化后的滤过液分别进行SDS-PAGE检测。超声破碎后的内含物中含有其他可被His标签检测到的杂蛋白,但经NTA-Ni2+柱洗脱纯化后只有单一的目的蛋白条带(图 4-A),进一步确认经NTA-Ni2+柱洗脱下的蛋白为目的蛋白(图 4-B)。
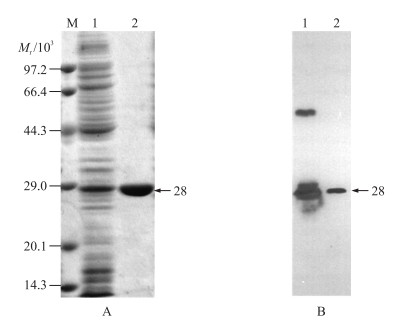 |
图 4 几丁质脱乙酰酶重组蛋白的Western blotting分析
Fig. 4 Analysis of purification recombination CDA proteins by Western blotting
A:几丁质脱乙酰酶重组蛋白SDS-PAGE分析(M.蛋白marker;1.CDA蛋白上清液;2.纯化后的CDA蛋白);B:几丁质脱乙酰酶重组蛋白Western blotting分析(1.CDA蛋白上清液;2.纯化后的CDA蛋白) A:Analysis of purification recombination CDA proteins by SDS-PAGE(M.Marker;1.Supernatant of CDA protein;2.Purified CDA protein);B:Analysis of purification recombination CDA proteins by Western blotting(1.Supernatant of CDA protein;2.Purified CDA protein) |
为了研究并确认S.melliferum CH-1 CDA蛋白的脱乙酰化功能,在釆用大肠杆菌原核表达系统来表达CDA重组蛋白后,期望能够测定到CDA重组蛋白的酶活力。根据上述几丁质脱乙酰酶活力单位定义以及酶活力计算公式,最终测得粗纯化CDA重组蛋白样品的酶活力约为10.14 U · mL-1。
2.5.2 几丁质脱乙酰酶的最适反应温度与温度稳定性测定由图 5可知:在不同温度梯度下酶的最适温度为50 ℃;50 ℃以下随着温度的升高酶活力随之增大,温度高于50 ℃时,酶活力有所下降,但仍高于45 ℃时的相对酶活力。该酶热稳定性较好,各个温度梯度对该酶处理30 min后,在35~60 ℃之间酶活力仍能保持60%以上,50 ℃最高酶活力能保持在80%左右。
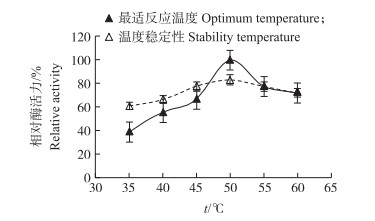 | 图 5 温度对几丁质脱乙酰酶活力的影响 Fig. 5 Effect of temperature on activity of chitin deacetylase |
由图 6可知:用不同pH值的缓冲液测定几丁质脱乙酰酶活力,在pH值为7.5时酶活力最高,并且是一种较耐碱性的酶,pH值在7.0~8.5之间酶活力可保持在60%以上,pH值在5.0~6.5只有20%~40%酶活力。几丁质脱乙酰酶的pH值稳定性不高,经不同pH缓冲液处理后酶活力普遍下降,在最适7.5时最高可保持60%左右活力,pH值在小于5和大于8.5时几乎检测不到酶活力。
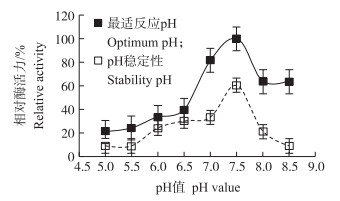 |
图 6 pH值对几丁质脱乙酰酶活力的影响
Fig. 6 Effect of pH value on activity of chitin deacetylase
所用缓冲溶液分别为磷酸盐缓冲液(pH5~7.5)和Tris-HCl缓冲液(pH8~8.5)。 Solution buffer used is phosphate buffer(pH5-7.5)and Tris-HCl buffer(pH8-8.5),respectively. |
Spiroplasma melliferum是蜜蜂“爬蜂病”的病原之一,Alexeev等[9]和本研究组在分析蜜蜂螺原体(S.melliferum)基因组时都发现有几丁质酶基因和几丁质脱乙酰酶基因,而系统发育学关系十分接近的其他几种昆虫非致病螺原体(如S.citri,S.kunkelli)中并没有,这2个基因也被认为与致病性直接相关。因此,研究几丁质脱乙酰酶基因对进一步揭示蜜蜂螺原体致病机制及螺原体与宿主蜜蜂的相互作用具有重要意义。本文构建了pETchid原核表达载体,在大肠杆菌中成功表达了几丁质脱乙酰酶基因chid,测得其酶活力高达10.14 U · mL-1,暗示S.melliferum CDA蛋白在宿主体内围食膜上能够行使去乙酰化的功能,为明确chid基因的功能提供重要依据。由于密码子TGA在一般生物中是终止密码子,而在螺原体中编码色氨酸,因此本研究中利用一种经济高效的定点突变方法overlap extension PCR(OE-PCR)实现螺原体基因在大肠杆菌中完整外源表达。另外,研究中设置一组BLchid菌株不用IPTG诱导表达目的蛋白作为阴性对照,另一组BLchid菌株不经过TGA密码子的定点突变,诱导表达出相对分子质量为26×103左右的蛋白作为阳性对照,其相对分子质量小于目的蛋白的相对分子质量(28×103),进一步验证了柔膜菌纲螺原体基因组的特殊性。
目前,螺原体几丁质脱乙酰酶和几丁质酶的研究报道较少,但在其他微生物中这2种酶都有不少研究。黄惠莉等[17]从海洋泥土中分离出产几丁质脱乙酰酶的产碱属芽孢杆菌并对其活性和酶学性质进行了相关研究,发现该酶在最适条件下酶活力为2.25 U · mL-1,酶解方式为外切酶型,最适温度为40~50 ℃,最适pH值为4.5~5.0,金属离子Mg2+对酶活有激活作用。本研究中通过大肠杆菌原核表达系统表达出几丁质脱乙酰酶蛋白,通过改良过的紫外分光光度法测定其活力和基本性质,与其比较,螺原体S.melliferum CH-1中几丁质脱乙酰酶在体外最适温度为50 ℃,在35~45 ℃之间能保持40%以上活力。Bonoan等[18]研究认为正常情况下蜂群能调节蜂巢温度在32~36 ℃之间。蜜蜂爬蜂病高发于春秋季,梅雨天气更甚,患病蜂聚集在蜂巢从而使蜂蜱温度升高,蜜蜂螺原体几丁质脱乙酰酶活力增强,使得螺原体对宿主蜜蜂的侵染能力增强,因此在蜜蜂“爬蜂病”防治过程中应及时清理出巢蜱中的死蜂。根据最适pH值,可以将几丁质脱乙酰酶分为酸性、中性和碱性,在pH值为7.5时酶活力最高,pH7.0~8.5之间酶活力可保持在60%以上,说明蜜蜂螺原体几丁质脱乙酰酶属于碱性几丁质脱乙酰酶,对蜜蜂危害较大。另外,有资料显示蜜蜂中肠pH值为7.5,有利于保持该酶最大活性。
螺原体的成功侵染需要通过昆虫的中肠屏障到达淋巴组织或血腔,并在其中大量繁殖,或者侵入唾液腺并在唾液管中释放。Lo等[8]发现昆虫致病性菌S.melliferum含有额外的涉及到能利用几丁质和N-乙酰胞壁酸有关的基因(例如:chiA、nagE、murP),降解几丁质的能力有助于螺原体侵入宿主组织(例如:透过几丁质基体间质,肠上皮细胞或几丁质外壳)。刘朋虎[19]研究了高产几丁质酶的蜜蜂球囊菌(Ascosphaera apis),分离纯化了其几丁质酶,该酶最适温度为40 ℃,最适pH值为7.5,也说明几丁质酶与蜜蜂球囊菌的致病性有关。研究表明微量的几丁质脱乙酰酶能有效阻止围食膜形成或者造成穿孔,破坏中肠细胞抵御微生物入侵的第一道屏障。几丁质酶和几丁质脱乙酰酶在蜜蜂螺原体中可能的作用方式为:第一,螺原体可以利用蜜蜂肠道几丁质为底物,转化为更利于自身利用的碳源以加强对蜜蜂肠道内环境的适应性;第二,利用几丁质与几丁质酶及几丁质脱乙酰酶的相互作用,螺原体可能黏附在蜜蜂肠道细胞为侵入细胞寻找有利条件;第三,这2种酶可能会改变蜜蜂肠道内围食膜的理化性质有利于螺原体的侵染[10]。我国在动物支原体(mycoplasma)和植原体(phytoplasma)已有较深入的研究,对于同属柔膜菌纲的导致中华绒螯蟹颤抖病的螺原体S.eriocheiris也取得突破性进展[5],但是对于蜜蜂螺原体S.melliferum的致病机制的研究很少。由于螺原体基因敲除等遗传操作系统在国内外尚不成熟,并且进行螺原体几丁质脱乙酰酶基因在蜜蜂体内的功能研究还存在一定困难,后续研究可尝试通过同源重组或转座子随机插入突变等方法获得该基因突变体,进一步确认其功能。本研究为后续确定该基因在蜜蜂螺原体致病过程中的作用及酶的结构与功能的关系奠定了基础。
本文中重组质粒pETchid的构建及Western blotting技术得到南京农业大学生命科学学院梁永恒教授指导,谨致谢意。
| [1] | Gasparich G E. Spiroplasmas and phytoplasmas:microbes associated with plant hosts[J]. Biologicals,2010,38(2):193-203. |
| [2] | Regassa L B,Gasparich G E. Spiroplasmas:evolutionary relationships and biodiversity[J]. Frontiers in Bioscience,2006,11:2983-3002. |
| [3] | Gasparich G E,Whitcomb R F,Dodge D,et al. The genus Spiroplasma and its non-helical descendants:phylogenetic classification,correlation with phenotype and roots of the Mycoplasma mycoides clade[J]. International Journal of Systematic and Evolutionary Microbiology,2004,54(3):893-918. |
| [4] | Wu M,Eisen J A. A simple,fast,and accurate method of phylogenomic inference[J]. Genome Biology,2008,9(10):151. |
| [5] | Wang W,Gu W,Gasparich G E,et al. Spiroplasma eriocheiris sp. nov.,associated with mortality in the Chinese mitten crab,Eriocheir sinensis[J]. International Journal of Systematic and Evolutionary Microbiology,2011,61(4):703-708. |
| [6] | Clark T,Whitcomb R,Tully J,et al. Spiroplasma melliferum,a new species from the honeybee(Apis mellifera)[J]. International Journal of Systematic Bacteriology,1985,35(3):296-308. |
| [7] | Chen Y X,Xue B D,Guo Y H. Studies on characteristics of the honey-bee spiroplasma in China[J]. Science in China Series B,1988,31(9):815-820. |
| [8] | Lo W S,Chen L L,Chung W C,et al. Comparative genome analysis of Spiroplasma melliferum IPMB4A,a honeybee-associated bacterium[J]. BMC Genomics,2013,14(1):22. |
| [9] | Alexeev D,Kostrjukova E,Aliper A,et al. Application of Spiroplasma melliferum proteogenomic profiling for the discovery of virulence factors and pathogenicity mechanisms in host-associated spiroplasmas[J]. Journal of Proteome Research,2011,11(1):224-236. |
| [10] | 俞徐斌. 牛虻和家蝇螺原体的生物学特性及蜜蜂螺原体致病相关因子的探索[D]. 南京:南京农业大学,2013. Yu X B. The biological characteristics of spiroplasma isolated from gadfly and searching for pathogenic related factors of Spiroplasma melliferum[D]. Nanjing:Nanjing Agricultural University,2013(in Chinese with English abstract). |
| [11] | Merzendorfer H,Zimoch L. Chitin metabolism in insects:structure,function and regulation of chitin synthases and chitinases[J]. Journal of Experimental Biology,2003,206(24):4393-4412. |
| [12] | Dixit R,Arakane Y,Specht C A,et al. Domain organization and phylogenetic analysis of proteins from the chitin deacetylase gene family of Tribolium castaneum and three other species of insects[J]. Insect Biochemistry and Molecular Biology,2008,38(4):440-451. |
| [13] | Citti C,Marechal-Drouard L,Saillard C,et al. Spiroplasma citri UGG and UGA tryptophan codons:sequence of the two tryptophanyl-tRNAs and organization of the corresponding genes[J]. Journal of Bacteriology,1992,174(20):6471-6478. |
| [14] | 阮康勤,于汉寿,张晶,等. 蜜蜂螺原体南京分离株M10形态的多样性[J]. 南京农业大学学报,2007,30(3):58-62.DOI:10.7685/j.issn.1000-2030.2007.03.011. Ruan K Q,Yu H S,Zhang J,et al. Morphological polymorophy of sprioplasmas isolated from honeybee in Nanjing[J]. Journal of Nanjing Agricultural University,2007,30(3):58-62(in Chinese with English abstract). |
| [15] | 叶伟民,韩焕兴,范列英,等. Bradford比色法简便、快速测定微量蛋白[J]. 上海医学检验杂志,1996,11(4):207-208. Ye W M,Han H X,Fan L Y,et al. Bradford colorimetric method is simple,rapid determination of trace proteins[J]. Shanghai Journal of Medical Test,1996,11(4):207-208(in Chinese with English abstract). |
| [16] | 刘丽萍,赵祥颖,刘建军,等. 一种简易,高效产几丁质脱乙酰酶菌种的筛选方法[J]. 食品与发酵工业,2008,34(1):65-68. Liu L P,Zhao X Y,Liu J J,et al. A simple and rapid method for screening chitin deacetylase producing strains[J]. Food and Fermentation Industries,2008,34(1):65-68(in Chinese with English abstract). |
| [17] | 黄惠莉,叶存印,姚云艳. 枯草芽胞杆菌甲壳素脱乙酰酶的筛选及酶学性质[J]. 微生物学通报,2004,31(5):33-37. Huang H L,Ye C Y,Yao Y Y. Screening and properties of chitin deacetylase from Bacillus subtilis[J]. Microbiology China,2004,31(5):33-37(in Chinese with English abstract). |
| [18] | Bonoan R E,Goldman R R,Wong P Y,et al. Vasculature of the hive:heat dissipation in the honey bee(Apis mellifera)hive[J]. Naturwissenschaften,2014,101(6):459-465. |
| [19] | 刘朋虎. 蜜蜂球囊菌几丁质酶纯化及酶学性质的研究[D]. 福州:福建农林大学,2007. Liu P H. Study on purification and properties of chitinase from Ascophaera apis[D]. Fuzhou:Fujian Agriculture and Forestry University,2007(in Chinese with English abstract). |




