文章信息
- 崔红米, 曹学伟, 王建军, 熊爱生, 侯喜林, 李英. 2016.
- CUI Hongmi, CAO Xuewei, WANG Jianjun, XIONG Aisheng, HOU Xilin, LI Ying. 2016.
- 外源GR24对不结球白菜腋芽生长的影响
- Effects of exogenous GR24 on the growth of axillary bud of non-heading Chinese cabbage
- 南京农业大学学报, 39(3): 366-372
- Journal of Nanjing Agricultural University, 39(3): 366-372.
- http://dx.doi.org/10.7685/jnau.201510023
-
文章历史
- 收稿日期:2015-10-17
独脚金内酯(strigolactones,SLs)是一种产生于植物根部的类胡萝卜衍生物,最早是作为寄生植物种子萌发刺激物而发现。近期研究发现,该类化合物能够抑制植物的分枝,是继生长素和细胞分裂素之后发现的调控植物分枝的新型植物激素[1, 2, 3]。GR24为独脚金内酯的人工类似物,现已应用于水稻、豌豆、拟南芥和矮牵牛等多分蘖/分枝突变体的研究中[4, 5, 6]。研究表明,低浓度的GR24能够使独脚金内酯合成缺失突变体恢复其野生型的表型,对于独脚金内酯信号途径缺失突变体却没有作用[4, 5, 6, 7, 8, 9, 10, 11]。同时,一定浓度的GR24能够抑制野生型植株分蘖/分枝的生长[11, 12, 13]。例如,100 nmol·L-1的GR24严重抑制豌豆SLs合成缺失突变体ccd8腋芽的生长,对豌豆SLs信号途径缺失突变体rms 4 的腋芽生长却没有作用[7];1 μmol·L-1的GR24能够完全抑制水稻SLs合成缺失突变体d10和d17 的生长,而对水稻SLs信号途径缺失突变体d3却没有作用[11];低浓度的GR24(1 μmol·L-1)不能影响野生型水稻分蘖芽的生长,而高浓度的GR24(10 μmol·L-1)能够明显抑制野生型水稻分蘖芽的生长[11]。
不结球白菜(Brassica campestris ssp.chinensis Makino)是十字花科芸薹属植物,俗称青菜、小白菜、油菜(北方)[14],在中国南方栽培广泛。不结球白菜的大部分品种不分蘖/分枝,但也有少数品种呈分蘖/分枝状,如‘如皋毛菜’和‘南通马耳头’[15]。分蘖/分枝影响不结球白菜的株型,进而影响其产量和品质等重要农艺性状。研究表明:分蘖/分枝的形成仅受基因型的控制,而分蘖/分枝的生长发育受到基因、环境和激素的共同调控,这些因素之间相互作用形成复杂的调控网络,共同调控腋芽的生长[16]。生长素通过顶端优势的作用间接抑制分蘖/分枝,细胞分裂素和独脚金内酯分别直接促进和抑制分蘖/分枝[17]。BRC 1/TB1 被认为是作为植物激素与环境信号互作的集成器来调控植物分枝发育,它编码TCP家族转录因子,在腋芽特异表达,其功能缺失突变体会产生更多的分枝[16]。MAX 2是独脚金内脂响应途径上的基因,位于BRC1/TB1 的下游,外源独脚金内酯类似物不能恢复其突变体的表型[18]。水稻中LOG能够编码一种新的细胞分裂素激活酶,能够催化细胞分裂素合成途径的最后一步[19]。拟南芥sps突变体分枝数大大增加,细胞分裂素含量是野生型植株的3~9倍,这说明SPS可能通过控制腋芽形成部位的细胞分裂素含量来抑制腋芽的生长[20]。SPL9抑制新叶的形成,spl9突变体分蘖/分枝数大大增加[21]。
不结球白菜分蘖/分枝的研究目前还处于起步阶段。因此,本研究采用不同浓度的外源GR24处理不结球白菜‘如皋毛菜’,调查其腋芽生长的动态变化,检测叶腋处细胞分裂素(Z+ZR)、生长素(IAA)含量和分蘖/分枝相关基因的表达量,以探究外源GR24对不结球白菜分蘖/分枝生长的影响机制,为激素调控不结球白菜分蘖/分枝生长的机制提供依据。
1 材料与方法 1.1 材料与外源GR24处理不结球白菜(Brassica campestris ssp.chinensis Makino)品种‘如皋毛菜’为南京农业大学白菜课题组保存材料。试验所用试剂GR24,购于北京大秦兴业科技有限公司。其余试剂均为分析纯。
不结球白菜播种穴盘,待4~5片真叶长出时,选取生长一致的幼苗,移栽到MS营养液中,气泵间断性通气,每周换1次营养液;11~12片真叶长出时,部分腋芽开始生长,将配好的一定量的GR24母液加入到MS营养液中(GR24母液先用少量的丙酮溶解后再用蒸馏水定容[22]),使其终浓度分别为0、1.5和4.5 μmol·L-1,对照加入与处理等量的丙酮。分别于GR24处理后0、3、6、12、24、36和48 h取腋芽(腋芽长度大于0.2 cm)及腋芽周围2 mm的植物组织,用于RNA提取(约0.1 g)和激素含量的测定(约1.0 g),-70 ℃保存备用。分别于处理后0、3、6、9、12和15 d测量‘如皋毛菜’从外到里每个叶片叶腋处腋芽的长度,并统计活动芽数和活动芽总长度。每个处理3次重复。
1.2 激素含量的测定叶腋处的Z+ZR和IAA含量参照刘旭[23]的方法并适当改动。将样品(1.00 g左右)放到预冷的研钵中,加入5 mL预冷的50%甲醇溶液(体积分数),冰浴研磨成浆;4 ℃下浸提12 h,10 000 r·min-1离心10 min,取上清液保存于4 ℃冰箱中;残渣加入预冷的50%甲醇溶液3 mL重复浸提2次,间隔12 h,离心同上,收集合并全部浸提液;向提取液中加入0.2 g PVPP吸附酚类物质及色素,在摇床上4 ℃振荡60 min,摇匀,离心同上;将上清液缓慢过C18小柱,流出液倒入50 mL小烧杯中进行冷冻干燥;冻干样品用2.5 mL预冷的50%甲醇溶液溶解,过0.22 μm的有机系超微滤膜,用于测定激素含量。超高效液相色谱(UPLC)仪为Agilent 1290 Infinity系统,色谱条件为:流动相为0.6%乙酸(体积分数)和色谱级甲醇梯度洗脱(表 1),柱温35 ℃,进样量2 μL,流速0.3 mL·min-1,检测波长为254 nm。
| t/min | V(甲醇):V(0.6%乙酸)V(Methanol):V(0.6% acetic acid) |
| 0 | 10:90 |
| 2 | 10:90 |
| 7 | 50:50 |
| 9 | 50:50 |
| 9.1 | 10:90 |
| 12 | 10:90 |
叶腋处RNA的具体提取方法参照植物RNA提取试剂盒说明书(TianGen公司)。按照PrimeScript RT试剂盒说明书(TaKaRa公司)将RNA反转录为cDNA。
实时定量PCR检测分蘖/分枝相关的5个基因表达量,引物采用Bioxm 2.7设计,内参基因为Actin,试验所用引物由南京金斯瑞生物公司合成,荧光引物信息序列见表 2。定量体系参照TaKaRa公司SYBR Premix Ex TaqTM试剂盒说明书。荧光定量PCR为美国应用生物系统公司的7500 Fast Real-Time PCR System。PCR程序采用两步法:95 ℃ 30 s;95 ℃ 3 s,60 ℃ 30 s,40个循环;设置60 ℃到95 ℃的熔解曲线。
| 基因名称Gene name | 引物对名称Primer name | 序列(5′→3′)Sequence |
| BRC1(BRANCHED 1) | q-BRC1 | AGAGAAGACGACCACAAGT/AAGTAGTCCAATTAACACCAGA |
| MAX2(MORE AXILLARY GROWTH 2) | q-MAX2 | GATGATGGTGATGATGAT/TAGGTAGTGGTGTTAGAA |
| LOG1(LONELY GUY Cytokinin-Activating Enzymes 1) | q-LOG1 | GGACTATTGAATGTGGAAGGATA/CGAGCAGTTGGTGTAATGA |
| SPS(SUPERSHOOT) | q-SPS | AGGAACTTACAACGGAACA/TATCACTCTCATCTAACACATCA |
| SPL9(SBP-box genes) | q-SPL9 | AGTGGAGGGCTCATGTTTGG/TTCCACGTACCCTTCTGTTTGA |
| Actin | q-Actin | GTTGCTATCCAGGCTGTTCT/AGCGTGAGGAAGAGCATAAC |
向营养液中加入GR24母液,使其终浓度分别为0、1.5和4.5 μmol·L-1,对照加入与处理等量的丙酮,每3 d换1次营养液并加入相应量的GR24母液。分别于处理后0、3、6、9、12和15 d统计单株活动芽的个数,并用直尺测量活动芽的长度,每处理10株,3次重复。
1.5 数据分析和处理数据采用Excel 2003和SPSS 17.0进行统计处理和单因素方差分析(One-way ANOVA),组间比较用Duncan′s检验。荧光定量PCR数据采用2-ΔΔCT进行计算分析。
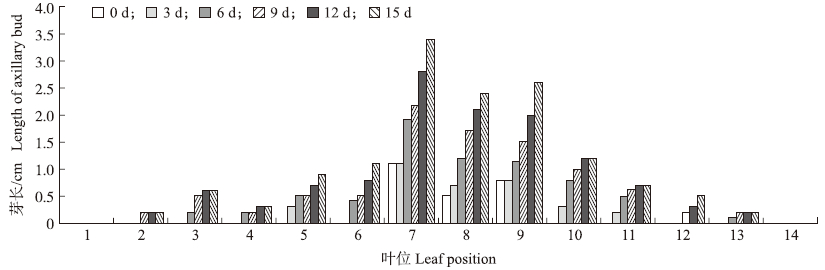
2 结果与分析 2.1 外源GR24对不结球白菜‘如皋毛菜’腋芽生长的影响 2.1.1 不结球白菜‘如皋毛菜’腋芽生长的动态调查‘如皋毛菜’长到约8片真叶时,腋芽形成,几乎每个叶片的叶腋内都有腋芽长出;长到11~12片真叶时,腋芽开始萌动。由图 1可知:当腋芽长度大于0.2 cm时,腋芽开始迅速伸长,而小于0.2 cm的腋芽,处于基本不伸长或休眠状态,因而将大于0.2 cm的腋芽定义为活动芽,小于或等于0.2 cm的腋芽定义为休眠芽。位于中间叶位的腋芽最先开始萌动,而最里面和最外面的腋芽生长比较晚或基本不生长。
|
图 1 不结球白菜每叶腋处腋芽长度
Fig. 1 Axillary bud length per leaf axil of non-heading Chinese cabbage
1~14按照叶片长出的先后顺序编号,1表示最外侧先长出真叶的叶位,14表示植株最内侧的叶位。 1-14 are the sequence number in accordance with the leaves,1 shows the leaf position which grow true leaf firstly,and 14 shows the leaf position which grow true leaf lastly. |
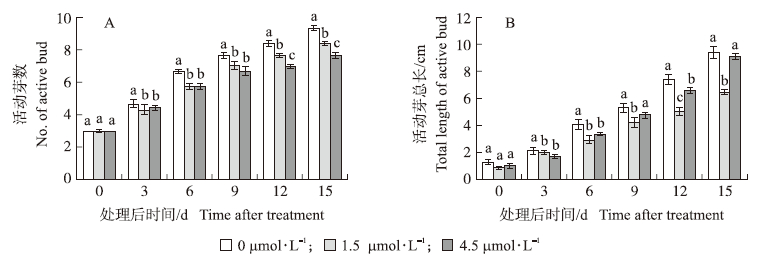
如图 2-A所示:与对照相比,外源GR24处理后3 d开始,活动芽的个数显著减少(P<0.05);且12 d以后,4.5 μmol·L-1 GR24处理的活动芽数比1.5 μmol·L-1 GR24处理显著减少;处理15 d后,1.5 μmol·L-1 GR24处理的活动芽个数比对照减少11%,4.5 μmol·L-1 GR24处理比对照活动芽个数减少18%。表明外源GR24能够抑制休眠芽的萌发,且随着处理时间的延长高浓度比低浓度对休眠芽萌发的抑制作用更为明显。从图 2-B可以看出:与对照相比,处理后3 d,外源GR24就开始明显抑制腋芽的伸长,且总体来看,低浓度的GR24比高浓度的GR24更能抑制腋芽的伸长,这说明低浓度的GR24比高浓度的GR24对腋芽伸长的抑制作用更为明显。这可能是随着GR24浓度的升高,GR24分子的有效性对活动芽丧失[22]。
|
图 2 外源GR24对不结球白菜活动芽数(A)和活动芽总长(B)的影响
Fig. 2 Effects of exogenous GR24 on the number(A)and the total length(B)of active buds in non-heading Chinese cabbage
不同小写字母表示同一时间不同处理间差异显著(P<0.05)。 Different small letters indicate significant difference between different treatments at the same time at 0.05 level. The same as follows. |
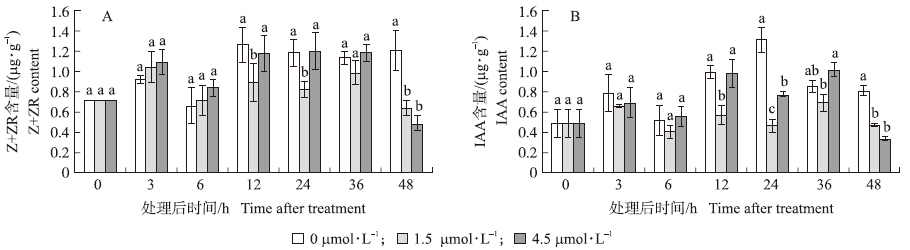
由图 3-A可见:1.5 μmol·L-1 GR24处理后12 h,叶腋内的Z+ZR含量比对照显著降低,到48 h时,比对照降低33%;而4.5 μmol·L-1 GR24处理后48 h,叶腋内的Z+ZR含量显著低于对照,比对照低49%。这说明,在降低叶腋处Z+ZR含量时,低浓度的GR24比高浓度的GR24发挥作用更早。
|
图 3 外源GR24对不结球白菜叶腋内Z+ZR(A)和IAA(B)含量的影响 Fig. 3 Effects of exogenous GR24 on the contents of Z+ZR(A)and IAA(B)in non-heading Chinese cabbage leaf axil |
由图 3-B可见:1.5 μmol·L-1的GR24处理后12 h开始,叶腋内的IAA含量比对照显著降低,到48 h时,叶腋内的IAA含量比对照低42%;4.5 μmol·L-1 GR24处理后24 h开始,叶腋内的IAA含量较对照有明显的降低,48 h时,比对照低48%。这说明外源GR24可能降低了IAA从源到库的运输能力,且低浓度的GR24的作用更为显著。
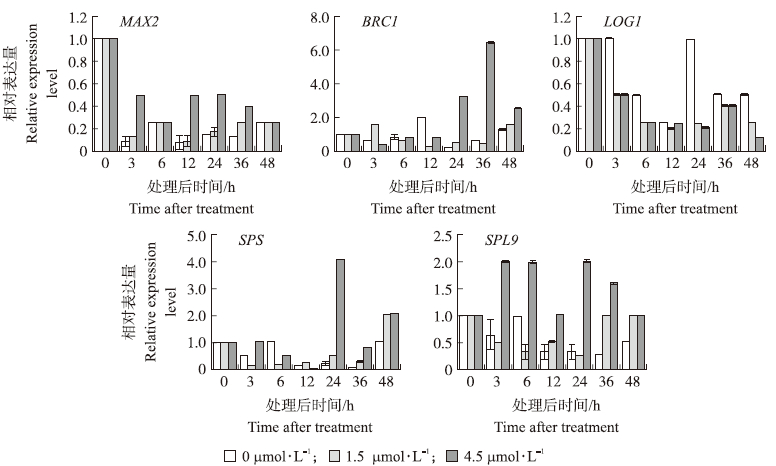
2.3 外源GR24对不结球白菜‘如皋毛菜’分蘖/分枝相关基因表达的影响由图 4可见:4.5 μmol·L-1 GR24处理后MAX 2基因的表达量快速下降,到6 h时降到最低,12 h时逐渐回升,36~48 h又逐渐降低;1.5 μmol·L-1 GR24处理和对照的MAX 2表达量在处理后3 h快速下降,之后变化平缓。4.5 μmol·L-1 GR24处理后3 h时,MAX 2的表达量比对照有明显的升高趋势,而处理后 48 h,MAX 2 的表达量与对照没有明显的区别;1.5 μmol·L-1的GR24处理后3 h,MAX 2 的表达量较对照升高,但没有高浓度的升高作用明显,48 h后,MAX 2的表达量与对照没有明显的区别。说明GR24施加到根部后,很快由根部运输到腋芽发挥其作用,且腋芽对高浓度的GR24的响应更为明显。4.5 μmol·L-1 GR24处理后24 h,BRC 1基因的表达量开始显著升高,36 h时升到最高,48 h又回降;1.5 μmol·L-1 GR24处理后BRC 1基因的表达量先升后降,12 h时降至最低,48 h又快速升高;对照的BRC 1基因表达量变化规律不明显。4.5和1.5 μmol·L-1 GR24处理后24 h开始,BRC 1基因的表达量均比对照有明显的升高,但4.5 μmol·L-1 GR24处理效果更明显。说明高浓度的GR24比低浓度对叶腋处BRC 1基因表达量的影响更为明显。
|
图 4 外源GR24对不结球白菜叶腋内分蘖相关基因表达的影响 Fig. 4 Effects of exogenous GR24 on the relative expression of branching related gene in non-heading Chinese cabbage leaf axil |
由图 4可见:4.5和1.5 μmol·L-1 GR24处理后,LOG 1基因表达量显著降低,48 h 时,4.5 μmol·L-1 GR24处理LOG 1基因的表达量显著低于1.5 μmol·L-1 GR24处理;对照LOG 1基因的表达量先降后升,之后再降并趋于平稳。GR24处理后3 h开始,叶腋处的LOG 1表达量显著低于对照,处理后24 h开始,4.5 μmol·L-1 GR24处理LOG 1的表达量低于1.5 μmol·L-1 GR24处理,说明由根部运输到腋芽内的GR24可以抑制腋芽内的LOG 1表达,且随着时间的延长,高浓度的抑制作用更为明显。
4.5 μmol·L-1 GR24处理后6 h,SPS基因的表达量降低,12 h时降至最低,24 h时迅速升至最高,之后回降;1.5 μmol·L-1 GR24处理后3 h,SPS表达量迅速降至最低,24 h时开始回升,并至48 h时升到最高;对照的SPS表达量变化趋势与1.5 μmol·L-1 GR24处理基本一致(图 4)。外源GR24处理后24 h开始,SPS表达量较对照升高,且4.5 μmol·L-1 GR24处理比1.5 μmol·L-1 GR24处理升高的更为明显。4.5 μmol·L-1 GR24处理后3 h,SPL 9基因的表达量迅速升高,12 h时回降,之后又升高,24~48 h又逐渐下降;1.5 μmol·L-1 GR24处理后,SPL 9表达量0~6 h呈下降趋势,6~24 h变化不大,36 h时又开始升高,之后趋于稳定;对照的SPL 9表达量12 h时开始下降,之后趋于平稳。4.5 μmol·L-1的GR24处理后3 h,SPL 9表达量较对照有明显的升高,1.5 μmol·L-1 GR24处理后12 h,SPL 9表达量较对照升高,且高浓度的升高作用更为明显。总体来看,高浓度的GR24处理比低浓度的GR24处理对SPL 9基因表达量的影响更大。
3 讨论与结论分蘖/分枝影响不结球白菜的株型,进而影响其产量和品质等重要农艺性状。分蘖/分枝的生长发育,可以分为腋芽的形成和腋芽的生长两个阶段。对分蘖/分枝生长影响最大的3种激素是生长素(IAA)、细胞分裂素(CTK)和独脚金内酯(SLs),这3种激素之间相互影响,共同调控分蘖/分枝的生长[24]。独脚金内酯作为一种新型的植物激素,受到了研究者的广泛重视,随着越来越多分蘖/分枝相关突变体的发现和研究,植物体内独脚金内酯合成和信号途径以及独脚金内酯与其他信号共同调控植物分蘖/分枝的网络,越来越清晰。
本研究结果表明:外源GR24能够抑制不结球白菜腋芽的萌发,且高浓度的GR24抑制作用更为明显;外源GR24能够抑制活动芽的伸长,且低浓度比高浓度的GR24的作用更为明显。Xu等[13]对水稻根部施用一定浓度的外源GR24(2 μmol·L-1)发现能够完全抑制水稻腋芽的生长;王玫等[12]对一串红腋芽处施用外源GR24的研究结果表明:GR24能够抑制一串红侧枝的伸长,且浓度越高,抑制作用越为明显,本研究结果与之相一致。
关于独脚金内酯与生长素和细胞分裂素相互作用的调控网络,研究者们做了大量的研究,也提出了各种假说,其中最具代表性的是渠化模型和第二信使模型。渠化模型研究者认为SLs通过影响IAA的运输调控腋芽的生长:第二信使模型研究者认为,SLs和CTK作为IAA的第二信使直接进入到腋芽内促进或抑制腋芽的生长[17]。Xu等[13]研究表明:GR24不能明显降低水稻茎节内的细胞分裂素含量或细胞分裂素合成相关基因的表达,但是却能够显著降低水稻茎节内IAA的含量和IAA的运输能力。在本研究中,外源GR24处理后3 h,不结球白菜叶腋内的细胞分裂素合成基因LOG 1基因的表达量明显降低,且低浓度的外源GR24处理12 h后,不结球白菜叶腋处的Z+ZR含量显著降低,高浓度的GR24处理后48 h,不结球白菜叶腋处的Z+ZR含量明显降低,这说明由根部运输到叶腋处的GR24通过抑制细胞分裂素合成基因的表达来降低叶腋内细胞分裂素的含量,从而抑制腋芽的生长。外源GR24处理后,不结球白菜叶腋处的IAA含量显著降低,这说明外源GR24会降低叶腋处IAA的含量,可能是外源GR24降低了IAA从源到库的运输能力。本研究结果与Xu等[13]的研究结果相一致。
SLs作为一类抑制植物分枝发育的植物激素,可与IAA和CTK协同调控植物的分蘖/分枝生长[19],同时,SLs也可通过调控分蘖/分枝相关基因的表达来调控分蘖/分枝的生长。BRC 1作为植物激素与环境信号互作的集成器来调控植物分枝发育[19],GR24处理后野生型豌豆腋芽内PsBRC 1 的表达量升高[13],CTK能够降低PsBRC 1的表达量[19]。Minakuchi等[8]对于水稻的研究结果表明FC 1(BRC1 在水稻中的同源基因)位于SLs下游抑制腋芽的生长。Aguilar-Martínez 等[25]对拟南芥的研究也同样表明BRC 1位于MAX途径的下游。本研究结果表明:不结球白菜叶腋处MAX 2基因的表达量在GR24处理后3 h较对照明显升高,且处理浓度越高升高越显著;BRC 1的表达量在GR24处理后24 h才明显升高,且浓度越高升高越明显,这一结果说明在不结球白菜中BRC 1基因可能在独角金内酯途径的下游发挥作用,即GR24可能通过直接影响BRC 1基因的表达来抑制腋芽的生长。
Tantikanjana等[20]的研究表明,在拟南芥中SPS负调控腋生分生组织的形成和生长,sps突变体产生大量的腋芽,细胞分裂素含量升高了3~9倍,因而推测SPS基因通过调控腋芽内细胞分裂素的含量来控制腋芽的生长。本研究表明,GR24处理后24 h,叶腋内的SPS基因的表达量明显比对照升高,且浓度越高升高作用越明显,这说明在不结球白菜中,外源GR24可能通过提高叶腋处SPS基因的表达量来抑制腋芽的生长,但是关于SPS与其他信号之间的关系,还有待于进一步研究。Schwarz等[21]的研究表明SPL9抑制新叶的形成,SPL9功能缺失突变体分蘖/分枝数明显增加,同时SPL9受到miRNA156的调控。在本研究中,较高浓度的GR24(4.5 μmol·L-1)处理后3 h,腋芽内的SPL9的表达量较对照有明显的升高,低浓度的GR24(1.5 μmol·L-1)处理后12 h,腋芽内的SPL9的表达量较对照升高,而高浓度的GR24对腋芽内的GR24表达量的影响更为明显。这说明,GR24可以通过促进SPL9的表达来抑制腋芽的生长,且高浓度的GR24的抑制作用更为明显。
综上所述,外源GR24能够通过不同的途径抑制不结球白菜腋芽的萌发和伸长;外源GR24可能由根部运输到叶腋处直接抑制腋芽的萌发和伸长;同时运输到叶腋处的GR24还可能通过抑制细胞分裂素合成基因的表达而降低叶腋处的细胞分裂素含量,从而抑制腋芽的生长;外源GR24还能够提高叶腋处SPS基因和SPL9基因的表达来抑制腋芽的生长,但是关于SPS基因和SPL9 基因与其他信号之间的关系,还有待于进一步研究。
| [1] | 冯丹,陈贵林. 独脚金内酯调控侧枝发育的研究进展[J]. 生态学杂志,2011,30(2):349-356. Feng D,Chen G L. Shoot-branching control with stirgolactones research progresss[J]. Chinese Jorunal of Ecology,2011,30(2):349-356(in Chinese with English abstract). |
| [2] | 张荣祥,杨清,赵德刚. 新型植物激素——独脚金内酯[J]. 生物学通报,2011,46(5):10-13. Zhang R X,Yang Q,Zhao D G. New plant hormone:strigolactones[J]. Bulletin of Biology,2011,46(5):10-13(in Chinese with English abstract). |
| [3] | Waldie T,McCulloch H,Leyser O. Strigolactones and the control of plant development:lessons from shoot branching[J]. The Plant Journal,2014,79(4):607-622. |
| [4] | Arite T,Umehara M,Ishikawa S,et al. d14,a strigolactone-insensitive mutant of rice,shows an accelerated outgrowth of tillers[J]. Plant and Cell Physiology,2009,50(8):1416-1424. |
| [5] | Sorefan K,Booker J,Haurogné K,et al. MAX4 and RMS1 are orthologous dioxygenase-like genes that regulate shoot branching in Arabidopsis and pea[J]. Genes and Development,2003,17(12):1469-1474. |
| [6] | Stirnberg P,van de Sande K,Leyser H M O. MAX1 and MAX2 control shoot lateral branching in Arabidopsis[J]. Development,2002,129(5):1131-1141. |
| [7] | Gomez-Roldan V,Fermas S,Brewer P B,et al. Strigolactone inhibition of shoot branching[J]. Nature,2008,4455(7210):189-194. |
| [8] | Minakuchi K,Kameoka H,Yasuno N,et al. FINE CULM1(FC1)works downstream of strigolactones to inhibit the outgrowth of axillary buds in rice[J]. Plant and Cell Physiology,2010,51(7):1127-1135. |
| [9] | Booker J,Auldridge M,Wills S,et al. MAX3/CCD7 is a carotenoid cleavage dioxygenase required for the synthesis of a novel plant signaling molecule[J]. Current Biology,2004,14(14):1232-1238. |
| [10] | Lin H,Wang R,Qian Q,et al. DWARF27,an iron-containing protein required for the biosynthesis of strigolactones,regulates rice tiller bud outgrowth[J]. The Plant Cell,2009,21(5):1512-1525. |
| [11] | Umehara M,Hanada A,Yoshida S,et al. Inhibition of shoot branching by new terpenoid plant hormones[J]. Nature,2008,455(7210):195-200. |
| [12] | 王玫,陈洪伟,刘克锋. 外源GR24对一串红生长发育的影响[J]. 江苏农业科学,2015,43(2):164-167. Wang M,Chen H W,Liu K F. Effects of exogenous GR24 on the growth and development of tropical sage[J]. Jiangsu Agricultural Sciences,2015,43(2):164-167(in Chinese with English abstract). |
| [13] | Xu J,Zha M,Li Y,et al. The interaction between nitrogen availability and auxin,cytokinin,and strigolactone in the control of shoot branching in rice(Oryza sativa L.)[J]. Plant Cell Reports,2015,34(9):1647-1662. |
| [14] | 侯喜林,宋小明. 不结球白菜种质资源的研究与利用[J]. 南京农业大学学报,2012,35(5):35-42. DOI:10.7685/j.issn.1000-2030.2012.05.005. Hou X L,Song X M. Research and utilization of Brassica campestris ssp.chinensis Makino(non-heading Chinese cabbage)germplasm resources[J]. Journal of Nanjing Agricultural University,2012,35(5):35-42(in Chinese with English abstract). |
| [15] | 曹寿椿,李式军. 白菜地方品种的初步研究[J]. 南京农学院学报,1980(2):32-38. DOI:10.7685/j.issn.1000-2030.1980.02.005. Cao S C,Li S J. Preliminary study on local varieties of Chinese cabbage[J]. Journal of Nanjing Agricultural College,1980(2):32-38(in Chinese with English abstract). |
| [16] | Kebrom T H,Spielmeyer W,Finnegan E J. Grasses provide new insights into regulation of shoot branching[J]. Trends in Plant Science,2013,18(1):41-48. |
| [17] | Cheng X,Ruyter-Spira C,Bouwmeester H. The interaction between strigolactones and other plant hormones in the regulation of plant development[J]. Frontiers in Plant Science,2013,4:199. |
| [18] | Germain A D S,Bonhomme S,Boyer F D,et al. Novel insights into strigolactone distribution and signalling[J]. Current Opinion in Plant Biology,2013,16(5):583-589. |
| [19] | 刘拥海,俞乐,丁君辉,等. 植物激素对分枝发育的协同调控作用研究进展[J]. 植物生理学报,2012,48(10):941-948. Liu Y H,Yu L,Ding J H,et al. Research progress in synerigistic regulatory roles of phytohormones in shoot branching[J]. Plant Physiology Journal,2012,48(10):941-948(in Chinese with English abstract). |
| [20] | Tantikanjana T,Yong J W H,Letham D S,et al. Control of axillary bud initiation and shoot architecture in Arabidopsis through the SUPERSHOOT gene[J]. Genes and Development,2001,15(12):1577-1588. |
| [21] | Schwarz S,Grande A V,Bujdoso N,et al. The microRNA regulated SBP-box genes SPL9 and SPL15 control shoot maturation in Arabidopsis[J]. Plant Molecular Biology,2008,67(1/2):183-195. |
| [22] | Luisi A,Lorenzi R,Sorce C. Strigolactone may interact with gibberellin to control apical dominance in pea(Pisum sativum)[J]. Plant Growth Regulation,2011,65(2):415-419. |
| [23] | 刘旭. 成熟期不同的梨品种果实生长发育机理探究[D]. 雅安:四川农业大学,2008:37-39. Liu X. Studies on mechanism of fruit growth and development of different ripening-season of pears[D]. Ya'an:Sichuan Agricultural University,2008:37-39(in Chinese with English abstract). |
| [24] | Durbak A,Yao H,McSteen P. Hormone signaling in plant development[J]. Current Opinion in Plant Biology,2012,15(1):92-96. |
| [25] | Aguilar-Martínez J A,Poza-Carrión C,Cubas P. Arabidopsis BRANCHED1 acts as an integrator of branching signals within axillary buds[J]. The Plant Cell,2007,19(2):458-472. |




