文章信息
- 孙文星, 南文婷, 谷淑华, 韩海银, 李艳, 褚维伟, 陈杰. 2016.
- SUN Wenxing, NAN Wenting, GU Shuhua, HAN Haiyin, LI Yan, CHU Weiwei, CHEN Jie. 2016.
- miR-27b及其靶基因PPARγ在肌内和皮下脂肪细胞中的差异表达分析
- Differential expression of miR-27b and its target gene PPARγ in intramuscular and subcutaneous adipocytes
- 南京农业大学学报, 39(2): 249-254
- Journal of Nanjing Agricultural University, 39(2): 249-254.
- http://dx.doi.org/10.7685/jnau.201505022
-
文章历史
- 收稿日期:2015-05-22
2. 南通大学公共卫生学院, 江苏 南通 226019
2. College of Public Health, Nantong University, Nantong 226019, China
肌内脂肪(intramuscular fat,IMF)含量可影响肌肉的肉色、嫩度和多汁性,是肉质指标中的关键参数[1, 2]。在国内外瘦肉型猪的选育过程中,在提高瘦肉率的同时也降低了IMF含量,现在瘦肉型猪中IMF含量约为1.5%左右,明显低于IMF的最适范围2%~3%,从而影响了猪肉的品质。所以,提高IMF含量,同时不影响其他部位的脂肪沉积,甚至降低皮下脂肪与内脏脂肪的沉积,已成为家畜育种者所关注的热点,而实现这一育种目标的关键是寻找调控脂肪在机体差异沉积的机制。
过氧化物酶体增殖物激活受体γ(peroxisome proliferator activated receptor γ,PPARγ)属于过氧化物酶体增殖物激活受体家族,可与类维生素 A 受体(RXR)形成异源二聚体,通过与靶基因上的过氧化体增殖反应元件结合来调控靶基因表达[3]。在脂肪分化沉积过程中,PPARγ与CCAATT增强子结合蛋白α(CCAAT enhancer binding protein α,C/EBPα)通过相互正反馈调节来促进脂肪的分化与脂质的沉积。对长白猪、巴克夏猪、汉普夏猪和杜洛克猪PPARγ基因的BsrI-PCR-RFLP进行多态性分析,发现PPARγ的多态性与猪肉的多汁性和嫩度显著相关,并且品种间的比较发现PPARγ可以显著影响猪肉的风味[4]。
microRNAs(miRNAs)是物种间保守的内源性表达的非编码小分子RNA,长度22 nt左右,于1993年在秀丽新小杆线虫中首次被发现[5]。近年研究发现,miRNAs在脂肪细胞分化和脂质代谢方面发挥着重要作用,如miR- 146 b[6]、miR- 103 [7]、miR- 21 [8]等可促进脂肪沉积,而miR- 130 [9]、miR- 145 [10]、miR- 155 [11]则抑制脂肪沉积,还发现miRNAs与机体不同部位的脂肪沉积相关[12]。
鉴于PPARγ在脂肪沉积过程中的关键作用,本研究分析了PPARγ在肌内脂肪细胞与皮下脂肪细胞中的差异表达,并从miRNAs的角度解释PPARγ在肌内脂肪细胞和皮下脂肪细胞差异表达的分子机制。
1 材料与方法 1.1 材料 1.1.1 试验动物3~7日龄雄性长白猪(3头)购于南京农业大学江浦农场。
1.1.2 试剂Ⅱ型胶原酶、胎牛血清(FBS)、高糖DMEM培养基、PBS液、0.25%胰蛋白酶购自Gibco公司;油红O购自南京生兴生物技术有限公司;双荧光酶报告基因检测试剂盒(E1910)购自Promega公司;Trizol、RNA反转录试剂盒(DRR036A),miRNAs反转录试剂盒(D350A),RNA荧光定量试剂盒(RR426A),miRNAs荧光定量试剂盒(RR716)均购自TaKaRa公司;地塞米松(dexamethasone,Dex)、胰岛素(insulin,INS)、3-异丁基-1-甲基黄嘌呤(3-isobutyl-1-methylxanthine,IBMX)购自Sigma公司;PPARγ一抗(sc-7273)、β-actin一抗(sc-47778)、羊抗鼠二抗购自Santa Cruz公司;miR- 27a、miR-27 b的mimic购于上海吉玛公司;X-tremeGENE siRNA(Cat.No.04476093001)转染试剂购于Roche;PMSF(ST506)、PIPA裂解液(P0013B)、BSA蛋白浓度测定试剂盒(P0012S)购于碧云天生物技术公司;其他试剂均为国产分析纯。
1.2 方法 1.2.1 前体脂肪细胞的获取通过成熟脂肪细胞去分化的方法[13]获取前体脂肪细胞。颈动脉放血处死仔猪,取背最长肌和背部皮下脂肪,经1 g · L-1 Ⅱ型胶原酶37 ℃消化30 min,200 g离心5 min,取上层脂肪细胞,将脂肪细胞接种到注满培养基的培养瓶中,倒置培养7~10 d,成熟脂肪细胞发生自动去分化,获得前体脂肪细胞。
1.2.2 前体脂肪细胞的诱导分化待前体脂肪细胞100%汇合后,利用“鸡尾酒法”诱导细胞分化,即用含10% FBS、2.5 μmo• L-1 Dex、5 μg • mL-1 INS、0.1 mmol• L-1 IBMX的成脂诱导液培养细胞3 d,用含体积分数为10% FBS的DMEM培养基培养细胞6 d。
1.2.3 反转录及荧光定量PCR(qRT-RCR)采用Trizol提取细胞总RNA,采用TaKaRa的反转录试剂盒(DRR036A)进行RNA反转录;用miRNAs反转录试剂盒(D350A)进行miRNAs反转录。具体步骤见试剂盒说明书。
采用qRT-PCR对PPARγ、PPARγ 2 、脂肪组织甘油三酯水解酶(adipose triglyceride lipase,ATGL)、激素敏感脂肪酶(hormose sensitive lipose,HSL)、乙酰CoA羧化酶(acetyl CoA carboxylase,ACC)、脂肪酸合成酶 (fatty acid synthase,FAS)基因和miR- 27a、miR-27b、miR-130a、miR-130b、miR-128、miR-301 的表达情况进行检测(引物见表 1)。qRT-RCR反应体系及反应条件参照TaKaRa的RNA荧光定量试剂盒(RR426A)、miRNAs 荧光定量试剂盒(RR716)说明书进行。对mRNA的检测以β-actin为内参;对miRNAs的检测以与猪基因 组无同源性的乱序片段E5(5′-GTGACCCACGATGTGTATTCGC-3′)为外参。定量数据通过2-ΔΔCT法进行计算。
| 基因名称Gene symbol | GenBank登录号Accession number | 引物(对)序列Primer(pairs)sequence(5′→3′) |
| PPARγ | NM_214379 | F/R:ATTCCCGAGAGCTGATCCAA/TGGAACCCCGAGGCTTTAT |
| PPARγ2 | NM_214379 | F/R:GACCCAGAAAGCGATGC/TGGTGAAGGGCTTGATGT |
| ACC | NM_001114269 | F/R:TTCCTATCGGCTATTGACA/CTTCGCACATACACCTCC |
| FAS | NM_001099930 | F/R:CATTCGGTGCGTCCTGGTG/AGGCGTGCTCCGTCTGCTT |
| ATGL | NM_001098605 | F/R:TCACCAACACCAGCATCCA/GCACATCTCTCGAAGCACCA |
| HSL | NM_214315 | F/R:CGGCGGCTGTCAGGTGTCTT/TACCCGTTGGCTGGCGTCTC |
| β-actin | DQ845171 | F/R:TGCTGTCCCTGTACGCCTCTG/ATGTCCCGCACGATCTCCC |
| miR-27a | MI0002442 | F:TTCACAGTGGCTAAGTTCCGC |
| miR-27b | MI0013109 | F:TTCACAGTGGCTAAGTTCTGC |
| miR-130a | MI0008271 | F:CAGTGCAATGTTAAAAGGGCAT |
| miR-130b | MI0013136 | F:CAGTGCAATGATGAAAGGGCAT |
| miR-128 | MI0002451 | F:TCACAGTGAACCGGTCTCTTT |
| miR-301 | MI0002432 | F:CAGTCCAATAGTATTGTCAAAGC |
利用RIPA蛋白裂解液裂解分化的脂肪细胞,提取总蛋白;经BCA蛋白试剂盒测定蛋白浓度;蛋白变性后,利用SDS-PAGE凝胶80 V、2 h进行蛋白分离,蛋白上样量为每孔20 μg,随后200 mA、2 h将蛋白转到聚偏二氟乙烯(PVDF)膜上;裁剪PPARγ、β-actin条带,用1%BSA封闭1 h,一抗4 ℃过夜,二抗室温孵育1 h,ECL显色,CDD成像系统拍照。
1.2.5 miRNA生物信息学预测利用在线网站TargetScan(http://www.targetscan.org/)与PicTar(http://pictar.mdc-berlin.de/)预测靶向PPARγ的miRNAs,通过网站miRanda(http://microrna.sanger.ac.uk/sequences/)获取预测miRNAs的序列。
1.2.6 构建PPARγ基因3′-UTR区荧光报告载体含有PPARγ基因3′-UTR质粒由南京农业大学动物生理生化实验室潘士锋博士赠送,质粒名为pGL3-Control/PPARγ。
1.2.7 miRNA靶向性验证利用双荧光报告系统检测候选 miRNAs 对PPARγ基因的靶向性。将PK-15细胞以1×105 mL-1的密度接种到12孔板中,用含10% FBS 的 DMEM 培养24 h。利用X-tremeGENE siRNA 转染试剂将mimic(50 μmo• L-1)或mimic阴性对照(NC)(50 μmo• L-1)、phRL-TK(0.05 μg)、pGL3-Control/PPARγ(1 μg)质粒共转染PK-15细胞,转染步骤参照转染试剂说明书。培养48 h,利用Promega双荧光检测试剂盒检测荧光活性,荧光强度以萤火虫荧光强度与海肾荧光强度的比值表示。
1.2.8 油红O染色及脂滴含量测定待前体脂肪细胞分化成熟后,采用油红O染色观察细胞分化情况,方法如前所述[13],即用10%甲醛固定细胞后,再用油红O染色15 min,并通过异丙醇萃取细胞内的油红O,通过油红O含量的多少反映细胞内甘油三酯含量。
1.3 数据的统计学分析采用SPSS 16.0统计软件对数据进行分析,每个试验重复3次,数据用平均数±标准差(x±SD)表示,采用配对t测验分析肌内和皮下前体脂肪细胞的分化能力以及基因在两种脂肪细胞中的表达差异,采用独立样本 t测验分析miRNAs对荧光素酶报告基因活性的影响。
2 结果与分析 2.1 肌内前体脂肪细胞与皮下前体脂肪细胞分化能力的比较将肌内前体脂肪细胞与皮下前体脂肪细胞经DMI诱导分化9 d后,发现肌内前体脂肪细胞的分化率高于皮下脂肪细胞(图 1-A),并且细胞内甘油三酯含量显著高于皮下脂肪前体细胞(P < 0.05)(图 1-B)。脂肪合成关键基因ACC与FAS在肌内脂肪细胞中的表达量显著高于其在皮下脂肪细胞中的表达,同时脂肪分解关键基因ATGL与HSL表达量也显著高于其在皮下脂肪细胞中的表达(P < 0.05)(图 1-C)。由此可见,在体外,肌内前体脂肪细胞的分化能力强于皮下前体脂肪细胞,并且肌内脂肪细胞的脂质代谢能力强于皮下脂肪细胞。
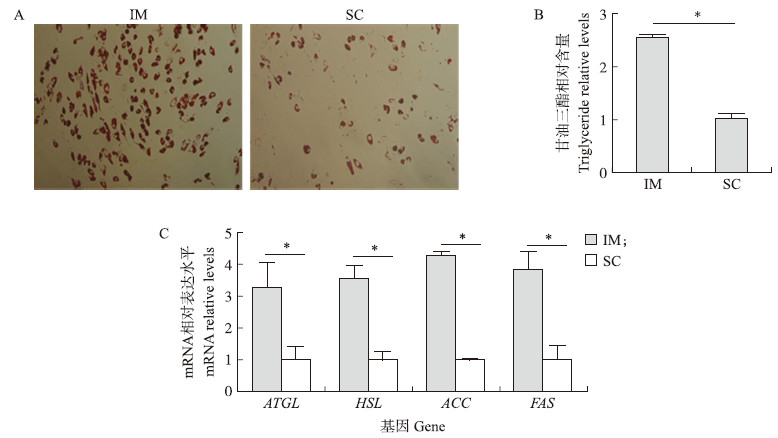 |
图 1 皮下前体脂肪(SC)细胞与肌内前体脂肪(IM)细胞分化能力比较
Fig. 1 The differentiation abilities of subcutaneous(SC)and intramuscular(IM)preadipocytes
A:油红O染色Oil red O staining of cells after induction;B:甘油三酯含量比较The comparison of cellular triglyceride between SC and IM adipocytes;C:脂肪合成与分解基因的表达情况The expression levels of lipid synthesis and lipolysis gene in SC and IM adipocytes. ATGL:甘油三酯水解酶Adipose triglyceride lipase;HSL:激素敏感脂肪酶Hormose sensitive lipose;ACC:乙酰CoA羧化酶Acetyl CoA carboxylase;FAS:脂肪酸合成酶Fatty acid synthase. |
qRT-PCR结果显示:PPARγ、PPARγ 2 在肌内脂肪细胞中的表达量显著高于其在皮下脂肪细胞中的表达量(P < 0.05)(图 2-A)。Western blot结果显示,PPARγ1、PPARγ2蛋白在肌内脂肪细胞中的表达量显著高于其在皮下脂肪细胞中的表达量(P < 0.05)(图 2-B)。
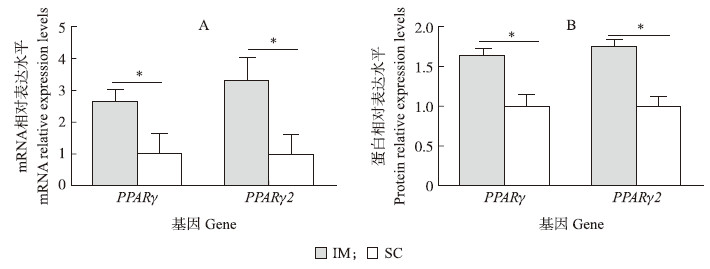 | 图 2 PPARγ的mRNA和蛋白在皮下脂肪(SC)细胞与肌内脂肪(IM)细胞中的表达 Fig. 2 mRNA and protein expression levels of PPARγ in subcutaneous(SC)and intramuscular(IM)adipocytes |
生物信息学预测发现6个候选miRNA可以靶向PPARγ基因。miRNAs的qRT-PCR结果显示:miR- 27a 与miR-27 b在皮下脂肪细胞的表达量显著高于其在肌内脂肪细胞中的表达量(P < 0.05),而miR- 130a、miR-130b、miR-128、miR-301 的表达量在皮下脂肪细胞与肌内脂肪细胞中无显著差异(P>0.05)(图 3)。
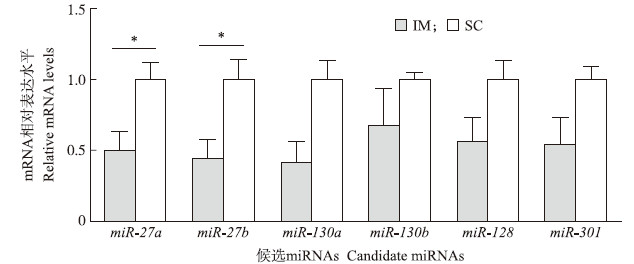 | 图 3 候选miRNA在IM细胞与SC细胞中的表达 Fig. 3 The expression levels of candidate miRNAs in IM and SC adipocytes |
为了验证miR- 27a与miR-27 b的靶向性,将pGL3-Control/PPARγ分别与miR- 27a或miR-27 b共转染PK-15细胞,48 h后检测荧光活性。结果显示:miR- 27 b可以显著抑制pGL3-Control/PPARγ的荧光活性(P < 0.05),而miR- 27 a与阴性对照(NC)相比没有显著差异(图 4)。
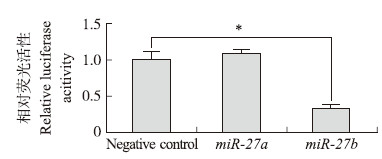 | 图 4 双荧光素酶报告基因分析 Fig. 4 Dual luciferase reporter gene assay |
为了实现提高胴体肌内脂肪含量同时不影响脂肪在其他部位的沉积,特别是不影响在皮下脂肪沉积的育种目的,了解脂肪在不同部位沉积的分子机制是非常重要的。本试验通过成熟脂肪细胞去分化获得前体脂肪细胞,并对肌内前体脂肪细胞与皮下前体脂肪细胞的分化聚脂能力进行了比较。本试验发现,肌内前体脂肪细胞的分化聚脂能力显著强于皮下前体脂肪细胞,并且与脂肪合成和脂肪分解有关的关键基因在肌内脂肪中的表达量也显著高于皮下脂肪,这表明肌内脂肪的脂肪代谢能力显著强于皮下脂肪,这与Chen等[14]在成年猪上的体外试验结果一致,但与Sun等[15]在体内芯片上研究结果完全相反,即在体情况下,皮下脂肪细胞的脂肪代谢能力强于肌内脂肪。肌内脂肪这种体内、体外脂肪代谢能力的差异可能是由细胞所处微环境的改变所导致的,即体内存在着抑制肌内脂肪沉积的因子,具体机制仍需进一步研究。
PPARγ作为脂肪分化的关键调控转录因子,研究发现,在成纤维细胞中过表达PPARγ可以促其向脂肪细胞分化[16];至今尚未发现细胞可以在PPARγ缺失的情况下向脂肪细胞分化。鉴于PPARγ在脂肪分化聚脂过程中的关键作用,笔者对PPARγ在肌内脂肪细胞与皮下脂肪细胞中的表达量进行比较,发现PPARγ、PPARγ 2 在肌内脂肪细胞中的mRNAs表达量显著高于其在皮下脂肪细胞中的表达量,这与在体PPARγ的表达模式完全相反[16],此结果说明在体内可能存在抑制肌内脂肪PPARγ表达的因子,进而抑制肌内脂肪的分化与沉积,仍需进一步研究。蛋白表达检测结果表明,PPARγ2与PPARγ1在肌内脂肪细胞中的表达量显著高于皮下脂肪细胞,这是首次发现PPARγ1蛋白的表达在肌内脂肪细胞与皮下脂肪细胞中存在显著差异。Ren等[17]发现PPARγ在脂肪分化聚脂中的关键作用,主要指的是PPARγ 2 [17],而本试验发现PPARγ 1 也参与了脂肪分化聚脂过程,并与脂肪在不同部位的差异沉积相关。
因为肌内脂肪被肌纤维所包裹,所处环境的差异可能导致表观遗传上的差异,所以我们推测PPARγ在皮下脂肪与肌内脂肪中的表达差异可能是由表观遗传差异所致,因此我们检测了靶向PPARγ的 miRNAs在两种组织中的表达水平。在候选的miRNAs 中,只有miR- 27a与miR-27 b在这两种脂肪细胞中存在显著差异。经双荧光报告系统检测,发现只有miR- 27 b可以靶向调控PPARγ,这与之前报道一致[18, 19],在肌内脂肪细胞和皮下脂肪细胞中差异表达的miR- 27 a可能是通过调控其他脂肪生成或脂肪分解有关基因来参与脂肪沉积过程[20]。所以我们认为,在体外脂肪前体细胞的分化过程中,miR- 27 b的差异表达是导致PPARγ差异表达原因之一,miR- 27 b可通过调控PPARγ的表达来实现对脂肪的差异调控,而miR- 27 b对脂肪差异沉积的影响是否依赖于靶向PPARγ仍需进一步研究。
| [1] | Hu H,Wang J,Zhu R,et al. Effect of myosin heavy chain composition of muscles on meat quality in Laiwu pigs and Duroc[J]. Sci China C:Life Sci,2008,51(2):127-132. |
| [2] | Webb E C,O'Neill H A. The animal fat paradox and meat quality[J]. Meat Sci,2008,80(1):28-36. |
| [3] | Ferré P. The biology of peroxisome proliferator-activated receptors relationship with lipid metabolism and insulin sensitivity[J]. Diabetes,2004,53(suppl 1):43-50. |
| [4] | Emnett R,Moeller S,Irvin K,et al. An investigation into the genetic controls of pork quality[J]. National Swine Improvement Federation,2000,26:62-67. |
| [5] | Lee R C,Feinbaum R L,Ambros V. The C.elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14[J]. Cell,1993,75(5):843-854. |
| [6] | Chen L,Dai Y M,Ji C B,et al. Mir-146b is a regulator of human visceral preadipocyte proliferation and differentiation and its expression is altered in human obesity[J]. Mol Cell Endocrinol,2014,393(1/2):65-74. |
| [7] | Xie H,Lim B,Lodish H F. MicroRNAs induced during adipogenesis that accelerate fat cell development are down regulated in obesity[J]. Diabetes,2009,58(5):1050-1057. |
| [8] | Kim S Y,Hwang S H,Cho H H,et al. MicroRNA21 regulates the proliferation of human adipose tissue-derived mesenchymal stem cells and high-fat diet induced obesity alters microRNA21 expression in white adipose tissues[J]. J Cell Physiol,2012,227:183-193. |
| [9] | Lee E K,Lee M J,Abdelmohsen K,et al. miR-130 suppresses adipogenesis by inhibiting peroxisome proliferator-activated receptor gamma expression[J]. Mol Cell Biol,2011,31:626-638. |
| [10] | Guo Y,Chen Y,Zhang Y,et al. Up-regulated miR-145 expression inhibits porcine preadipocytes differentiation by targeting IRS1[J]. Int J Biol Sci,2012,8:1408-1417. |
| [11] | Liu S,Yang Y,Wu J. TNFalpha-induced up-regualtion of miR-155 inhibits adipogenesis by down-regulating early adipogenic transcription factors[J]. Biochem Biophys Res Commun,2011,414:618-624. |
| [12] | Heneghan H M,Miller N,McAnena O J,et al. Differential miRNA expression in omental adipose tissue and in the circulation of obese patients identifies novel metabolic biomarkers[J]. J Clin Endocrinol Metab,2011,96(5):846-850. |
| [13] | 王欢欢,孙文星,徐春瑛,等. 猪成熟脂肪细胞分离培养及去分化研究[J]. 农业生物技术学报,2012,20(8):915-921. Wang H H,Sun W X,Xu C Y,et al. Optimizing cultivation of mature adipocytes and obtaining preadipocytes by mature adipocyte dedifferentiation in pigs(Sus scrofa)[J]. Journal of Agricultural Biotechnology,2012,20(8):915-921(in Chinese with English abstract). |
| [14] | Chen J,Dodson M V,Jiang Z. Cellular and molecular comparison of redifferentiation of intramuscular- and visceral-adipocyte derived progeny cells[J]. Int J Biol Sci,2010,6(1):80-88. |
| [15] | Sun W X,Wang H H,Jiang B C,et al. Global comparison of gene expression between subcutaneous and intramuscular adipose tissue of mature Erhualian pig[J]. Genet Mol Res,2012,12(4):5085-5101. |
| [16] | Tontonoz P,Hu E,Spiegelman B M. Stimulation of adipogenesis in fibroblasts by PPARγ2,a lipid-activated transcription factor[J]. Cell,1994,79(7):1147-1156. |
| [17] | Ren D,Collingwood T N,Rebar E J,et al. PPARγ knockdown by engineered transcription factors:exogenous PPARγ2 but not PPARγ1 reactivates adipogenesis[J]. Genes Dev,2002,16(1):27-32. |
| [18] | Karbiener M,Fischer C,Nowitsch S,et al. microRNA miR-27b impairs human adipocyte differentiation and targets PPARγ[J]. Biochem Biophys Res Commun,2009,390(2):247-251. |
| [19] | Lin Q,Gao Z,Alarcon R M,et al. A role of miR-27 in the regulation of adipogenesis[J]. FEBS J,2009,276(8):2348-2358. |
| [20] | Wang T,Li M,Guan J,et al. MicroRNAs miR-27a and miR-143 regulate porcine adipocyte lipid metabolism[J]. Int J Mol Sci,2011,12(11):7950-7959. |




