文章信息
- 李妍, 王雪花, 陈忠文, 段伟科, 侯喜林, 李英. 2016.
- LI Yan, WANG Xuehua, CHEN Zhongwen, DUAN Weike, HOU Xilin, LI Ying. 2016.
- 不结球白菜抗坏血酸合成基因BcGME的同源克隆及胁迫下的表达分析
- Homologous cloning and expression analysis of ascorbic acid biosynthesis gene BcGME under stress from non-heading Chinese cabbage
- 南京农业大学学报, 39(2): 205-212
- Journal of Nanjing Agricultural University, 39(2): 205-212.
- http://dx.doi.org/10.7685/jnau.201507026
-
文章历史
- 收稿日期:2015-07-13
不结球白菜(Brassica campestris ssp.chinensis Makino)是我国长江中下游地区的大众蔬菜种类。如何提高不结球白菜的抗坏血酸(L-ascorbic acid,AsA)含量,增强其对环境胁迫的耐受力,是近年来不结球白菜育种的目标之一。
研究表明,AsA在植物体内主要有2个功能:作为酶的辅因子或者作为抗氧化剂。另外,AsA在DNA甲基化[1]、抗逆性[2]、细胞分裂[3]、光合结构保护[4]、离子吸收[5]和调节气孔运动[6]中均发挥重要作用。目前AsA的已发现4条合成途径,分别为肌醇途径[7]、古洛糖途径[8]、甘露糖/L-半乳糖途径[9]和半乳糖醛酸途径[10],其中L-半乳糖途径是植物体内AsA合成的主要途径。GDP-D-甘露糖-3′,5′-差向异构酶 (GME)在L-半乳糖途径中催化GDP-D-甘露糖形成GDP-半乳糖,还可以在L-古洛糖途径中催化GDP-D- 甘露糖形成GDP-古洛糖,是AsA生物合成中的一个关键酶。在AsA的合成途径中,GME是最保守的蛋白[11]。有研究发现,张氏江蓠GcGME的5′端区域包含一个光响应顺式调节元件[12],水稻中GME存在保守的NAD结合域,并且NAD+能加速GME催化的反应[13]。GME的沉默会影响番茄果胶糖的结构[14],Bulley等[15]认为猕猴桃中GME的高表达可能是其果实AsA含量较高的原因之一。通过抑制番茄中GME基因的表达发现,转基因植株的叶片和果实中AsA含量均有下降,并且植株在生长发育过程中存在缺陷,影响其细胞分裂和细胞伸长[16]。与之相反,番茄中GME基因过量表达,转基因植株叶片和成熟果实中的AsA含量均比野生型番茄显著提高,并且在非生物胁迫下转基因植株具有更高的抗逆性[17]。此外,在绿藻中的研究发现,GME的活性和AsA的含量之间存在紧密关联性[18]。
本研究以不结球白菜品种‘苏州青’为材料,同源克隆了抗坏血酸合成基因BcGME并且进行了相关的生物信息学分析。同时以不结球白菜‘苏州青’为试验材料,分别进行了水淹胁迫和过氧化氢(H2O2)胁迫处理,利用液相色谱测定了AsA含量的变化并采用实时荧光定量PCR检测了BcGME基因的表达量,为进一步了解不结球白菜抗坏血酸的调节机制,培育高品质的不结球白菜奠定基础。
1 材料与方法 1.1 试验材料供试材料为不结球白菜(Brassica campestris ssp.chinensis Makino)品种‘苏州青’,由南京农业大学园艺学院不结球白菜课题组提供。
1.2 试验设计 1.2.1 过氧化氢(H2O2)胁迫将不结球白菜品种‘苏州青’种子用去离子水冲洗干净,25 ℃催芽,2 d后播种于含基质(泥炭与蛭石的体积比为3:1)的穴盘中。将穴盘置于温度为25 ℃/16 ℃(昼/夜),光照时间为16 h/8 h(昼/夜,08:00开始光照),湿度为75%的人工气候室中。在植株4叶1心时,选取生长整齐一致的幼苗,定植于装有Hoagland营养液[19]的水培槽中。水培条件为:营养液pH值调至6.5,试验期间,每隔0.5 h用气泵通气0.5 h,每4 d更换1次营养液。水培缓苗1周后,于09:00喷施200 μmol • L-1的过氧化氢溶液,对照组喷施去离子水。两组分别喷施后均用透光塑料罩罩住,于0、6、12、24和48 h,取第2片完全展开叶,并沿主叶脉切开,一半叶片称质量,测定AsA的含量,另一半叶片提取总RNA。3次重复。
1.2.2 水淹胁迫不结球白菜品种‘苏州青’按1.2.1节中的方法催芽后播于穴盘,在大棚里自然生长1个半月后转移到人工气候室中,温度为25 ℃/16 ℃(昼/夜),光照时间为16 h/8 h(昼/夜),湿度为75%。缓苗2~3 d后,水淹处理组置于水培槽中,加入一定量的自来水至水面高出植株根部基质1~2 cm;对照组进行常规水分管理,保持土壤湿润状态。两组分别在0、1、3、5、7 d时,取第2片完全展开叶,并沿主叶脉切开,一半叶片称质量,测定AsA的含量,另一半叶片提取总RNA。3次重复。
1.3 试验方法 1.3.1 抗坏血酸(AsA)含量的测定不结球白菜叶片中还原型抗坏血酸含量的测定采用高效液相色谱法(HPLC)[20],并适当改进。取0.2 g叶片,加入1.5 mL 0.1%(体积分数)草酸充分研磨,转移至2 mL离心管中,4 ℃ 12 000 r • min-1 离心15 min。上清液用0.22 μm过滤器滤到一个洁净的离心管中,用于测定还原型抗坏血酸含量。流动相为0.1%乙酸,流速1 mL• min-1,进样20 μL,柱温30 ℃,检测波长245 nm,HPLC仪型号为Agilent 1120 Compact LC。
1.3.2 RNA的提取与反转录RNA提取试剂盒购自天根生化科技有限公司,具体方法参照RNAprep Pure植物总RNA提取试剂盒说明书。用‘苏州青’叶片的总RNA为模板,按照PrimeScript® RT(TaKaRa,Japan)试剂盒说明书反转录合成cDNA。
1.3.3 实时荧光定量PCR实时荧光定量的体系参照SYBR® PrimeScript® RT-PCR Kit Ⅱ(TaKaRa,Japan)试剂盒说明书。荧光定量PCR仪为Step One Plus(ABI公司),PCR程序采用两步法:95 ℃ 30 s;95 ℃ 5 s,60 ℃ 30 s,40个循环;设置65 ℃到95 ℃的熔解曲线。所得数据用Excel 2010软件分析。内参引物序列:Actin-F:GTTGCTATCCAGGCTGTTCT,Actin-R:AGCGTGAGGAAGAGCATAAC;GME引物序列:qAtGME-F:GGTGAGCATGAATGAGATGG,qAtGME-R:TATTAGGAGCCCAACCAAGC。
1.3.4 不结球白菜BcGME基因的同源克隆BcGME基因的cDNA序列参考张硕[21]的方法,NCBI数据库登录号为AET14213。在完整ORF的两端设计正向引物和反向引物GME1(GGATCCCTCCTCCGCTCAAATCCTTC)和GME2(GGTACCTACCACCACAGCATCACCAA)。以不结球白菜‘苏州青’叶片cDNA作为模板进行PCR反应,反应体系按照TaKaRa公司的rTaq酶说明书进行,程序为:95 ℃预变性5 min;95 ℃解链30 s,58 ℃退火30 s,72 ℃延伸1.5 min,35个循环;72 ℃延伸10 min;4 ℃保存。PCR产物进行琼脂糖凝胶电泳检测,用凝胶回收试剂盒对目的片段进行回收、纯化。回收产物用T4-DNA连接酶连接到pMD18-T-simple载体,连接产物转化大肠杆菌DH5α(由本实验室保存),涂于氨苄青霉素抗性的LB平板37 ℃暗培养12 h,挑取阳性单克隆送到南京金斯瑞生物科技有限公司测序分析。
1.3.5 序列分析用BioEdit软件查找BcGME基因序列的开放阅读框(ORF)。不同物种GME的氨基酸序列从NCBI(http://www.ncbi.nih.gov/)GenBank数据库数据库中搜索获得。多重序列比对和进化树构建用MEGA 5.2软件[22]进行。蛋白预测通过在线软件完成,包括SMART(http://smart.embl-heidelberg.de/)、Protparam tool(http://web.expasy.org/protparam/)、ProtScale(http://web.expasy.org/protscale/)、Signalp 4.0(http://www.cbs.dtu.dk/services/SignalP/)、TMHMM 2.0(http://www.cbs.dtu.dk/services/TMHMM/)、PredictProtein(http://www.cbi.pku.edu.cn/predictprotein/)、SOPMA(http://pbil.ibcp.fr/)和 Phyre 2(http://www.sbg.bio.ic.ac.uk/phyre2/html/)。
2 结果与分析 2.1 不结球白菜BcGME基因的同源克隆以‘苏州青’cDNA为模板,经PCR扩增得到1 500 bp左右的片段(图 1)。不结球白菜BcGME基因全长为1 495 bp,包含一个长度为1 137 bp的开放式阅读框(ORF),编码379个氨基酸。测序结果与拟南芥中GME基因的编码产物长度完全一致,相似度为98%,因此得到的cDNA序列即为不结球白菜的BcGME且CDS完整。
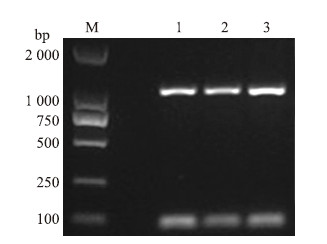 | 图 1 BcGME基因的全长扩增产物 Fig. 1 The full length amplification products of BcGME M:DL2000 DNA maker;1-3:BcGME基因扩增产物 The amplification products of BcGME |
将不结球白菜GME氨基酸序列与21个物种进行BLASTp同源比对,结果(图 2)发现:其与十字花科大部分植物的相似性为90%以上,如大白菜(XP_009151267.1)为99%,甘蓝型油菜(CDX86211.1)为 99%,琴叶拟南芥(XP_002874451.1)为97%,拟南芥(AED93843.1)为97%。另外与大豆(XP_003521749.1)、 苹果(XP_008366872.1)、梅(XP_008224440.1)、川桑(XP_010111559.1)、葡萄(XP_010649980.1)、毛果杨(XP_006382789.1)、马铃薯(XP_006362157.1)和黄瓜(XP_004139232.1)相似性为90%~91%;而与番茄(NP_001234589.1)、二穗短柄草(XP_010234732.1)、水稻(NP_001064609.1)、乌拉尔图小麦(EMS65770.1)、高粱(XP_002467242.1)、玉米(ACG32271.1)、卷柏(XP_002986045.1)、小立碗藓(XP_001778348.1)和莱茵衣藻(XP_001689497.1)的相似性为90%以下。
 |
图 2 BcGME与其他物种GME的氨基酸序列比较
Fig. 2 Alignment of aminoacid sequences of BcGME and homologs from other plants
红色虚线为NAD结构域(GxxGxxG/A),红色实线为短链脱氢酶催化结构域(YxxxK)。 The NAD-binding domain(GxxGxxG/A)was red dash line and the catalytic domain was red line. |
通过保守结构域分析发现,该蛋白属于NADB Rossmann超级家族。利用SMART软件在线分析,该蛋白含有Ⅰ:3 Beta_HSD结构域(Ser33-Phe210),Ⅱ:NAD_binding_4结构域(Asp70-Met279),Ⅲ:GDP Man Dehyd结构域(Ile34-Thr334),Ⅳ:Epimerase 结构域(Ile32-Ile272)(图 3)。通过Protparam tool分析发现,BcGME蛋白理论相对分子质量为42.97×103,酸性氨基酸为55个,碱性氨基酸为47个,理论等电点为5.84,分子式为C1907H2949N519O570S22,不稳定指数(instability index)为40.47,属于不稳定蛋白。总平均疏水指数(grand average of hydropathicity,GRAVY)为-0.440。采用ProtScale进行亲疏水性预测显示,该蛋白亲水性区域多于疏水性区域,属于亲水蛋白(图 4)。通过Signalp 4.0对不结球白菜BcGME序列进行信号肽预测,结果显示BcGME序列不存在信号肽也无分泌蛋白。采用TMHMM软件对BcGME序列进行跨膜区预测,结果显示该蛋白不存在跨膜区域。通过Predict Protein进行亚细胞定位预测,结果表明该蛋白分布在细胞质中。采用SOPMA进行卷曲螺旋分析显示,α螺旋占37.73%,延伸链占17.41%,β转角占10.55%,无规卷曲占34.30%。利用Phyre 2构建了BcGME蛋白(图 5-A)和AtGME蛋白(图 5-B)的三级结构模型,其中363个氨基酸(96%)参与建模,可信度较高。
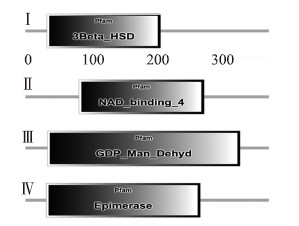 |
图 3 BcGME蛋白结构的预测
Fig. 3 The predicted domain structure of BcGME
Ⅰ:3 Beta_HSD结构域(Ser33-Phe210);Ⅱ:NAD_binding_4结构域(Asp70-Met279);Ⅲ:GDP Man Dehyd结构域(Ile34-Thr334);Ⅳ:Epimerase 结构域(Ile32-Ile272)。 Ⅰ:3 Beta_HSD domain was from Ser33 to Phe210;Ⅱ:NAD_binding_4 domain was from Asp70 to Met279;Ⅲ:GDP Man Dehyd was from Ile34 to Thr334;Ⅳ:Epimerase domain was from Ile32 to Ile272. |
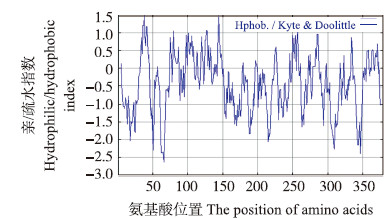 | 图 4 不结球白菜BcGME氨基酸序列亲/疏水性预测 Fig. 4 Predicted hydrophilic and hydrophobic properties of BcGME amino acid sequences from non-heading Chinese cabbage |
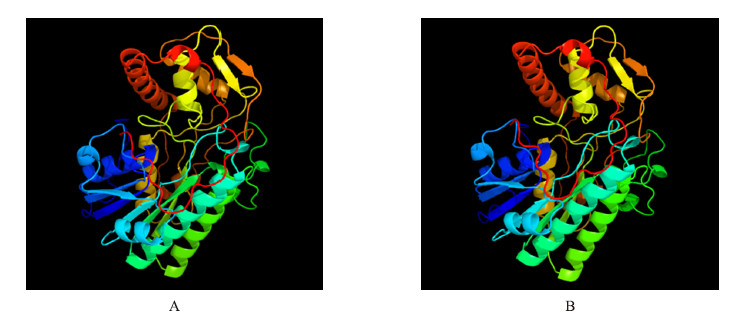 | 图 5 不结球白菜BcGME(A)和拟南芥AtGME(B)蛋白的三级结构模型比较 Fig. 5 Tertiary structure prediction of BcGME from non-heading Chinese cabbage(A)and Arabidopsis thaliana(B) |
利用MEGA 5.1构建进化树,结果(图 6)显示:不结球白菜与大白菜高度同源,位于同一进化分支,另外与同属十字花科的甘蓝型油菜、拟南芥以及琴叶拟南芥进化距离较近;其次,与梅、川桑、苹果、大豆进化距离较近;与莱茵衣藻进化 距离最远,原因可能是GME基因较为保守,从原生生物开始广泛存在于植物界。
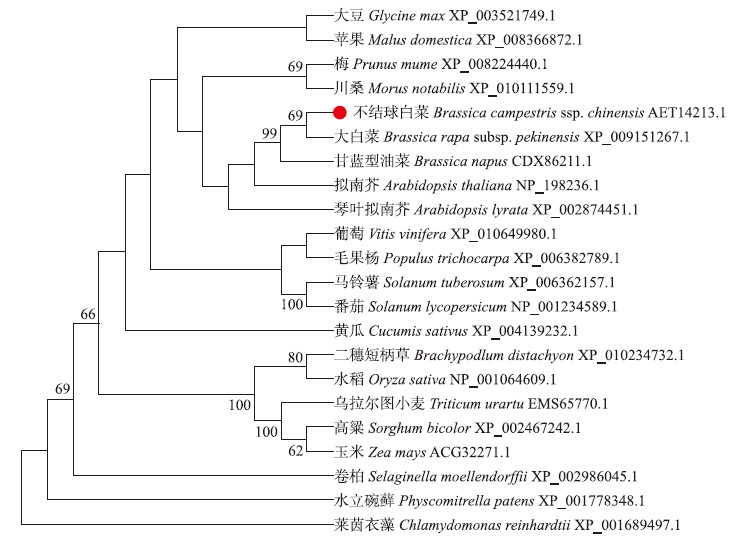 | 图 6 BcGME蛋白进化树 Fig. 6 Protein phylogenetic tree of BcGME |
由图 7-A可见:H2O2胁迫后,不结球白菜AsA含量在6 h达到峰值,在12 h最低,随后12~48 h缓慢恢复趋于平缓;对照组AsA含量变化缓慢,并且在12~48 h时高于H2O2处理。植株体内BcGME基因的表达量变化趋势与AsA含量变化趋势一致,AsA含量随着BcGME基因表达量的升高而升高(图 7-B)。 H2O2胁迫后,6 h的BcGME基因表达量为初始表达量的2倍,而12 h的表达量降低,为初始表达量的25%。
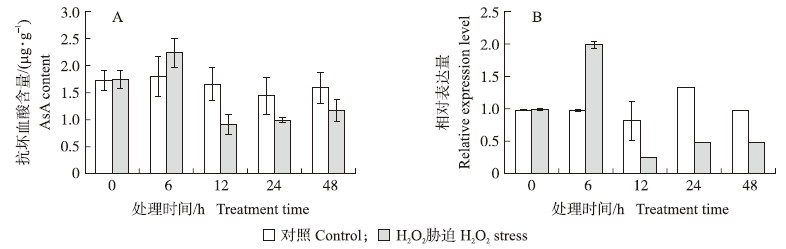 | 图 7 过氧化氢(H2O2)胁迫对不结球白菜的抗坏血酸含量(A)和BcGME相对表达量(B)的影响 Fig. 7 The effect of H2O2 stress on AsA content(A)and relative expression level of BcGME(B) in non-heading Chinese cabbage |
由图 8-A可见:水淹胁迫后,不结球白菜AsA含量急速下降,1 d时AsA含量最高为12.99 μg · g-1,随后AsA含量急速下降,7 d时仅为0.58 μg · g-1,另外水淹胁迫后3~7 d的AsA含量均低于对照组。水淹胁迫后,1 d时的表达量是0 d的1.5倍,随后逐渐下降,与AsA含量变化趋势一致(图 8-B)。
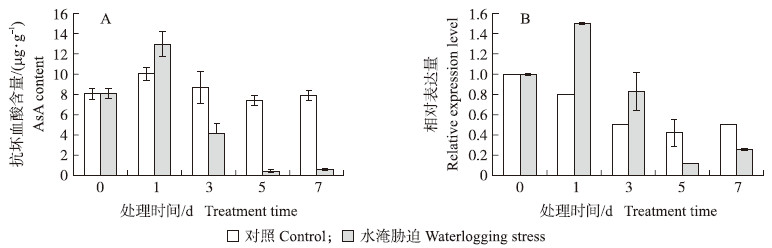 | 图 8 水淹胁迫对不结球白菜的抗坏血酸含量(A)和BcGME相对表达量(B)的影响 Fig. 8 The effect of waterlogging stress on AsA content(A)and relative expression level of BcGME(B) in non-heading Chinese cabbage |
以上数据显示,H2O2及水淹胁迫后,AsA含量与BcGME基因表达量的变化一致,推测GME是AsA合成途径中的关键调控基因。
3 讨论与结论大部分植物中的AsA含量与抗逆性呈正相关,可通过提高AsA含量或促进氧化态的AsA还原来提高植物的抗逆性[23]。本文在王雪花[24]研究的基础上,完成了GME基因相关生物信息学分析,并且探究了GME基因在H2O2胁迫和水淹胁迫下的表达情况。
本研究发现,GDP-D-甘露糖-3′,5′-差向异构酶(GME)比较保守,物种间的同源性较高,BcGME与其他21个物种GME氨基酸序列的同源性均为70%以上,其中NAD结构域(GxxGxxG/A)和短链脱氢酶催化结构域(YxxxK)为GME的2个保守区域[12],这2个区域可能和脱水酶以及差向异构酶催化机制第一步产生的中间产物核苷酸-4-酮糖有关[13]。进化树分析发现,不结球白菜不仅与十字花科的物种进化距离较近,还与豆科的大豆、桑科的川桑以及蔷薇科的苹果和梅进化距离较近。但同属蔷薇科的苹果和梅不在同一进化分支,可能与起源地环境条件及后期驯化管理差异有关。BcGME蛋白三级结构为二聚体不对称单位,与拟南芥GME蛋白三级结构相似[25],推测BcGME基因与AtGME在功能上存在相似性,均在抗坏血酸合成途径中起到关键作用[15]。本研究中,在H2O2和水淹胁迫下,不结球白菜中GME基因表达量变化趋势与AsA含量变化趋势一致,说明GME在这两种胁迫下与AsA含量为正调控关系。Li等[26]的研究证明,在茉莉酸甲酯和冷胁迫处理下,GME基因的表达量和AsA含量同时上调,但是其他胁迫处理的结果中GME与AsA含量不存在正调控关系。原因可能主要是由于AsA含量受多种因素影响,不同胁迫下单一基因不能决定其含量的变化。因此,GME基因的生物学功能分析还需要采用转基因技术继续研究。紫苜蓿的MsGME基因在拟南芥中过表达后,转基因植株可以通过提高AsA含量来有效地抵抗酸性胁迫、干旱胁迫和盐胁迫[27]。Voxeur等[14]研究表明,番茄中GME基因抑制表达后植株与对照相比AsA含量下降了40%~60%,并且植株生长表型产生了变化。这些研究表明,GME基因在AsA合成的L-半乳糖途径中发挥重要作用。本研究中,200 μmol • L-1的过氧化氢胁迫后,AsA含量在6 h达到峰值,而对照组AsA含量变化缓慢,对照组AsA含量在12~48 h均高于H2O2胁迫组。同样水淹胁迫下,1 d时AsA含量达到最高,但是随后3~7 d水淹胁迫的AsA含量均低于对照组。说明在这两种胁迫下,AsA含量应激性提高来抵抗外界环境变化。而且外施AsA对盐胁迫下抑制的小麦幼苗生长起到缓解作用[28]。不结球白菜普遍种植于长江中下游及其以南地区,而这些地区雨水充沛易发生涝害,给不结球白菜的生产造成了危害。除此之外,在植株生长过程中不可避免地会遭受各种非生物胁迫,如何提高不结球白菜AsA含量使其更好地适应逆境是目前育种的一个难题。然而,抗坏血酸调节机制十分复杂,目前还有待进一步研究。
| [1] | Blaschke K,Ebata K T,Karimi M M,et al. Vitamin C induces Tet-dependent DNA demethylation and a blastocyst-like state in ES cells[J]. Nature,2013,500(7461):222-226. |
| [2] | Gallie D R. The role of L-ascorbic acid recycling in respondingto environmental stress and in promoting plant growth[J]. Journal of Experimental Bbotany,2013,64(2):433-443. |
| [3] | Smirnoff N. Vitamin C:the metabolism and functions of ascorbic acid in plants[J]. Advances in Botanical Research,2011,59:107-177. |
| [4] | Toth S Z,Schansker G,Garab G. The physiological roles and metabolism of ascorbate in chloroplasts[J]. Physiologia Plantarum,2013,148(2):161-175. |
| [5] | Balestrini R,Ott T,Guther M,et al. Ascorbate oxidase:the unexpected involvement of a'wasteful enzyme'in the symbioses with nitrogen-fixing bacteriaand arbuscular mycorrhizal fungi[J]. Plant Physiology and Biochemistry,2012,59:71-79. |
| [6] | Shi Y C,Fu Y P,Liu W Q. NADPH oxidase in plasma membrane is involved in stomatal closure induced by dehydroascorbate[J]. Plant Physiology and Biochemistry,2012,51:26-30. |
| [7] | Lorence A,Chevone B I,Mendes P,et al. myo-Inositoloxygenase offers a possible entry point into plant ascorbate biosynthesis[J]. Plant Physiology,2004,134(3):1200-1205. |
| [8] | Wolucka B A,Montagu M V. GDP-mannose-3',5'-epimerase forms GDP-L-gulose,a putative intermediate for the de novo biosynthesis of vitamin C in plants[J]. Journal of Biological Chemistry,2003,278(48):47483-47490. |
| [9] | Wheeler G L,Jones M A,Smirnoff N. The biosyntheticpathway of vitamin C in higher plants[J]. Nature,1998,393(6683):365-369. |
| [10] | Agius F,Gonzalez-Lamothe R,Caballero J L,et al. Engineering increased vitamin C levels in plants by over-expression of a D-galacturonic acid reductase[J]. Nature Biotechnology,2003,21(2):177-181. |
| [11] | Wolucka B A,van Montagu M. The VTC2 cycle and the de novo biosynthesis pathways for vitamin C in plants:an opinion[J]. Phytochemistry,2007,68(21):2602-2613. |
| [12] | Siow R S,Teoh S,Teo S S,et al. Molecular cloning and characterization of GDP-mannose-3',5'-epimerase from Gracilaria changii[J]. Journal of Applied Phycology,2013,25(5):1309-1318. |
| [13] | Watanabe K,Suzuki K,Kitamura S. Characterization of a GDP-D-mannose-3',5'-epimerase from rice[J]. Phytochemistry,2006,67(4):338-346. |
| [14] | Voxeur A,Gilbert L,Rihouey C,et al. Silencing of the GDP-D-mannose-3,5-Epimerase affects the structure and cross-linking of the pecticpolysaccharide rhamnogalacturonan Ⅱ and plant growth in tomato[J]. The Journal of Biological Chemistry,2011,286(10):8014-8020. |
| [15] | Bulley S M,Rassam M,Hoser D,et al. Gene expression studies in kiwifruit and gene over-expression in Arabidopsis indicates that GDP-L-galactose guanyltransferase is a majorcontrol point of vitamin C biosynthesis[J]. Journal of Experimental Botany,2009,60(3):765-768. |
| [16] | Gilbert L,Alhagdow M,Nunes-Nesi A,et al. GDP-D-mannose-3,5-epimerase(GME)plays a key role at the intersection of ascorbate and non-cellulosic cell-wall biosynthesis in tomato[J]. The Plant Journal,2009,60(3):499-508. |
| [17] | Zhang C J,Liu J X,Zhang Y Y,et al. Overexpression of SlGMEs leads to ascorbate accumulation with enhanced oxidative stress,cold,and salt tolerance in tomato[J]. Plant Cell Reports,2011,30(3):389-398. |
| [18] | Running J A,Burlingame R P,Berry A. The pathway of L-ascorbic acid biosynthesis in the colourlessmicroalga Prototheca moriformis[J]. Journal of Experimental Botany,2003,54(389):1841-1849. |
| [19] | 郭世荣. 无土栽培学[M]. 北京:中国农业出版社,2003:77-118. Guo S R. Science of Soilless Culture[M]. Beijing:Chinese Agricultural Press,2003:77-118(in Chinese). |
| [20] | Bartoli C G,Yu J,Gómez F,et al. Inter-relationships between light and respiration in the control of ascorbic acid synthesis and accumulation in Arabidopsis thaliana leaves[J]. Journal of Experimental Botany,2006,57(8):1621-1631. |
| [21] | 张硕. 不结球白菜抗坏血酸合成相关基因的克隆与表达及BcPMI2的功能分析[D]. 南京:南京农业大学,2011. Zhang S. Gene cloning and expression profiling of ascorbic acid biosynthesis in non-heading Chinese cabbage and functional analysis of BcPMI[D]. Nanjing:Nanjing Agricultural University,2011(in Chinese with English abstract). |
| [22] | Tamura K,Peterson D,Peterson N,et al. MEGA5:molecular evolutionary genetics analysis using maximum likelihood,evolutionary distance,and maximum parsimony methods[J]. Mol Biol Evol,2011,28(10):2731-2739. |
| [23] | Gallie D R. The role of L-ascorbic acid recycling in responding to environmental stress and in promoting plant growth[J]. Journal of Experimental Botany,2013,64(2):433-443. |
| [24] | 王雪花. 不结球白菜抗坏血酸合成相关基因的表达及BcPMI2和BcGME功能分析[D]. 南京:南京农业大学,2013. Wang X H. Gene expression profiling of ascorbic acid biosynthesis pathway in non-heading Chinese cabbage and functional analysis of BcPMI2 and BcGME[D]. Nanjing:Nanjing Agricultural University,2013(in Chinese with English abstract). |
| [25] | Major L L,Wolucka B A,Naismith J H. Structure and function of GDP-Mannose-3',5'-epimerase:Anenzyme which performs three chemical reactions at thesame active site[J]. Journal of the American Chemical Society,2005,127:18309-18320. |
| [26] | Li J,Cui M,Li M J,et al. Expression pattern and promoter analysis of the gene encoding GDP-D-mannose-3',5'-epimerase under abiotic stresses and applications of hormones by kiwifruit[J]. Scientia Horticulturae,2013,150:187-194. |
| [27] | Ma L C,Wang Y R,Liu W X,et al. Overexpression of an alfalfa GDP-mannose-3,5-epimerase gene enhances acid,drought and salt tolerance in transgenic Arabidopsis by increasing ascorbate accumulation[J]. Biotechnol Lett,2014,36(11):2331-2341. |
| [28] | 常云霞,徐克东,周琳,等. 抗坏血酸对盐胁迫下小麦幼苗生长抑制的缓解效应[J]. 麦类作物学报,2013,33(1):151-155. Chang Y X,Xu K D,Zhou L,et al. Ascorbic acid mitigating the inhibition of salt stress to wheat seedling growth[J]. Journal of Triticeae Crops,2013,33(1):151-155(in Chinese with English abstract). |




